L’accident vasculaire cérébral (AVC), qui touche 150 000 personnes en France chaque année (soit un AVC toutes les quatre minutes en moyenne), est la troisième cause de décès et la première cause de handicap acquis de l’adulte dans les pays développés. Des progrès considérables ont été faits concernant la prise en charge diagnostique et thérapeutique des AVC ces dernières années. Cependant, l’efficacité de la prise en charge reste très étroitement liée à son délai de mise en place. Cette urgence diagnostique et thérapeutique est valable pour tous les types d’AVC (ischémie constituée ou transitoire, hémorragie), car si elle peut permettre dans certains cas d’améliorer – parfois de manière spectaculaire – l’état neurologique des patients, elle vise également à prévenir une aggravation clinique, la survenue de complications ou une récidive précoce.
Qu’est-ce qu’un AVC ?
Selon la définition de l’Organisation mondiale de la santé, l’accident vasculaire cérébral est « un déficit neurologique soudain d’origine vasculaire ». Cette définition simple masque néanmoins une grande hétérogénéité clinique, étiopathogénique, pronostique et thérapeutique.
Ischémie cérébrale
Les accidents ischémiques cérébraux représentent 80 % des AVC et regroupent les infarctus cérébraux et les accidents ischémiques transitoires (AIT). Selon la durée de l’occlusion et l’importance de la baisse de perfusion en aval, l’ischémie cérébrale peut n’être que transitoire, responsable d’un déficit neurologique très bref et spontanément réversible, qualifié d’AIT. À l’inverse, elle peut conduire à la constitution d’un infarctus cérébral, dont la taille et les conséquences sont extrêmement variables. Il n’existe donc qu’une différence de degré entre AIT et infarctus cérébral, mais les objectifs de prise en charge sont différents :
- pour les infarctus cérébraux, l’urgence thérapeutique est extrême, car le traitement visant à recanaliser l’artère occluse (thrombolyse intraveineuse et/ou thrombectomie mécanique) n’est efficace que dans une fenêtre thérapeutique étroite, et doit être débuté le plus vite possible ;
- pour les AIT, il existe une urgence de prévention compte tenu du risque élevé de récidive précoce, potentiellement grave (5 % de récidive à 7 jours ; 30 % des infarctus cérébraux ont été précédés d’AIT). Le patient doit donc être examiné et les explorations réalisées dans les meilleurs délais pour instaurer le traitement le plus approprié.
Hémorragie cérébrale
Les hématomes intraparenchymateux (également appelés hématomes cérébraux ou AVC hémorragiques) représentent 20 % des AVC et sont liés à la rupture d’une artère intracrânienne. Il existe un risque élevé d’extension de l’hématome au cours des premières heures, qui peut être limité par une prise en charge très rapide de l’hypertension artérielle sévère.
Quels sont les signes évocateurs d’AVC ?
Il est important de préciser qu’aucun symptôme ou signe d’examen ne permet de différencier les infarctus cérébraux des hématomes de manière fiable.L’imagerie cérébrale en urgence est donc indispensable.
Le tableau clinique varie considérablement selon le sujet et selon la taille et le siège de la lésion. Le diagnostic d’AVC est parfois facile à évoquer devant un tableau clinique typique, en particulier sévère, mais il peut être plus difficile dans certains cas, notamment en cas de symptômes transitoires (AIT), du fait du caractère rétrospectif de l’anamnèse et des nombreux diagnostics différentiels. C’est principalement l’interrogatoire du patient, de son entourage ou des deux qui suggère la nature vasculaire du tableau neurologique ; il est donc très important de le mener avec exhaustivité. L’examen clinique neurologique doit être complet pour préciser la plainte du patient et rechercher des signes cliniques pour pour lesquels le patient ne ressent parfois aucune gêne.
Quatre critères pour parler d’AVC
La nature vasculaire d’un déficit neurologique est quasi certaine lorsque quatre critères cliniques sont réunis :
- une installation soudaine (d’une minute à l’autre) ;
- une intensité d’emblée maximale ;
- un caractère focal du déficit neurologique : les symptômes et les signes peuvent tous s’expliquer par une seule lésion anatomique (les principaux déficits neurologiques considérés comme focaux sont décrits ci-après) ;
- un caractère « déficitaire » des symptômes (hémiplégie, aphasie, hémianopsie, etc.), et non pas « positif » (clonies, scotome scintillant, tremblements, etc.).
L’association de ces quatre éléments cliniques est hautement évocatrice. Toutefois, certains AVC peuvent avoir une expression clinique qui ne répond pas à l’une ou l’autre de ces caractéristiques. Par exemple, peuvent parfois survenir : une aggravation des troubles sur quelques heures, des cas de fluctuations ou encore des symptômes cliniques atypiques. Dans ces circonstances, le diagnostic d’AVC est plus difficile et l’imagerie joue un rôle encore plus important.
Certains symptômes neurologiques sont compatibles avec le diagnostic d’AVC mais ne doivent pas faire retenir le diagnostic en première intention s’ils sont isolés : vertige, diplopie, dysarthrie, troubles de la déglutition, symptômes sensitifs ne touchant qu’une partie d’un membre ou qu’une hémiface. En revanche, le diagnostic d’AVC devient probable si ces signes s’associent, de façon successive ou concomitante, entre eux ou aux signes plus classiques d’AVC. En présence de symptômes douteux d’AVC, la présence de facteurs de risque vasculaires doit également être recherchée, car elle augmente la probabilité d’AVC.
Symptômes moteurs
L’atteinte de la voie motrice est à l’origine d’un déficit moteur dont la reconnaissance clinique est le plus souvent aisée. Ses caractéristiques sont variables dans leur sévérité (de la paralysie partielle, dite parésie, à complète, dite plégie) mais également dans leur topographie. Il est donc important d’explorer les trois étages de chaque hémicorps (face, membres supérieurs, membres inférieurs). L’atteinte est, dans la grande majorité des cas, unilatérale car l’atteinte cérébrale l’est également (atteinte clinique controlatérale à l’atteinte cérébrale). Il existe de rares cas d’ischémie de la moelle épinière ou du tronc cérébral se révélant par une para- ou une tétraparésie soudaine. L’asymétrie faciale est parfois visible spontanément, mais l’examen peut être sensibilisé en demandant au patient de sourire. Dans le cadre de l’urgence, l’évaluation d’un déficit moteur des membres supérieurs peut se limiter à demander au patient de maintenir les bras tendus en fermant les yeux (cette épreuve peut révéler un signe de Barré). De la même manière, la motricité des membres inférieurs est évaluée rapidement en mettant le patient en décubitus dorsal et en lui demandant de maintenir les jambes en l’air pendant quelques secondes (manœuvre de Mingazzini avec les cuisses à la verticale et les jambes à l’horizontale).
Symptômes sensitifs
La perte de la sensibilité d’un hémicorps est également l’un des symptômes classiques d’AVC. Cependant, les diagnostics différentiels sont fréquents en cas de trouble sensitif très localisé d’un membre ou d’une hémiface (par exemple, une compression nerveuse périphérique). La recherche de symptômes neurologiques associés permet alors de renforcer la suspicion clinique. Le patient décrit habituellement une plainte à type de paresthésies (fourmillements) ou d’anesthésie. L’examen clinique en urgence doit rechercher une hypoesthésie à la douleur (piqûre par exemple) ou au tact.
Troubles du langage
Si l’apparition d’un mutisme (incapacité totale à s’exprimer), très impressionnante, pousse les patients et leurs proches à donner l’alerte, les troubles du langage sont parfois plus discrets et sont souvent banalisés, à tort. Le patient peut se plaindre de difficultés à articuler, à trouver ses mots, d’utiliser un mot pour un autre (paraphasie) ou encore de difficultés de compréhension.
Troubles visuels
Les troubles visuels révélateurs d’un AVC sont multiples, les plus évocateurs étant une cécité monoculaire (transitoire ou non) à type de rideau noir ou d’amputation du champ visuel monoculaire lié à l’occlusion de l’artère ophtalmique ou de l’une de ses branches, et une hémianopsie latérale homonyme liée à une lésion occipitale. La cécité corticale est également possible – liée à des lésions occipitales bilatérales – mais très rare. L’examinateur doit préciser la nature des troubles en examinant le champ visuel au doigt de chaque œil (cacher un œil puis l’autre). La survenue d’une diplopie binoculaire (vision double, uniquement lorsque les deux yeux sont ouverts) peut révéler un AVC, mais elle s’associe habituellement à d’autres symptômes neurologiques ; et il faut remettre en question le diagnostic si elle est isolée.
Troubles de l’équilibre
L’apparition soudaine de troubles de l’équilibre peut révéler un AVC, en cas de lésion de la fosse postérieure, et notamment au niveau du cervelet. Les patients décrivent alors une instabilité à la marche (sensation pseudo-ébrieuse) et parfois une sensation de vertige rotatoire avec nausées et vomissements. Il faut alors s’efforcer de rechercher d’autres symptômes neurologiques associés qui renforceraient l’hypothèse neurovasculaire et écarteraient les nombreux diagnostics différentiels, notamment ORL. L’examen clinique doit rechercher un syndrome cérébelleux dont les principaux signes sont la présence d’un élargissement du polygone de sustentation à la marche et une incoordination d’un membre ou d’un hémicorps à la manœuvre doigt-nez ou talon-genou.
Symptômes non évocateurs d’un AVC
Les symptômes non évocateurs d’AVC s’opposent à l’une ou plusieurs des règles générales exposées précédemment : apparition progressive d’un déficit neurologique, symptômes positifs (phosphènes, tremblements, etc.) ou symptômes neurologiques non focaux. Parmi les principaux symptômes cliniques non focaux peu évocateurs d’AVC, on peut citer une sensation généralisée de faiblesse motrice ou anesthésie, une lipothymie, un malaise, une perte brève de connaissance, des acouphènes, une amnésie aiguë, un syndrome confusionnel, un coma, des troubles neuropsychiatriques ou des troubles sphinctériens.
Filière AVC, un système bien rodé de prévention et de prise en charge
Le poids croissant des AVC, lié au vieillissement de la population et aux facteurs de risque de cette pathologie, justifie la mise en œuvre d’une politique globale de prévention et de prise en charge structurée afin d’en diminuer l’incidence et la gravité.
Place centrale des unités neurovasculaires
Pour répondre à cette problématique, la prise en charge de l’AVC s’est construite autour d’unités spécialisées, appelées unités neurovasculaires (UNV). Les UNV sont composées de personnel spécialisé dans la prise en charge des AVC, disponibles 24 heures sur 24 et 7 jours sur 7 : aides-soignants, infirmiers, kinésithérapeutes, orthophonistes, ergothérapeutes, neurologues, permettant de réduire la morbi-mortalité post-AVC de plus de 20 % à deux ans. Le bénéfice de la filière est observé pour tout AVC, ischémique ou hémorragique, quelle que soit la sévérité clinique initiale (de l’AIT à l’AVC grave). Son efficacité est plurifactorielle :
partiellement liée aux bénéfices des traitements de reperfusion (thrombolyse ou thrombectomie). En effet, ces traitements sont très efficaces mais ne concernent qu’une minorité des patients admis en UNV (< 10 à 15 %) ;
diminution des complications post-AVC : neurologiques (aggravation neurologique dont les mécanismes sont multiples) mais également extraneurologiques (infections pulmonaires liées aux troubles de la déglutition, escarres, complications orthorhumatologiques liées à un mauvais positionnement, pathologie thromboembolique veineuse, etc.) ;
prévention des récidives précoces, par l’introduction d’une prévention secondaire rapide et individualisée.
En France, il existe environ 140 UNV. Bien qu’ayant un rôle central, ces unités ne représentent que la partie émergée de l’iceberg : la filière s’est ensuite organisée en amont et en aval pour accompagner le patient du début à la fin de sa maladie, et le médecin généraliste y occupe une place importante.
Une prise en charge de A à Z
La filière AVC repose sur quatre principes fondateurs :
- la prévention est efficace. La récidive d’AVC peut être évitée grâce à une prise en charge adaptée ;
- il existe des traitements de phase aiguë efficaces pour limiter les séquelles causées par l’AVC, à condition d’être administrés de manière très précoce ;
- l’UNV, avec son personnel spécifiquement formé et dédié, permet une diminution de la dépendance et la mortalité de plus de 20 % à deux ans ;
- la rééducation a un impact favorable sur la réautonomisation à distance de l’AVC et sur la qualité de vie.
Phase préhospitalière
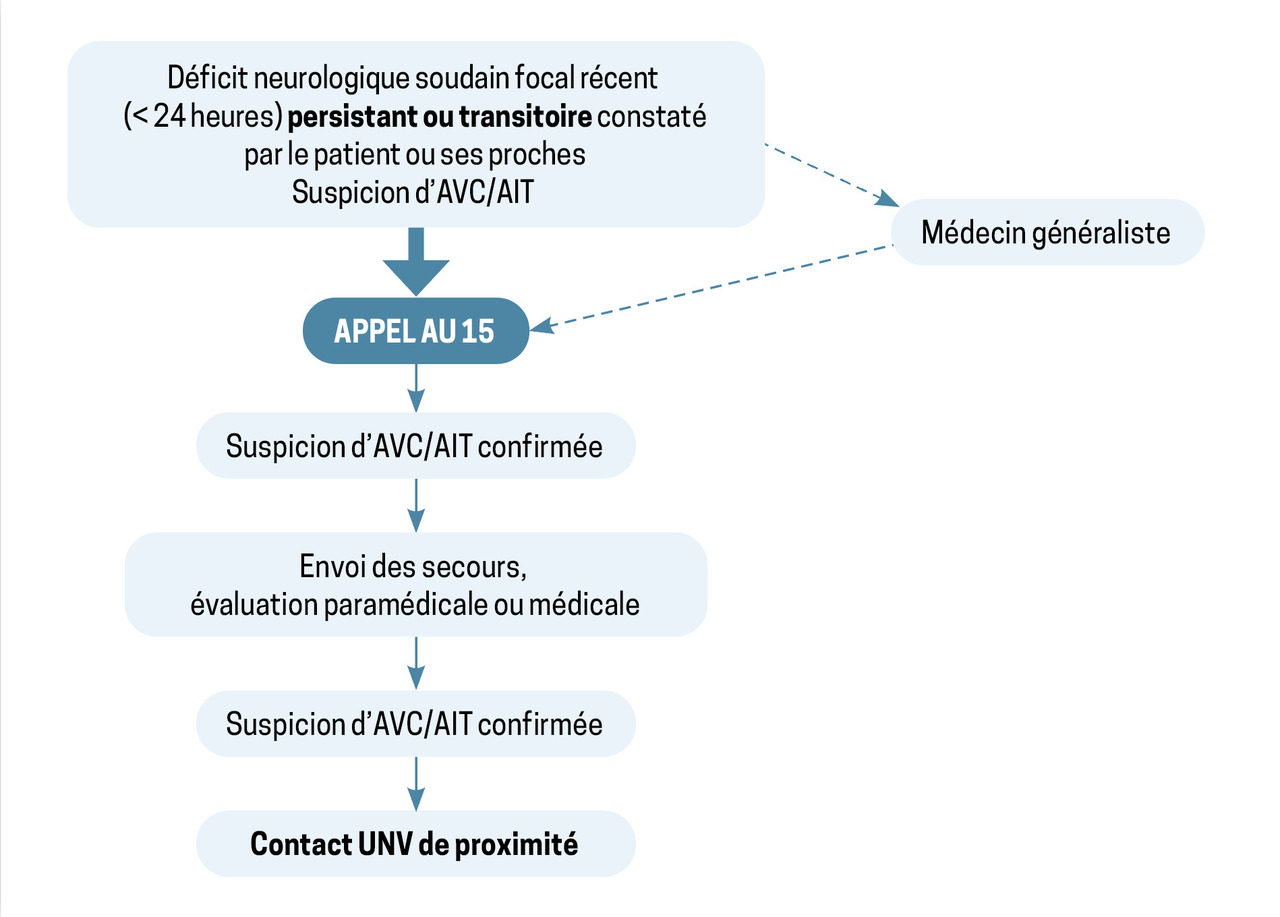
L’entrée dans la filière AVC doit se faire le plus tôt possible. L’identification de signes évocateurs d’AVC par le patient ou son entourage, améliorée par les différentes campagnes de prévention et la sensibilisation régulière des professionnels de santé, doit déboucher sur un appel au centre 15, qui déclenche alors l’intervention des premiers secours (fig. 1).
L’éducation des patients est essentielle et le médecin généraliste y joue un rôle majeur. Actuellement, les patients attendent trop longtemps avant d’appeler le 15 (« pour voir si les troubles régressent spontanément ») ou n’osent pas appeler en cas de symptômes modérés ou régressifs. Beaucoup se présentent directement chez leur médecin généraliste ou aux urgences de l’hôpital de proximité (qui ne dispose pas forcément d’une UNV), occasionnant un retard préjudiciable à la prise en charge.
La régulation préhospitalière varie d’une région à l’autre, mais ne nécessite pas, de manière obligatoire, une présence médicale. L’objectif premier étant la rapidité, certaines régions ont démédicalisé le transport de phase aiguë de l’AVC. Une fois l’évaluation médicale ou paramédicale faite sur place, les premiers secours entrent en contact téléphonique avec l’UNV la plus proche, pour discuter de l’orientation la plus adaptée du patient en fonction de son histoire clinique et des signes constatés.
Phase UNV
En cas de suspicion d’AVC, le patient est pris en charge directement en UNV, sans passer par les urgences générales. Il est évalué en urgence par le personnel de l’UNV, incluant un neurologue et l’équipe paramédicale, qui se charge de faire l’interrogatoire du patient et/ou de sa famille, un examen clinique neurologique rapide (calcul du score NIHSS ; tableau) permettant d’évaluer la sévérité du déficit neurologique, une surveillance des signes vitaux (pression artérielle, température, glycémie, fréquence cardiaque, saturation en oxygène) et un bilan sanguin. Une imagerie cérébrale est ensuite réalisée en urgence. En France, il s’agit le plus souvent d’une IRM avec angiographie par résonance magnétique (durée : dix minutes), mais la réalisation d’un scanner avec angioscanner est une alternative tout à fait valide pour une prise en charge adaptée. Au terme de cette évaluation clinico-radiologique urgente, la décision de traitement de reperfusion est prise (thrombolyse intraveineuse et/ou thrombectomie mécanique). L’objectif – tout à fait atteignable si la filière intrahospitalière est bien organisée – est de débuter la thrombolyse intraveineuse moins de trente minutes après l’arrivée du patient à l’hôpital.
Les autres objectifs de la prise en charge en UNV sont la prévention des complications et la réalisation d’un bilan étiologique complet afin d’identifier la cause probable de l’AVC et d’introduire rapidement le traitement de prévention secondaire adapté à chaque patient. Enfin viennent l’évaluation des besoins en rééducation et l’orientation rapide vers un service adapté aux besoins du patient.
Phase de rééducation post-UNV
Au décours du séjour en UNV, le patient nécessite fréquemment une prise en charge en rééducation, même en cas de déficit d’apparence minime, car le retentissement sur le quotidien peut être majeur.
Il existe désormais de nombreuses modalités de rééducation. Pour citer les plus utilisées :
- les soins médicaux et de réadaptation neurologique (SMR neurologique, ex-SSR neurologique) en séjour complet pour les patients avec un déficit neurologique nécessitant une prise en charge pluridisciplinaire intensive et prolongée ;
- l’hospitalisation de jour de rééducation, se déroulant en centre de rééducation, habituellement dans les mêmes services que les SMR neurologiques, permet une prise en charge pluridisciplinaire et intensive mais autorise le patient à retourner plus précocement au domicile ;
- l’hospitalisation à domicile de rééducation (HADR) permet une rééducation en situation écologique, ainsi que l’adaptation du domicile aux besoins du patient ;
- les équipes mobiles de rééducation, intervenant directement au domicile, évaluent les besoins du patient en rééducation et pour adaptation du domicile ;
- la kinésithérapie ou l’orthophonie en libéral dont la mise en place est désormais facilitée par le dispositif PRADO d’accompagnement au domicile à la sortie de l’hôpital.
Suivi post-AVC
Un dispositif de consultation pluriprofessionnelle post-AVC a été mis en place par les agences régionales de santé (ARS) dans chaque UNV, faisant intervenir infirmière spécialisée, neurologue, gériatre, ergothérapeute, orthophoniste, kinésithérapeute, neuropsychologue, en fonction des besoins du patient. Cette évaluation pluri-professionnelle a un double objectif :
- éviter la récidive en vérifiant qu’un bilan étiologique complet a été réalisé, que le traitement de prévention secondaire est adapté à la cause de l’AVC et que le contrôle des facteurs de risque vasculaires est optimal ;
- évaluer les séquelles neurologiques (y compris « cachées ») pour adapter la prise en charge rééducative et le mode de vie dans le but d’optimiser l’autonomie et la qualité de vie.
Les ARS recommandent que chaque patient soit revu une fois en consultation pluriprofessionnelle dans l’année suivant son AVC. Si le patient n’est pas entré dans la filière AVC en phase aiguë (ce qui est malheureusement fréquent, soit par erreur d’orientation, soit faute de place en UNV), il est important de le réadresser vers la consultation pluriprofessionnelle post-AVC en contactant l’UNV la plus proche de son lieu de vie.
Le risque de récidive d’AVC, bien que maximal lors des premiers jours, persiste au long cours. Un suivi médical prolongé est ainsi indispensable, avec notamment une prise en charge optimale des facteurs de risque vasculaire. Ce suivi est réalisé par le médecin généraliste, en coordination avec un neurologue vasculaire.
Traitements de reperfusion en phase aiguë : essor de deux techniques
La thrombolyse intraveineuse et la thrombectomie mécanique sont les deux traitements de reperfusion efficaces en phase aiguë des AVC ischémiques, avec des évolutions rapides des indications ces dernières années.
Cas de la thrombolyse intraveineuse
Plusieurs essais randomisés datant d’une vingtaine d’années ont démontré que la thrombolyse par voie intraveineuse par altéplase, administrée dans les quatre heures trente suivant le début des symptômes, permet d’améliorer le pronostic fonctionnel à trois mois. Ce traitement pharmacologique permet l’activation du plasminogène en plasmine, une enzyme protéolytique très puissante capable de dégrader la fibrine contenue dans le thrombus intracrânien responsable de l’ischémie cérébrale aiguë. L’altéplase a pour avantage d’être largement et rapidement disponible, pouvant être administrée dans toutes les UNV mais également dans certains services d’urgence dotés de télémédecine ou de personnel formé. Le bénéfice du traitement se réduit au cours du temps (« time is brain »), car la zone de tissu cérébral hypoperfusé mais pas encore infarci (la zone de pénombre, que l’on souhaite sauver via la recanalisation artérielle rapide) diminue au fil du temps, même s’il existe une grande variabilité interindividuelle. Le bénéfice absolu de la thrombolyse versus placebo pour obtenir une excellente évolution clinique à trois mois est de 12 % si elle est administrée dans les trois premières heures, et de 5 % entre quatre heures trente et six heures. Malheureusement, plusieurs contre-indications empêchent sa plus large utilisation, et elle expose à un risque d’hémorragie cérébrale symptomatique. Néanmoins, le rapport bénéfice/risque de la thrombolyse intraveineuse reste très en faveur de ses bénéfices.
Plusieurs actualités sont à signaler concernant les indications de thrombolyse intraveineuse :
- celle-ci est désormais recommandée en cas d’heure inconnue de début des symptômes (notamment les AVC découverts le matin au réveil : près de 30 % des patients), sous condition de critères d’imagerie particuliers : la présence d’un « mismatch » entre la séquence de diffusion et la séquence FLAIR en IRM (témoignant d’un AVC survenu il y a moins de 4 heures 30) ou la présence d’une zone de pénombre significative sur une imagerie de perfusion en scanner ou IRM ;
- elle est également recommandée entre quatre heures trente et neuf heures après l’installation des troubles, à condition qu’une imagerie de perfusion (scanner ou IRM) mette en évidence une zone de pénombre significative. En effet, il existe une grande variabilité interindividuelle de vitesse de progression de l’infarctus cérébral : certains patients conservent une zone de pénombre longtemps après la survenue de l’occlusion artérielle – gardant ainsi un bénéfice tardif de la recanalisation artérielle – et d’autres non ;
- la ténectéplase, un autre agent thrombolytique beaucoup plus simple d’administration que l’altéplase (bolus de 10 secondes versus perfusion continue sur une heure pour l’altéplase), a récemment montré un rapport bénéfice/risque équivalent à l’altéplase et le remplacera donc à l’avenir ;
- plusieurs études internationales ont montré le bénéfice d’une prise en charge en « UNV mobile », des ambulances spécialisées équipées d’un médecin, d’un scanner et d’un laboratoire d’analyses biologiques : ce type de prise en charge permet d’augmenter le taux de thrombolyse intraveineuse (via une prise en charge très précoce) et de réduire le handicap fonctionnel. Une telle prise en charge est désormais disponible en routine dans certains pays ; une première étude a récemment débuté en France.
Thrombectomie mécanique
La thrombectomie mécanique consiste à extraire le thrombus intracrânien par voie endovasculaire, en utilisant divers types de dispositifs. Cette intervention est le plus souvent réalisée sous anesthésie locale, avec une sédation légère. Elle est indiquée en complément de la thrombolyse intraveineuse (si indiquée) mais également en cas de contre-indication à celle-ci. La thrombectomie a fait preuve de sa nette supériorité en matière de recanalisation (obtenue dans 85 % des cas) et de pronostic fonctionnel, en comparaison au traitement médical seul (incluant la thrombolyse intraveineuse si indiquée), sans sur-risque de complication hémorragique. Cependant, son efficacité n’est démontrée qu’en cas d’occlusion artérielle proximale, représentant une minorité des patients évalués à la phase aiguë d’un AVC (environ 30 %, généralement les plus sévères).
Des études évaluant son efficacité en cas d’occlusion de moyen calibre sont en cours. Malheureusement, la thrombectomie ne peut être réalisée rapidement que chez une minorité de patients, car seules 35 % des UNV disposent du personnel et du plateau technique adapté, ce qui limite son efficacité, qui est – comme pour la thrombolyse – dépendante du temps.
La plupart des patients sont donc initialement admis dans une UNV sans thrombectomie, où le diagnostic d’AVC ischémique avec occlusion artérielle proximale est posé, la thrombolyse intraveineuse débutée, puis le patient transféré vers un centre de thrombectomie. L’ouverture de nouveaux centres de thrombectomie se fait progressivement sur le territoire.
Les indications de thrombectomie mécanique s’élargissent rapidement, depuis les premières preuves de son efficacité en 2015. Elle est actuellement recommandée chez une majorité de patients avec occlusion artérielle proximale admis dans les six premières heures suivant l’apparition des symptômes, quels que soient l’âge et la taille de l’infarctus cérébral, sous réserve de l’absence de handicap sévère préalable à l’AVC.
Plus récemment, des études ont prouvé son bénéfice jusqu’à vingt-quatre heures après l’apparition des symptômes, sous certaines conditions d’imagerie (persistance d’une zone de pénombre significative sur une imagerie de perfusion en scanner ou IRM).
Médecin généraliste, pilier à tous les stades de la prise en charge
Le médecin généraliste joue un rôle important dans la prise en charge des AVC. Il est en première ligne dans l’éducation des patients et de leur famille pour la reconnaissance des signes évocateurs et pour la conduite à tenir en cas d’urgence. Cette information doit être répétée régulièrement, notamment aux patients ayant un risque cardiovasculaire élevé.
Par ailleurs, son rôle est central pour la réorientation des patients qui ne sont pas entrés dans la filière AVC à la phase aiguë, quelle qu’en soit la raison. Ces patients peuvent bénéficier d’une évaluation pluridisciplinaire post-AVC dans l’UNV de leur secteur pour adapter la prise en charge et compléter le bilan étiologique si nécessaire.
Enfin, le médecin généraliste reste le garant d’une prise en charge coordonnée dans le suivi au long cours post-AVC.
Que dire à vos patients ?
L’accident vasculaire cérébral se manifeste soudainement par :
- une déformation de la bouche (par exemple, lorsque la personne sourit, le sourire n’est pas symétrique) ;
- une faiblesse d’un côté du corps, bras ou jambe (par exemple, lorsqu’on demande à la personne de lever les deux bras devant elle, l’un des bras ne peut être levé ou ne peut rester en hauteur, il retombe) ;
- des troubles de la parole (par exemple, lorsqu’on demande à la personne de répéter une phrase, elle rencontre des difficultés à parler ou à comprendre).
Si vous êtes témoin de l’un de ces trois signes, réagissez ! Appelez immédiatement le SAMU, faites le 15.
Quelle prise en charge des AIT ?
L’AIT est une urgence thérapeutique (5 % de récidive à 7 jours, 10 % à 3 mois). Les traitements de prévention des récidives sont efficaces, à condition d’être introduits rapidement (moins de 24 à 48 heures).
L’entrée dans la filière AVC suit donc les mêmes règles que celles décrites dans l’article (appel au 15). Si le patient consulte directement le médecin généraliste, ce dernier doit contacter l’UNV du secteur.
En UNV, une évaluation clinico-radiologique rapide est réalisée (le patient ne reste, le plus souvent, que quelques heures ; il n’y a pas d’hospitalisation) : bilans cliniques médical et paramédical, bilan biologique, électrocardiogramme, IRM cérébrale et bilans artériels cérébral et cervical, prescription du traitement de prévention adapté, organisation du suivi.

 Encadrés
Encadrés