Repérer, diagnostiquer, évaluer le retentissement d’une addiction au tabac.
Indications et principes du sevrage thérapeutique. Argumenter l’attitude thérapeutique et planifier le suivi du patient.
Données épidémiologiques
Dans le monde
Le tabagisme a entraîné 100 millions de décès au XXe siècle, et l’épidémie mondiale, liée au savoir-faire de l’industrie cigarettière, continue de se propager, ciblant dorénavant les pays en voie de développement, et, en Occident depuis quelques décennies, de nouvelles populations comme les femmes et les adolescents.
Le taux de mortalité standardisé sur l’âge (TMSA) à l’échelle mondiale concernant le cancer du poumon chez la femme devrait s’accroître de 43 % de 2015 à 2030 selon une analyse de données provenant de 52 pays. L’Europe et l’Océanie devraient connaître les taux de mortalité par cancer du poumon chez la femme les plus élevés d’ici 2030.
En France
Après une baisse entre 2000 et 2005, puis une hausse entre 2005 et 2010, le tabagisme des Français s’est stabilisé jusqu’en 2010, pour les hommes comme pour les femmes.
Les données du Baromètre santé 2017 de Santé publique France dénombrent 1 million de fumeurs en moins en 2017 par rapport à 2016. La prévalence du tabagisme quotidien est passée de 29,4 % en 2016 à 26,9 % en 2017.
On recense en France 78 000 décès annuels imputables au tabac. C’est la drogue qui tue le plus en France, loin devant l’alcool (49 000 décès/an). Actuellement, 12,2 millions de Français fument au lieu de 13,2 millions en 2016.
Un fumeur sur deux mourra des complications de son tabagisme.
Femmes et tabac
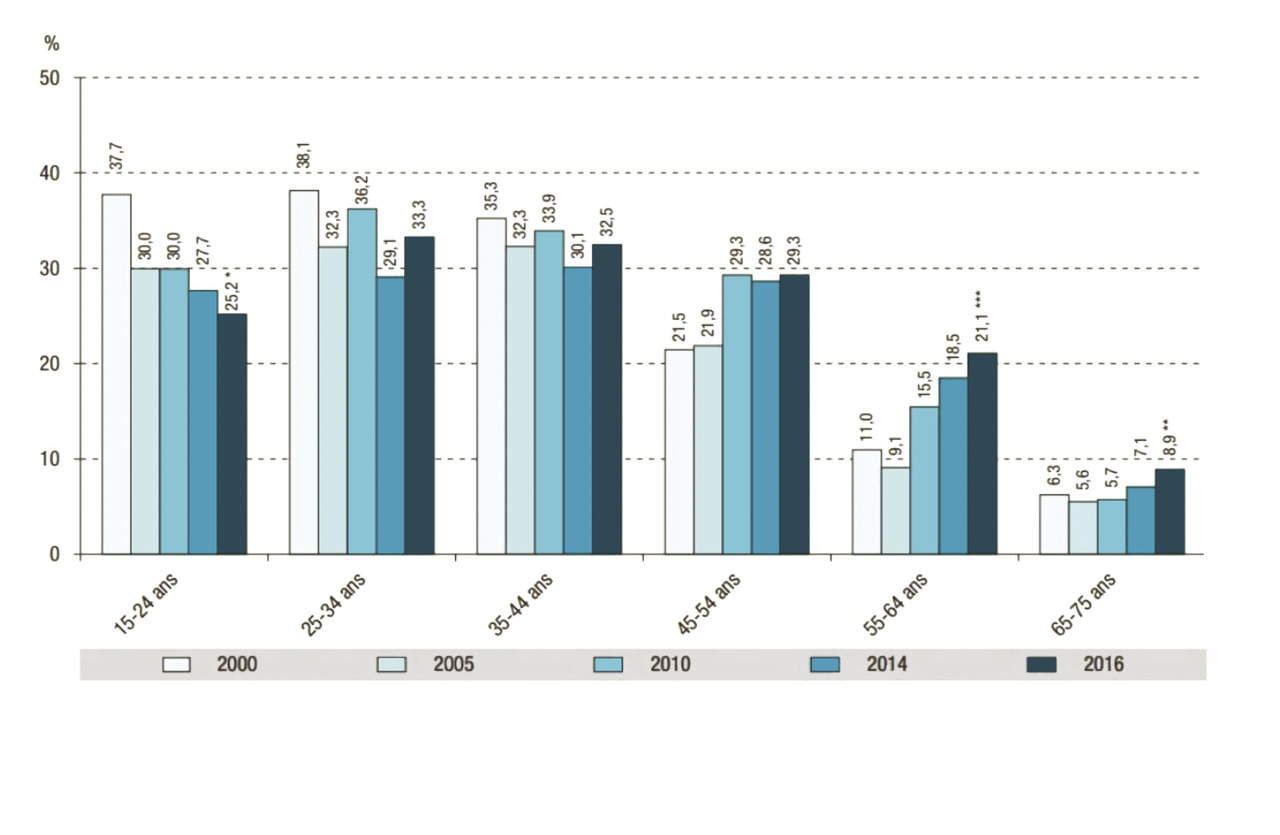
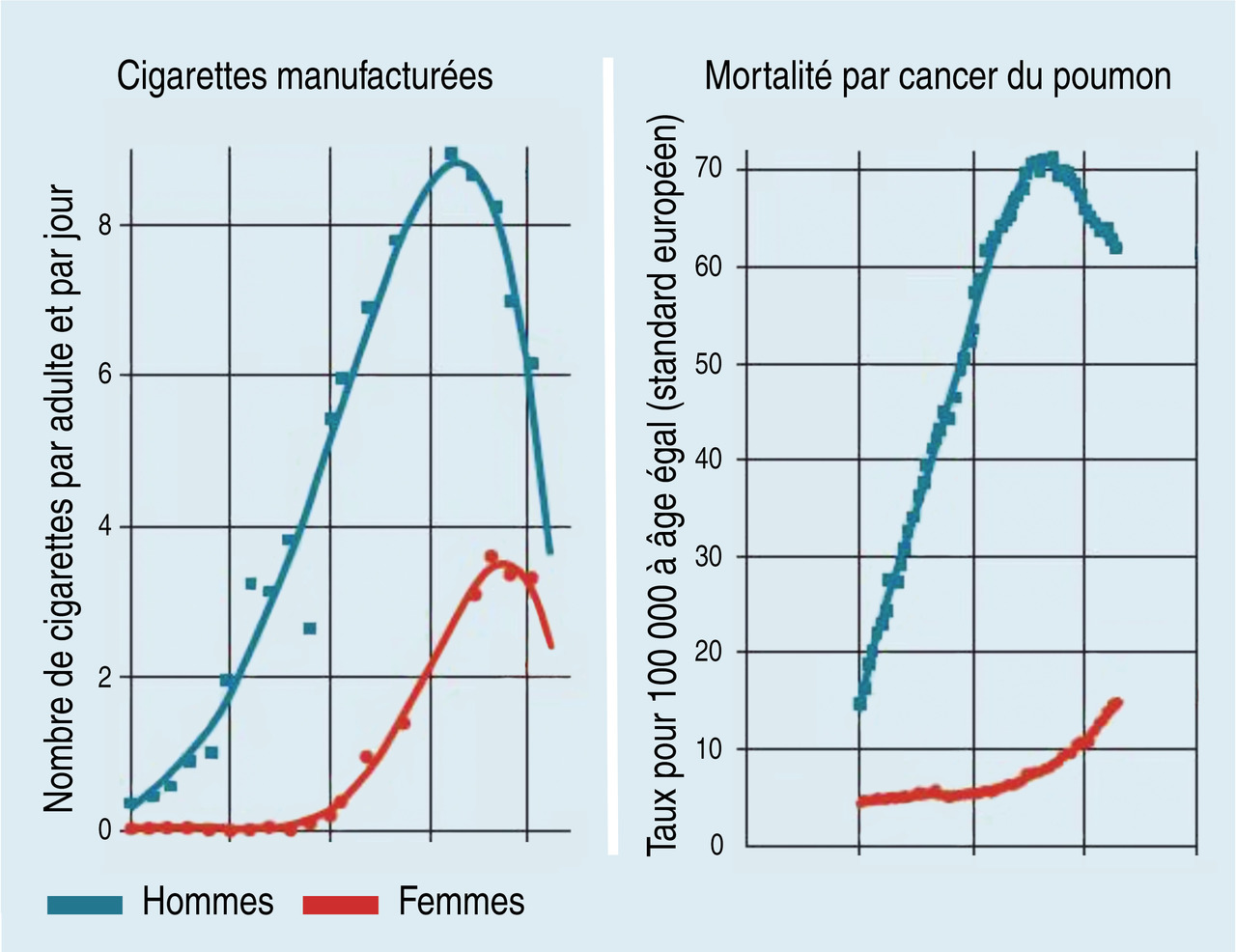
En 2016, 31 % des femmes se déclaraient fumeuses, contre 38 % des hommes. On observe une augmentation du tabagisme chez les femmes âgées de plus de 55 ans (fig. 1).L’augmentation de la consommation féminine, corollaire de l’émancipation, a provoqué une augmentation du cancer bronchique féminin qui s’est multiplié par 4 en 15 ans, avec des prévisions très sombres pour les années à venir (fig. 2). Actuellement, l’incidence du taux de mortalité par cancer bronchique est supérieure chez la femme à celle de la mortalité par cancer du sein.
Précarité et tabac
L’effet-crise a entraîné dans un premier temps une augmentation de la consommation chez les plus démunis, pratiquement un chômeur sur deux étant fumeur (44 % à 50 %). Pour les personnes défavorisées, le tabac constituerait une priorité, une forme « d’anxiolytique du pauvre », et un « loisir ». Le Baromètre santé 2017 met en évidence pour la première fois depuis le début des années 2000 l’arrêt de la croissance des inégalités sociales en matière de tabagisme. Le tabagisme quotidien est passé de 39 % en 2016 à 34 % en 2017 parmi les fumeurs les plus défavorisés.Adolescents et tabac : enquête ESCAPAD 2017
En 2017, 6 adolescents de 17 ans sur 10 (59,0 %) ont déclaré avoir déjà fumé au moins une cigarette au cours de leur vie. Ce niveau est en nette baisse par rapport à 2014 et largement en deçà de celui mesuré au début des années 2000 (77,6 %). De même, le tabagisme quotidien se révèle en très nette diminution, avec 1 jeune adolescent sur 4 (25,1 %) concerné. Malgré cette baisse bénéfique, les adolescents restent fréquemment exposés à la fumée de tabac, et les produits du tabac leur demeurent encore trop largement accessibles au regard de la loi (interdiction de vente aux mineurs). La prévention primaire est une priorité car plus le début de la consommation est précoce (11-15 ans), plus le risque de dépendance est élevé.Addictions et société
Le monde actuel, de plus en plus addictogène, incite à toutes les consommations et à la recherche du plaisir individuel, ne facilitant pas l’apprentissage du contrôle des pulsions.La législation et ses effets
Depuis les lois Veil (1976) et Évin (1991), la France consolide sa politique de santé publique en renforçant la législation. L’image sociale du tabac en a été fortement modifiée, voire dénormalisée. Depuis fin 1999, les substituts nicotiniques sont en vente libre et disponibles dans les hôpitaux. L’interdiction de fumer dans les lieux publics et de convivialité (décret Bertrand, novembre 2006) a également constitué une étape symbolique dans la lutte contre le tabagisme. Récemment, le ministère de la Santé a proposé un forfait de 150 €/an depuis fin 2016 pour les moyens de sevrage tabagique. Courant 2018, les substituts nicotiniques sont pris en charge à 65 % par la Sécurité sociale avec une extension à toutes les marques, et la varénicline est remboursée. Depuis le 1er janvier 2019, le forfait 2019 a disparu et tous les moyens de sevrage, dont les substituts, sont pris en charge au tiers payant. La ministre de la Santé Agnès Buzyn souhaite un prix du paquet de cigarettes à 10 € en 2020. Ces différentes mesures constituent le Programme national de réduction du tabagisme (PNRT) 2014-2019 dont l’objectif est de passer en dessous de 20 % de tabagisme quotidien d’ici 2024 et de parvenir à la première « génération d’adultes sans tabac » d’ici 2032. Trois axes ont été retenus : protéger les jeunes, aider les fumeurs à s’arrêter et agir sur l’économie du tabac.Composition de la fumée du tabac
Composants
- la nicotine, agent de dépendance, dont le caractère naturellement très addictogène est renforcé par certains additifs, comme l’ammoniac. Lors de l’inhalation de tabac, la nicotine parvient au cerveau en 8 secondes. C’est le « shoot nicotinique », qui est 2 fois plus rapide qu’une intraveineuse. Il y a alors activation du circuit de la récompense dans le mésencéphale et libération de dopamine. Outre son action majeure dans l’addiction, la nicotine est vasoconstrictrice, mais ses effets sympathomimétiques ne concernent pas les substituts nicotiniques (absence de shoot) ;
- le monoxyde de carbone (CO), mesuré par les tabacologues à l’aide d’un analyseur de l’air expiré, est responsable de l’hypoxie à cause de sa très forte affinité pour l’hémoglobine (200 fois plus que l’oxygène). Le produit formé est la carboxyhémoglobine. Le monoxyde de carbone est fortement pathogène en raison de l’hypoxie tissulaire et de l’athérogenèse. Il existe une corrélation entre sa valeur expirée, exprimée en particules par million (ppm) et l’inhalation de la fumée. Sa demi-vie est courte, de 2 heures à 6 heures ;
- les goudrons (250 mL inhalés par an pour un paquet journalier) dont des hydrocarbures comme le benzopyrène, sont principalement responsables des cancers. Il y a une cinquantaine d’autres agents cancérigènes.
La quantité de tabac auto-administrée est très variable en fonction de la manière dont la cigarette est fumée (intérêt de la mesure du CO expiré permettant de chiffrer la force de l’inhalation).
Les 3 courants de la fumée et le tabagisme passif
Le courant secondaire est très toxique : par rapport au courant primaire, il contient 3 à 10 fois plus de CO, 4 fois plus de nicotine, et 4 fois plus de benzopyrène (cancérigène). Au-delà de la gêne occasionnée, c’est ce courant secondaire qui crée le tabagisme passif et ses complications, notamment chez l’enfant, sans oublier quelques milliers de décès annuels en France.
Tabagisme passif
Chez l’enfant, il entraîne des risques de retard de croissance intra-utérine ou un petit poids de naissance si la mère non fumeuse est victime du tabagisme passif, un risque de mort subite du nourrisson (risque doublé) si un des parents fume.
Chez l’enfant plus grand, on observe des infections respiratoires basses ou des otites récidivantes.
Chez l’adulte, il augmente le risque de cancer bronchique, de maladies cardiovasculaires (les accidents cardiovasculaires concernant 4 sur 5 des victimes du tabagisme passif), aggrave l’asthme et la bronchopneumopathie chronique obstructive (BPCO)…
Physiopathologie
Complications somatiques
Cancers
Le tabagisme actif est responsable de 20 % des cancers en France. Près de la moitié des nouveaux cas de cancers liés au tabac sont des cancers du poumon, la part attribuable au tabagisme actif s’élevant à 81 % (88 % pour les hommes et 63 % pour les femmes). Le tabac est également responsable de cancers de la sphère aéro-digestive (cavité buccale, pharynx, larynx, œsophage), l’alcool agissant en synergie avec le tabac, et urologique (vessie et reins). Le tabac est aussi impliqué dans la genèse de nombreux autres cancers : pancréas, col de l’utérus et certaines leucémies.Maladies cardiovasculaires
On recense en France 22 000 décès cardiovasculaires chez des fumeurs, le nombre total de décès annuels par cause vasculaire étant de 180 000. Avant 45 ans, 80 % des victimes d’infarctus sont des fumeurs. Il existe un risque accru d’infarctus du myocarde chez la femme fumeuse sous contraceptifs oraux.Au niveau cérébral, le tabac est un facteur de risque d’accident vasculaire cérébral aussi important que l’hypertension artérielle, avec un risque multiplié de 2,5 à 6 selon le tabagisme. Le tabac est responsable de 90 % des artérites avant 65 ans.
Le tabac interagit dans de nombreuses autres pathologies : insuffisance cardiaque, hypertension artérielle, anévrismes…
Tabac et appareil respiratoire
La bronchopneumopathie chronique obstructive constitue la troisième cause de décès en France (17 000/an). Elle touche 3,5 millions de personnes, dont deux tiers l’ignorent.Le tabac favorise les exacerbations et constitue un facteur de mauvais contrôle de l’asthme.
Autres complications somatiques
Le tabac est à l’origine de nombreuses autres complications : impuissance sexuelle, diminution de la fertilité, pathologies ORL, métaboliques (lipides), thyroïdiennes, parodontopathies, ainsi que d’une augmentation du risque opératoire.Complications thymiques
Les liens entre le tabac et les maladies psychiatriques sont intriqués de façon complexe.Une relation bidirectionnelle est démontrée entre tabagisme et dépression. La dépression conduit au tabagisme mais fumer déprime au long cours.
L’anxiété est fréquente chez les fumeurs. Les ex-fumeurs sont plus sereins, car le tabac est un excitant (ce qui calme est de soulager le manque).
En cas de schizophrénie ou trouble bipolaire, le sevrage est complexe.
Prise en charge du fumeur
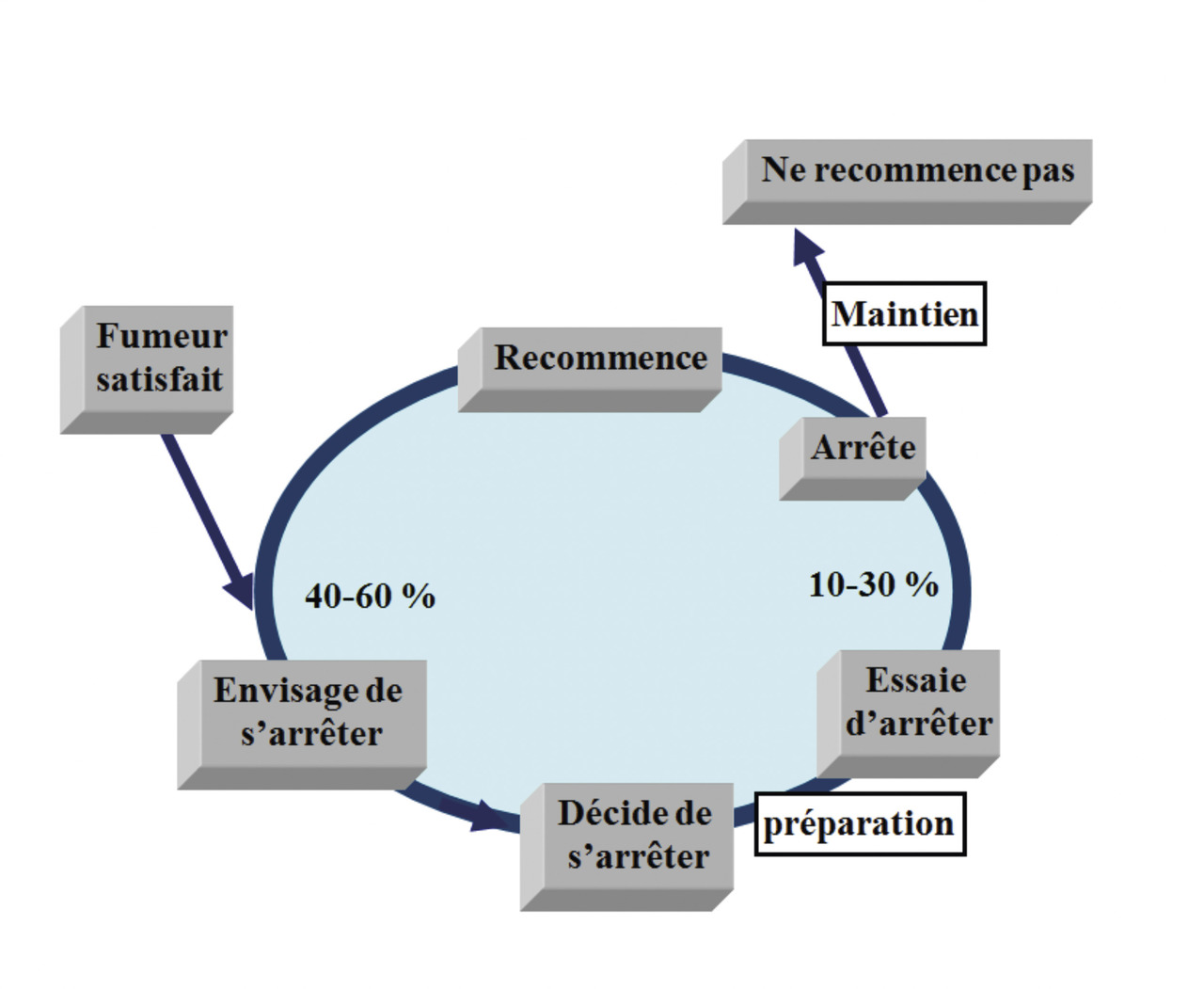
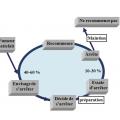
Cycle du fumeur
Le premier stade est celui du fumeur dit « en lune de miel » ou heureux. Il n’a aucune envie d’arrêter. « Où est le problème ? » : le déni, plus ou moins conscient, est fort.
Ensuite, le fumeur est ambivalent, indécis, c’est le stade de la dissonance. « Il voudrait bien mais… »
Puis le fumeur prend la décision de l’arrêt.
Vient alors le stade de la préparation avec l’anticipation de la stratégie, les petits changements.
Au stade de l’action, le fumeur est dans l’arrêt.
Enfin, le maintien chez cet ex-fumeur, ou la reprise, qui est la règle (rechutes fréquentes), qui ne ramènera jamais le fumeur à la lune de miel.
Prérequis indispensables
Comment évaluer la consommation ?
Classiquement, la consommation du tabac était jusque-là mesurée de manière consensuelle en « paquets-années » (P/A). La quantité en P/A est le nombre de paquets consommés par jour multiplié par le nombre d’années pendant lesquelles la personne a fumé cette quantité : 10 P/A peuvent correspondre soit à 20 cigarettes par jour pendant 10 ans ou 10 cigarettes par jour pendant 20 ans.Bien qu’il soit admis par tous en pratique clinique quotidienne que le nombre de P/A est corrélé à la sévérité de la BPCO, par exemple, on sait actuellement que la durée du tabagisme est plus fidèlement corrélée à l’importance de l’obstruction bronchique.
En matière de cancers, la quantité de tabac augmente le risque de développer un cancer avec un facteur à la puissance 2, alors que la durée de l’exposition le multiplie avec un facteur à la puissance 4.
Il est important d’évaluer :
- l’âge de début du tabagisme ;
- les tentatives d’arrêt et ou de réduction du tabagisme, en profitant d’interroger le patient sur les bénéfices ressentis pendant ces arrêts et les conditions de la reprise ;
- le mode de consommation : cigarettes manufacturées, roulées, consommation de cigarillos, de cannabis (fig. 4).
Comment évaluer la dépendance ?
La dépendance du fumeur est une résultante, variable, de trois éléments.Dépendance physique : le test de Fagerström évalue la dépendance pharmacologique à la nicotine. Il peut être réalisé de manière simplifiée en deux questions avec la recherche de la consommation et le délai réveil-première cigarette. On obtient alors un score sur 6.
Dépendance comportementale : le fumeur consomme de façon rituelle, avec habitudes et réflexes conditionnés : café, alcool, fin des repas, convivialité, entrée dans la voiture, téléphone, etc. C’est une participation automatique à son addiction.
Dépendance psychique : le fumeur gère ses émotions grâce au tabac. C’est un mécanisme de défense, généralement mis en place à l’adolescence, qui peut manquer au fumeur lors du sevrage. Le fumeur devra faire l’apprentissage des émotions sans le tabac.
Il est important d’identifier les signes de sevrage et de craving.
Le syndrome de sevrage, survenant dès l’arrêt du tabac, constitue le facteur de rechute principal, consécutif au manque de nicotine. Tous les signes ne sont pas présents selon les fumeurs. Il se traduit par différents symptômes : troubles de l’humeur, insomnie, irritabilité, frustration, colère, anxiété, difficultés de concentration, fébrilité, augmentation de l’appétit et/ou prise de poids.
Le craving est la pulsion à consommer du tabac, c’est le reflet de la dépendance psychologique et comportementale.
Comment donner le conseil d’arrêt ?
Pour le soignant, la règle est de toujours solliciter le fumeur à parler de son comportement.Le conseil d’arrêt (HAS) a supplanté le conseil minimal qui consistait à demander au fumeur : « Fumez-vous ? », puis : « Voulez-vous arrêter de fumer ? » en donnant un document sur le tabac si la réponse est positive.
Le conseil d’arrêt consiste pour un professionnel de santé à indiquer à un fumeur qu’il est bénéfique pour sa santé d’arrêter de fumer. Le conseil d’arrêt s’adresse à tous les fumeurs, qu’ils soient prêts ou non à arrêter de fumer (HAS).
Comment évaluer la motivation à l’arrêt ?
La motivation est indispensable à la réussite, en gardant à l’esprit que le confort pharmacologique de la substitution est fondamental.L’abord du fumeur est différent des soins traditionnels. Le soignant ne prescrit pas l’arrêt du tabac : son rôle est plus subtil, associant le fait de le guider dans un parcours dont seul le fumeur a les clés. On ne doit plus se contenter de l’étiquette fumeur ou non-fumeur, ni même du nombre de cigarettes, mais provoquer un discours, où l’« entretien motivationnel » est une aide précieuse pour le soignant, empêchant le découragement et la résistance au changement du patient.
La maladie est une raison (du côté du soignant) mais ne motive pas l’arrêt. Elle peut entraîner une peur qui fait arrêter, transitoirement, le comportement problématique, mais ne suffit pas le plus souvent à construire une motivation au changement solide et durable. Admettre que le patient fumeur a des bénéfices à fumer est très important, de même qu’admettre que changer prend du temps. L’aider à comprendre et résoudre ses freins au changement, questionner son ambivalence font partie des missions du soignant.
L’entretien motivationnel est une approche relationnelle centrée sur le patient, un état d’esprit visant à faire réfléchir le patient grâce à une attitude empathique excluant tout jugement dans un esprit positif, serein et décontracté en faisant alliance avec le patient.
Les outils utilisés pour cette approche comportent écoute active avec reformulations, questions ouvertes, valorisations, résumés.
Comment évaluer les comorbidités anxieuses et dépressives et co-addictions ?
Les fumeurs ayant des antécédents dépressifs sont plus exposés à la décompensation d’un trouble de l’humeur à l’arrêt du tabac.Les fumeurs souffrant de troubles anxieux présenteront en moyenne un syndrome de sevrage tabagique plus intense que les fumeurs sans trouble psychiatrique. Cependant, bien que le niveau d’anxiété augmente au cours des deux semaines suivant le sevrage tabagique, il diminue après un mois de sevrage à un niveau plus faible qu’avant l’arrêt du tabac.
Il est recommandé d’explorer auprès du patient sa consommation d’autres substances psycho-actives : alcool, cannabis, opiacés, cocaïne, médicaments. Il faut également rechercher des addictions comportementales.
Le sevrage tabagique en pratique
Traitement de substitution nicotinique (TSN)
C’est le traitement de première intention. Le principe est de combler l’absence de nicotine. La posologie en TSN tient également compte du score au test de Fagerström. Les patchs multiplient par 2 les chances de succès à 6 mois, et l’ajout des formes orales les multiplie par 2,5. Il n’y a pas de contre-indication aux patchs, sauf pour les mineurs de moins de 15 ans et l’allaitement. Il faut utiliser des patchs sur 16 heures chez la femme enceinte. Il est établi depuis 2003 que la substitution nicotinique chez un coronarien (connu ou en post-infarctus) n’est pas risquée et doit faire appel à une posologie classique.Contrairement à certaines idées reçues, il n’y a pas de danger à fumer sous patch, et les patchs peuvent être utiles dans la réduction du tabac. Si le patient continue de fumer en étant patché, le médecin peut chercher un meilleur confort en augmentant la posologie.
Le suivi doit être rapproché pour s’assurer d’une substitution suffisante, renforcer la motivation, et s’enquérir des bénéfices au changement. La durée d’utilisation, en diminuant par paliers successifs, est de plusieurs mois (au moins 3) sans schéma fixe.
Les formes disponibles sont :
- les patchs : diffusion en continu, sur 16 heures, à 10 mg, 15 mg et 25 mg ou sur 24 heures, à 7 mg, 14 mg, et 21 mg. Il est possible d’associer plusieurs patchs ;
- les formes orales en comprimés à sucer de 1 mg, 1,5 mg, 2 mg, 2,5 mg et 4 mg, les gommes à 2 mg ou 4 mg ;
- l’inhaleur et le spray.
Varénicline (Champix) et bupropion (Zyban)
La varénicline est un agoniste partiel des récepteurs nicotiniques à l’acétylcholine (inhibiteur sélectif des récepteurs α2β4), triplant le taux d’arrêt chez les fumeurs mais nécessitant un suivi attentif. La posologie d’installation est progressive.Les effets secondaires sont : nausées, céphalées, cauchemars, insomnies, dépression et risques cardiovasculaires.
Le bupropion est un inhibiteur de la recapture des catécholamines. Il comporte un risque de dépression, de comportements suicidaires et de troubles neurologiques (vertiges et convulsions). Ce produit est un traitement de seconde intention.
Traitements annexes
Les antidépresseurs et anxiolytiques peuvent exceptionnellement être nécessaires.Les thérapies comportementales et cognitives ont pour principe d’apprendre au patient à modifier son comportement et à gérer ses pensées vis-à-vis du tabac. C’est un outil intéressant pour anticiper et prévenir les rechutes.
Le suivi diététique est important. Fumer 20 cigarettes permet de brûler environ 200 kcalories et de diminuer la sensation de faim. Pour éviter la prise de poids classique, le fumeur doit modifier son alimentation, plus salée et plus grasse que celle des non-fumeurs.
Place de la cigarette électronique
C’est un outil intéressant car il n’y a pas de combustion donc pas de dégagement de CO, et une cigarette électronique contient environ 100 substances au lieu des 4 000 du tabac en combustion.Selon le Haut Conseil de la santé publique, « elle peut être considérée comme une aide pour arrêter ou réduire la consommation de tabac, et peut s’ajouter aux traitements classiques. Elle n’est pas recommandée chez la femme enceinte ni chez le non-fumeur ».
Suivi : prévenir les rechutes
Les reprises du tabac sont très fréquentes : environ 50 % entre la fin du traitement et les neuf mois suivants. Les causes sont multiples : la démotivation, le stress, la prise de poids, les situations de convivialité, le cerveau n’oubliant pas la nicotine.Conclusion
- le premier temps permet d’évaluer et de renforcer la motivation, puis d'évaluer la dépendance ;
- la deuxième étape est la période de « sevrage proprement dite ». Cette période peut durer plusieurs mois ;
- la troisième phase consiste à prévenir et à traiter les fréquentes rechutes de tabagisme dont les causes sont multiples. Ces reprises ne doivent pas être considérées comme des échecs, mais comme une étape vers le succès final.•
Addiction au tabac
La consommation de tabac recule en France : 1 million de fumeurs en moins en 2017.
Le tabac est un excitant, un stresseur : la vision d’apaisement du fumeur en reprenant sa cigarette vient du soulagement du manque. Lui donner cet éclairage sous forme d’information motivationnelle (v. focus) peut l’aider à comprendre la mécanique de la dépendance. C’est pour cette raison que les patchs peuvent entraîner des insomnies, il faut alors les retirer au coucher.
Le changement ne se prescrit pas : il ne sert à rien de prescrire des substituts à un patient non motivé, car vouloir aller trop vite rend le patient réfractaire au changement. C’est l’abord motivationnel qui est à privilégier.
Surdosage et sous-dosage en nicotine
• Le traitement substitutif nicotinique doit être suffisamment dosé pour apporter confort et efficacité lors du sevrage. Les surdosages sont exceptionnels, il faut toutefois en expliquer les signes au patient (céphalées, tachycardie, insomnie, diarrhées, impression d’avoir trop fumé, bouche pâteuse).
• Savoir reconnaître les signes de manque en nicotine : pulsion à fumer, fringales, nervosité, irritabilité et insomnie. Il est important de se souvenir des équivalences tabac roulé versus tabac manufacturé.
Parler du tabac permet de rendre le sujet important, et toute consultation médicale doit pouvoir être l’occasion d’un conseil d’arrêt.

 Encadrés
Encadrés