L’arrivée des inhibiteurs de JAK marque une avancée dans le traitement des pathologies inflammatoires, notamment rhumatologiques : aussi efficaces que les biothérapies, ils ont l’avantage d’une prise par voie orale et d’une action plus rapide. Mais il existe des craintes sur la tolérance de ces molécules, et des précautions d’emploi viennent d’être recommandées par l’EMA.
Inhibiteurs de JAK : comment marchent-ils ?
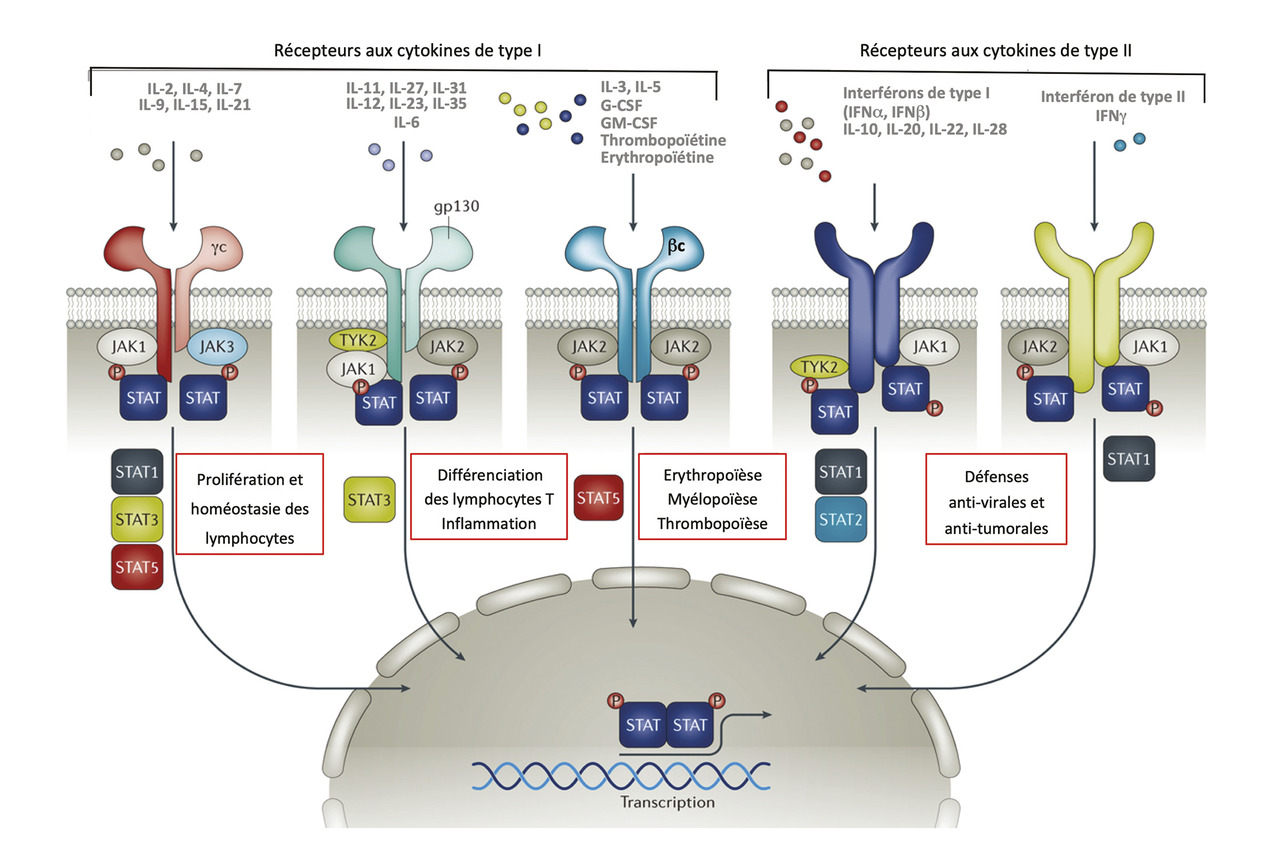
Les JAK sont un groupe de tyrosine kinases (JAK1, JAK2, JAK3 et TYK2) dont la fonction est de phosphoryler les protéines STAT. La voie de signalisation JAK-STAT (Janus kinases-Signal transducers and activators of transcription) est le point de convergence intracellulaire de nombreux signaux extracellulaires issus de cytokines dont certaines jouent un rôle déterminant dans la physiopathologie des maladies inflammatoires.
Les inhibiteurs de JAK sont des analogues de l’ATP capables d’inhiber l’action des enzymes JAK (figure). Suivant leur conformation, ces inhibiteurs sont plus ou moins sélectifs pour certaines isoformes de JAK. Par exemple, le tofacitinib – qui possède des concentrations inhibitrices médianes très proches pour JAK1 et JAK3 – est considéré comme un inhibiteur préférentiel de ces deux isoformes d’enzyme. Le baricitinib agit préférentiellement sur JAK1 et JAK2, alors que le filgotinib est un inhibiteur spécifique de JAK1 (tableau). L’intérêt d’une sélectivité étroite serait de cibler préférentiellement le groupe des cytokines pro-inflammatoires, IL-6 et IL-23 en particulier, tout en préservant les voies de signalisation des cytokines anti-inflammatoires (IL-4 et IL-10), limitant ainsi les risques d’effets indésirables. Néanmoins, cette sélectivité in vitro ne se retrouve pas si l’on étudie l’impact des différents inhibiteurs de JAK sur la production des cytokines in vivo,1 sans doute du fait de la complexité du système JAK-STAT.
À la différence des biothérapies – qui comportent une injection toutes les 2 ou 4 semaines le plus souvent – les inhibiteurs de JAK sont des substances chimiques à demi-vie courte, dont la prise se fait par voie orale quotidienne. Ce sont des traitements de fond synthétiques ciblés (tsDMARD [targeted synthetic disease-modifying antirheumatic drug]).
Quelles indications ?
Les inhibiteurs de JAK sont indiqués actuellement en rhumatologie, dans la polyarthrite rhumatoïde (PR), le rhumatisme psoriasique, la spondylarthrite ankylosante et l’arthrite juvénile idiopathique, mais aussi dans la dermatite atopique, la rectocolite hémorragique, la pelade. Le tableau ci-contre résume l’ensemble des indications actuelles des inhibiteurs de JAK commercialisés en Europe et en France.
Quelle efficacité dans la PR ?
La PR est sans aucun doute la pathologie qui a bénéficié du plus grand nombre d’études contrôlées avec des molécules de cette classe. Quatre inhibiteurs de JAK (baricitinib, tofacitinib, filgotinib, upadacitinib) ont une AMM pour le traitement de la PR active, modérée à sévère, en situation de réponse inadéquate ou d’intolérance à un ou plusieurs traitements de fond (DMARD). Dans cette indication, les études de phase III pour ces inhibiteurs de JAK ont montré une supériorité par rapport au placebo, que ce soit après échec d’un traitement de fond conventionnel synthétique (le méthotrexate le plus souvent) ou après échec d’une ou plusieurs biothérapies. Comparé à un anti-TNF de référence, le tofacitinib et le filgotinib ont démontré une non-infériorité. Pour le baricitinib et l’upadacitinib, une supériorité statistiquement significative par rapport à l’adalimumab est observée mais dont la pertinence clinique est discutable. L’action des inhibiteurs de JAK semble plus rapide que celle des anti-TNF. Tous les inhibiteurs de JAK ont prouvé également une capacité à protéger l’articulation des lésions structurales.
Tolérance : en cours d’évaluation
Les données de la littérature montrent que le risque d’événements indésirables est identique pour les quatre molécules, permettant d’analyser ces événements indésirables comme ceux d’une classe thérapeutique.
Les inhibiteurs de JAK appartiennent à la classe des médicaments dits immunosuppresseurs et, à ce titre, peuvent être responsables d’infections sévères : infections bactériennes, opportunistes (en particulier tuberculose), réaction virale. Les cas de tuberculose sont rares, mais tous les patients bénéficient systématiquement d’un dépistage et d’un traitement des tuberculoses latentes, comme pour les traitements biologiques. Le taux d’incidence pour des infections sévères est similaire à celui observé avec les anti-TNF, de l’ordre de 3 pour 100 patients-années. Les infections les plus fréquentes concernent la sphère ORL, les poumons, l’appareil urinaire, la peau et les tissus mous.2
Une franche augmentation de la réactivation du virus varicelle-zona (VZV) est observée, favorisée par l’âge et la présence d’une corticothérapie associée à l’inhibiteur de JAK. Le taux d’incidence du zona au cours de la PR traitée par inhibiteur de JAK est ainsi évalué à 4,4 pour 100 patients-années, soit 1,5 à 2 fois plus élevé que ce qui est observé au cours de la PR.3 La fréquence de cette réactivation du VZV est 2 à 3 fois plus importante dans les pays asiatiques qu’en Europe. Les formes graves de zona restent exceptionnelles. Le vaccin Zostavax, seul vaccin contre le zona actuellement disponible en France, ne peut malheureusement pas être utilisé pour prévenir cet effet indésirable car il s’agit d’un vaccin vivant atténué, contre-indiqué dans ce contexte.
Des modifications biologiques peuvent être observées : neutropénie, lymphopénie, thrombopénie, rares augmentations des transaminases ou de la créatinine... Certaines d’entre elles sont liées à l’inhibition de l’IL-6 (augmentation du cholestérol LDL). Des modifications sévères de ces paramètres biologiques restent très rares.
Les résultats de l’étude ORALSurveillance ont mis en évidence une possible augmentation du risque thromboembolique veineux, d’accidents CV et de cancers sous tofacitinib.4 Cette étude de phase IIIB-IV, initiée en 2014 à la demande de la FDA, visait, à travers une étude randomisée ouverte, à comparer la tolérance du tofacitinib avec celle des anti-TNF au sein d’une population atteinte de PR ne répondant pas au méthotrexate. Les patients inclus étaient des patients à risque de maladie CV (plus de 50 ans avec au moins un facteur de risque CV). Plus de 4 300 patients ont été inclus, répartis en trois bras : tofacitinib 5 mg 2 fois par jour, tofacitinib 10 mg 2 fois par jour et anti-TNF (adalimumab ou étanercept). La médiane de durée du suivi a été de 4 ans. Cette étude conclut à trois sur-risques :
– une augmentation de l’incidence des accidents thromboemboliques veineux graves, dose-dépendante, surtout à la posologie de 10 mg 2 fois par jour (posologie non indiquée en rhumatologie en France) ;
– un nombre plus élevé d’événements CV majeurs sous tofacitinib (3,4 %) comparé à celui observé chez les patients sous anti-TNF (2,5 %) ; ce risque est d’autant plus important que les patients cumulent des facteurs de risque (âge > 65 ans, sexe masculin, tabagisme, antécédent d’infarctus du myocarde) ;
– une augmentation de l’incidence des maladies néoplasiques, en particulier cancer du poumon et lymphome (4,2 % avec le tofacitinib et 2,9 % avec l’anti-TNF).
Une étude similaire est en cours avec le baricitinib, également initiée à la demande de la FDA.
De plus, les résultats préliminaires d’une étude observationnelle impliquant un autre inhibiteur de JAK, Olumiant (baricitinib), suggèrent également un risque augmenté d’événements CV majeurs et thromboemboliques veineux chez les patients avec PR traités par Olumiant comparativement à ceux traités par inhibiteurs du TNF-alpha.
De nouvelles précautions d’emploi
Cinq contre-indications sont à connaître :
– infections graves (dont la tuberculose) actives ;
– insuffisance hépatique sévère (grade C de Child-Pugh) ;
– insuffisance rénale sévère ;
– présence d’une neutropénie, d’une lymphopénie ou d’une anémie sévère ;
– grossesse, allaitement et absence de contraception efficace chez la femme.
À la suite des données de l’étude ORAL, le comité de pharmacovigilance de l’EMA a lancé en février 2022 une procédure pour réévaluer le rapport bénéfice/risque des inhibiteurs de JAK.
Depuis peu, le comité de pharmacovigilance (PRAC) de l’EMA a émis plusieurs recommandations afin de réduire le risque d’effets secondaires :
– Les inhibiteurs de JAK ne doivent être utilisés qu’en l’absence d’alternative thérapeutique appropriée chez les patients :
- âgés de plus de 65 ans,
- avec des facteurs de risque d’événements CV majeurs (tels qu’une crise cardiaque ou un AVC),
- avec des facteurs de risque de cancer,
- avec un tabagisme (présent ou passé).
– Les inhibiteurs de JAK doivent être utilisés avec prudence chez les patients ayant des facteurs de risque de thrombose.
– La posologie doit être réduite pour certains groupes de patients ayant un risque de thromboembolie veineuse, de cancer ou d’événements CV majeurs.
L’EULAR a déjà modifié en juin sa recommandation concernant les traitements de la PR à proposer en cas de réponse inadéquate au méthotrexate. Si, auparavant, biothérapies et inhibiteurs de JAK étaient placés sur une même ligne après échec du méthotrexate, la recommandation propose actuellement l’addition d’une biothérapie au méthotrexate, un inhibiteur de JAK pouvant être considéré mais en tenant compte des facteurs de risque pertinents.
Attention ! Ces recommandations concernent les inhibiteurs de JAK indiqués dans les pathologies inflammatoires mais non ceux utilisés en hématologie pour le traitement de troubles myéloprolifératifs : Jakavi (ruxolitinib) et Inrebic (fédratinib).
Cantagrel A. Inhibiteurs de JAK en rhumatologie. Rev Prat 2022;72(9);935-40.
Références :
1. Dowty ME, Lin TH, Jesson MI, et al. Janus kinase inhibitors for the treatment of rheumatoid arthritis demonstrate similar profiles of in vitro cytokine receptor inhibition. Pharmacol Res Perspect 2019;7:e00537.
2. Bechman K, Subesinghe S, Norton S, et al. A systematic review and meta-analysis of infection risk with small molecule JAK inhibitors in rheumatoid arthritis. Rheumatology 2019;58:1755-66.
3. Winthrop KL. The emerging safety profile of JAK inhibitors in rheumatic disease. Nature Rev Rheumatol 2017;13:234-43.
4. Ytterberg SR, Bhatt DL, Mikuls TR, et al. Cardiovascular and cancer risk with tofacitinib in rheumatoid arthritis. N Engl J Med 2022;386:316-26.
Pour en savoir plus :
ANSM. Retour d’information sur le PRAC de novembre 2022 (24-27 octobre). 4 novembre 2022.