Des progrès importants sont intervenus en Europe pour limiter et encadrer la prescription des antibiotiques en médecine animale et limiter ainsi significativement l’antibiorésistance. Mais leur utilisation comme facteurs de croissance reste incontrôlée dans les pays du Sud.
La médecine humaine utilise des antibiotiques, la médecine vétérinaire aussi… En 2018, en France, 728 tonnes pour la première, 471 tonnes pour la seconde. Rien d’anormal puisque les infections bactériennes affectent les animaux comme l’homme, on pourrait en rester là. Pourtant, le sujet ne se résume pas au simple constat d’un exercice partagé de la médecine. Il a récemment cristallisé les tensions entre les deux professions, les uns reprochant aux autres d’être les contributeurs principaux à ce fléau qu’est la résistance aux antibiotiques, ou antibiorésistance. Le problème est loin d’être neuf car l’antibiorésistance acquise – par opposition à l’antibiorésistance naturelle – est connue depuis que nous utilisons massivement ces molécules. En revanche, sur cette question, les secteurs humain et vétérinaire diffèrent parfois largement, une compréhension mutuelle des enjeux est donc essentielle. Ensuite, il faut agir ensemble. Car chaque profession a des efforts à faire, de préférence dans la même direction. À ce titre, les années 2012-2017 ont constitué une étape charnière de prise de conscience et de rapprochement constructif des deux médecines sur le sujet des antibiotiques. C’est désormais la voie à suivre, dans l’approche moderne de la santé globale (ou « One Health ») et avec l’objectif de préserver ce bien commun que sont les antibiotiques, malheureusement déjà pour nous-mêmes, et a fortiori pour les générations futures.1
Pierre angulaire du mauvais usage chez l’animal
La dérive majeure observée dans le secteur animal est (ou a été) l’utilisation des antibiotiques en dehors de toute action de soin. On parle d’antibiotiques « facteurs (ou promoteurs) de croissance ». Cela consiste à ajouter de façon systématique des antibiotiques dans l’alimentation des animaux de production, dans un objectif supposé de favoriser leur croissance. En fait, cette pratique n’a aucun effet direct sur le développement des animaux, sauf à considérer que, dans des contextes d’élevage à très faibles niveaux d’hygiène, l’ajout d’antibiotiques contribue à un certain assainissement des flores bactériennes, permettant aux animaux de davantage consacrer leur énergie à leur gain de poids. Cette pratique est évidemment à proscrire… mais elle perdure malheureusement dans 75 % des pays dans le monde. Elle est au contraire interdite en Europe depuis le 1er janvier 2006,2 certains pays européens l’ayant même anticipée plusieurs années auparavant. Les antibiotiques n’y sont autorisés que pour un usage thérapeutique, et une autorisation indique dans quelle infection et pour quelles espèces animales utiliser un antibiotique. Par ailleurs, la France porte haut la nécessité de supprimer l’usage des antibiotiques comme promoteurs de croissance dans le monde. Notamment, dans le cadre du nouveau règlement vétérinaire européen, les denrées alimentaires animales importées doivent provenir de pays tiers démontrant l’absence de telles pratiques en élevage.
Action du ministère de l’Agriculture : les plans EcoAntibio
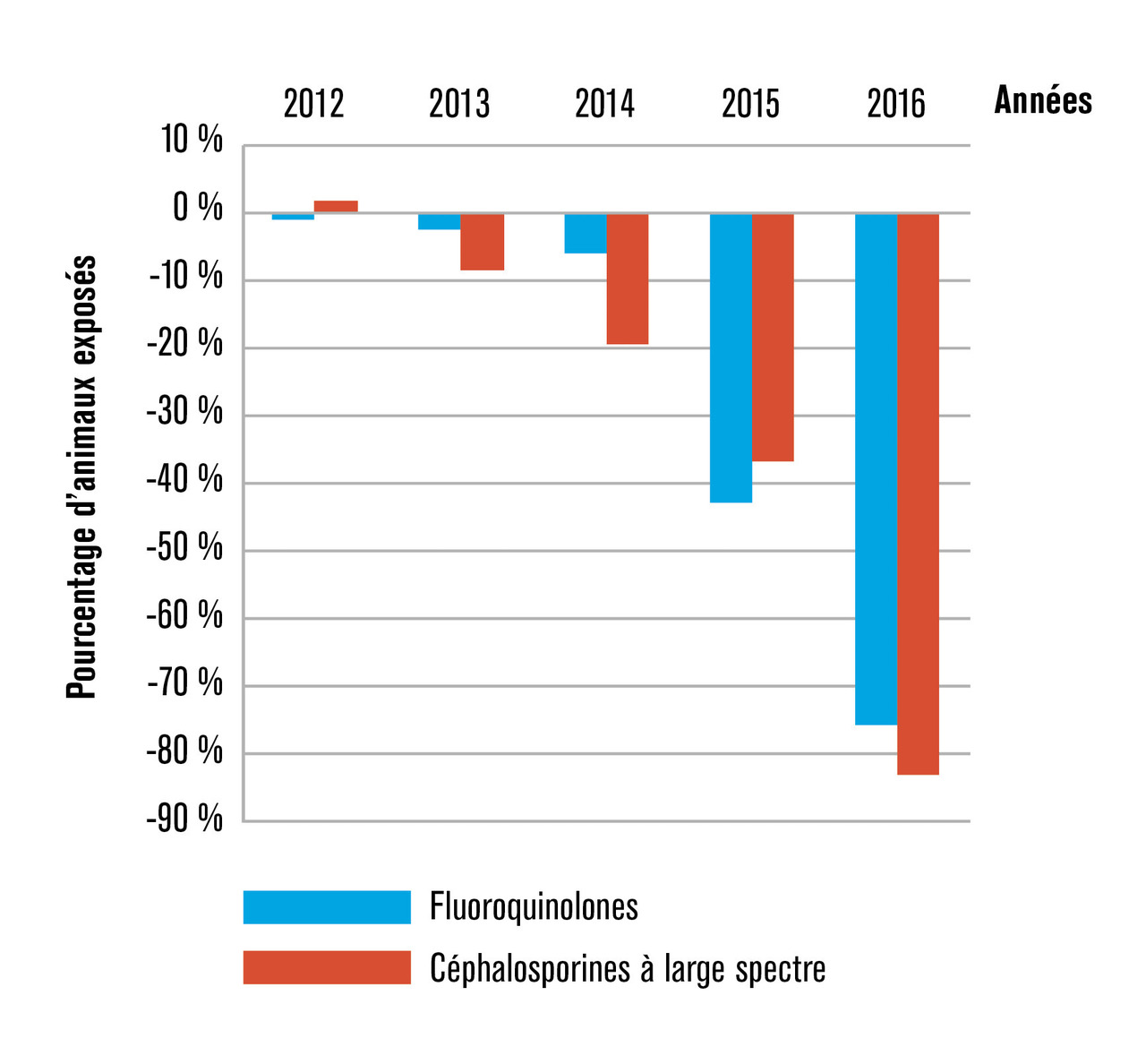
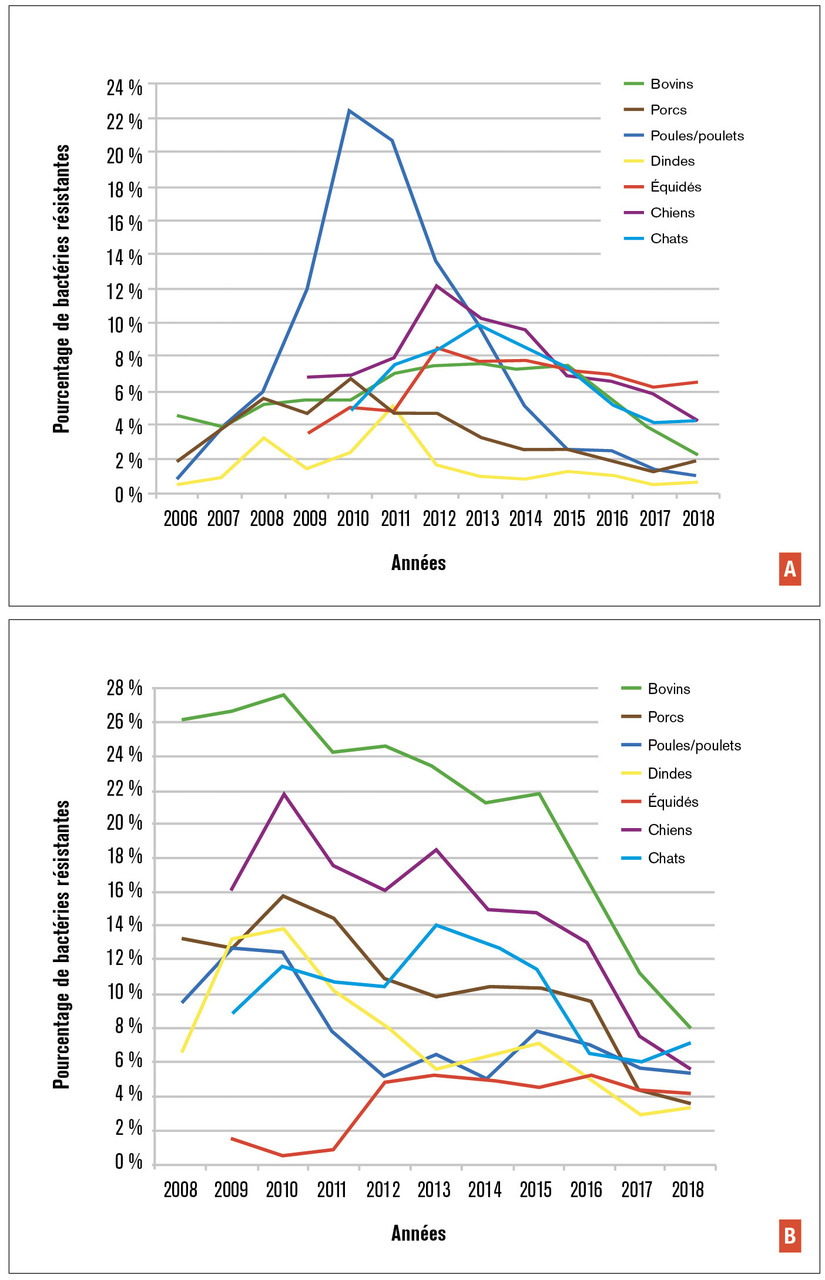
Interdire les antibiotiques comme facteurs de croissance depuis près de 15 ans en France ne suffit évidemment pas. Parlons maintenant de réelle antibiothérapie. Au sein de l’Europe, des disparités d’usage des antibiotiques vétérinaires existent, et les plus fortes réductions en élevage ont été obtenues au Danemark, aux Pays-Bas et en France alors que les pays du sud de l’Europe (Chypre, Grèce, Italie, Espagne) restent très consommateurs.3 En 2005, les Pays-Bas étaient parmi les plus faibles consommateurs européens d’antibiotiques en médecine humaine et les plus forts en agriculture. Ils sont désormais de très faibles consommateurs dans les deux secteurs. En France, ce sont les plans EcoAntibio qui ont prouvé leur efficacité.4 Mis en place en 2012, ils ont permis une diminution de près de 40 % de l’exposition des animaux aux antibiotiques en 5 ans, toutes familles confondues. Et de l’ordre de 80 % pour les deux familles d’antibiotiques d’importance critique pour l’homme, que sont les fluoroquinolones et les céphalosporines à large spectre (fig. 1 ). Un réel succès donc. Comme attendu, les résistances aux antibiotiques ont également fortement diminué, comme le montrent, par exemple, les tendances des proportions d’Escherichia coli résistants à ces deux familles dans les infections animales (fig. 2 ).
Rôle de la réglementation
L’efficacité des plans EcoAntibio a reposé sur une mobilisation forte de l’ensemble des acteurs, et notamment du couple vétérinaire-éleveur. De nombreuses actions ont été mises en place, de formation et de communication. Elles ont porté sur l’antibiothérapie mais également sur l’hygiène, la biosécurité, l’importance de la vaccination, d’une bonne alimentation et d’une eau de boisson de qualité en élevage. Les mesures incitatives ont donc été multiples, mais d’autres mesures, réglementaires, ont également encadré les pratiques d’usages des antibiotiques. Depuis 2016, une longue liste d’antibiotiques est interdite à la médecine vétérinaire. De plus, par la loi, le vétérinaire ne peut plus prescrire un antibiotique d’importance critique sans réaliser un antibiogramme démontrant cette nécessité.5 Le rôle de la loi pour contraindre la prescription des antibiotiques est propre à la médecine vétérinaire, et revient parfois comme un élément de débat avec la médecine humaine.
Spécificités de l’antibiothérapie vétérinaire
Elles sont souvent méconnues, notamment des médecins qui ont tendance à faire le parallèle – au demeurant bien naturel – avec leur propre exercice. La médecine vétérinaire est principalement une médecine collective, et non individuelle. Les poulets de chair sont élevés en lots de plusieurs milliers d’individus dans le même bâtiment. L’administration des antibiotiques se fait par voie orale dans l’eau de boisson. Et le traitement est principalement métaphylactique, c’est-à-dire que l’ensemble du lot d’animaux doit être traité à partir du moment où une fraction d’entre eux est malade. Impossible de traiter chaque animal malade individuellement, sauf à revoir en profondeur l’organisation de notre agriculture. Plus globalement, ce sont les animaux de production (volailles, porcs, bovins) qui pèsent le plus sur la consommation d’antibiotiques, et l’essentiel de l’antibiothérapie se pratique sur des individus jeunes (donc immunocompétents) puisque la durée de vie économique de ces animaux est bien inférieure à la durée de vie de leur espèce. De fait, le vétérinaire soigne de nombreuses espèces animales (et non une seule !), et l’arsenal antibiotique est parfois très limité pour certaines d’entre elles (les chèvres et les moutons par exemple, ou encore les nouveaux animaux de compagnie [NAC] tels que perroquets, serpents, rongeurs…). Les dossiers d’autorisation de mise sur le marché (AMM) des antibiotiques vétérinaires comportent un volet démontrant l’absence d’écotoxicité de la molécule active (ce volet est absent des dossiers d’AMM en médecine humaine). Enfin, la réglementation prévoit un délai d’attente entre la dernière antibiothérapie et l’abattage de l’animal, ce qui est un paramètre majeur pour protéger les consommateurs des résidus d’antibiotiques dans les denrées alimentaires.
Quand les disparités géographiques font converger les deux médecines
Au plan international (hors Europe, rappelons-le), c’est l’usage des antibiotiques comme facteurs de croissance qui constitue le principal enjeu chez l’animal. Mais à part cette spécificité notable, les mêmes disparités géographiques observées chez l’homme existent chez l’animal. L’Inde, l’Asie du Sud-Est, la Chine, l’Afrique et l’Amérique du Sud constituent les régions du monde à forts taux d’antibiorésistances. Les antibiotiques sont accessibles avec peu de contrôles, et la contrefaçon y est importante. Les pays qui affichent de tels taux de résistance cumulent aussi des contraintes majeures de différents ordres (sanitaires, démographiques, culturelles, organisationnelles…). Ces pays concentrent aussi l’essentiel de la fabrication industrielle des antibiotiques (notamment l’Inde et la Chine), avec des normes de rejet environnemental quasi inexistantes. En 2007, une étude a montré que la concentration de certains antibiotiques (fluoroquinolones) dans l’eau en aval de sites industriels était de 8 à 62 fois supérieure à celle nécessaire pour traiter un patient.6 Au Chili, la production de saumons a connu un essor considérable, avec un usage des fluoroquinolones 10 fois plus élevé qu’en médecine humaine. En Thaïlande, la conversion des rizières et des étangs en fermes industrielles de crevettes est associée à un usage massif d’antibiotiques, avec un impact sur les écosystèmes aquatiques puisque les antibiotiques sont administrés dans l’eau.
Dynamique des antibiorésistances animales
La mondialisation est un facteur important de dissémination des antibiorésistances. La Chine fournit le tiers des produits de la mer consommés dans le monde. En 2019, 40 % des crevettes consommées en Suisse (principalement importées de Thaïlande) sont contaminées par des bactéries multirésistantes. En Europe, une étude de 2008 montre que la prévalence nationale de staphylocoques dorés résistants à la méticilline chez le porc est proportionnelle à la fréquence des échanges commerciaux de porcs entre pays européens.7 Des niveaux d’antibiorésistance élevés ont été trouvés dans des poulets d’élevage suédois en l’absence d’usage d’antibiotiques, pour la seule raison que la Suède importait des poussins du Royaume-Uni où l’antibiothérapie était massive.9 Chez l’homme, il est connu que les voyages à l’étranger sont un risque d’acquisition de bactéries multirésistantes, avec des taux d’acquisition variables selon les régions géographiques. Chez l’animal, ce sont surtout les échanges commerciaux qui jouent ce rôle.
Transmission de l’antibiorésistance entre l’animal et l’homme
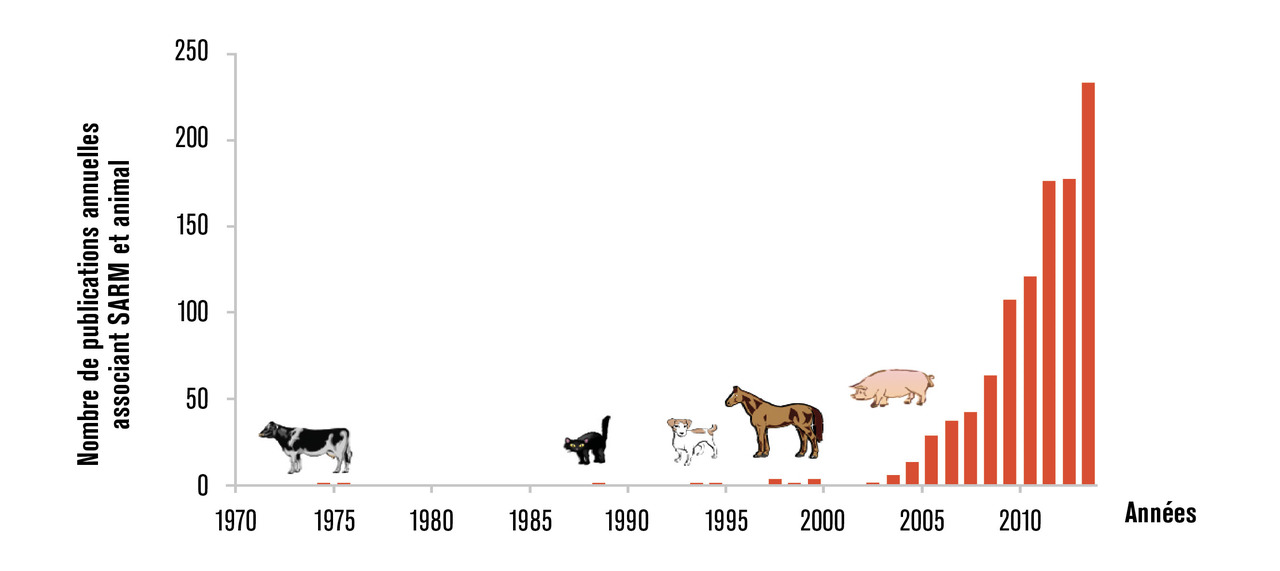
Il s’agit d’un sujet parmi les plus complexes. Il nourrit souvent les commentaires des observateurs, et sous-tend globalement la mise en place des politiques publiques sur l’antibiorésistance animale. Probablement que les transferts d’antibiorésistance entre les secteurs animaux et humain sont, en fait, plus rares qu’on ne le pense. Certes, certaines situations sont claires, comme la contamination des éleveurs de porcs entre 2004 et 2007 aux Pays-Bas et au Danemark par les staphylocoques dorés résistants à la méticilline hébergés par leurs animaux.8 Ce n’est d’ailleurs qu’à cette occasion – c’est-à-dire 50 ans plus tard qu’en médecine humaine – que les vétérinaires se sont préoccupés de ces staphylocoques dorés résistants à la méticilline, comme le montre l’activité bibliographique sur le sujet (fig. 3 ). Pour autant, cette exposition professionnelle bien réelle n’a pas valeur générale. En France, la situation est différente malgré un élevage porcin équivalent ; les très bons résultats d’usage des antibiotiques obtenus en médecine vétérinaire ont conduit à une réduction de l’antibiorésistance chez les animaux, mais pas chez l’homme. Sans doute ignorons-nous encore bien des choses sur les voies de transmission de l’antibiorésistance entre les secteurs humain et animaux. Le questionnement sur leurs parts attributives respectives n’est intellectuellement pas hors de propos, mais il ne doit conduire qu’à mieux affiner nos actions, et non à servir la polémique. En fait, retenons surtout que les deux populations, animale et humaine, s’enrichissent davantage en gènes de résistance à la suite de leurs propres usages plutôt que par transfert massif d’un compartiment dans l’autre.
Antibiothérapie : un enjeu écologique
Les antibiotiques sont une formidable solution thérapeutique face aux infections bactériennes, chacun en conviendra. Mais leur usage est aussi un facteur majeur de sélection de souches résistantes. De ce fait, il est de la plus haute importance que tout prescripteur d’antibiotiques (et la profession vétérinaire est concernée, au même titre que les médecins) soit conscient des conséquences de ces usages. L’enjeu est aujourd’hui de nature écologique, c’est-à-dire que tous les écosystèmes dans lesquels vivent les hommes et les animaux s’enrichissent régulièrement en bactéries antibiorésistantes, à la suite de l’usage d’antibiotiques, même ceux qui sont médicalement légitimes. Pour autant, il ne s’agit pas de se « passer » d’antibiotiques. Mais il est devenu essentiel de reconsidérer leur place dans l’acte thérapeutique, c’est-à-dire de savoir les utiliser quand il le faut, et de savoir les oublier quand il est possible de faire autrement. Chez l’animal comme chez l’homme.
Encadre
Hommage
Cet article est dédié à la mémoire du Professeur Jacques Acar, brutalement décédé le 27 mars 2020 d’une infection par le nouveau coronavirus SRAS-CoV-2 (Covid-19). Microbiologiste médical de renommée mondiale, fin connaisseur des antibiotiques et de l’antibiorésistance, il soutenait aussi activement, en France comme au plan international, les évolutions du monde vétérinaire sur ces questions, dans une vision résolument globale qu’on qualifie de « une seule santé ». Son regard aiguisé et parfois provocateur, et sa voix de cathédrale, manquent déjà à plusieurs générations de médecins. Vaincu par un virus et non par une bactérie, il aurait sans doute trouvé que l’honneur était sauf ! Qu’il repose en paix.
J.-Y. Madec
Références
1. WHO 2014. Antimicrobial resistance global report on surveillance. WHO 2014. https://bit.ly/39jkv2w
2. Commission européenne. Interdiction des antibiotiques comme facteurs de croissance dans les aliments pour animaux. Eur Commission, 2006. https://bit.ly/39dHdbW
3. European Medicine Agency. Sales of veterinary antimicrobial agents in 31 European countries in 2017. EMA, 2019. https://bit.ly/3abGCZW
4. Ministère de l’Agriculture et de l’Alimentation. Plan EcoAntibio 2012-2017 : lutte contre l’antibiorésistance. 2019. https://bit.ly/2J9GoXb
5. Journal officiel de la République française. 2016. Décret n° 2016-1788 du 19 décembre 2016 relatif à la transmission de données de cession des médicaments utilisés en médecine vétérinaire comportant une ou plusieurs substances antibiotiques. https://bit.ly/2QCeRSA
6. Larsson DG, de Pedro C, Paxeus N. Effluent from drug manufactures contains extremely high levels of pharmaceuticals. J Hazard Mater 2007;148:751-5.
7. European Food Safety Authority. Analysis of the baseline survey on the prevalence of methicillin-resistant Staphylococcus aureus (MRSA) in holdings with breeding pigs in the EU. EFSA Journal 2010;8:1597.
8. Lewis HC1, Mølbak K, Reese C, et al. Pigs as source of methicillin-resistant Staphylococcus aureus CC398 infections in humans, Denmark. Emerg Infect Di 2008;14:1383-9.
9. Nilsson O, Börjesson S, Landén A, Bengtsson B. Vertical transmission of Escherichia coli carrying plasmid-mediated AmpC (pAmpC) through the broiler production pyramid. J Antimicrob Chemother 2014;69:1497-500.
2. Commission européenne. Interdiction des antibiotiques comme facteurs de croissance dans les aliments pour animaux. Eur Commission, 2006. https://bit.ly/39dHdbW
3. European Medicine Agency. Sales of veterinary antimicrobial agents in 31 European countries in 2017. EMA, 2019. https://bit.ly/3abGCZW
4. Ministère de l’Agriculture et de l’Alimentation. Plan EcoAntibio 2012-2017 : lutte contre l’antibiorésistance. 2019. https://bit.ly/2J9GoXb
5. Journal officiel de la République française. 2016. Décret n° 2016-1788 du 19 décembre 2016 relatif à la transmission de données de cession des médicaments utilisés en médecine vétérinaire comportant une ou plusieurs substances antibiotiques. https://bit.ly/2QCeRSA
6. Larsson DG, de Pedro C, Paxeus N. Effluent from drug manufactures contains extremely high levels of pharmaceuticals. J Hazard Mater 2007;148:751-5.
7. European Food Safety Authority. Analysis of the baseline survey on the prevalence of methicillin-resistant Staphylococcus aureus (MRSA) in holdings with breeding pigs in the EU. EFSA Journal 2010;8:1597.
8. Lewis HC1, Mølbak K, Reese C, et al. Pigs as source of methicillin-resistant Staphylococcus aureus CC398 infections in humans, Denmark. Emerg Infect Di 2008;14:1383-9.
9. Nilsson O, Börjesson S, Landén A, Bengtsson B. Vertical transmission of Escherichia coli carrying plasmid-mediated AmpC (pAmpC) through the broiler production pyramid. J Antimicrob Chemother 2014;69:1497-500.
Dans cet article
- Pierre angulaire du mauvais usage chez l’animal
- Action du ministère de l’Agriculture : les plans EcoAntibio
- Rôle de la réglementation
- Spécificités de l’antibiothérapie vétérinaire
- Quand les disparités géographiques font converger les deux médecines
- Dynamique des antibiorésistances animales
- Transmission de l’antibiorésistance entre l’animal et l’homme
- Antibiothérapie : un enjeu écologique

 Encadrés
Encadrés