La consommation d’antibiotiques repart à la hausse…
La France consomme beaucoup trop d’antibiotiques, et paie ses excès par une émergence des résistances bactériennes. Longtemps limitées aux hôpitaux (et responsables d’infections nosocomiales), ces dernières ont ensuite émergé en ville (contaminations liées aux soins), et concernent désormais aussi des patients sans aucun facteur de risque classique (infections communautaires). Cette évolution n’est pas surprenante, car plus de 90 % des antibiotiques consommés en France sont prescrits en dehors des établissements de santé.
Ce constat incite à engager des actions efficaces pour réduire les utilisations inappropriées en ville.
Cela est possible, et sans conséquence néfaste pour le patient. Il ne s’agit pas de restreindre l’accès aux soins des individus pour remédier à une problématique collective, mais de viser au « juste ou bon usage » de ces médicaments, bénéfiques pour chacun comme pour la collectivité. L’exemple des Pays-Bas est édifiant, car il ne s’agit pas d’un pays en développement, ni d’un territoire où l’accès aux soins est limité : les habitants y vivent aussi longtemps qu’en France, avec une santé au moins aussi bonne, en consommant 3 fois moins d’antibiotiques durant leur vie !
Ce constat incite à engager des actions efficaces pour réduire les utilisations inappropriées en ville.
Cela est possible, et sans conséquence néfaste pour le patient. Il ne s’agit pas de restreindre l’accès aux soins des individus pour remédier à une problématique collective, mais de viser au « juste ou bon usage » de ces médicaments, bénéfiques pour chacun comme pour la collectivité. L’exemple des Pays-Bas est édifiant, car il ne s’agit pas d’un pays en développement, ni d’un territoire où l’accès aux soins est limité : les habitants y vivent aussi longtemps qu’en France, avec une santé au moins aussi bonne, en consommant 3 fois moins d’antibiotiques durant leur vie !
Quelles actions ?
Parmi les principaux leviers permettant de réduire significativement les consommations sans risque pour les patients, la première grande campagne française (« Les antibiotiques, c’est pas automatique ») avait ciblé, avec succès, les situations où l’absence d’indication est relativement simple à reconnaître, notamment les infections des voies aérodigestives supérieures virales (rhinopharyngites, angines, sinusites).
Résultat : elle a permis d’éviter plus de 17 millions de prescriptions en 4 ans, confirmant sa pertinence !
Plus de 15 ans après, la consommation s’est stabilisée en France, avec une tendance à la hausse ces dernières années, contemporaine à l’émergence de nombreuses résistances dans le monde.
La directrice de l’OMS, Margaret Chan, a tiré la sonnette d’alarme en 2012. Selon elle, la progression des bactéries toto-résistantes menace toute la médecine moderne : alors que le développement de nouveaux antibiotiques innovants s’est tari au fil des années, on doit redouter le retour à une situation proche de celle du début du XXe siècle : certaines procédures médicales (greffes d’organes ou de cellules souches hématopoïétiques, dispositifs intracardiaques, prothèses ostéo-articulaires, biothérapies ou chimiothérapies aplasiantes) ne seraient plus envisageables en l’absence d’antibiothérapies prophylactiques et curatives efficaces capables de protéger les patients de complications infectieuses fatales.1
La baisse des durées de traitement, prônée par de nombreux experts depuis déjà une dizaine d’années,2 est probablement un levier simple pour diminuer les consommations. Les praticiens en acceptent beaucoup plus facilement le principe, plutôt que celui de ne pas prescrire ces médicaments, dans les situations où leur intérêt est discuté. On peut, certes, regretter la frilosité ambiante vis-à-vis de leur non-utilisation, mais celle-ci est réelle et partagée, avec quelques justifications : trop peu de tests diagnostiques rapides permettent de différencier les causes bactériennes des virales ; en cas d’infection bactérienne grave, le retard à l’instauration d’une antibiothérapie adaptée a des conséquences pronostiques majeures. Ce constat ne doit pas conduire à abandonner les actions en faveur de la non-prescription dans les multiples situations où c’est justifié, mais il incite à développer des interventions autres, comme notamment raccourcir la durée.
À l’appui de cette stratégie, la littérature s’est considérablement enrichie en études randomisées de qualité. Au fil des années, il a été prouvé qu’on pouvait se contenter de 3 jours de traitement pour les pneumopathies aiguës communautaires en cas d’évolution rapidement favorable,3 de 4 jours pour les infections intra-abdominales opérées, de 7 jours pour les pyélonéphrites aiguës non compliquées, même bactériémiques,4 de 8 jours pour les pneumopathies acquises sous ventilation mécanique, de 6 semaines pour les spondylodiscites bactériennes.5
Freins à l’application au quotidien : les discordances parfois nettes avec les durées préconisées officiellement par les sociétés savantes et l’impossibilité, pour les principaux prescripteurs en France (le généralistes), de suivre l’actualité de toutes les spécialités.
Résultat : elle a permis d’éviter plus de 17 millions de prescriptions en 4 ans, confirmant sa pertinence !
Plus de 15 ans après, la consommation s’est stabilisée en France, avec une tendance à la hausse ces dernières années, contemporaine à l’émergence de nombreuses résistances dans le monde.
La directrice de l’OMS, Margaret Chan, a tiré la sonnette d’alarme en 2012. Selon elle, la progression des bactéries toto-résistantes menace toute la médecine moderne : alors que le développement de nouveaux antibiotiques innovants s’est tari au fil des années, on doit redouter le retour à une situation proche de celle du début du XXe siècle : certaines procédures médicales (greffes d’organes ou de cellules souches hématopoïétiques, dispositifs intracardiaques, prothèses ostéo-articulaires, biothérapies ou chimiothérapies aplasiantes) ne seraient plus envisageables en l’absence d’antibiothérapies prophylactiques et curatives efficaces capables de protéger les patients de complications infectieuses fatales.1
La baisse des durées de traitement, prônée par de nombreux experts depuis déjà une dizaine d’années,2 est probablement un levier simple pour diminuer les consommations. Les praticiens en acceptent beaucoup plus facilement le principe, plutôt que celui de ne pas prescrire ces médicaments, dans les situations où leur intérêt est discuté. On peut, certes, regretter la frilosité ambiante vis-à-vis de leur non-utilisation, mais celle-ci est réelle et partagée, avec quelques justifications : trop peu de tests diagnostiques rapides permettent de différencier les causes bactériennes des virales ; en cas d’infection bactérienne grave, le retard à l’instauration d’une antibiothérapie adaptée a des conséquences pronostiques majeures. Ce constat ne doit pas conduire à abandonner les actions en faveur de la non-prescription dans les multiples situations où c’est justifié, mais il incite à développer des interventions autres, comme notamment raccourcir la durée.
À l’appui de cette stratégie, la littérature s’est considérablement enrichie en études randomisées de qualité. Au fil des années, il a été prouvé qu’on pouvait se contenter de 3 jours de traitement pour les pneumopathies aiguës communautaires en cas d’évolution rapidement favorable,3 de 4 jours pour les infections intra-abdominales opérées, de 7 jours pour les pyélonéphrites aiguës non compliquées, même bactériémiques,4 de 8 jours pour les pneumopathies acquises sous ventilation mécanique, de 6 semaines pour les spondylodiscites bactériennes.5
Freins à l’application au quotidien : les discordances parfois nettes avec les durées préconisées officiellement par les sociétés savantes et l’impossibilité, pour les principaux prescripteurs en France (le généralistes), de suivre l’actualité de toutes les spécialités.
En pratique
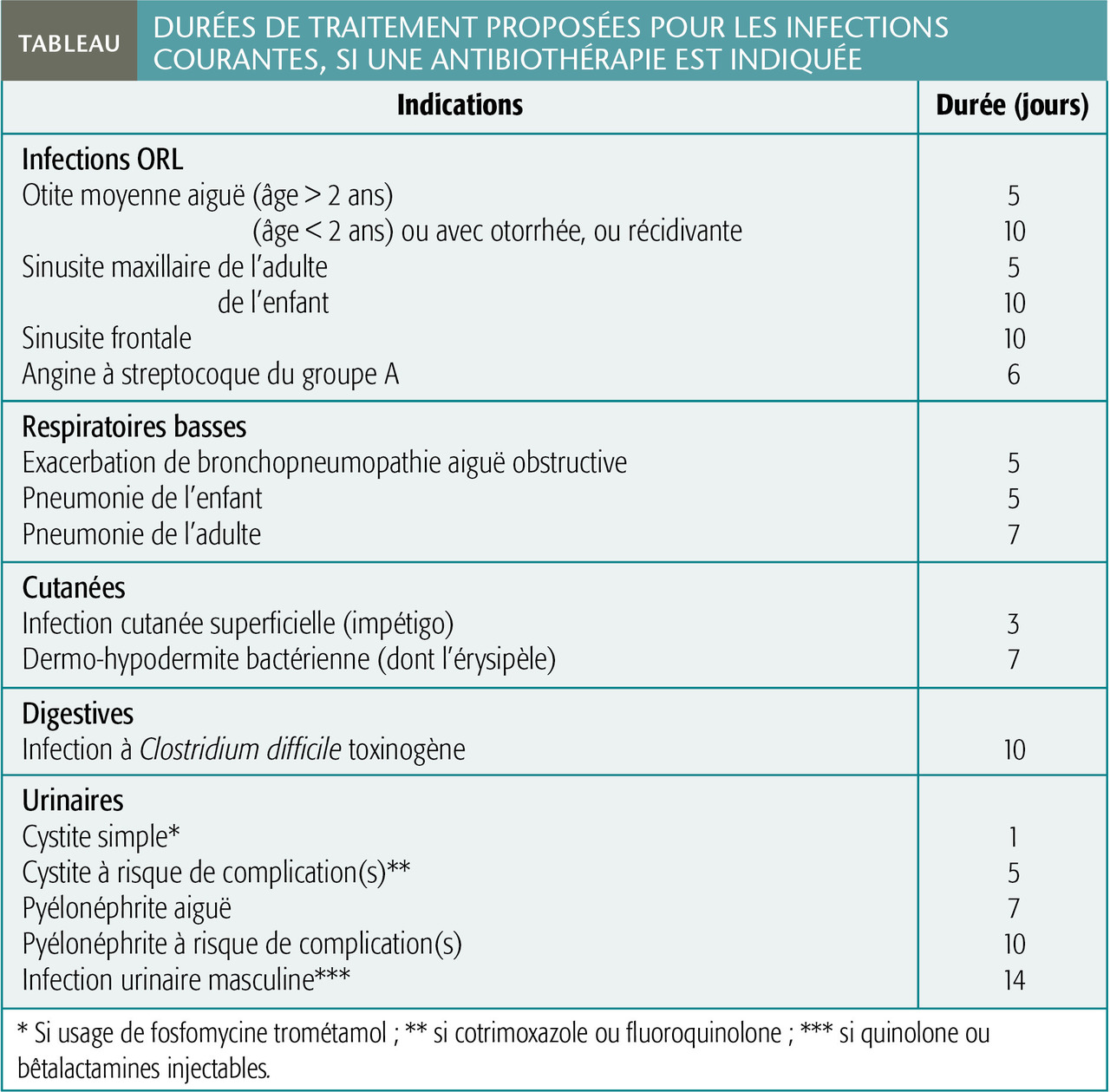
La Société de pathologie infectieuse de langue française (SPILF) s’est emparée de ce problème en publiant, en 2017, des propositions fondées sur une analyse systématique de la littérature médicale, soit des durées d’antibiothérapie qui correspondent au temps nécessaire à la guérison pour la majorité des patients, sans perte de chance (tableau).5 Trois commentaires s’imposent :
– les fourchettes de durées ont été bannies, car l’expérience a montré que les médecins français sont tentés de choisir la limite supérieure, pour des raisons mal connues (désir de faire « le maximum » pour le patient, considérations médico-légales, angoisses non motivées…) ;
– on constate des discordances nettes avec les durées préconisées par les instances officielles françaises. Ainsi, l’érysipèle devrait être traité 10 à 20 jours d’après les guidelines communes SPILF-Société française de dermatologie de 2000,6 contre 7 jours selon les nouvelles propositions.5 De même, pour une pneumonie aiguë communautaire : 7 à 14 jours (SPILF-Société de pneumologie de langue française, 2010)7 versus 7 jours d’après des textes récents,5 qui précisent même qu’on peut envisager d’interrompre l’antibiothérapie après 3 jours (si évolution rapidement favorable), et que 5 jours suffisent chez l’enfant ! Ces divergences seront résolues lorsque les recommandations officielles seront mises à jour (ce qui est en cours pour l’érysipèle) ;
– la méthodologie (travail en binôme, sans collaboration avec d’autres sociétés savantes ou des instances nationales) ne permet pas de leur donner le label de « recommandations ». Cela est problématique : les outils d’aide à la prescription, comme Antibioclic, n’ont pas osé s’affranchir des recos institutionnelles ; les interventions par les délégués de l’Assurance maladie auprès des médecins généralistes ne peuvent pas être envisagées en l’absence de texte officiel. Ce dernier point devrait prochainement faire l’objet d’une collaboration entre la HAS et la SPILF.
– les fourchettes de durées ont été bannies, car l’expérience a montré que les médecins français sont tentés de choisir la limite supérieure, pour des raisons mal connues (désir de faire « le maximum » pour le patient, considérations médico-légales, angoisses non motivées…) ;
– on constate des discordances nettes avec les durées préconisées par les instances officielles françaises. Ainsi, l’érysipèle devrait être traité 10 à 20 jours d’après les guidelines communes SPILF-Société française de dermatologie de 2000,6 contre 7 jours selon les nouvelles propositions.5 De même, pour une pneumonie aiguë communautaire : 7 à 14 jours (SPILF-Société de pneumologie de langue française, 2010)7 versus 7 jours d’après des textes récents,5 qui précisent même qu’on peut envisager d’interrompre l’antibiothérapie après 3 jours (si évolution rapidement favorable), et que 5 jours suffisent chez l’enfant ! Ces divergences seront résolues lorsque les recommandations officielles seront mises à jour (ce qui est en cours pour l’érysipèle) ;
– la méthodologie (travail en binôme, sans collaboration avec d’autres sociétés savantes ou des instances nationales) ne permet pas de leur donner le label de « recommandations ». Cela est problématique : les outils d’aide à la prescription, comme Antibioclic, n’ont pas osé s’affranchir des recos institutionnelles ; les interventions par les délégués de l’Assurance maladie auprès des médecins généralistes ne peuvent pas être envisagées en l’absence de texte officiel. Ce dernier point devrait prochainement faire l’objet d’une collaboration entre la HAS et la SPILF.
Quel impact ?
L’application de ces propositions pourrait réduire l’utilisation des antibiotiques de plus d’un tiers à l’hôpital, cette économie serait au moins de la même ampleur en ville. En revanche, si ces nouvelles modalités semblent non risquées, compte tenu de la solidité des preuves dont on dispose (études randomisées de qualité), et bien acceptées par les praticiens, il n’est pas certain qu’elles règlent le problème de l’émergence des multirésistances. En effet, des études suggèrent que leur sélection sous antibiothérapie survient dès les tout premiers jours... En attendant que ce point soit clarifié, il est néanmoins acquis qu’on peut diminuer les durées de traitement, sans risque, dans de nombreuses infections.
RÉFÉRENCES
1. Tattevin P. Ce qui est nouveau en infectiologie : des avancées, des reculs. Rev Prat 2015;65: 295-8.
2. Rice LB. The Maxwell Finland Lecture: for the duration-rational antibiotic administration in an era of antimicrobial resistance and Clostridium difficile. Clin Infect Dis 2008;46:491-6.
3. el Moussaoui R, de Borgie CA, van den Broek P, et al. Effectiveness of discontinuing antibiotic treatment after three days versus eight days in mild to moderate-severe community acquired pneumonia: randomised, double blind study. BMJ 2006;332:1355.
4. Sandberg T, Skoog G, Hermansson AB, et al. Ciprofloxacin for 7 days versus 14 days in women with acute pyelonephritis: a randomised, open-label and double-blind, placebo-controlled, non-inferiority trial. Lancet 2012; 380:484-90.
5. Wintenberger C, Guery B, Bonnet E, et al. Recommendation Group of the SPILF. Proposal for shorter antibiotic therapies. Med Mal Infect 2017;47:92-141.
6. SPILF. Erysipèle et fasciite nécrosante. Prise en charge. Conférence de consensus. Janvier 2000.
https://bit.ly/2R3YcVN
7. Afssaps. Antibiothérapie par voie générale dans les infections respiratoires basses de l’adulte. Mise au point. Juillet 2010.
https://bit.ly/2CUWByD
2. Rice LB. The Maxwell Finland Lecture: for the duration-rational antibiotic administration in an era of antimicrobial resistance and Clostridium difficile. Clin Infect Dis 2008;46:491-6.
3. el Moussaoui R, de Borgie CA, van den Broek P, et al. Effectiveness of discontinuing antibiotic treatment after three days versus eight days in mild to moderate-severe community acquired pneumonia: randomised, double blind study. BMJ 2006;332:1355.
4. Sandberg T, Skoog G, Hermansson AB, et al. Ciprofloxacin for 7 days versus 14 days in women with acute pyelonephritis: a randomised, open-label and double-blind, placebo-controlled, non-inferiority trial. Lancet 2012; 380:484-90.
5. Wintenberger C, Guery B, Bonnet E, et al. Recommendation Group of the SPILF. Proposal for shorter antibiotic therapies. Med Mal Infect 2017;47:92-141.
6. SPILF. Erysipèle et fasciite nécrosante. Prise en charge. Conférence de consensus. Janvier 2000.
https://bit.ly/2R3YcVN
7. Afssaps. Antibiothérapie par voie générale dans les infections respiratoires basses de l’adulte. Mise au point. Juillet 2010.
https://bit.ly/2CUWByD