Diagnostiquer une maladie de Horton, une pseudo-polyarthrite rhizomélique, une maladie de Takayasu.
Argumenter l'attitude thérapeutique et planifier le suivi du patient.
Introduction
La pathogénie de l’artérite à cellules géantes n’est pas complètement élucidée. On suspecte une stimulation antigénique initiale d’origine infectieuse. Sur un terrain génétique favorisant, lié à certains variants du marqueur HLA-DR4, des lésions inflammatoires vasculaires apparaissent suite à l’activation de cellules dendritiques adventicielles présentatrices d’antigène, qui vont stimuler des lymphocytes T. Ces lymphocytes T migrent et prolifèrent dans la média, permettant le recrutement de macrophages qui peuvent fusionner en cellules géantes sous l’effet de l’interféron gamma. L’artérite à cellules géantes s’accompagne typiquement d’une réaction inflammatoire systémique intense, essentiellement liée à la production macrophagique d’interleukine-6 (IL-6) et d’interleukine-1 (IL-1).
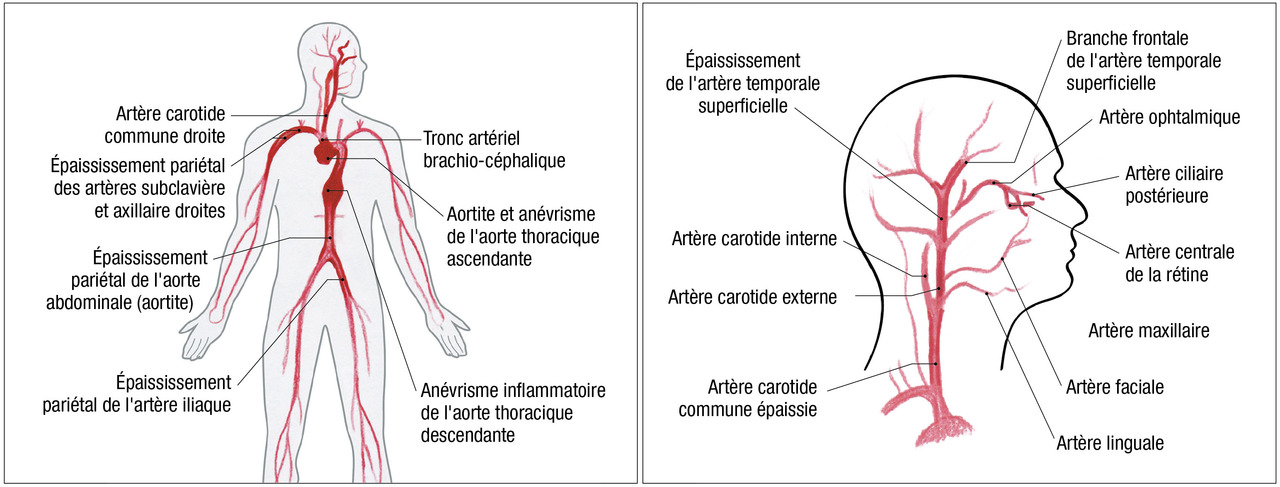
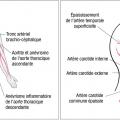
Dans l’artérite à cellules géantes, l’inflammation peut concerner l’aorte et ses principales branches, notamment les artères issues de la crosse aortique, mais elle prédomine volontiers au niveau des branches de l’artère carotide externe, dont l’artère temporale. L’artérite à cellules géantes a également un tropisme particulier pour les branches des artères ophtalmiques, issues de la carotide interne, notamment les artères ciliaires postérieures.
Toutes ces localisations expliquent les manifestations cliniques classiques de la maladie, comme les céphalées, et l’atteinte oculaire par neuropathie optique ischémique antérieure aiguë. La présence fréquente d’une pseudo-polyarthrite rhizomélique est également une particularité clinique de l’artérite à cellules géantes.
Ces dernières années, les progrès techniques de l’imagerie vasculaire ont conduit à mieux caractériser les atteintes des artères de gros calibre de l’artérite à cellules géantes, ce qui a conduit à proposer d’adapter les classiques critères de classification de l’ACR (American College of Rheumatology) 1990 (
L’artérite à cellules géantes est typiquement corticosensible, mais les rechutes sont fréquentes. La survie globale de l’artérite à cellules géantes est superposable à celle de la population générale du même âge. Néanmoins, les patients ayant une artérite à cellules géantes se singularisent par un risque accru de comorbidités, qui ont-elles-mêmes une mortalité non négligeable : événements cardiovasculaires, anévrisme de l’aorte, complications de la corticothérapie prolongée comme les événements infectieux, l’ostéoporose, l’hypertension artérielle (HTA) ou le diabète.
Présentation clinique
Signes généraux
Manifestations céphaliques
Elles sont la conséquence de l’ischémie tissulaire secondaire aux lésions inflammatoires des artères issues de la carotide externe.
Il s’agit essentiellement des céphalées, temporales, fronto-temporales, occipitales, ou diffuses, uni ou bilatérales, mais de caractère inhabituel et répondant peu ou pas au paracétamol. Ces céphalées s’installent plutôt progressivement, mais un mode de début aigu est également possible. Elles peuvent être insomniantes.
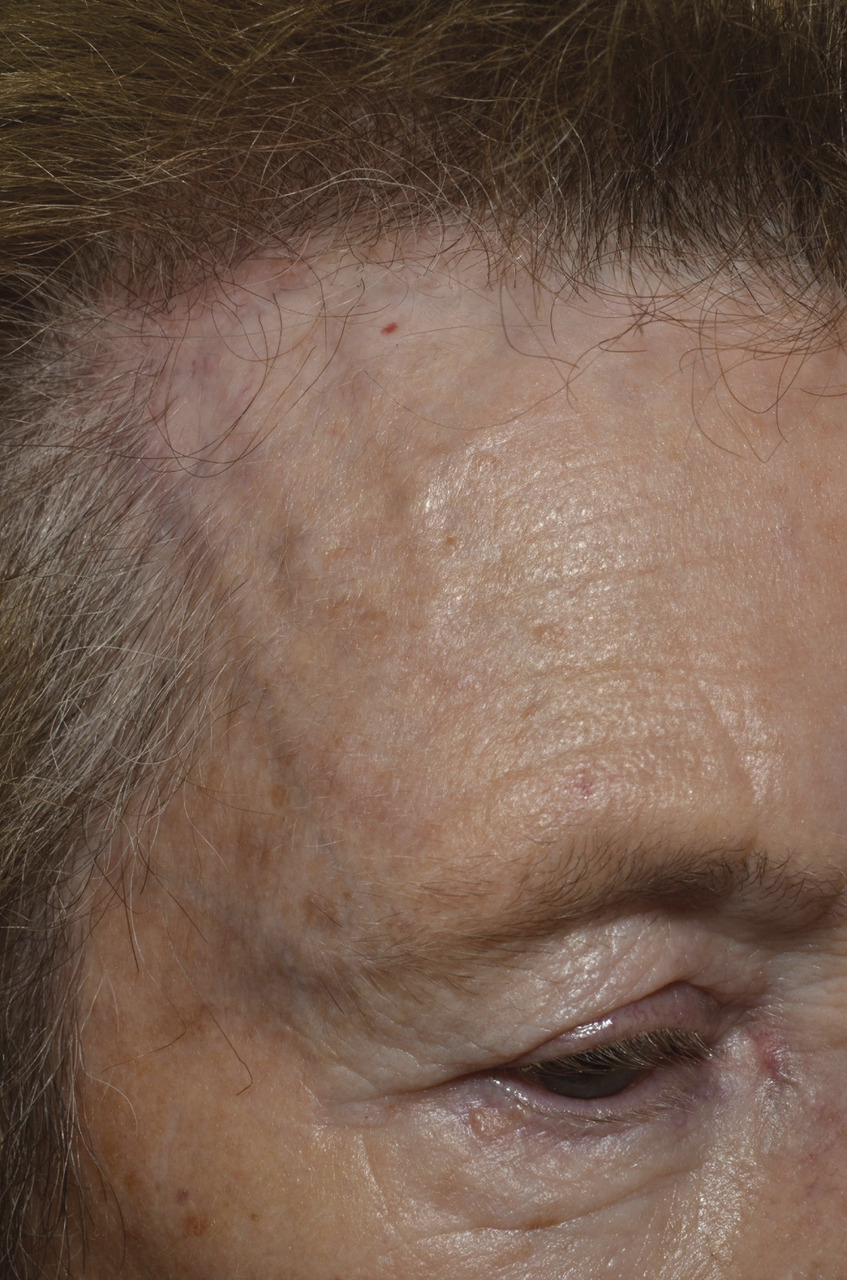
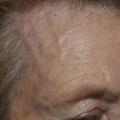
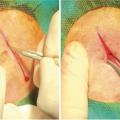
Les patients peuvent parfois percevoir des sensations douloureuses de gonflement, d’induration, de stries, en regard des artères temporales (
L’hyperesthésie du cuir chevelu est également évocatrice du diagnostic. Des sensations douloureuses peuvent être perçues en se coiffant (signe du peigne), au port d’un couvre-chef (signe du chapeau) ou de lunettes, ou durant la nuit (signe de l’oreiller).
Les patients peuvent signaler des douleurs musculaires des masséters lors de la mastication (claudication intermittente des mâchoires). L’ischémie des masséters, secondaire à l’atteinte de l’artère maxillaire, peut aussi conduire à un trismus de repos.
Il peut également exister des douleurs faciales, linguales (glossodynie), buccales, gingivales, ainsi qu’une odynophagie.
L’ischémie tissulaire peut, à l’extrême, conduire à une nécrose cutanée du cuir chevelu, et beaucoup plus rarement à une nécrose de la langue ou du voile du palais.
L’examen clinique des artères temporales, et du revêtement cutané en regard, doit être minutieux, à la recherche des signes évocateurs d’artérite à cellules géantes, uni ou bilatéraux : aspect inflammatoire, gonflé (cordon saillant), strié, sensible, induré, avec abolition ou asymétrie des pouls temporaux.
Pseudo-polyarthrite rhizomélique
Signes visuels
Dans 10 à 15 % des cas d’artérite à cellules géantes, une atteinte oculaire grave survient, et elle est responsable d’une perte permanente de la vision, pouvant aller jusqu’à l’amaurose définitive, qui est malheureusement bilatérale dans de rares cas.
Le mécanisme principal (80 % des cas) est représenté par la neuropathie optique ischémique antérieure aiguë, conséquence de l’atteinte des artères ciliaires courtes qui vascularisent le nerf optique (
C’est cette atteinte visuelle qui conditionne en grande partie le pronostic de l’artérite à cellules géantes. Chez un patient suspect d’artérite à cellules géantes, des signes visuels transitoires doivent être considérés comme une menace imminente d’amaurose définitive, et justifient une corticothérapie immédiate. En revanche, quand l’amaurose est installée, la récupération sous corticoïdes est illusoire. Il faut préciser qu’une neuropathie optique ischémique antérieure aiguë n’est pas synonyme d’artérite à cellules géantes, et que l’athérome en est une autre cause classique. La recherche d’un syndrome inflammatoire est donc à faire en urgence devant toute neuropathie optique ischémique antérieure aiguë au-delà de 50 ans.
En dehors de la neuropathie optique ischémique antérieure aiguë, d’autres atteintes oculaires peuvent survenir : neuropathie optique ischémique postérieure, occlusion de l’artère centrale de la rétine, atteinte oculomotrice (atteinte du III notamment), ou exceptionnellement une cécité corticale due à un accident vasculaire cérébral (AVC) occipital.
Signes d’atteinte des artères de gros calibre
Des symptômes peuvent néanmoins exister : claudication ou fatigabilité des membres supérieurs en lien avec une artérite inflammatoire des artères sous-clavières et axillaires, artérite des membres inférieurs (plus rare), acrosyndrome, ischémie distale des membres, ischémie mésentérique (très rares).
Un AVC ischémique peut exceptionnellement être une circonstance du diagnostic d’artérite à cellules géantes. Il s’agit alors de patients qui ont une artérite inflammatoire, parfois des carotides internes, mais le plus souvent des artères vertébrales, avec une fréquence plus importante des AVC dans le territoire postérieur. Imputer un AVC à la seule artérite à cellules géantes est souvent difficile chez ces patients qui ont bien souvent des lésions athéromateuses concomitantes.
Un syndrome coronarien par coronarite inflammatoire est possible, mais très rare.
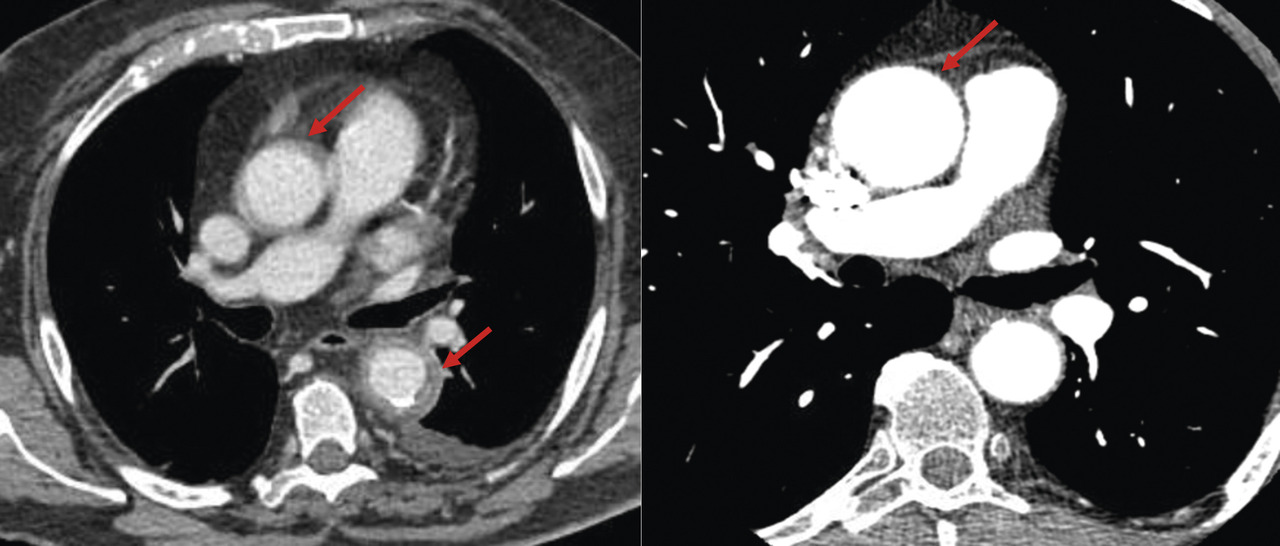
Enfin, des signes d’atteinte aortique peuvent être au premier plan. Il existe de rares cas d’artérite à cellules géantes, qui dès la période du diagnostic, ont une aortite grave, compliquée d’une dilatation anévrismale. Ces anévrismes de l’aorte peuvent s’exprimer par un souffle d’insuffisance aortique, une dyspnée, des douleurs thoraciques ou dorsales (étage thoracique), des douleurs abdominales, lombaires, ou la présence d’un signe de De Bakey (anévrisme de l’aorte abdominale, plus rare). Une dissection aortique peut être un mode de révélation de l’artérite à cellules géantes. C’est exceptionnel, mais doit être connu du clinicien, étant donné sa gravité.
Autres manifestations cliniques
D’autres manifestations sont possibles mais rares, comme une péricardite, une pleurésie. Certains patients peuvent se plaindre de troubles du goût ou de l’odorat, d’une dysphonie (voix rauque), de douleurs pharyngées, de signes audiovestibulaires.
De manière très exceptionnelle, des lésions de vascularite à cellules géantes ont pu parfois être retrouvées sur des localisations inhabituelles (poumon, foie, sein, ovaire, utérus, testicule, peau).
Formes cliniques
Tableau typique
La présentation clinique typique comporte un ou plusieurs signe(s) céphalique(s), un (ou plusieurs) signe(s) général(aux), éventuellement associé(s) à une pseudopolyarthrite rhizomélique et/ou une neuropathie optique ischémique antérieure aiguë. En ce cas, l’artérite à cellules géantes est l’hypothèse diagnostique principale, voire unique. Même dans les formes les plus typiques, il est préférable de compléter le diagnostic clinique par une preuve diagnostique formelle (biopsie d’artère temporale) ou par une donnée convaincante d’imagerie.Formes atypiques
Il peut arriver que le diagnostic d’artérite à cellules géantes soit plus difficile à évoquer. En effet, aucune manifestation clinique n’est présente chez 100 % des patients et chacune d’entre elles peut être au premier plan et/ou s’associer à d’autres.L’artérite à cellules géantes doit rester une hypothèse à envisager systématiquement devant tout patient de plus de 50 ans qui présente un syndrome général isolé, associé à un syndrome inflammatoire. On parle alors de formes d’artérite à cellules géantes « systémiques », « extracéphaliques », ou « extracrâniennes », qui peuvent comporter des signes d’atteinte inflammatoire des artères de gros calibre, touchant alors volontiers des patients un peu plus jeunes, 65 ans en moyenne.
Enfin, les formes « tussigènes », où la toux est au premier plan, sont aussi un piège diagnostique.
Formes compliquées
De manière conventionnelle, le terme « formes compliquées » regroupe les cas d’artérite à cellules géantes avec atteinte oculaire, ainsi que les cas d’artérite à cellules géantes avec atteinte symptomatique ou anévrismale des artères de gros calibre.Examens complémentaires
Biologie
Une anémie inflammatoire, microcytaire, est fréquente, de même qu’une thrombocytose. Une hyperleucocytose à polynucléaires neutrophiles est possible.
Le bilan hépatique peut être discrètement perturbé, notamment sous la forme d’une cholestase anictérique.
Un bilan d’hémostase est à faire avant réalisation de la biopsie d’artère temporale.
Dès lors qu’une corticothérapie est envisagée, un bilan pré-thérapeutique est à prescrire : glycémie, HbA1C, fonction rénale, calcémie, vitamine D.
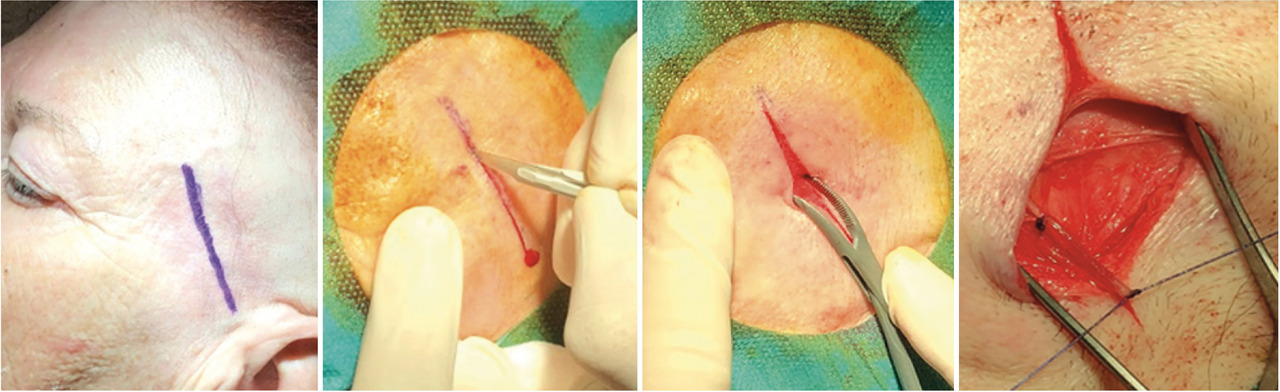
Biopsie d’artère temporale
L’aspect histologique typique est celui d’une pan-artérite giganto-cellulaire, avec un infiltrat inflammatoire fait de cellules mononucléées, prédominant dans la média, associées à des cellules géantes au contact de la média et de l’intima (pathognomonique), à une rupture de la limitante élastique interne, à une hyperplasie intimale, et à des lésions thrombotiques obstructives de la lumière. Il n’y a pas de nécrose fibrinoïde de la paroi vasculaire, à la différence des vascularites nécrosantes comme la péri-artérite noueuse. La présence d’un infiltrat inflammatoire mononucléé de la média et/ou de l’intima est la seule anomalie nécessaire pour conclure au diagnostic d’artérite à cellules géantes.
La biopsie d’artère temporale est positive dans 50 à 70% des cas, mais comme les lésions inflammatoires sont focales, la biopsie d’artère temporale peut être négative, sans que cela ne remette en cause le diagnostic. La réalisation d’une biopsie d’artère temporale controlatérale est alors une option possible. Le diagnostic d’artérite à cellules géantes à biopsie d’artère temporale négative sera retenu avec plus ou moins de certitude selon le degré de conviction clinique, selon les données d’imagerie vasculaire, selon la réponse à la corticothérapie, et enfin selon les données du suivi.
Imagerie vasculaire
Imagerie des artères temporales
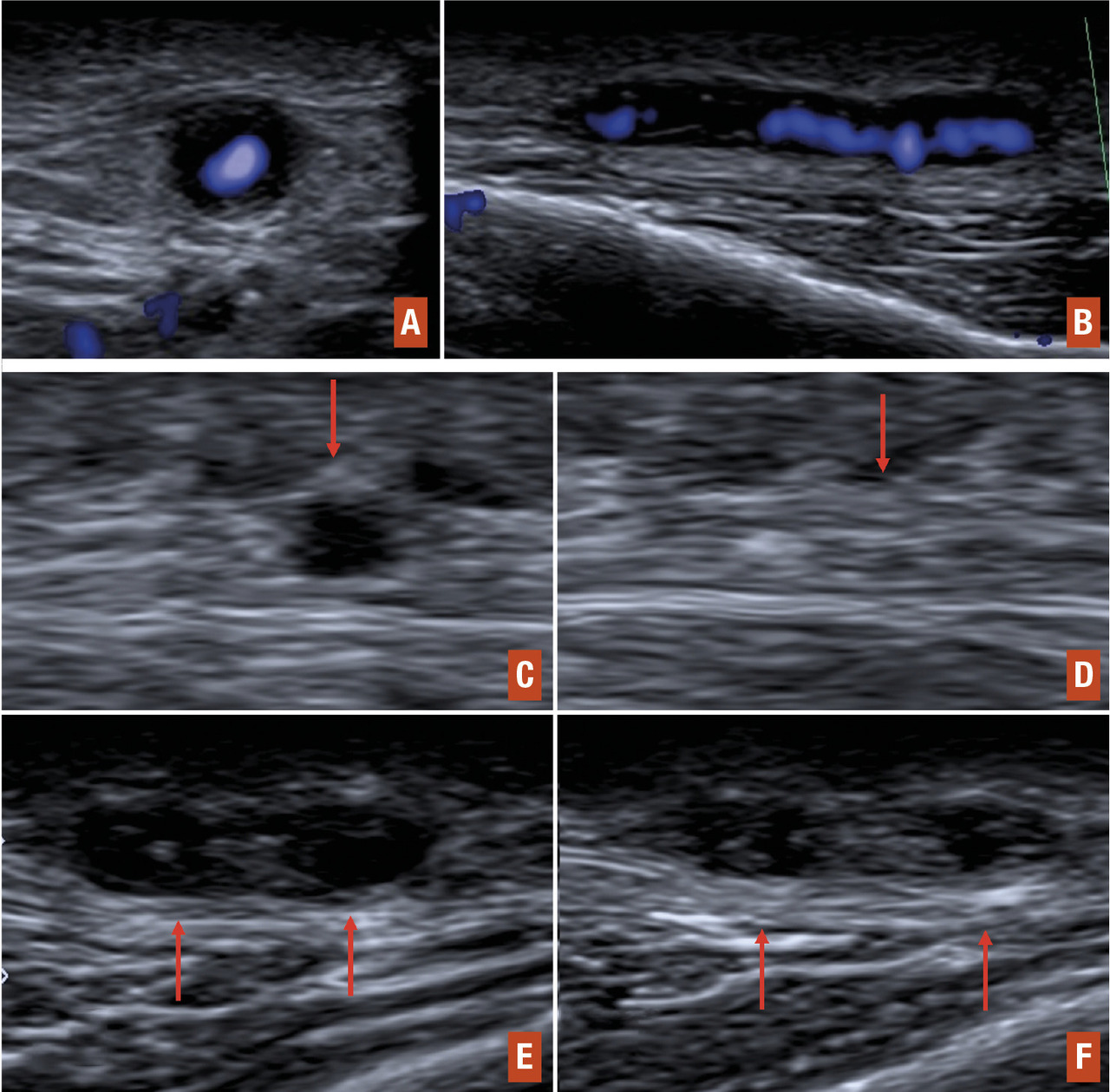
L’examen par écho-Doppler des artères temporales, s’il est effectué par un opérateur expérimenté, apparaît désormais comme un outil non invasif performant pour le diagnostic d’artérite à cellules géantes (L’avantage de l’écho-Doppler est qu’il permet dans le même temps de rechercher un signe du halo au niveau d’autres artères (occipitales, faciales, axillaires, sous-clavières, carotides).
L’imagerie par résonance magnétique (IRM) des artères temporales est un examen performant pour diagnostiquer une inflammation, mais reste d’accès difficile.
Imagerie de l’aorte
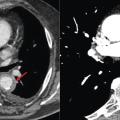
La recherche d’une aortite est recommandée chez tout patient ayant une artérite à cellules géantes. il peut en effet exister des lésions inflammatoires de l’aorte (40 % des cas), parfois associées à une dilatation voire un anévrisme de l’aorte (Par ailleurs, en cas d’étiologie incertaine (par exemple, présentation clinique atypique, biopsie d’artère temporale négative, absence d’artérite temporale sur l’écho-Doppler), ces examens peuvent avoir une contribution significative à l’enquête diagnostique. Ainsi, la mise en évidence d’une aortite par l’un de ces examens peut permettre au clinicien de retenir prioritairement le diagnostic d’artérite à cellules géantes (
Il faut rappeler néanmoins que dans certains cas, il peut être difficile de distinguer formellement une atteinte inflammatoire spécifique de lésions athéromateuses, qui sont fréquentes à cet âge.
Imagerie des autres artères de gros calibre
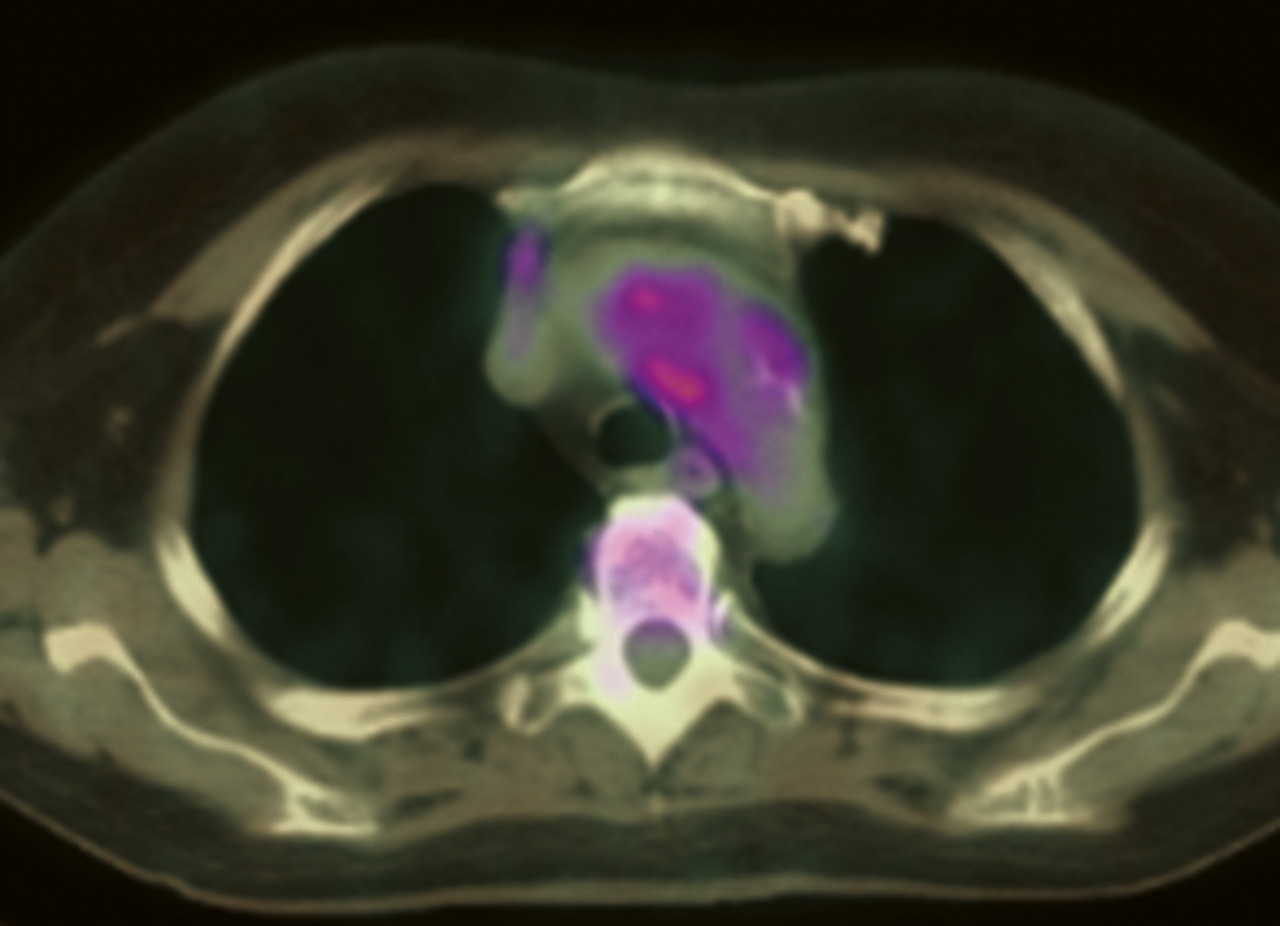
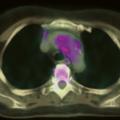
Si un écho-Doppler des artères temporales est fait, il est désormais habituel d’explorer d’autres territoires artériels, comme déjà vu précédemment.Sinon, une exploration des artères de gros calibre sera faite en cas de signe d’appel clinique (abolition d’un pouls, claudication), par écho-Doppler, angio-IRM, angio-TDM, ou TEP-TDM. Il faut noter qu’au moins 1 de ces 3 derniers examens sera de toutes façons déjà réalisé pour rechercher une aortite. La 18-FDG TEP-TDM est intéressante de ce point de vue car elle permet de visualiser des hypermétabolismes d’origine inflammatoire, tant au niveau de l’aorte (
Enfin, comme signalé plus haut pour l’aortite, la mise en évidence d’un aspect d’artérite inflammatoire des artères de gros calibre, sur un examen d’imagerie, peut contribuer à l’enquête diagnostique (
Exploration ophtalmologique
Prise en charge thérapeutique
Corticothérapie
Phase initiale
La corticothérapie à forte dose représente la pierre angulaire du traitement d’attaque de l’artérite à cellules géantes. Elle doit être instaurée en urgence absolue en cas de signes visuels. Typiquement, cette corticothérapie est efficace de manière rapide et spectaculaire, notamment sur les signes céphaliques et l’état inflammatoire qui s’améliorent de manière significative en 48-72 heures.Devant une artérite à cellules géantes non compliquée, le traitement par prednisone est débuté à la dose de 0,7 mg/kg/j par voie orale en une seule prise le matin. Devant une forme compliquée (atteinte oculaire, atteinte symptomatique des artères de gros calibre), la dose initiale de prednisone est celle de 1 mg/kg/j. Des bolus IV de méthylprednisolone, pendant 1 à 3 jours, sont généralement prescrits en cas d’atteinte oculaire. En cas d’administration de bolus, les doses quotidiennes de méthylprednisolone sont variables, allant de 250 mg à 15 mg/kg (sans dépasser 1 000 mg), en tenant compte de l’âge et des comorbidités, notamment cardiovasculaires. Une kaliémie et un ECG sont à faire avant chaque bolus.
Phase de décroissance
La dose initiale de prednisone est maintenue jusqu’à la normalisation de la CRP, soit 10 à 15 jours généralement. La corticothérapie est ensuite réduite progressivement, pour arriver à 50 % de la dose initiale à 4-6 semaines de l’initiation. Vient ensuite une phase de décroissance plus progressive de la corticothérapie, en visant les objectifs de doses quotidiennes de prednisone suivants : 15-20 mg à 3 mois, 10 mg à 6 mois, 7,5 mg à 9 mois, 5 mg à 12 mois. Ces paliers sont indicatifs, et chaque baisse de dose ne peut s’envisager qu’en cas de rémission clinique.Sevrage
Chez un patient stable et en rémission prolongée sous 5 mg/j de prednisone, un sevrage sera tenté, en réduisant très progressivement la dose, de 1 mg toutes les 4 semaines. Cette réduction très progressive permet d’identifier une éventuelle dose « seuil » à partir de laquelle l’artérite à cellules géantes rechute, mais elle permet aussi de réduire le risque d’insuffisance surrénalienne. Différentes attitudes sont possibles pour tenter de gérer au mieux ce risque (Mesures associées à la corticothérapie
Les complications immédiates principales, dès l’initiation de la corticothérapie, sont l’HTA, le diabète cortico-induit, les manifestations neuropsychiques (insomnies, tremblements, troubles psychiatriques), et parfois, une hypokaliémie. Elles peuvent survenir de novo, ou préexister au diagnostic d’artérite à cellules géantes et être décompensées à l’occasion de la corticothérapie. La corticothérapie prolongée expose également à d’autres complications, souvent plus tardives. Il s’agit du risque infectieux, du risque d’ostéoporose cortico-induite, de la prise de poids (souvent liée à une hyperphagie), de la myopathie cortisonique, des complications oculaires (cataracte, glaucome), de l’atrophie cutanée ou encore de l’ostéonécrose des têtes fémorales ou humérales. La prévention de ces complications passe avant tout par le souci constant de réduire autant que possible la dose cumulée de corticoïdes.
Traitements d’épargne cortisonique utilisés
Tocilizumab
Le tolicizumab est un anticorps monoclonal qui neutralise le récepteur de l’interleukine-6 (IL-6). Cet agent biologique (biothérapie) a obtenu récemment une autorisation de mise sur le marché (AMM) pour le traitement de l’artérite à cellules géantes. Il est administré par voie sous-cutanée à la dose de 162 mg par semaine, et sa prescription ne peut se faire qu’après un avis spécialisé.Le plus souvent, ce traitement est utilisé en deuxième ligne, dans certains cas de cortico-dépendance avérée à un niveau ≥ 7,5 mg/j de prednisone, ou encore en cas d’effet indésirable grave de la corticothérapie. Il peut être également envisagé dès la phase d’attaque si le clinicien juge que la corticothérapie est à haut risque d’une mauvaise tolérance et que l’épargne cortisonique représente à l’évidence un enjeu majeur. C’est par exemple le cas s’il existe un diabète compliqué mal équilibré, une dépression ou une psychose sévère, une ostéoporose fracturaire sévère, une hypertension artérielle sévère. Si le tocilizumab est utilisé dès la phase d’attaque, c’est en association avec la corticothérapie, mais la durée de celle-ci sera courte, en visant un sevrage à 6 mois.
La durée optimale de traitement par tocilizumab n’est pas bien établie. Après 12 mois de traitement, des rechutes sont possibles, motivant sa reprise.
Méthotrexate
Le méthotrexate est l’autre traitement pouvant être utilisé dans un but d’épargne cortisonique, et il doit être discuté dans les mêmes circonstances que celles évoquées précédemment avec le tocilizumab. Il peut être prescrit par voie orale ou sous-cutanée, à la dose habituelle de 0,3 mg/kg/semaine, le plus souvent entre 10 et 15 mg/semaine, à adapter à la tolérance.Autres traitements d’épargne cortisonique
Ils sont à discuter au cas par cas, très rarement, et sur avis spécialisé, en cas de corticodépendance à un haut niveau et d’échec, de contre-indication ou d’intolérance du tocilizumab et du méthotrexate. Il peut s’agir d’un autre immunosuppresseur (cyclophosphamide, azathioprine) ou d’une autre biothérapie (abatacept).Autres aspects de la prise en charge thérapeutique
Antiagrégant plaquettaire
Un traitement par aspirine à la dose de 75 à 300 mg/j est indiqué pendant la phase initiale chez les patients ayant une artérite à cellules géantes avec atteinte oculaire. Ce traitement est généralement interrompu au bout de 4 à 6 semaines.Chez les autres patients, ce traitement n’est pas systématique, sauf indication autre, en tenant compte des facteurs de risque cardiovasculaire, qui sont fréquents au sein de cette population.
Héparine de bas poids moléculaire (HBPM)
Un traitement par HBPM à dose préventive (énoxaparine SC, 4 000 UI/j) est volontiers prescrit à la phase initiale, pour prévenir la thrombose veineuse profonde, chez les patients âgés peu ambulatoires.Contrôle des facteurs de risque cardiovasculaire
Les événements cardiovasculaires sont fréquents, et tous les facteurs de risque de maladie athéromateuse doivent être contrôlés de manière stricte.Chirurgie vasculaire
Les dissections aortiques sont prises en charge en urgence selon les protocoles chirurgicaux habituels (endoprothèse ou remplacement de l’aorte). Le traitement endovasculaire ou chirurgical des anévrismes de l’aorte (diagnostiqués le plus souvent au cours du suivi) s’envisage idéalement une fois que le syndrome inflammatoire biologique est bien contrôlé. Il en est de même pour les rares cas où un geste de revascularisation doit être réalisé sur une artère périphérique.Éducation thérapeutique
Dans ce contexte de maladie inflammatoire chronique et de corticothérapie prolongée, l’éducation thérapeutique constitue un complément utile, voire indispensable, dans la prise en charge des patients. L’aide d’associations de patients ne doit pas non plus être négligée.Suivi du patient
Consultations de suivi
Ces consultations permettent de s’assurer de l’absence de signes d’activité d’artérite à cellules géantes, de rechercher tout signe d’atteinte des artères de gros calibre, et d’identifier toute manifestation d’intolérance du traitement (
Surveillance du bilan inflammatoire
Surveillance des artères de gros calibre
L’artérite à cellules géantes s’accompagne d’un surrisque d’anévrisme de l’aorte, notamment de l’aorte thoracique, et ces lésions morphologiques sont parfois diagnostiquées plusieurs années après le diagnostic initial (
En dehors de ces cas, les examens d’imagerie vasculaire sont également à envisager au cours du suivi quand apparaît un signe d’appel, quand surviennent des rechutes multiples ou encore devant la reprise persistante et inexpliquée d’un syndrome inflammatoire.
Rechutes
L’artérite à cellules géantes est une maladie qui rechute fréquemment, 40 % des patients font au moins 1 rechute, le plus souvent lors de la phase de décroissance lente de la corticothérapie, quand la dose quotidienne de prednisone se situe entre 5 et 15 mg/j.
En cas de rechute, il convient de remettre le patient à la dose de prednisone correspondant au palier antérieurement efficace, à conserver plus longtemps, avant de tenter à nouveau une décroissance prudente.
En cas de rechutes multiples (plus de 2 rechutes), la corticothérapie à la dose efficace devra être maintenue. Si cette dose est < 7,5 mg/j, ce traitement peut être maintenu sur le long terme, parfois à vie, selon l’âge et la tolérance. Si cette dose est ≥ 7,5 mg/j et/ou si la corticothérapie est mal tolérée, un traitement d’épargne cortisonique sera envisagé, soit le tocilizumab (ayant l’AMM), soit le méthotrexate.
Il peut arriver que les patients rechutent à distance de l’arrêt de la corticothérapie, après avoir été considérés comme guéris. La reprise d’une corticothérapie à forte dose peut être nécessaire en traitement d’attaque, mais il est logique d’introduire précocement un traitement d’épargne cortisonique.
Conclusion
POINTS FORTS À RETENIR
L’artérite à cellules géantes, qui touche le sujet > 50 ans et la maladie de Takayasu (aorto-artérite de la femme jeune, très rare) sont les 2 maladies qui constituent le groupe des vascularites primitives des artères de gros calibre.
La pseudo-polyarthrite rhizomélique est un rhumatisme inflammatoire des ceintures, touchant surtout les épaules, chez le sujet >50 ans, et qui se traite par une corticothérapie prolongée avec une dose d’attaque de 12,5 à 25 mg/j de prednisone. La pseudo-polyarthrite rhizomélique est présente chez 40 % des patients au moment du diagnostic d’artérite à cellules géantes.
La présentation typique de l’artérite à cellules géantes comporte des céphalées inhabituelles, des signes généraux, un syndrome inflammatoire marqué, éventuellement associé(s) à une pseudo-polyarthrite rhizomélique et/ou une neuropathie optique ischémique antérieure aiguë.
L’artérite à cellules géantes peut se présenter de manière plus atypique, sans signes céphaliques, mais avec un état inflammatoire et fébrile isolé, ou associé à des signes d’artérite inflammatoire des artères de gros calibre, notamment une aortite.
Le pronostic de l’artérite à cellules géantes est dominé par le risque d’amaurose définitive, qui est souvent inaugurale, et qui est le plus souvent secondaire à une neuropathie optique ischémique antérieure aiguë.
Le diagnostic de certitude d’artérite à cellules géantes ne peut être affirmé qu’avec la biopsie de l’artère temporale, qui montre typiquement une pan-artérite inflammatoire, avec une média infiltrée de cellules mononuclées, des cellules géantes au contact de l’intima et de la média, une rupture de la limitante élastique interne, et une hyperplasie intimale.
L’écho-Doppler des artères temporales, aux mains d’opérateurs entraînés, est un moyen performant pour le diagnostic d’artérite à cellules géantes.
En l’absence de preuve d’atteinte de l’artère temporale (biopsie de l’artère temporale, écho-Doppler), une preuve d’atteinte inflammatoire au niveau des artères de gros calibre, notamment l’aorte, peut être obtenue par une imagerie vasculaire (angio-TDM, IRM, 18-FDG TEP-TDM, écho-Doppler).
Chez tout patient ayant une artérite à cellules géantes, la recherche d’une aortite est indiquée, cette atteinte pouvant être source de complications, notamment des anévrismes de l’aorte thoracique, habituellement diagnostiqués après plusieurs années de suivi.
Le traitement de l’artérite à cellules géantes repose sur la corticothérapie à forte dose, avec une dose initiale de prednisone de 0,7 mg/kg/j dans les formes simples, et de 1 mg/kg/j dans les formes compliquées (atteinte oculaire, atteinte symptomatique des artères de gros calibre).
En cas de rechutes multiples à une dose de prednisone ≥ 7,5 mg/j, ou en cas de mauvaise tolérance de la corticothérapie, un traitement d’épargne cortisonique est à envisager, soit par tocilizumab (AMM), soit par méthotrexate.
Artérite à cellules géantes
Une situation clinique de fièvre prolongée, ou d’altération de l’état général d’allure isolée, chez un sujet de plus de 50 ans, volontiers 70 à 75 ans, peut être le point de départ d’un dossier pour tester différentes hypothèses diagnostiques dont l’artérite à cellules géantes (ACG). À cet âge-là, il faut avoir en tête que tout syndrome inflammatoire isolé d’allure subaiguë/chronique, ainsi qu’une anémie microcytaire inflammatoire doivent conduire à en évoquer rapidement le diagnostic. Il peut être demandé de reconnaître les différents éléments de l’interrogatoire, de l’examen clinique, du bilan biologique de première intention, permettant d’étayer l’hypothèse d’une ACG.
Le point de départ d’un dossier peut aussi être une présentation classique, avec des signes céphaliques d’emblée évocateurs, ou bien être une pseudopolyarthrite rhizomélique, avec survenue progressive d’éléments amenant à suspecter une ACG.
La stratégie diagnostique peut faire également l’objet de questions, en gardant à l’esprit que la biopsie d’artère temporale est l’examen de référence, mais qu’elle peut être négative. Des documents d’imagerie vasculaire peuvent être présentés (image d’aortite en angio-TDM p. ex.), révélant des éléments qui peuvent aller en faveur, ou en défaveur, du diagnostic d’ACG.
Un dossier peut aussi décrire la survenue d’une neuropathie optique ischémique antérieure aiguë, qui peut être soit le motif initial d’admission, soit survenir rapidement alors que le patient est hospitalisé pour enquête diagnostique. Il faudra alors avoir en tête l’urgence de la situation, les examens complémentaires diagnostiques ne devant en aucun cas retarder la mise en route d’une corticothérapie.
Des questions aborderont certainement la prise en charge thérapeutique, la corticothérapie à forte dose avec les posologies initiales de prednisone, la conduite globale du traitement, les risques inhérents à cette corticothérapie, et les mesures associées qu’il faut envisager. Un dossier peut également aborder les rechutes de l’ACG, ou les effets secondaires graves de la corticothérapie, devant faire discuter alors un traitement d’épargne cortisonique (tocilizumab, méthotrexate).
Parmi les effets secondaires graves de la corticothérapie, il pourrait notamment s’agir d’une complication infectieuse (cf. item 187, Fièvre chez un patient immunodéprimé), de la survenue d’un diabète cortico-induit (cf. item 245, Diabète sucré de types 1 et 2 de l’enfant et de l’adulte) ou d’une ostéoporose fracturaire (cf. item 124, Ostéopathies fragilisantes).

 Encadrés
Encadrés