L’asthme est la maladie chronique infantile la plus fréquente ; elle débute souvent chez le nourrisson à la suite d’agressions virales. Une participation allergique doit être systématiquement recherchée car elle modifie la prise en charge. La gestion de la crise doit conduire à la rédaction d’un plan d’action pour les parents. Une activité sportive est possible et encouragée. L’éducation fait partie intégrante du parcours thérapeutique, notamment pour la prise correcte des traitements inhalés. Le contrôle de l’asthme, c’est-à-dire l’absence de symptômes, est le but visé par les traitements de fond. La disponibilité d’anticorps monoclonaux ciblant des phénotypes particuliers enrichit les possibilités thérapeutiques.
Une définition qui fait consensus
L'asthme correspond à l’association de symptômes respiratoires – tels que respiration sifflante, essoufflement, oppression thoracique et toux, variables dans le temps et en intensité – à une limitation variable du débit expiratoire. Cette définition, proposée par le groupe Global Initiative for Asthma en 2022, fait l’objet d’un consensus d’experts.1
Attention aux diagnostics différentiels !
Succédant souvent à une bronchiolite virale, l’asthme du nourrisson est fréquent et parfois difficile à traiter. Son diagnostic est essentiellement clinique, reposant sur la survenue d’épisodes de sifflements (au moins deux durant les douze derniers mois) ou de gêne respiratoire, sans épisode infectieux associé.
La radiographie thoracique est le seul examen complémentaire indispensable avant d’envisager un traitement de fond prolongé.
Les diagnostics différentiels, résumés dans le tableau 1, doivent être éliminés. L’absence de symptômes intercritiques et de retentissement sur l’état général (notamment la croissance staturopondérale) sont des arguments puissants en faveur du diagnostic.
La prise en charge repose sur l’administration à la demande de bêta- 2 -mimétiques et l’utilisation des corticostéroïdes inhalés en traitement de fond.
Bilan de l’enfant asthmatique
La première étape est diagnostique : pour s’assurer qu’il s’agit bien d’un asthme, il est essentiel d’éliminer tout autre maladie en lien avec une toux chronique, y compris chez les grands enfants et adolescents. Une radiographie thoracique réalisée de face est l’examen indispensable permettant d’écarter d’autres diagnostics.
Dès l’âge de 3 - 4 ans, une exploration fonctionnelle respiratoire permet d’apporter des informations complémentaires sur l’importance de l’obstruction bronchique et sa réversibilité.
Le dépistage d’un terrain allergique fait partie intégrante du bilan à réaliser. L’enquête allergologique repose en premier lieu sur un interrogatoire précis et peut être complétée par des tests de dépistage du terrain allergique. Dans ce cas, il faut privilégier les tests à réponse positive et négative, comme le Phadiatop (allergie aux pneumallergènes), qui a une bonne valeur prédictive – à nuancer néanmoins en fonction de la zone géographique concernée. On peut également demander le dosage d’immunoglobulines (IgE) spécifiques vis-à-vis des allergènes de l’environnement (5 au maximum). La confirmation d’une participation allergique modifie la prise en charge tant préventive (gestion des accès prévisibles, comme l’asthme pollinique) que curative (ajout de médicaments spécifiques en cas d’asthme mal contrôlé).
Gestion de la crise et plan d’action
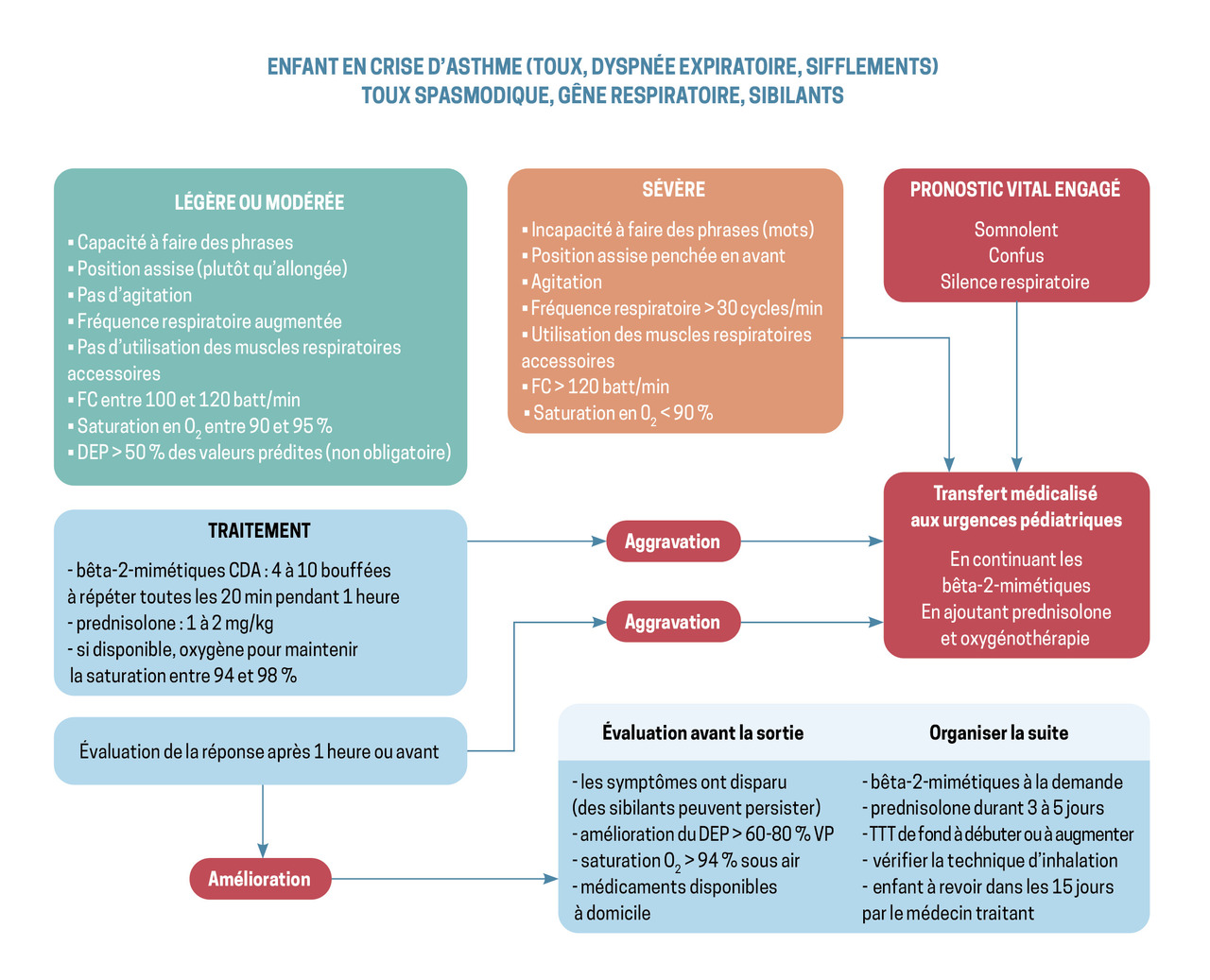
La toux spasmodique, la gêne respiratoire, les sifflements et l’oppression thoracique doivent conduire à l’utilisation des bêta- 2 -mimétiques par voie inhalée. Ce traitement des accès est bien codifié (figure). Il repose sur l’appréciation de la gravité de la crise et l’utilisation systématique des bêta- 2 -mimétiques, associée aux corticoïdes par voie orale selon l’intensité. L’analyse objective de la fréquence respiratoire, de l’existence ou non d’un tirage intercostal, de la saturation en oxygène complète cette évaluation. Un silence auscultatoire est préoccupant.
Le comportement de l’enfant est important à observer, en particulier sa capacité à s'exprimer clairement.
L’administration des bronchodilatateurs se fait toutes les vingt minutes au cours de la première heure et doit, dans la majorité des cas, améliorer la situation.
Le traitement des crises nécessite une éducation des parents à la reconnaissance des principaux signes. Un protocole écrit en cas de crise – appelé plan d’action – doit être remis et expliqué aux parents. La posologie, le maniement des chambres d’inhalation ou des dispositifs inhalés doivent être énoncés et vérifiés lors de chaque consultation.
Traitement de fond : clé de voute du contrôle de l’asthme
Deux impératifs
Le traitement de fond est indiqué, quel que soit l’âge de l’enfant, quand l’asthme retentit sur la qualité de vie. Il repose sur l’établissement de paliers en fonction du contrôle ou non de l’affection (encadré). Le but est avant tout le contrôle total de l’asthme, c’est-à-dire l’absence de symptômes. Pour cela, la gestion de l’environnement domestique est essentielle (pollution aux composés organiques volatils, inhalation de fumée de tabac, allergènes, type de chauffage…), même s’il n’est pas toujours facile de changer les habitudes familiales.
Le maniement des dispositifs des traitements inhalés est le deuxième impératif. Avant 4 ans, la priorité est donnée aux chambres d’inhalation avec masque, puis sans. À partir de 6 ans, selon l’aptitude de l’enfant, on peut opter pour un inhalateur déclenché par l’inspiration. Par ailleurs, l’emploi d’un aérosol-doseur (spray) est plus complexe et est responsable de plus d’effets indésirables locaux (avec les corticoïdes inhalés). Le choix du système de délivrance des traitements inhalés entre 6 et 12 ans dépend des préférences de l’enfant pour un système donné, de ses capacités à inhaler correctement le traitement via ce système et du choix des principes actifs disponibles avec le système choisi. La prescription d’un aérosol-doseur pressurisé avec chambre d’inhalation et embout buccal reste préférable, mais les systèmes avec poudre peuvent aussi être intéressants. La démonstration répétée de l’utilisation correcte du système au fil des consultations est indispensable. Il est par ailleurs préférable d’harmoniser les systèmes d’inhalation prescrits pour le traitement de fond et celui de la crise afin de limiter au minimum les erreurs techniques.
Un traitement de fond adapté à l’âge de l’enfant
On distingue trois catégories d’âge concernant les classes thérapeutiques : avant 4 ans, de 4 à 11 ans et 12 ans et plus.
Avant 4 ans : deux options
Chez le petit enfant, deux classes sont utilisables : les corticostéroïdes inhalés (CSI) et un antileucotriène (le montélukast). L’utilisation d’une dose faible de CSI (tableau 2) est l’option à privilégier pour une durée minimale de trois mois. Souvent, elle couvre toute la période hivernale et printanière. L’escalade thérapeutique doit faire orienter vers le spécialiste.
Traitements combinés possibles à partir de 4 ans
À partir de 4 ans, l’utilisation de traitements combinés devient possible, associant un bronchodilatateur de longue durée d’action (BDLA) [type formotérol ou salmétérol] et un CSI en traitement continu à faible dose. Des études utilisant cette combinaison (BDLA + CSI) en traitement d’entretien et de secours ont été publiées, avec des résultats encourageants, mais ne font pour l’heure l’objet d’aucune recommandation en France. L’instauration de ce type d’association thérapeutique nécessite de bien en expliquer le principe aux parents, qui doivent arriver à distinguer la place des bêta- 2 -mimétiques de courte durée d’action par rapport à ce schéma d’adjonction du traitement combiné à la demande.
Au-delà de 6 ans : les biothérapies !
Entre 6 et 12 ans, des biothérapies sont désormais disponibles (omalizumab, dupilumab, mépolizumab). Chez les plus de 12 ans, l’observance thérapeutique est la clé du succès. En effet, avec l’âge, la scolarité et l’indépendance, il faut privilégier un traitement nécessitant le minimum d’administrations par jour.
Une quatrième biothérapie, le tézépélumab, est maintenant disponible à partir de 12 ans.
Essor des biothérapies grâce au phénotypage de l’asthme
L’asthme est une affection hétérogène. Chez l’enfant, il existe des différences évolutives et certaines caractéristiques, depuis longtemps établies, comme l’existence d’un terrain atopique dans la majorité des cas.
Depuis quelques années, grâce aux progrès de la biologie, est apparu le concept de phénotypage de la maladie, permettant de s’approcher au plus près de la physiopathologie et de proposer un traitement ciblé.2 Un phénotype se définit par l’ensemble des caractéristiques observables d’un individu résultant de l’interaction de son patrimoine génétique avec l’environnement. Pour le déterminer, un interrogatoire minutieux (antécédents familiaux et personnels) doit être mené, complété d’examens biologiques simples, comme l’éosinophilie sanguine. D’autres examens plus invasifs sont parfois nécessaires, mais ils s’adressent aux asthmes sévères.
Il est ainsi possible de distinguer des asthmes dont l’inflammation est essentiellement éosinophilique, purement neutrophilique ou mixte.
Les anticorps monoclonaux élargissent le panel thérapeutique
L’asthme est une maladie inflammatoire mettant en jeu une cascade d’événements biologiques déclenchés par la réaction de la muqueuse respiratoire à des agresseurs bien connus (virus, allergènes, polluants domestiques ou urbains, tabac…). Il s’ensuit une stimulation immunologique intense qui fait intervenir les cellules lymphocytaires innées (ILC2,3) les lymphocytes T, B et une série d’interleukines (IL- 4, 5, 13, 17, 33, Thymic Stromal Lymphopoietin [TSLP]) qui amplifient les réactions en stimulant les cellules effectrices, parmi lesquelles les éosinophiles et les mastocytes jouent un rôle essentiel.
L’asthme sévère ne répondant pas au traitement conventionnel est heureusement rare chez l’enfant (moins de 5 % des patients asthmatiques). Différents phénotypes d’asthme sévère existent, distingués par leur caractère allergique pur (hyperimmunoglobulinémie E, hyperéosinophilie sanguine) ou non allergique (absence d’éosinophilie, prédominance des neutrophiles) et histologique (épaississement de la membrane basale, notamment). Des anticorps monoclonaux humanisés ou humains ont été développés pour essayer de répondre à ces phénotypes.3
Quatre médicaments sont actuellement disponibles en France (omalizumab, mépolizumab, dupilumab, tézépélumab). Ils sont administrés par voie sous-cutanée à un rythme mensuel le plus souvent. Le recul le plus important concerne l’omalizumab (Xolair), qui a révolutionné l’approche thérapeutique des asthmes sévères allergiques, surtout chez les enfants polysensibilisés, permettant le plus souvent une épargne des corticoïdes et une stabilisation de l’asthme. Les trois autres médicaments sont plus récents mais ouvrent des perspectives intéressantes, notamment le dupilumab, utilisable également en cas de dermatite atopique sévère.
Quand passer la main ?
Un asthme léger répondant bien au traitement doit être suivi par le médecin traitant.
Cependant, il existe des circonstances qui exigent un avis complémentaire. Il en est ainsi lorsque le diagnostic est remis en cause par une symptomatologie atypique : toux isolée, stridor associé, mauvaise croissance staturopondérale, réponse imparfaite aux bêta- 2 -mimétiques de courte durée d’action. Des examens invasifs sont alors parfois nécessaires, comme l’endoscopie bronchique.
La recherche d’un terrain allergique peut être effectuée par le médecin généraliste. Si celle-ci se révèle positive, il est utile d’avoir une expertise allergologique plus complète pour faire la part entre sensibilité et allergie.
Une exploration fonctionnelle respiratoire est un examen incontournable permettant d’apprécier la sévérité de l’obstruction bronchique. Elle peut être effectuée dans un laboratoire d’exploration fonctionnelle à la demande du médecin traitant. Néanmoins, il est souvent préférable d’adresser le patient une première fois à un médecin spécialiste (pneumopédiatre de préférence) pour effectuer ce bilan initial, dont les conclusions, comprenant la conduite thérapeutique et le rythme de surveillance, sont communiquées au médecin traitant.
Dans le cas d’une évolution défavorable malgré un traitement bien conduit, le recours à un avis complémentaire, en particulier pour décider de l’escalade thérapeutique et de l’utilisation éventuelle d’anticorps monoclonaux, est indispensable.
Quel suivi et à quel rythme ?
Le suivi d’un asthmatique doit être adapté en fonction de la sévérité de la maladie. Un minimum d’une consultation annuelle chez le médecin traitant est indispensable pour apprécier l’évolution.
Dès qu’un traitement de fond est envisagé, il est nécessaire de faire un point régulier pour savoir si le traitement est adapté. Un rythme trimestriel est alors une proposition qui permet de fixer des objectifs, d’apprécier l’observance, de diminuer ou d’augmenter la charge thérapeutique en fonction des résultats.
L’évaluation de la fonction respiratoire nécessite un contrôle au moins annuel.
Durant le suivi, le recours au pneumopédiatre permet de répondre précisément aux questions qui se posent : peut-on interrompre le traitement ? n’est-il pas nécessaire d’entreprendre une désensibilisation devant le caractère de plus en plus allergique d’un patient ? etc.
Éducation thérapeutique et hygiène de vie
Ce qu’il est possible de faire au cabinet de médecine générale
Un médecin traitant est souvent confronté à un dilemme non encore résolu : concilier une prise en charge optimale en respectant un temps de consultation très contraint. Il est ainsi difficilement possible d’intégrer un programme d’éducation quand on connaît le caractère chronophage d’une telle démarche au sein de services spécifiques développés généralement en centre hospitalo-universitaire.
Néanmoins, à chaque consultation, des points spécifiques peuvent être vérifiés :
- demander à la famille comment elle utilise les thérapeutiques inhalées (le mieux est que l’enfant vienne avec son dispositif) ;
- interroger sur l’emploi des bêta- 2 -mimétiques lors des accès de toux notamment ;
- anticiper le questionnement sur les effets indésirables des médicaments, en particulier les corticoïdes inhalés, pour améliorer l’observance thérapeutique.
Asthme et sport : non seulement compatible mais recommandé !
Maintenir une activité physique chez l’enfant asthmatique est essentiel pour éviter un déconditionnement, source d’incapacité et de surcharge pondérale.
Seule la plongée avec bouteille nécessite une évaluation rigoureuse, en raison des risques d’accident de décompression ou de la survenue d’une crise d’asthme en profondeur (pour beaucoup de médecins, ce sport est absolument contre-indiqué tant que l’asthme n’est pas contrôlé sur une longue période).
Tous les autres sports sont possibles en privilégiant autant que possible les sports d’intérieur, moins générateurs de bronchospasme induit par l’exercice. Pour les sports de course ou d’endurance, la prise d’un bêta- 2 -mimétique avant l’effort prévisible est encouragé. Dans tous les cas, un échauffement est fortement conseillé.
Le projet d’accueil individualisé (PAI) fait partie intégrante de la prise en charge
Le PAI a changé en 2021, avec la mise en place de documents nationaux, valables dans tous les établissements scolaires de France. Unique, il comprend trois parties : les deux premiers feuillets (I et II) sont d’ordre administratif (signatures des parents et du personnel de l’école, aménagements et adaptations éventuellement pédagogiques). Le dernier feuillet fait référence à la gestion de la crise d’asthme et à la liaison avec le médecin de l’Éducation nationale.4
Contributions de la désensibilisation et des médecines complémentaires
Désensibilisation : un intérêt si l’allergène influe sur l’évolution de l’asthme
Le phénotype allergique est de loin dominant chez l’enfant.5 Il est donc logique d’essayer d’en diminuer l’impact chez les enfants les plus sensibles ; la désensibilisation, maintenant bien codifiée, en est un des moyens. Elle s’adresse aux patients dont l’asthme est stabilisé par le traitement de fond et pour lesquels on espère tirer un bénéfice mesurable par l’adjonction d’une désensibilisation. Ce sont essentiellement vis-à-vis des pollens de graminées et des acariens qu’elle est proposée car l’impact potentiel de ces allergènes sur l’évolution de l’asthme est bien connu.
Dans tous les cas, elle est indiquée quand il est certain que l’allergène entraîne des conséquences délétères sur l’évolution de l’asthme et non sur la simple positivité des tests allergiques. Cette réalité est à confirmer par l’interrogatoire, ce qui est facile avec les pollens (aggravation durant la saison printanière ou estivale), plus difficile avec les acariens. Pour les trophallergènes – comme l’arachide –, qui peuvent constituer un danger réel pour le patient allergique, une induction de tolérance est fréquemment proposée afin d’en diminuer le risque. Il faut garder à l’esprit que, même si la désensibilisation est maintenant accessible par voie orale ou sublinguale, c’est un traitement long (au moins trois ans) pour lequel il est indispensable de prendre en compte les autres traitements déjà mis en place afin de ne pas trop compliquer la prise en charge.
Y a-t-il une place pour les médecines alternatives et complémentaires ?
Si l’on se fonde sur la médecine par les preuves, il n’y a aucune indication à recourir à l’homéopathie, ou à tout autre médecine alternative, car aucune n’a démontré de résultats probants dans l’évolution d’un asthme infantile.
Plus difficile à trancher est le cas de la médecine thermale et des séjours climatiques : sans avoir une action de facto sur l’évolution d’une affection immunologique, elles peuvent être utilisées à bon escient chez des enfants dont la pathologie ORL est prégnante (soins locaux souvent performants) ou à l’atteinte cutanée sévère nécessitant des soins constants. Beaucoup de ces stations proposent, durant le séjour, de l’éducation thérapeutique, ce qui peut conforter le traitement mis en place. Les séjours climatiques de longue durée s’adressent à des cas particuliers d’asthme sévère, d’enfants non observants, vivant parfois dans des milieux sociaux ou environnementaux difficiles. Plusieurs établissements disposent de la double compétence scolaire et médicale, avec, à leur disposition, une équipe spécialisée permettant un suivi clinique et paraclinique de qualité. Cette indication doit malgré tout rester marginale, car la séparation de longue durée d’un enfant avec sa famille est toujours à prendre en compte.
Enfin, il n’y a évidemment aucune contre-indication aux vaccinations chez l’enfant asthmatique – bien au contraire. En particulier, la vaccination antigrippale est fortement recommandée.
Que dire à vos patients ?
- L’asthme est une maladie fréquente chez l’enfant, quel que soit son âge, et nécessite un suivi régulier.
- Les parents doivent être partie prenante du traitement, savoir gérer les crises et maîtriser les thérapeutiques inhalées.
- Un traitement de fond, durant plusieurs mois, est souvent nécessaire pour arriver à combattre l’inflammation bronchique chronique.
- Les corticoïdes inhalés sont la pierre angulaire de la prise en charge. Leurs effets indésirables sont limités, connus des médecins. Ils ont plus de bénéfices que de risques, parmi lesquels une évolution défavorable vers une bronchopathie chronique obstructive.
- Une évaluation régulière trimestrielle ou annuelle est nécessaire, selon la gravité de l’asthme.
- Il n’y a aucune contre-indication à la vaccination chez l’enfant asthmatique. La vaccination antigrippale est fortement recommandée.
Évaluation du contrôle de l’asthme sur les 4 dernières semaines
Durant les 4 dernières semaines, l’enfant a-t-il eu :
- des symptômes d’asthme plus de 2 fois par semaine ?
- des réveils nocturnes liés à l’asthme ?
- une utilisation de bêta- 2 -mimétiques plus de 2 fois par semaine ?
- une limitation de ses activités liée à l’asthme ?
2. Conrad LA, Cabana MD, Rastogi D. Defining pediatric asthma: Phenotypes to endotypes and beyond. Pediatr Res 2021;90:45-51.
3. Bacharier LB, Jackson DJ. Biologics in the treatment of asthma in children and adolescents. J Allergy Clin Immunol 2023;151:581-9.
4. Lambert N, Wanin S. Asthme, allergies et collectivité : le projet d’accueil individualisé. Rev Prat Med Gen 2022;36(1069):343-50.
5. Rodriguez Del Rio P, Liu AH, Borres MP, et al. Asthma and allergy: Unravelling a tangled relationship with a focus on new biomarkers and treatment. Int J Mol Sci 2022;23:3881.
Dans cet article
- Une définition qui fait consensus
- Attention aux diagnostics différentiels !
- Bilan de l’enfant asthmatique
- Gestion de la crise et plan d’action
- Traitement de fond : clé de voute du contrôle de l’asthme
- Quand passer la main ?
- Quel suivi et à quel rythme ?
- Éducation thérapeutique et hygiène de vie
- Le projet d’accueil individualisé (PAI) fait partie intégrante de la prise en charge
- Contributions de la désensibilisation et des médecines complémentaires

 Encadrés
Encadrés