Larva migrans cutanée (ankylostomose)
La larva migrans est due à une larve d’ankylostome parasitant habituellement des animaux (surtout chiens et chats) : Ancylostoma spp ou Ancylostoma braziliense, le plus souvent en cause, sont endémiques en Amérique intertropicale, Afrique subsaharienne, dans le Sud-Est asiatique et les Antilles ; Uncinaria stenocephala est plus commune en zone tempérée.
Présents dans les excréments de ces animaux hôtes, les œufs d’ankylostomes se développent en larves infectantes dans les sols ou sables chauds et humides. La transmission à l’homme se produit lorsque la peau est en contact avec ces surfaces contaminées et que les larves pénètrent la peau non protégée.
Cette dermatose survient donc souvent au retour d’un voyage en zone tropicale et après de longues marches pieds nus sur la plage ou les sols humides ; c’est la plus fréquente des dermatoses tropicales touchant les voyageurs. Toutefois, quelques cas autochtones en France et en Europe ont été recensés ces dernières années : plus de 50 au total, dont une quinzaine en France, en particulier en Bretagne, où la présence d’un foyer endémique a été discutée, dans le Sud ou encore à Bordeaux.
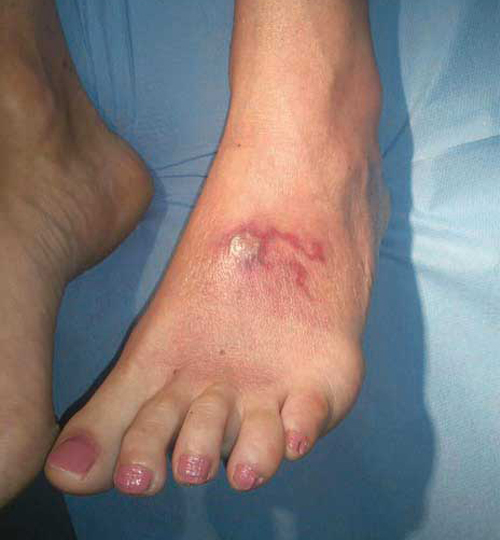
Le diagnostic est clinique : au point de pénétration, une forme de folliculite papulo-pustuleuse peut apparaître, mais le tableau classique est un sillon serpigineux, érythémateux, mobile (pouvant mesurer plusieurs dizaines de centimètres car il persiste alors que la larve a déjà poursuivi sa progression) et extrêmement prurigineux (fig. 1).
Le prurit peut entraîner une eczématisation avec une surinfection, et une impétiginisation.
Ces lésions apparaissent dans les heures ou les jours après l’infestation et peuvent durer plusieurs semaines.
Les examens complémentaires sont peu contributifs : l’éosinophilie est inconstante et le sérodiagnostic est rarement positif au début de l’affection. Diagnostics différentiels : filariose à Loa-Loa, myiase, dermatite rampante à anguillule (larva currens, v. ci-après), dermatite des nageurs à schistosome.
La guérison spontanée peut prendre plusieurs mois. L’inconfort et le risque d’infection bactérienne justifient le traitement : ivermectine per os à la dose de 200 mg/kg en une prise, éventuellement répétée si les troubles persistent.
Strongyloïdose (anguillulose)
Tout comme l’ankylostomose, la strongyloïdose est due à la pénétration transcutanée d’un nématode (Strongyloides stercoralis, également appelé anguillule) dont les larves vivent dans les sols humides contaminés par des selles humaines. À la différence des ankylostomes, l’humain est l’hôte naturel.
Après la pénétration, les larves migrent à travers l’organisme : par voie lymphatique, puis sanguine, elles arrivent au poumon, dans les bronches, la trachée et l’œsophage, pour gagner enfin l’intestin (les vers adultes vivent dans la muqueuse et la sous-muqueuse du duodénum et du jéjunum). En outre, une réinfestation par voie interne est possible (au niveau de l’intestin, les larves assurent l’auto-infestation du malade), ce qui explique les cas d’infestation chronique ou d’hyperinfestation massive chez les immunodéprimés.
Dans près de la moitié des cas, la strongyloïdose est asymptomatique. Dans sa phase aiguë, elle peut se manifester par une éruption urticarienne serpigineuse (larva currens ), une toux, une dyspnée, des symptômes gastro-intestinaux (douleurs et selles molles).
Si ces parasites sont endémiques des régions tropicales et subtropicales (y compris les zones rurales du sud des États-Unis), les strongyloïdoses restent moins fréquentes que les ankylostomoses chez les patients au retour de voyage. Il est surtout important de les dépister (par examens des selles ou tests sérologiques), chez les patients – voyageurs ou migrants – provenant des zones d’endémie lorsqu’ils vont entamer un traitement immunosuppresseur (corticostéroïdes notamment), même de courte durée : toute immunosuppression peut engendrer un syndrome d’hyperinfestation parfois gravissime (sepsis, syndrome de détresse respiratoire aigüe).
Le traitement repose sur l’ivermectine (dont la supériorité a été démontrée par rapport à l’albendazole) : 200 μg/kg 1 fois/j durant 2 jours en cas de sérologie positive ou d’infection chronique. Les cas sévères, chez le sujet immunodéprimé, sont à adresser au spécialiste.
Tungose
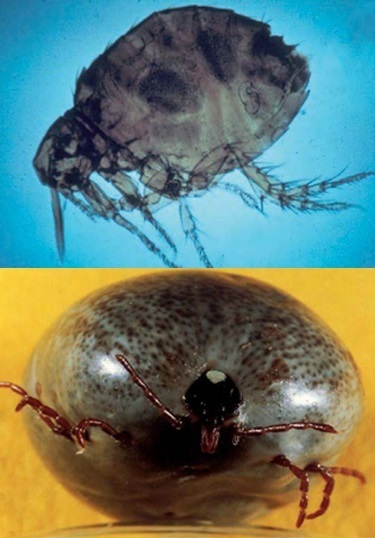
La tungose est une parasitose cutanée causée par l’infestation par la puce de sable femelleTunga penetrans (et T. trimamillata dans certaines zones) ou puce chique, qui pénètre dans la peau et y pond ses œufs (fig. 2). Endémique en Afrique subsaharienne, dans l’océan Indien (Madagascar, Seychelles), au Pakistan et en Amérique intertropicale, cette parasitose est fréquente chez les personnes marchant pieds nus dans le sable, en particulier les enfants. La seule prévention efficace – souvent illusoire – consiste donc à ne pas marcher pieds nus, mais l’application sur la peau de répulsifs à base d’huile de coco, de jojoba et d’aloès semble montrer une certaine efficacité.
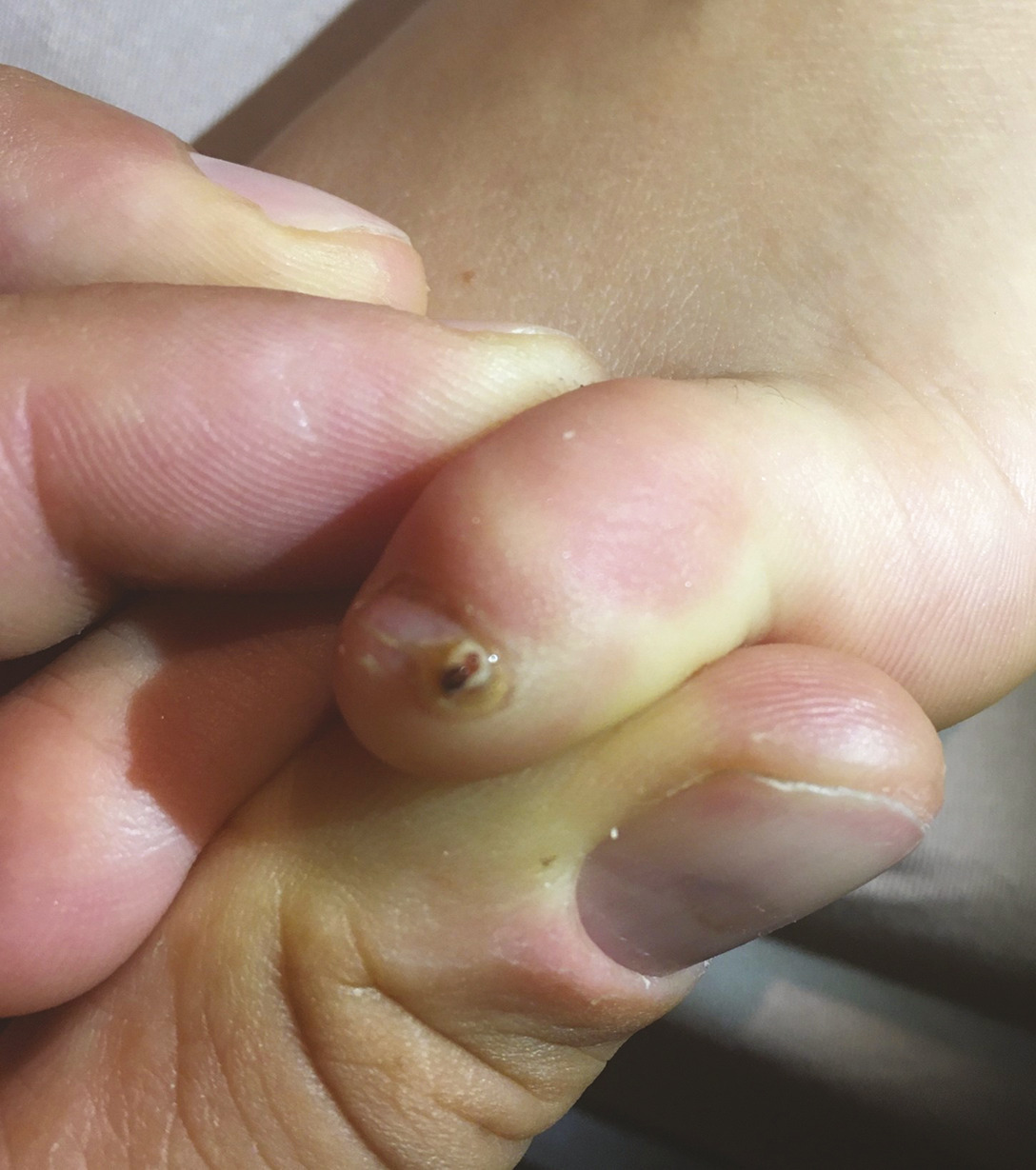
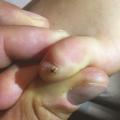
Lors du contact avec le sol, la puce chique se localise, dans la majorité des cas, au pied et essentiellement au niveau du sillon péri-unguéal ou sous-unguéal (fig. 3) ou encore des plis interdigitaux. Cette puce a, en effet, une faible capacité de saut, mais d’autres localisations sont possibles (genoux, cuisses, fesses, mains, coudes) en fonction des habitudes du patient.
L’infestation se manifeste par une tuméfaction enchâssée dans le derme, de couleur blanchâtre, centrée par un point noir (correspondant à l’orifice de ponte), souvent entourée d’une réaction érythémateuse inflammatoire. Pendant la phase aiguë, érythème, œdème, desquamation, douleur et démangeaisons sont constants. Le prurit, induisant le grattage, peut favoriser une surinfection bactérienne. Les abcès sont fréquents.
L’extraction de l’ensemble de la puce chique est le traitement le plus efficace des formes simples, après désinfection soigneuse et avec un vaccinostyle ou une curette, sans blesser le parasite. Si le geste provoque sa rupture, il faut alors pratiquer un curetage du cratère (sous anesthésie locale). Dans les formes profuses, des pansements occlusifs à base de vaseline salicylée à 20 % peuvent être proposés, facilitant l’extraction du parasite après sa mort.
Après l’extraction, il est indispensable de vérifier la vaccination du patient contre le tétanos.
Gastro-entérites
Enfin, si ces risques parasitaires sont surtout liés aux voyages tropicaux, les plages françaises ne sont pas dénuées de risques infectieux. Ceux-ci seraient en particulier d’ordre digestif, selon des études qui ont montré que le sables des plages des climats tempérés contiennent des quantités significatives de pathogènes, notamment d’origine fécale (entérocoques, E. coli…), à des concentrations plus élevées que dans l’eau. Des études américaines ont ainsi trouvé une augmentation des troubles digestifs (gastro-entérites) chez des personnes ayant visité les plages, en particulier les enfants – du fait des jeux tels que les « enterrements » dans le sable…
Ansart S, Desme D, Jaffuel S, et al. Larva migrans cutanée acquise en Bretagne. Rev Prat 2016;66(8):861.
Bourée P, Osse L, Rabenandrasana F. La tungose : une ectoparasitose mal connue. Rev Prat 2009;59(2):163-5.
Vanhecke C, Batsalle B, Girerd R. Tungose. Rev Prat 2021;71(2);171.
OMS. Tungose. 6 novembre 2020.
Merz L. Strongyloïdose : qui est à risque d’infection sévère et comment la prévenir ? Rev Med Suisse 15 avril 2015.
Paris L. Strongyloidiasis.Orphanet, juin 2019.
Korsia-Meffre S. Sur la plage surpeuplée, coquillages et… pathogènes !Vidal 19 juillet 2022.