En France, leur nombre est stable, voire en légère augmentation.
Par Patrice Bourée 1, Pascale Sarrand 2
Appelée aussi fièvre de Malte, c’est une des principales zoonoses dans le monde. Cosmopolite, elle est endémique dans de nombreux pays.
Appelée aussi fièvre de Malte, c’est une des principales zoonoses dans le monde. Cosmopolite, elle est endémique dans de nombreux pays.
Un vaste réservoir animal
Les Brucella sont regroupés en 10 espèces dont 4 (B. melitensis, B. abortus, B. suis et B. canis) sont pathogènes pour l’homme. Ce sont de petits coccobacilles (1 x 0,5 mm), à Gram négatif, immobiles, non capsulés et non sporulés. Le réservoir est important, comprenant les ruminants domestiques (bovins, ovins, caprins) ainsi que les porcins, et accessoirement d’autres animaux (chameaux, lamas, rennes, chamois et même des dauphins). Il existe une relative spécificité d’espèce : les bovins hébergent B. abortus, les ovins et les caprins B. melitensis et les porcins B. suis. En outre, de nouvelles souches ont été isolées chez des babouins (B. papionis), des renards (B. vulpis) ou encore plus récemment chez des patients transplantés ou atteints d’infections pulmonaires (B. inopinata).1
Chez l’animal, la maladie est le plus souvent asymptomatique, ne se manifestant que par une atteinte des organes génitaux (orchite, avortements). La bactérie peut coloniser les glandes mammaires et contaminer le lait.
La transmission à l’homme est soit directe, par contact avec les animaux infectés et les produits d’avortements, tels que placentas, sécrétions génitales, litières (professions particulièrement exposées : éleveurs, vétérinaires, bouchers, employés d’abattoirs, techniciens de laboratoire) ; soit indirecte, par voie alimentaire, via l’ingestion de lait cru non pasteurisé et d’abats.
Chez l’animal, la maladie est le plus souvent asymptomatique, ne se manifestant que par une atteinte des organes génitaux (orchite, avortements). La bactérie peut coloniser les glandes mammaires et contaminer le lait.
La transmission à l’homme est soit directe, par contact avec les animaux infectés et les produits d’avortements, tels que placentas, sécrétions génitales, litières (professions particulièrement exposées : éleveurs, vétérinaires, bouchers, employés d’abattoirs, techniciens de laboratoire) ; soit indirecte, par voie alimentaire, via l’ingestion de lait cru non pasteurisé et d’abats.
Formes cliniques
Après la contamination, les bactéries disséminent par voie lymphatico-sanguine vers les cellules réticulo-histiocytaires, où elles se multiplient en provoquant des réactions granulomateuses. Le plus souvent, l’infection est asymptomatique, surtout avec B. abortus. Dans les autres cas, les signes cliniques sont assez variables mais évoluent habituellement en 3 phases.
Après une incubation de 8 à 30 jours, une fièvre « ondulante » apparaît, accompagnée de frissons, courbatures, arthralgies et sueurs2 (forme aiguë, tableau 1). L’examen retrouve une hépatosplénomégalie et des adénopathies périphériques.
Une forme subaiguë peut soit lui succéder, soit survenir d’emblée. Elle se manifeste par des arthralgies au niveau des vertèbres dorso-lombaires, des sacro-iliaques, des épaules mais aussi des douleurs osseuses (tibia).
Enfin, une phase chronique est décrite : plusieurs mois ou années après la contamination, les patients se plaignent d’une asthénie physique, psychique et sexuelle pouvant évoluer vers un syndrome dépressif. Une fébricule et des sueurs à l’effort sont possibles. Des foyers infectieux localisés, limités et d’évolution lente, sont parfois retrouvés (os, rachis, foie, rate, rein).
Après une incubation de 8 à 30 jours, une fièvre « ondulante » apparaît, accompagnée de frissons, courbatures, arthralgies et sueurs2 (forme aiguë, tableau 1). L’examen retrouve une hépatosplénomégalie et des adénopathies périphériques.
Une forme subaiguë peut soit lui succéder, soit survenir d’emblée. Elle se manifeste par des arthralgies au niveau des vertèbres dorso-lombaires, des sacro-iliaques, des épaules mais aussi des douleurs osseuses (tibia).
Enfin, une phase chronique est décrite : plusieurs mois ou années après la contamination, les patients se plaignent d’une asthénie physique, psychique et sexuelle pouvant évoluer vers un syndrome dépressif. Une fébricule et des sueurs à l’effort sont possibles. Des foyers infectieux localisés, limités et d’évolution lente, sont parfois retrouvés (os, rachis, foie, rate, rein).
Diagnostic
Les constantes sanguines habituelles (hémogramme, CRP, bilan hépatique) étant peu perturbées en dehors d’une leuconeutropénie lors de la primo-invasion, le diag-nostic repose sur le contexte (profession, contact avec des animaux, consommation de produits laitiers) et la mise en évidence des bactéries.
Les Brucella sont recherchées, lors de la phase aiguë, dans les hémocultures, puis en période subaiguë dans les foyers secondaires (liquide articulaire, LCR, moelle osseuse…). La culture sur gélose enrichie est aisée à ce stade (positive dans 90 % des cas) mais les manipulations nécessitent beaucoup de précautions (risque élevé de contamination).
La PCR permet d’identifier les bactéries dans le sang et dans différents liquides biologiques.
Les anticorps ne sont décelés qu’à partir de la deuxième semaine, par détection de l’antigène au rose Bengale (positif si taux > 1/8e), test d’agglutination, ou sérodiagnostic de Wright (positif si taux > 1/80e), et par les techniques d’immuno-chimie ou d’immunocapture, avec dosage des IgM, IgG et IgA (tableau 2).
Les diagnostics différentiels doivent être évoqués selon les zones géographiques : paludisme, fièvre Q, yersiniose, infection à CMV ou typhoïde.
Les Brucella sont recherchées, lors de la phase aiguë, dans les hémocultures, puis en période subaiguë dans les foyers secondaires (liquide articulaire, LCR, moelle osseuse…). La culture sur gélose enrichie est aisée à ce stade (positive dans 90 % des cas) mais les manipulations nécessitent beaucoup de précautions (risque élevé de contamination).
La PCR permet d’identifier les bactéries dans le sang et dans différents liquides biologiques.
Les anticorps ne sont décelés qu’à partir de la deuxième semaine, par détection de l’antigène au rose Bengale (positif si taux > 1/8e), test d’agglutination, ou sérodiagnostic de Wright (positif si taux > 1/80e), et par les techniques d’immuno-chimie ou d’immunocapture, avec dosage des IgM, IgG et IgA (tableau 2).
Les diagnostics différentiels doivent être évoqués selon les zones géographiques : paludisme, fièvre Q, yersiniose, infection à CMV ou typhoïde.
épidémiologie en France
à partir des années 1960, la pasteurisation obligatoire et la déclaration systématique des cas ont entraîné une baisse significative de cette affection.
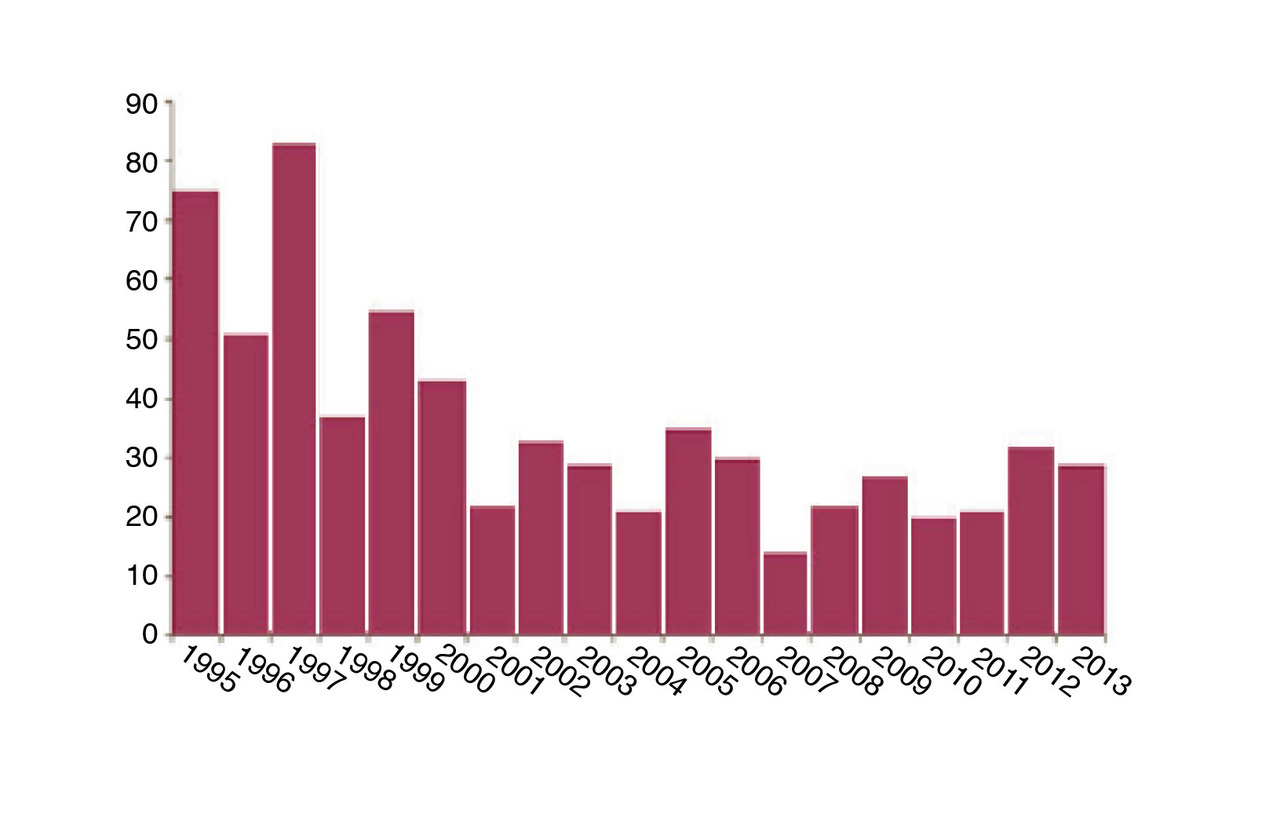
Selon une enquête menée par Santé publique France sur une période de 10 ans (début 2004-fin 2013), 250 cas de brucellose ont été recensés, soit environ 25 par an (figure). L’incidence annuelle a été de 0,3 cas par million d’habitants, avec 2 pics, en mai-juin et septembre-octobre. Parmi ces patients, 63 % étaient des hommes, âgés en moyenne de 52 ans (de 1 à 84 ans). Les cas étaient surtout sporadiques, mais 45 étaient inclus dans des petits foyers de 2 à 6 personnes. Les régions île-de-France, Rhône-Alpes et Provence-Alpes-Côte d’Azur étaient les plus touchées.
La majorité des cas étaient « importés », les sujets ayant été contaminés lors d’un séjour en zone endémique (pays du pourtour méditerranéen notamment ; tableau 3). Parmi les 37 cas autochtones, 17 (soit 46 %) concernaient des techniciens de laboratoire ayant manipulé des prélèvements infectés (cas index identifié dans 16 cas).3 Les patients avaient consommé des produits laitiers et 53 % avaient été en contact avec des animaux réservoirs (moutons, chèvres vaches) ; 13 avaient une profession à risque.4
à noter qu’en Arabie saoudite, la prévalence est de 10 % chez les enfants qui vivent en contact avec les animaux. Ils ont surtout des monoarthrites fébriles.5
Derniers chiffres disponibles en France : 22 cas recensés en 2016, dont 19 importés de zones d’endémie et 2 cas autochtones de B. suis contaminés par des sangliers. Moyenne d’âge : 64 ans (11 à 77 ans), répartis dans 8 régions de l’Hexagone, dont 11 cas en île-de-France. Aucune contamination de laboratoire n’a été répertoriée en 2016.
Selon une enquête menée par Santé publique France sur une période de 10 ans (début 2004-fin 2013), 250 cas de brucellose ont été recensés, soit environ 25 par an (figure). L’incidence annuelle a été de 0,3 cas par million d’habitants, avec 2 pics, en mai-juin et septembre-octobre. Parmi ces patients, 63 % étaient des hommes, âgés en moyenne de 52 ans (de 1 à 84 ans). Les cas étaient surtout sporadiques, mais 45 étaient inclus dans des petits foyers de 2 à 6 personnes. Les régions île-de-France, Rhône-Alpes et Provence-Alpes-Côte d’Azur étaient les plus touchées.
La majorité des cas étaient « importés », les sujets ayant été contaminés lors d’un séjour en zone endémique (pays du pourtour méditerranéen notamment ; tableau 3). Parmi les 37 cas autochtones, 17 (soit 46 %) concernaient des techniciens de laboratoire ayant manipulé des prélèvements infectés (cas index identifié dans 16 cas).3 Les patients avaient consommé des produits laitiers et 53 % avaient été en contact avec des animaux réservoirs (moutons, chèvres vaches) ; 13 avaient une profession à risque.4
à noter qu’en Arabie saoudite, la prévalence est de 10 % chez les enfants qui vivent en contact avec les animaux. Ils ont surtout des monoarthrites fébriles.5
Derniers chiffres disponibles en France : 22 cas recensés en 2016, dont 19 importés de zones d’endémie et 2 cas autochtones de B. suis contaminés par des sangliers. Moyenne d’âge : 64 ans (11 à 77 ans), répartis dans 8 régions de l’Hexagone, dont 11 cas en île-de-France. Aucune contamination de laboratoire n’a été répertoriée en 2016.
Prise en charge
Une antibiothérapie associant cyclines et aminosides ou rifampicine est efficace pour traiter l’infection aiguë et éviter les rechutes. Un antibiogramme est recommandé (E-test) mais non obligatoire, car la manipulation des Brucella est délicate et en Europe toutes les souches sont sensibles aux antibiotiques.
Dans la forme aiguë : doxycycline per os 200 mg/j pendant 6 semaines associée soit à la rifampicine per os 15 mg/kg/j pendant 6 semaines également, soit à un aminoside (gentamicine 5 mg/kg/j durant 3 semaines en IM ou streptomycine 1 g/j pendant 3 semaines en IM).
Dans la forme subaiguë : doxycycline + aminoside/6 semaines puis doxycycline + rifampicine pendant 3 mois.
En cas de brucellose chronique, les antibiotiques sont inutiles sauf si un foyer infectieux est détecté (traitement symptomatique par antalgiques et anti-inflammatoires).
Chez la femme enceinte, la doxycycline étant contre-indiquée, on associe rifam-picine 15 mg/kg/j et cotrimoxazole 800 mg/ 160 mg/j pendant 6 semaines.
La prévention est essentielle : dépistage des cheptels, campagnes de vaccination animale ou d’abattage, pasteurisation du lait et des produits dérivés.
Chez l’homme, il n’y a pas de vaccin disponible et la chimioprophylaxie n’est pas efficace. Pour les professionnels exposés, les mesures d’hygiène (gants, tenues de protection, lavage fréquent des mains) sont cruciales. Il faut recommander aux voyageurs séjournant dans les pays d’endémie de ne pas consommer de produits laitiers non pasteurisés.
Une surveillance constante est effectuée par Santé publique France : elle s’appuie sur la déclaration obligatoire de la maladie et sur les diagnostics réalisés par le Centre national de référence et son laboratoire associé.
La contamination se fait par voie directe (contact avec des animaux) ou indirecte, via l’ingestion de lait cru.
Le diagnostic repose sur l’hémoculture (à manipuler avec précautions) et la PCR.
La prévention est primordiale : vêtements de protection (chez les professionnels à risque), pasteurisation du lait.
Dans la forme aiguë : doxycycline per os 200 mg/j pendant 6 semaines associée soit à la rifampicine per os 15 mg/kg/j pendant 6 semaines également, soit à un aminoside (gentamicine 5 mg/kg/j durant 3 semaines en IM ou streptomycine 1 g/j pendant 3 semaines en IM).
Dans la forme subaiguë : doxycycline + aminoside/6 semaines puis doxycycline + rifampicine pendant 3 mois.
En cas de brucellose chronique, les antibiotiques sont inutiles sauf si un foyer infectieux est détecté (traitement symptomatique par antalgiques et anti-inflammatoires).
Chez la femme enceinte, la doxycycline étant contre-indiquée, on associe rifam-picine 15 mg/kg/j et cotrimoxazole 800 mg/ 160 mg/j pendant 6 semaines.
La prévention est essentielle : dépistage des cheptels, campagnes de vaccination animale ou d’abattage, pasteurisation du lait et des produits dérivés.
Chez l’homme, il n’y a pas de vaccin disponible et la chimioprophylaxie n’est pas efficace. Pour les professionnels exposés, les mesures d’hygiène (gants, tenues de protection, lavage fréquent des mains) sont cruciales. Il faut recommander aux voyageurs séjournant dans les pays d’endémie de ne pas consommer de produits laitiers non pasteurisés.
Une surveillance constante est effectuée par Santé publique France : elle s’appuie sur la déclaration obligatoire de la maladie et sur les diagnostics réalisés par le Centre national de référence et son laboratoire associé.
La contamination se fait par voie directe (contact avec des animaux) ou indirecte, via l’ingestion de lait cru.
Le diagnostic repose sur l’hémoculture (à manipuler avec précautions) et la PCR.
La prévention est primordiale : vêtements de protection (chez les professionnels à risque), pasteurisation du lait.