Avec plus de 50 000 nouveaux cas en 2015, c’est le cancer le plus fréquent en France et la 3e cause de décès par cancer : 8 000 morts par an (formes métastatiques).
Les tumeurs métastatiques d’emblée sont plus agressives que les récidives après prise en charge d’une maladie localisée. Le cancer de la prostate métastatique (CPm) a un tropisme principalement ganglionnaire et osseux ; les atteintes viscérales sont rares et tardives dans l’histoire de la maladie, ou bien l’apanage de formes agressives peu sensibles aux traitements hormonaux.
Les tumeurs métastatiques d’emblée sont plus agressives que les récidives après prise en charge d’une maladie localisée. Le cancer de la prostate métastatique (CPm) a un tropisme principalement ganglionnaire et osseux ; les atteintes viscérales sont rares et tardives dans l’histoire de la maladie, ou bien l’apanage de formes agressives peu sensibles aux traitements hormonaux.
Déprivation androgénique
Cet adénocarcinome est dépendant du signal de prolifération fourni par le récepteur aux androgènes (RA). Pour cette raison, le premier traitement des CPm est encore aujourd’hui la déprivation androgénique (DA) ou « castration », c’est-à-dire l’abolition de la sécrétion testiculaire de testostérone, obtenue généralement en France après administration sous- cutanée d’antagonistes ou d’agonistes de la LH-RH. La chute de testostéronémie a des effets immédiatement perceptibles : bouffées de chaleur, fatigue ou perte de la libido. Elle entraîne à long terme prise de poids, fonte musculaire, insulinorésistance, dyslipidémies ; hausse du risque cardiovasculaire et ostéopénie justifient des mesures hygiénodiététiques, une surveillance et parfois des traitements spécifiques. L’activité physique améliore la tolérance de la DA. Chez les sujets âgés, rechercher une majoration des troubles cognitifs.
Malgré cela, la DA est incontournable : on obtient un contrôle de la maladie dans la quasi-totalité des cas, qui persiste de quelques semaines à plusieurs années. La DA continue à vie est la règle, mais une administration discontinue déclenchée par un seuil de PSA chez des patients asymptomatiques est parfois discutée en phase d’hormonosensibilité pour raison de tolérance.
Le suivi de l’évolution sous traitement repose sur la clinique et le dosage du PSA. Au-delà du bilan d’extension initial, le recours à l’imagerie (scanner, scintigraphie osseuse) est possible mais moins consensuel. Un CPm progressant malgré une DA efficace (testostérone < 200 ng/mL) est dit résistant à la castration (CPRCm), tournant évolutif majeur.
Malgré cela, la DA est incontournable : on obtient un contrôle de la maladie dans la quasi-totalité des cas, qui persiste de quelques semaines à plusieurs années. La DA continue à vie est la règle, mais une administration discontinue déclenchée par un seuil de PSA chez des patients asymptomatiques est parfois discutée en phase d’hormonosensibilité pour raison de tolérance.
Le suivi de l’évolution sous traitement repose sur la clinique et le dosage du PSA. Au-delà du bilan d’extension initial, le recours à l’imagerie (scanner, scintigraphie osseuse) est possible mais moins consensuel. Un CPm progressant malgré une DA efficace (testostérone < 200 ng/mL) est dit résistant à la castration (CPRCm), tournant évolutif majeur.
Résistance à la castration
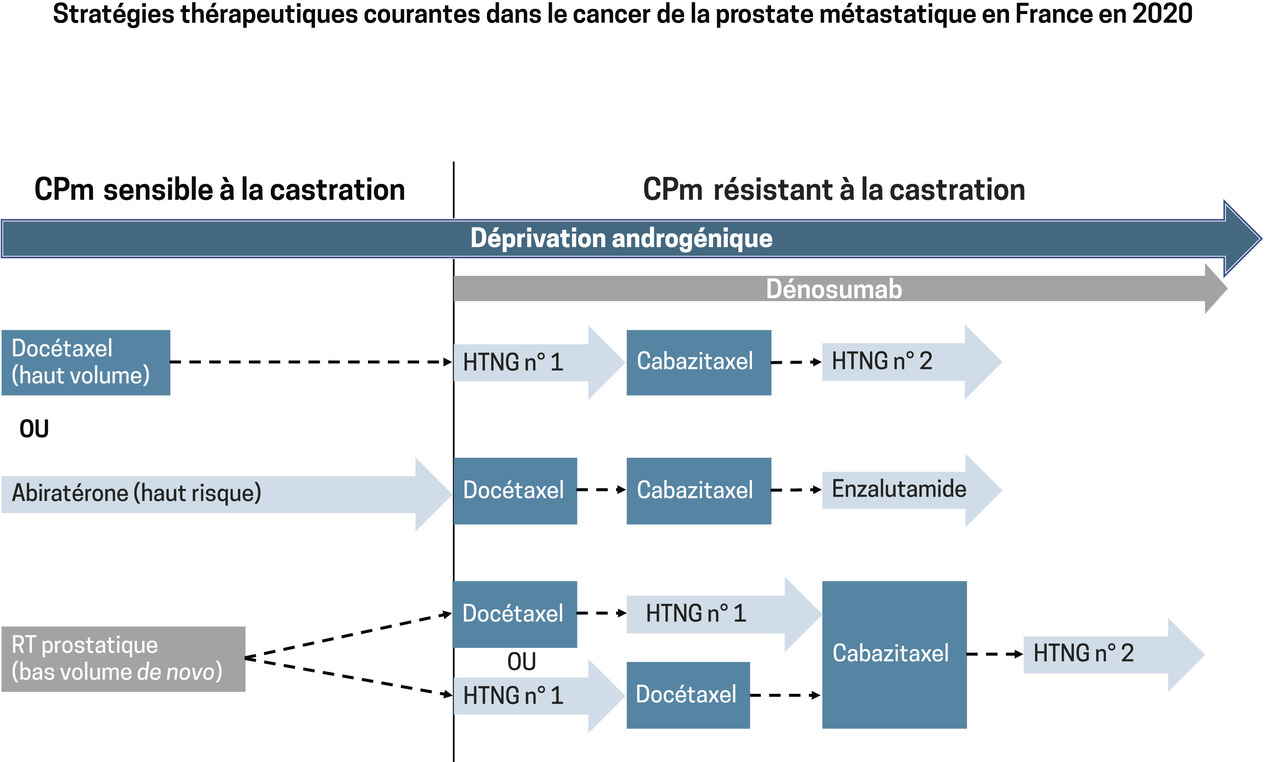
Les chimiothérapies cytotoxiques intraveineuses de la famille des taxanes ont été les premiers médicaments efficaces en survie globale (SG). Le docétaxel (Taxotere) est ainsi employé depuis les années 2000. Le cabazitaxel (Jevtana) a montré son intérêt en 2010 chez des patients prétraités par docétaxel, ce qui est encore aujourd’hui son indication. Ces taxanes sont administrées sous couvert de corticoïdes (p. ex. 10 mg de prednisone par jour), de G-CSF et de traitements symptomatiques pour limiter leurs effets digestifs aigus. Le docétaxel engendre des toxicités cumulatives, surtout des neuropathies, qui limitent son usage à long terme ; le cabazitaxel peut être utilisé à plusieurs reprises chez un même patient s’il a auparavant permis une stabilisation.
Apparues en 2011, les hormonothérapies de nouvelle génération (HTNG) s’appuient sur la notion que résistance à la castration n’est pas synonyme d’indépendance au signal fourni par le RA. L’acétate d’abiratérone (Zytiga) inhibe la synthèse enzymatique des androgènes d’origine non testiculaire (par exemple surrénalienne) ou tumorale exploités par la cellule cancéreuse pour maintenir l’activation du RA. L’enzalutamide (Xtandi), inhibiteur de nouvelle génération du RA, agissant plus directement, est également efficace devant certaines modifications activatrices du RA.
Ces 2 HTNG développées en parallèle ont montré un bénéfice en SG à la fois après docétaxel et avant ce taxane. Elles ont aujourd’hui ces mêmes indications sans jamais avoir été comparées directement. Le choix est fondé sur leurs profils de toxicité : l’abiratérone provoque une rétention hydrosodée qui limite son utilisation chez des patients déjà hypertendus ou cardiopathes ; l’enzalutamide accentue les symptômes de la castration, sa toxicité neurocognitive va jusqu’à provoquer malaises, chutes et crises d’épilepsie, surtout chez les sujets âgés.
Plusieurs questions se posent sur l’utilisation séquentielle de ces options. 1°/ entre docétaxel et HTNG, difficile de préjuger lequel employer en premier. 2°/ le choix de l’HTNG initiale est souvent arbitraire, et les résistances croisées fréquentes font que l’efficacité de la seconde est incertaine. Utiliser d’abord l’abiratérone semblerait être la meilleure stratégie.
Ainsi, après que la place du cabazitaxel a été remise en cause par les HTNG, l’étude CARD a montré en 2019 qu’après docétaxel et une première HTNG, le cabazitaxel était supérieur en SG à la seconde HTNG.1 La stratégie classique alternant chimiothérapie-HTNG est donc remise en question.
À noter : la radiothérapie vectorisée osseuse par radium 223 (Xofigo) qui améliore la SG des patients prétraités par docétaxel avec atteinte osseuse mais pas viscérale n’est pas remboursée en France.
En parallèle des antitumoraux, la prévention des événements osseux est indispensable. Le dénosumab (Xgeva), indiqué si métastases osseuses dès le début de l’hormonorésistance, est supérieur aux bisphosphonates. Le risque d’ostéonécrose mandibulaire justifie toutefois une évaluation odontologique préalable.
Apparues en 2011, les hormonothérapies de nouvelle génération (HTNG) s’appuient sur la notion que résistance à la castration n’est pas synonyme d’indépendance au signal fourni par le RA. L’acétate d’abiratérone (Zytiga) inhibe la synthèse enzymatique des androgènes d’origine non testiculaire (par exemple surrénalienne) ou tumorale exploités par la cellule cancéreuse pour maintenir l’activation du RA. L’enzalutamide (Xtandi), inhibiteur de nouvelle génération du RA, agissant plus directement, est également efficace devant certaines modifications activatrices du RA.
Ces 2 HTNG développées en parallèle ont montré un bénéfice en SG à la fois après docétaxel et avant ce taxane. Elles ont aujourd’hui ces mêmes indications sans jamais avoir été comparées directement. Le choix est fondé sur leurs profils de toxicité : l’abiratérone provoque une rétention hydrosodée qui limite son utilisation chez des patients déjà hypertendus ou cardiopathes ; l’enzalutamide accentue les symptômes de la castration, sa toxicité neurocognitive va jusqu’à provoquer malaises, chutes et crises d’épilepsie, surtout chez les sujets âgés.
Plusieurs questions se posent sur l’utilisation séquentielle de ces options. 1°/ entre docétaxel et HTNG, difficile de préjuger lequel employer en premier. 2°/ le choix de l’HTNG initiale est souvent arbitraire, et les résistances croisées fréquentes font que l’efficacité de la seconde est incertaine. Utiliser d’abord l’abiratérone semblerait être la meilleure stratégie.
Ainsi, après que la place du cabazitaxel a été remise en cause par les HTNG, l’étude CARD a montré en 2019 qu’après docétaxel et une première HTNG, le cabazitaxel était supérieur en SG à la seconde HTNG.1 La stratégie classique alternant chimiothérapie-HTNG est donc remise en question.
À noter : la radiothérapie vectorisée osseuse par radium 223 (Xofigo) qui améliore la SG des patients prétraités par docétaxel avec atteinte osseuse mais pas viscérale n’est pas remboursée en France.
En parallèle des antitumoraux, la prévention des événements osseux est indispensable. Le dénosumab (Xgeva), indiqué si métastases osseuses dès le début de l’hormonorésistance, est supérieur aux bisphosphonates. Le risque d’ostéonécrose mandibulaire justifie toutefois une évaluation odontologique préalable.
Cancers hormonosensibles
Seul traitement jusqu’en 2015 : la DA. L’essai CHAARTED a renversé ce dogme en montrant le bénéfice en SG de l’administration précoce de docétaxel en parallèle à la DA dans des maladies de mauvais pronostic définies comme à haut volume : atteinte viscérale et/ou au moins 4 métastases osseuses dont 1 en dehors du rachis et du pelvis.2
Puis, en 2017, LATITUDE révèle l’intérêt de l’abiratérone en continu avec la DA dans la maladie d’emblée métastatique à haut risque (2 critères parmi : Gleason ≥ 8, métastases viscérales, ≥ 3 métastases osseuses).3 L’abiratérone (+ prednisone) a cette indication depuis 2019 .
Les définitions de haut risque et haut volume se recoupent dans 80 % des cas. Selon STAMPEDE, confirmant CHAARTED et LATITUDE, l’abiratérone offre un contrôle plus prolongé en retardant la résistance à la castration, sans être supérieur au docétaxel en SG. In fine, comme dans les CPRCm, le choix se porte plus souvent sur l’abiratérone en raison des toxicités et contraintes de la chimiothérapie (alopécie, hospitalisations de jour, chambre implantable…). Question cruciale dans les maladies les plus agressives : faudra-t-il combiner précocement DA + taxane + HTNG, et avec quelle tolérance ?
Pour les CPm hormonosensibles à faible volume et/ou si récidives après traitement local, une radiothérapie prostatique peut être proposée dans les formes d’emblée métastatiques comme en témoigne STAMPEDE.4 S’il est établi qu’une chimiothérapie précoce n’améliore pas la survie de ces patients, les HTNG semblent avoir un rôle à jouer. STAMPEDE a montré un bénéfice à l’adjonction d’abiratérone, sans qu’une AMM n’en découle. Des études récentes menées avec des inhibiteurs du RAde nouvelle génération (enzalutamide et apalutamide) sur des populations moins sélectionnées que les patients à haut risque de LATITUDE sont également positives en SG, y compris dans des maladies à faible volume comme avec l’enzalutamide dans ENZAMET.5 Cette indication n’est pas encore reconnue en France.
Puis, en 2017, LATITUDE révèle l’intérêt de l’abiratérone en continu avec la DA dans la maladie d’emblée métastatique à haut risque (2 critères parmi : Gleason ≥ 8, métastases viscérales, ≥ 3 métastases osseuses).3 L’abiratérone (+ prednisone) a cette indication depuis 2019 .
Les définitions de haut risque et haut volume se recoupent dans 80 % des cas. Selon STAMPEDE, confirmant CHAARTED et LATITUDE, l’abiratérone offre un contrôle plus prolongé en retardant la résistance à la castration, sans être supérieur au docétaxel en SG. In fine, comme dans les CPRCm, le choix se porte plus souvent sur l’abiratérone en raison des toxicités et contraintes de la chimiothérapie (alopécie, hospitalisations de jour, chambre implantable…). Question cruciale dans les maladies les plus agressives : faudra-t-il combiner précocement DA + taxane + HTNG, et avec quelle tolérance ?
Pour les CPm hormonosensibles à faible volume et/ou si récidives après traitement local, une radiothérapie prostatique peut être proposée dans les formes d’emblée métastatiques comme en témoigne STAMPEDE.4 S’il est établi qu’une chimiothérapie précoce n’améliore pas la survie de ces patients, les HTNG semblent avoir un rôle à jouer. STAMPEDE a montré un bénéfice à l’adjonction d’abiratérone, sans qu’une AMM n’en découle. Des études récentes menées avec des inhibiteurs du RAde nouvelle génération (enzalutamide et apalutamide) sur des populations moins sélectionnées que les patients à haut risque de LATITUDE sont également positives en SG, y compris dans des maladies à faible volume comme avec l’enzalutamide dans ENZAMET.5 Cette indication n’est pas encore reconnue en France.