Les traitements systémiques en oncologie se sont très largement développés et complexifiés ces dernières années. Les cytotoxiques, ou poisons cellulaires, qui détruisent toutes les cellules vivantes, qu’elles soient cancéreuses ou saines, ne sont plus les molécules de premier choix : elles ont été supplantées par l’immunothérapie et par les thérapies ciblées (tableau 1). Ces 2 nouvelles familles de « chimiothérapie » ont des actions totalement différentes, potentiellement complémentaires.
L’immunothérapie vise à stimuler les défenses naturelles de l’organisme pour rétablir une activité antinéoplasique ; les thérapies ciblées sont capables de se fixer sur une cible moléculaire particulière et spécifique de la cellule cancéreuse afin de la neutraliser.
Nous exposerons ici les toxicités cutanées par catégorie de symptômes et non par molécules, afin d’éviter les redondances.
Le
Folliculite
Elle apparaît dès les premiers jours en cas de prise par voie intraveineuse, et au bout de 1 à 2 semaines après administration per os. Les lésions s’améliorent de manière spontanée en quelques semaines ou mois, et ce malgré le maintien de la molécule. Seuls de rares patients souffrent d’épisodes répétés tout au long de leur traitement.
Les inhibiteurs du récepteur à l’EGF (EGFR), de mTOR et les anti-MEK en sont les plus importants pourvoyeurs. Néanmoins, l’aspect des lésions diffère quelque peu : sous bloqueurs de mTOR, elles sont moins profuses mais profondes, kystiques, alors qu’elles sont denses mais superficielles avec les anti- EGFR et les anti-MEK.
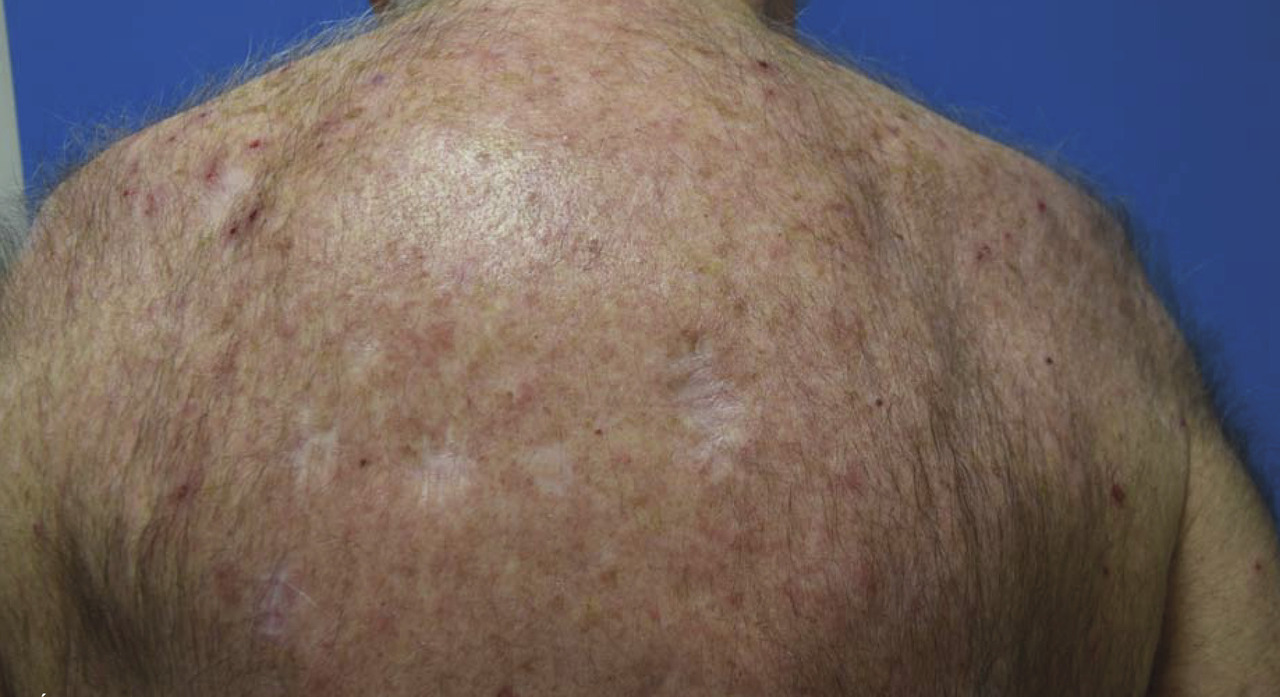
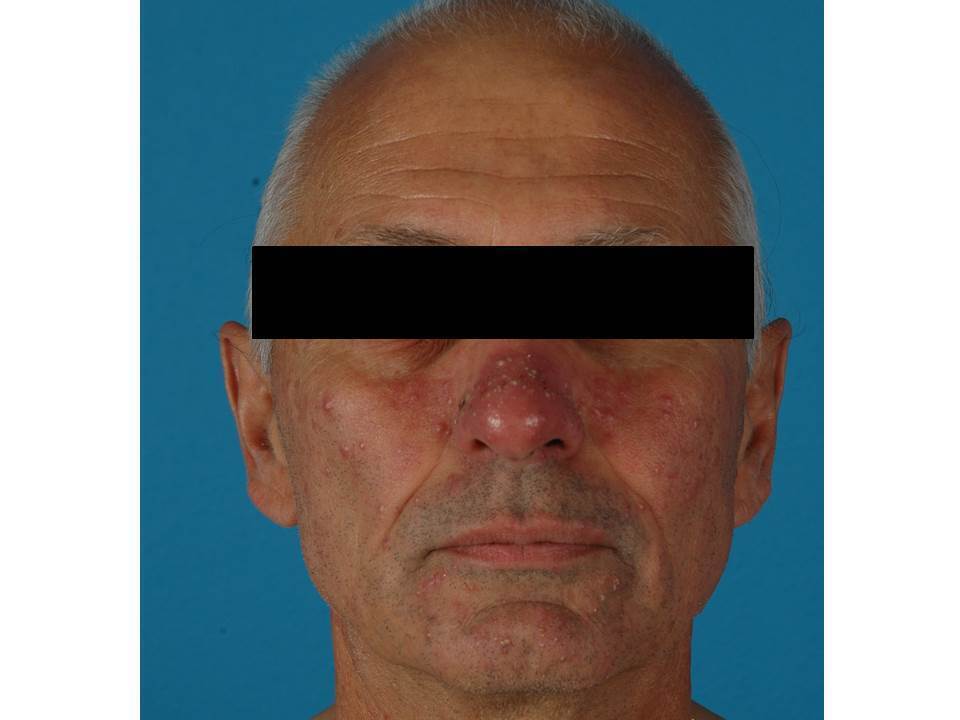
Les atteintes, souvent appelées à tort « acnéiformes », sont des papulopustules monomorphes, prédominant sur le visage et pouvant parfois s’étendre au tronc (
Soins locaux : des antibiotiques en crème ou pommade (acide fusidique, mupirocine, métronidazole 1 application/j, 3 à 4 semaines) et des émollients ; préférer ceux à base de cuivre et zinc qui limitent les surinfections bactériennes et diminuent le prurit (Cicaplast, Cicalfate, Dermocuivre...). Associer des produits d’hygiène peu agressifs (syndets) et une photoprotection. Les dermocorticoïdes (Diprosone, Betneval, Locoid) sont inconstamment efficaces mais ils sont utiles lors des poussées inflammatoires. Les antimycotiques auraient peu d’intérêt.
En cas d’éruption diffuse ou intense, il faut associer une antibiothérapie systémique : en première intention, les cyclines améliorent considérablement les symptômes (doxycycline 50 à 200 mg/j, lymécycline ou tétracycline 300 mg/j pendant 4 à 8 semaines). Si les symptômes ne régressent pas après 2-3 mois (chez de rares patients), leur poursuite au long cours est préconisée. La minocycline est à éviter en raison de sa mauvaise tolérance. Les patients doivent être prévenus du risque de photosensibilité et de diarrhées induites car il s’ajoute à celui des autres traitements. Néanmoins, il est parfois nécessaire de diminuer les doses de la thérapie anticancéreuse, voire de l’arrêter. Les lésions régressent alors très rapidement sans cicatrice ; la reprise du traitement aux posologies initiales ou diminuées est la plupart du temps possible (pas de récidive ou symptômes de moindre intensité).
En prévention, les cyclines (doxycycline à 100 mg/j pendant 2 mois) réduisent l’intensité des signes cutanés sans en diminuer la fréquence.
Modification des poils et cheveux
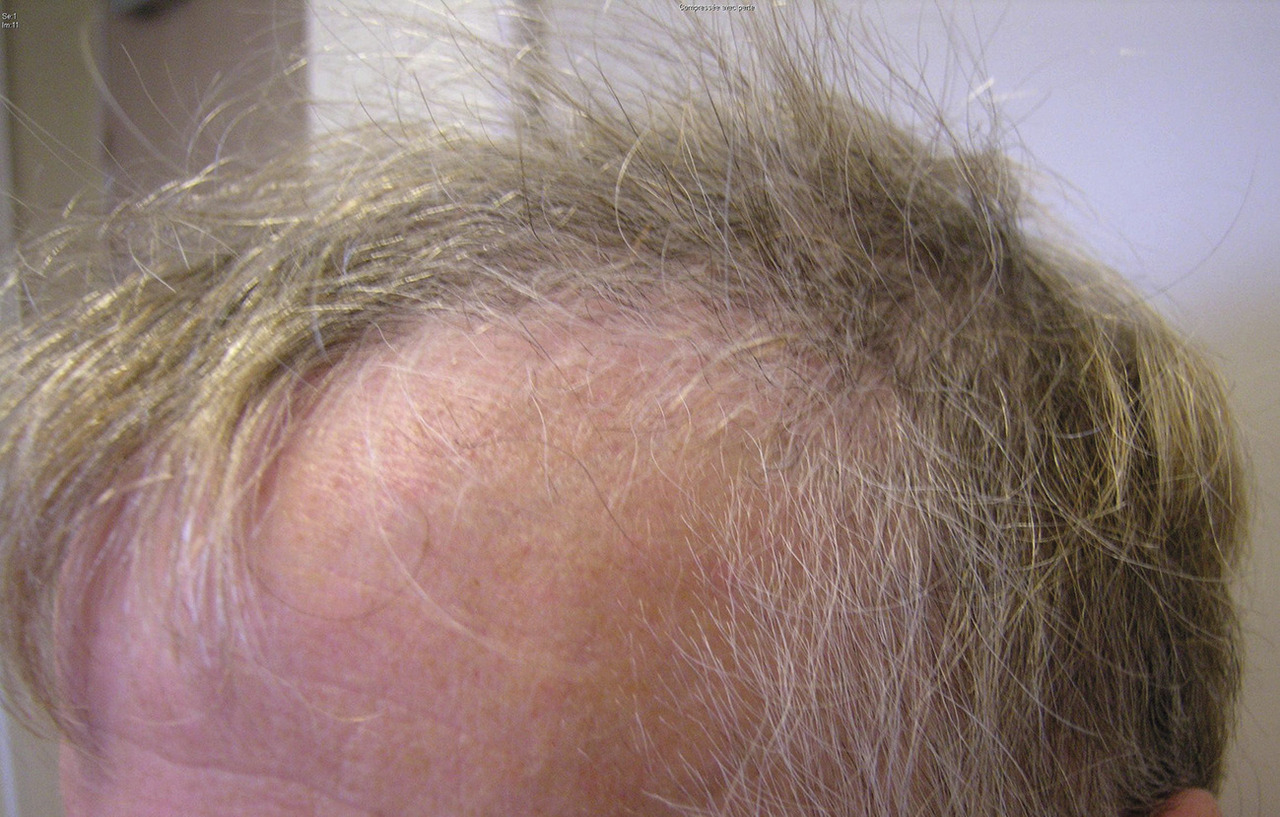
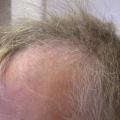
Les autres thérapies ciblées provoquent un ralentissement de la repousse des cheveux qui est frontale pour les inhibiteurs de l’EGFR (aspect de recul d’implantation des cheveux), et plus diffuse avec les anti-angiogéniques et les anti-BRAF.
Presque constamment, lorsque le traitement est prolongé plusieurs mois, la texture des cheveux est modifiée : ces derniers deviennent secs, cassants, difficiles à coiffer avec les anti-EGFR (
Une modification de la couleur est rapportée avec les inhibiteurs de c-KIT. La molécule phare de cet effet est le pazopanib (Votrient) : les patients deviennent « tout blancs » en quelques semaines. Sous sunitinib (Sutent), on observe le « signe du drapeau » déjà décrit avec le méthotrexate, correspondant à un éclaircissement des cheveux sous traitement et un retour à la couleur normale durant les fenêtres thérapeutiques (alternance zones claires/sombres).
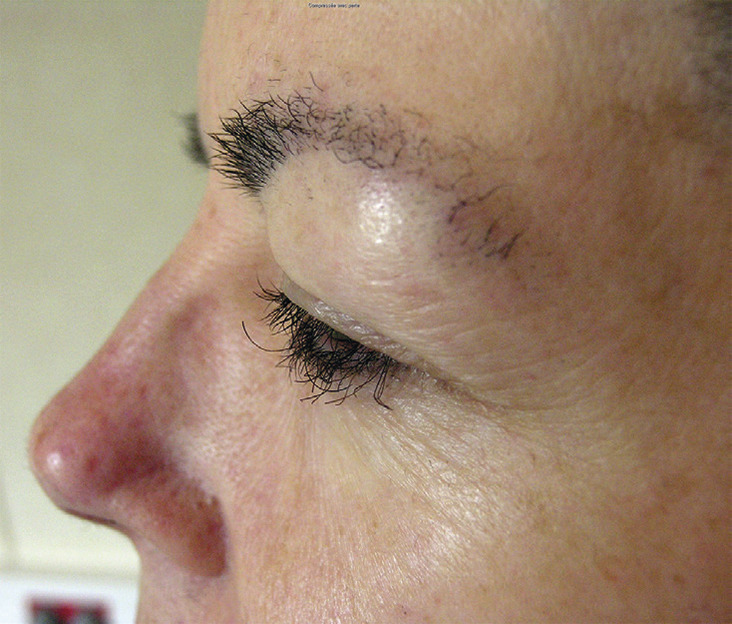
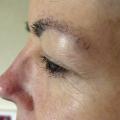
Sur le corps, contrairement aux cytotoxiques qui induisent une hypotrichose, les inhibiteurs de l’EGFR provoquent une hypertrichose très affichante au niveau du visage, notamment chez les femmes. Cette même classe thérapeutique est responsable d’une trichomégalie ciliaire, c’est-à-dire une pousse excessive de « cils de biche » (
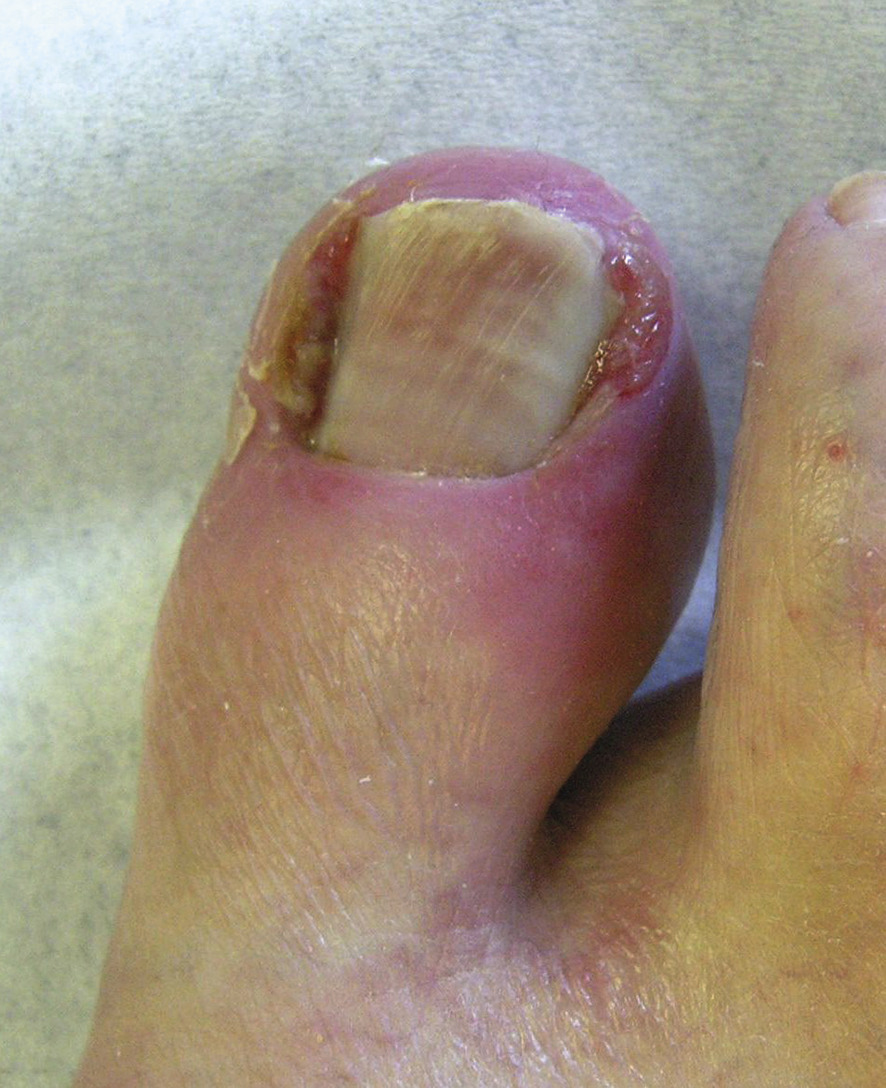
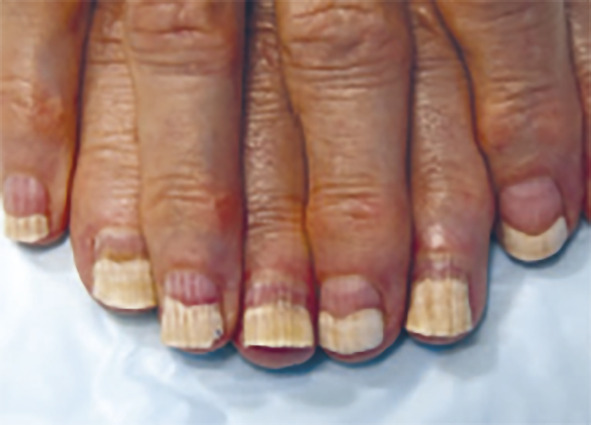
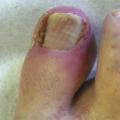
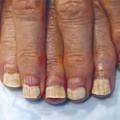
Atteinte unguéale
Il est indispensable de rappeler aux malades la nécessité d’une antisepsie rigoureuse pour prévenir les surinfections, et le port de chaussures confortables et larges pour éviter le frottement (aggravant la réaction inflammatoire).
Traitement, détruire les bourgeons charnus :
– soit de manière mécanique : nitrate d’argent en bâtonnet, dermocorticoïdes, acide trichloroacétique ;
– soit en pratiquant une exérèse de la matrice latérale de l’ongle sous anesthésie locale avec phénolisation. Cette intervention peut être réalisée en cabinet par des praticiens entraînés à la chirurgie des ongles incarnés. Une fois la bande latérale éliminée, l’ongle repoussant plus étroit n’est plus en contact avec le bord.
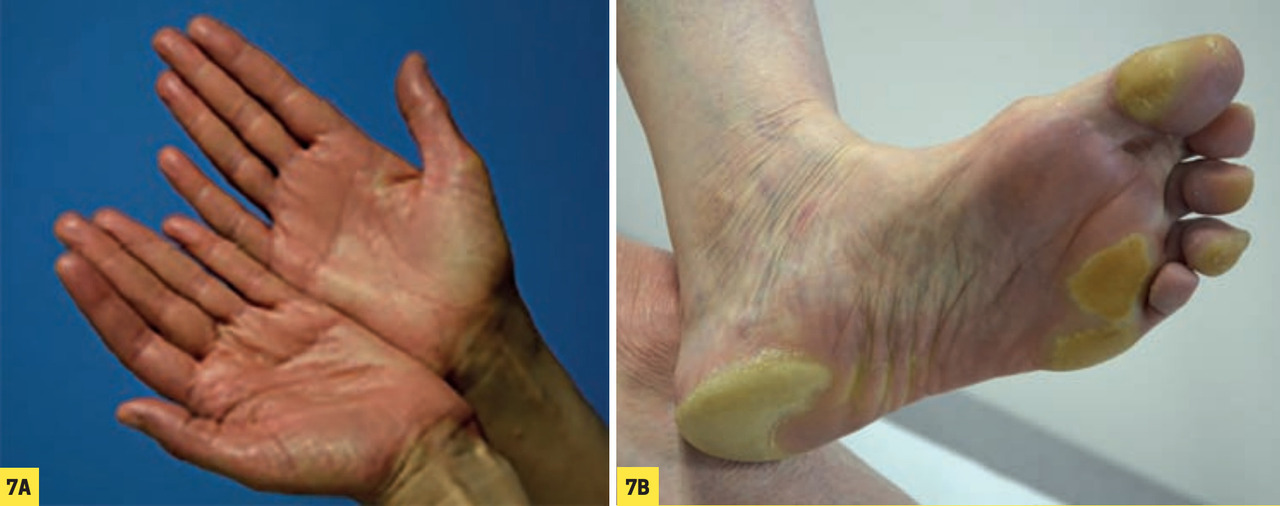
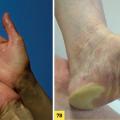
Syndrome mains-pieds
La prévention est essentielle : soins de pédicurie pour tenter de réduire au maximum l’hyperkératose physiologique avant de débuter le traitement ; port de chaussures confortables, voire de semelles orthopédiques afin de répartir au mieux les zones de pression.
En curatif, la prise en charge est symptomatique : émollients kératolytiques (urée dans les formes modérées, solution à base d’acide salicylique et de vaseline officinale dans les formes sévères, éventuellement sous pansement occlusif la nuit), soins de pédicurie, dermocorticoïdes si les lésions sont particulièrement inflammatoires. Les décollements bulleux douloureux imposent parfois l’arrêt transitoire (quelques jours ou semaines) de la thérapie anticancéreuse. Sa reprise (à dose pleine ou réduite) est le plus souvent possible.
Lésions tumorales
Sous anti-BRAF, des hyperkératoses à type de papillomes ou verrues sont décrites, d’apparition précoce, pouvant évoluer soit vers l’invagination pour former des kystes, voire des dermatites perforantes, soit vers la prolifération, à type de kératoacanthomes ou de véritables carcinomes épidermoïdes. Mais aussi des carcinomes urinaires, pulmonaires ayant pour caractéristique commune d’être mutés NRAS. En effet, un anti-BRAF stimule de manière paradoxale la proli- fération des cellules mutées NRAS : ces cellules de l’épiderme ayant subi l’impact de l’exposition aux ultraviolets (UV) ou autres inducteurs – en état de « dormance » – sont « réveillées » par ces molécules.
Cet effet secondaire a pu être contrôlé par l’adjonction des anti-MEK aux anti-BRAF, qui bloquent le signal cellulaire en aval de Ras et empêchent l’induction des cellules RAS mutées, limitant ainsi la toxicité cancérigène.
Xérose et Retard à la cicatrisation
Mucites : très fréquentes
La prise en charge repose sur des bains de bouche antiseptiques pour éviter une surinfection. La muqueuse étant fragilisée, les excipients alcooliques contenus dans les préparations commerciales sont mal tolérés ; ainsi, il est préférable d’utiliser du bicarbonate de sodium à 1,4 %.
Si les lésions sont douloureuses, on peut y associer des bains de bouche au sucralfate ou à la Xylocaïne. L’utilisation de cette dernière doit être prudente car elle induit une anesthésie du carrefour oropharyngé et favorise les fausses routes. Il faut bien indiquer au patient de ne pas manger dans les 2 heures qui suivent son application (directe ou en bains de bouche).
En cas d’inflammation importante, d’aphtes ou de bulles, les dermocorticoïdes peuvent être utiles. Ils sont utilisables en bains de bouche en dissolvant 1 comprimé de Solupred dans un peu d’eau ou en application directe (Dermoval gel ou Buccobet cp à sucer). Le patient doit être prévenu du risque infectieux et observer des mesures préventives : se brosser les dents et la langue très régulièrement avec une brosse souple et une pâte gingivale ; éviter les aliments durs ou acides (pain, tomates, condiments, alcools, fruits crus).
Sucer des glaçons pendant les perfusions de chimiothérapie permet d’obtenir une vasoconstriction comme celle induite par le port de casque ou de gants réfrigérés pour prévenir l’alopécie et le syndrome mains-pieds.
Cette mesure n’est hélas pas adaptée à la plupart des thérapies ciblées qui sont administrées par voie orale. Mais les glaçons peuvent soulager parfois les patients (effet « anesthésique » du froid).
Photosensibilité
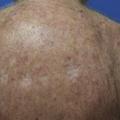
Phototoxicités : l’érythème apparaît sur les zones photo-exposées (visage, dos des mains…) dans les heures qui suivent l’administration de la molécule. Sous thérapie per os, le risque est constant tout au long du traitement. L’érythème évolue comme un « coup de soleil » avec bulles, desquamation, nécrose si l’exposition est poursuivie. C’est ce type de réaction que l’on observe avec les inhibiteurs de BRAF (Tafinlar, Zelboraf) et de manière moins importante avec les anti-EGFR.
Photo-allergies : l’éruption peut prendre l’aspect d’un simple « coup de soleil » ou être photo-induite (lupus, érythème polymorphe…). Elle débute sur les zones photo-exposées plusieurs jours (environ 10) après l’administration du traitement et s’étend rapidement. On l’observe notamment avec le vandétanib (Caprelsa), sans que le mécanisme d’action soit réellement élucidé.
Les mesures préventives sont essentielles : photo- protection efficace par les vêtements, crèmes solaires et surtout évitement de l’exposition aux UV. En curatif, les soins locaux avec des crèmes émollientes cicatrisantes, voire des dermocorticoïdes – classe forte sur le corps, modérée sur le visage – (en cas d’inflammation très importante), sont habituellement suffisants.
Grade 1 : lésions limitées à une zone (visage ou tronc), sans retentissement psychosocial.
Grade 2 : lésions étendues au visage et au tronc, impactant la vie sociale.
Grade 3 : éruption diffuse, sévère et affichante.
La toxicité dermatologique des anticorps monoclonaux ciblant PD-1 (programmed cell death protein-1 ; nivolumab, Opdivo ; pembrolizumab, Keytruda), son ligand (PD-L1 ; atézolizumab, Tecentriq ; durvalumab, Imfinzi ; avélumab, Bavencio) ou le CTLA-4 (cytotoxic T-lymphocyte-associated antigen-4 ; ipilimumab, Yervoy) est un des plus fréquents effets indésirables immunologiques des inhibiteurs de checkpoint.1
Elle est le plus souvent d’intensité légère à modérée, autorisant la poursuite du traitement avec des mesures symptomatiques. Cependant, elle est parfois sévère ou grave, notamment en cas d’association de molécules.
TOXICITÉ CUTANÉE
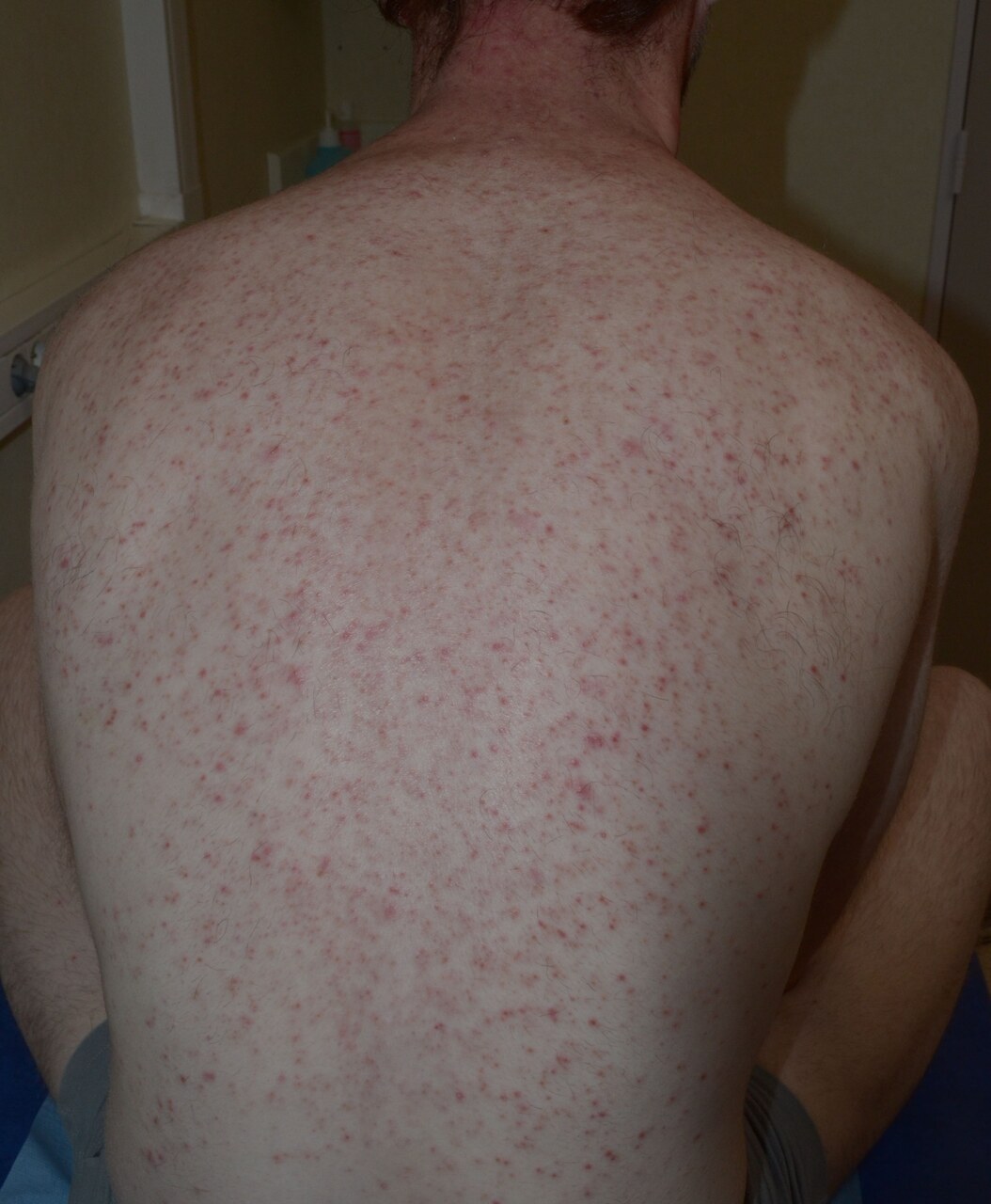
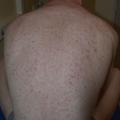
Exanthème maculopapuleux et prurit touchent plus de 15 % des patients avec les anti-PD-1. Les lésions sont volontiers eczématiformes et non spécifiques (
La réaction lichénoïde, 2e type d’atteinte cutanée en termes de fréquence, n’est diagnostiquée qu’après examen histologique. Les formes palmoplantaires sont possibles, tout comme l’atteinte des muqueuses génitales ou buccales.
Le psoriasis est un effet indésirable bien individualisé. Il peut s’agir d’une réactivation d’un psoriasis préexistant ou du déclenchement de novo.
La dermatose auto-immune la plus caractéristique est la pemphigoïde bulleuse.
Les réactions vitiligoïdes plus fréquentes avec les anti-PD-1 (8 % environ) concernent exclusivement les patients traités pour un mélanome. Une dépigmentation des poils et cheveux peut s’y associer.
TOXICITÉ MUQUEUSE
L’incidence des toxicités endobuccales est à déterminer. Les réactions lichénoïdes ne sont pas rares, que ce soit sous forme d’un réseau réticulé ou de lésions ulcérées. Une atteinte génitale de même type est possible. La xérostomie est fréquente.
FOLLICULES PILEUX
Une pelade auto-immune peut être de type universalis, notamment avec l’ipilimumab.
Folliculite : 3 stades de gravité
Grade 1 : lésions limitées à une zone (visage ou tronc), sans retentissement psychosocial.
Grade 2 : lésions étendues au visage et au tronc, impactant la vie sociale.
Grade 3 : éruption diffuse, sévère et affichante.
Immunothérapie : mauvaise pour la peau ?*
La toxicité dermatologique des anticorps monoclonaux ciblant PD-1 (programmed cell death protein-1 ; nivolumab, Opdivo ; pembrolizumab, Keytruda), son ligand (PD-L1 ; atézolizumab, Tecentriq ; durvalumab, Imfinzi ; avélumab, Bavencio) ou le CTLA-4 (cytotoxic T-lymphocyte-associated antigen-4 ; ipilimumab, Yervoy) est un des plus fréquents effets indésirables immunologiques des inhibiteurs de checkpoint.1
Elle est le plus souvent d’intensité légère à modérée, autorisant la poursuite du traitement avec des mesures symptomatiques. Cependant, elle est parfois sévère ou grave, notamment en cas d’association de molécules.
TOXICITÉ CUTANÉE
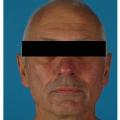
Exanthème maculopapuleux et prurit touchent plus de 15 % des patients avec les anti-PD-1. Les lésions sont volontiers eczématiformes et non spécifiques (figure), respectant le visage. Le prurit est souvent au 1er plan. Une biopsie cutanée est nécessaire en cas de forme atypique, persistante ou sévère, notamment pour éliminer une dermatose induite plus spécifique (v. infra). Traitement des rashs peu sévères : dermocorticoïdes et émollients.
La réaction lichénoïde, 2e type d’atteinte cutanée en termes de fréquence, n’est diagnostiquée qu’après examen histologique. Les formes palmoplantaires sont possibles, tout comme l’atteinte des muqueuses génitales ou buccales.
Le psoriasis est un effet indésirable bien individualisé. Il peut s’agir d’une réactivation d’un psoriasis préexistant ou du déclenchement de novo.
La dermatose auto-immune la plus caractéristique est la pemphigoïde bulleuse.
Les réactions vitiligoïdes plus fréquentes avec les anti-PD-1 (8 % environ) concernent exclusivement les patients traités pour un mélanome. Une dépigmentation des poils et cheveux peut s’y associer.
TOXICITÉ MUQUEUSE
L’incidence des toxicités endobuccales est à déterminer. Les réactions lichénoïdes ne sont pas rares, que ce soit sous forme d’un réseau réticulé ou de lésions ulcérées. Une atteinte génitale de même type est possible. La xérostomie est fréquente.
FOLLICULES PILEUX
Une pelade auto-immune peut être de type universalis, notamment avec l’ipilimumab.
2. Robert C, Sibaud V, Mateus C, Cherpelis BS. Advances in the management of cutaneous toxicities of targeted therapies. Semin Oncol 2012;39:227‑40.
3. Robert C, Sibaud V, Mateus C, et al. Nail toxicities induced by systemic anticancer treatments. Lancet Oncol 2015;16:e181-9.
4. Arnault JP, Mateus C, Escudier B, et al. Skin tumors induced by sora- fenib; paradoxic RAS-RAF pathway activation and oncogenic mutations of HRAS, TP53, and TGFBR1. Clin Cancer Res 2012;18:263‑72.
5. Boussemart L, Routier E, Mateus C, et al. Prospective study of cuta- neous side-effects associated with the BRAF inhibitor vemurafenib: a study of 42 patients. Ann Oncol 2013;24:1691-7.

 Encadrés
Encadrés