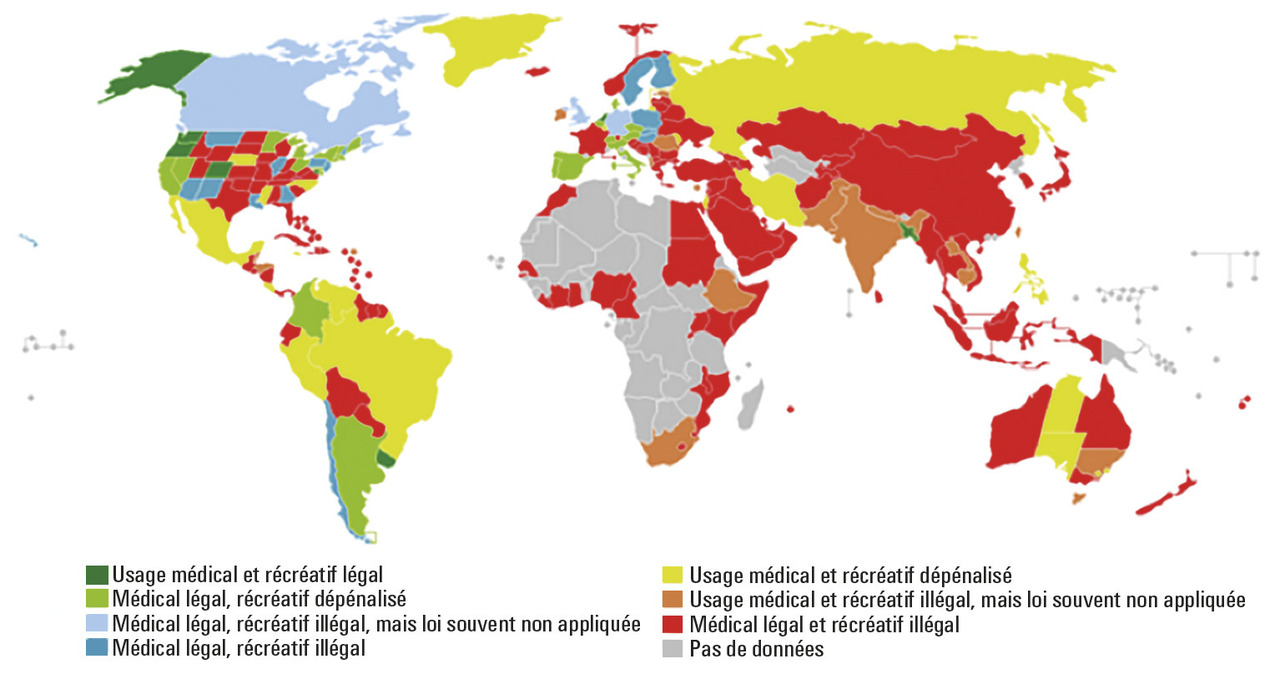
Le cannabis est la substance illicite la plus consommée dans le monde. Le composant principal responsable des effets psychotropes est le Δ9- tétrahydrocannabinol (THC), mais 120 phytocannabinoïdes naturels dont le cannabidiol (CBD) ont été identifiés. La connaissance de ses propriétés « médicales » date de plusieurs milliers d’années. Néanmoins, le statut juridique restrictif instauré en occident au début du XXe siècle n’a pas permis une évaluation clinique rigoureuse de ses effets thérapeutiques.
à l’heure de la crise des opioïdes, il est nécessaire de trouver des alternatives aux antalgiques actuels, et de nombreux pays ont légalisé l’usage médical du cannabis : Canada, Allemagne, Italie, Finlande, Pays-Bas, 29 états américains et celui de Washington…1, 2
Selon la loi actuelle en France, toutes les transactions commerciales sont strictement interdites. Il existe une dérogation concernant certaines variétés dépourvues d’action stupéfiante, comme les graines et les fibres des plantes, dont la teneur en THC doit être inférieure à 0,2 % (toute utilisation des fleurs est strictement interdite).
Récemment, l’Ansm a créé un Comité scientifique spécialisé temporaire (CSST). Mission : évaluer l’intérêt et la faisabilité de la mise à disposition du cannabis « médicament » en France. Premières conclusions du rapport (décembre 2018) : il est pertinent d’autoriser un usage thérapeutique dans certaines situations cliniques, en deuxième ligne (antalgie insuffisante ou mauvaise tolérance des options accessibles, médicamenteuses ou non ; encadré). L’Ansm devrait rendre fin juin son avis sur l’expérimentation.
Actuellement, 3 médicaments à base de cannabinoïdes sont autorisés en France :
– Marinol (dronabinol, THC de synthèse) a une ATU nominative pour les douleurs neuropathiques réfractaires ;
– Sativex (nabiximols - THC + CBD - en spray buccal) a une AMM depuis 2014 (spasticité dans la sclérose en plaques après échec des autres thérapeutiques) mais il n’est pas commercialisé faute d’accord sur son prix entre le laboratoire et les autorités de santé ;
– Epidyolex (cannabidiol), destiné aux enfants souffrant de 2 formes rares d’épilepsie, le syndrome de Lennox- Gastaut et celui de Dravet, bénéficie d’une ATU.
Cesamet (nabilone, dérivé synthétique du THC) est autorisé aux états-Unis dans les nausées et vomissements dus à la chimiothérapie.
à l’heure de la crise des opioïdes, il est nécessaire de trouver des alternatives aux antalgiques actuels, et de nombreux pays ont légalisé l’usage médical du cannabis : Canada, Allemagne, Italie, Finlande, Pays-Bas, 29 états américains et celui de Washington…1, 2
Selon la loi actuelle en France, toutes les transactions commerciales sont strictement interdites. Il existe une dérogation concernant certaines variétés dépourvues d’action stupéfiante, comme les graines et les fibres des plantes, dont la teneur en THC doit être inférieure à 0,2 % (toute utilisation des fleurs est strictement interdite).
Récemment, l’Ansm a créé un Comité scientifique spécialisé temporaire (CSST). Mission : évaluer l’intérêt et la faisabilité de la mise à disposition du cannabis « médicament » en France. Premières conclusions du rapport (décembre 2018) : il est pertinent d’autoriser un usage thérapeutique dans certaines situations cliniques, en deuxième ligne (antalgie insuffisante ou mauvaise tolérance des options accessibles, médicamenteuses ou non ; encadré). L’Ansm devrait rendre fin juin son avis sur l’expérimentation.
Actuellement, 3 médicaments à base de cannabinoïdes sont autorisés en France :
– Marinol (dronabinol, THC de synthèse) a une ATU nominative pour les douleurs neuropathiques réfractaires ;
– Sativex (nabiximols - THC + CBD - en spray buccal) a une AMM depuis 2014 (spasticité dans la sclérose en plaques après échec des autres thérapeutiques) mais il n’est pas commercialisé faute d’accord sur son prix entre le laboratoire et les autorités de santé ;
– Epidyolex (cannabidiol), destiné aux enfants souffrant de 2 formes rares d’épilepsie, le syndrome de Lennox- Gastaut et celui de Dravet, bénéficie d’une ATU.
Cesamet (nabilone, dérivé synthétique du THC) est autorisé aux états-Unis dans les nausées et vomissements dus à la chimiothérapie.
Quelles maladies ?
Les pathologies douloureuses (cancers, polyarthrite rhumatoïde, fibromyalgie…) sont les plus étudiées dans la littérature (pas de risque d’overdose en raison de l’absence de récepteurs cannabinoïdes dans le tronc cérébral). Le cannabis thérapeutique a montré un intérêt dans l’épilepsie, les maladies d’Alzheimer et de Parkinson, les cancers (douleurs, nausées).
Les cannabinoïdes ont également une capacité immunomodulatrice, qui se traduit par une réduction globale de l’expression des cytokines pro-inflammatoires et une augmentation de celles anti-inflammatoires ; une corrélation intéressante a été retrouvée entre les cannabinoïdes et l’activité de plusieurs maladies (fibromyalgie, MICI, SEP, poly- arthrite rhumatoïde, diabète de type 1, sclérodermie).3
Les symptômes psychodysleptiques sont essentiellement induits par le THC. Le CBD ne provoque pas d’épisode psychotique et pourrait au contraire contrer ces effets néfastes (rôle protecteur) lorsqu’il est administré avant le THC (en particulier l’anxiété, l’euphorie, les épisodes aigus et transitoires type bouffée délirante).
L’intérêt pour le CBD est croissant dans les troubles psychotiques. Les schizophrènes consommateurs de cannabis ayant un rapport CBD/THC plus élevé ont des symptômes positifs moins intenses et un meilleur score de fonctionnement global.1 Des résultats prometteurs en termes de réduction de l’insomnie et de meilleure gestion des affects négatifs4 ont aussi été décrits chez les personnes souffrant de troubles anxieux (phobies sociales par exemple) ou de syndrome de stress post-traumatique, qui auraient une disponibilité accrue des récepteurs aux cannabinoïdes.
Malgré cette littérature foisonnante, de nombreuses questions restent en suspens.
Les cannabinoïdes ont également une capacité immunomodulatrice, qui se traduit par une réduction globale de l’expression des cytokines pro-inflammatoires et une augmentation de celles anti-inflammatoires ; une corrélation intéressante a été retrouvée entre les cannabinoïdes et l’activité de plusieurs maladies (fibromyalgie, MICI, SEP, poly- arthrite rhumatoïde, diabète de type 1, sclérodermie).3
Les symptômes psychodysleptiques sont essentiellement induits par le THC. Le CBD ne provoque pas d’épisode psychotique et pourrait au contraire contrer ces effets néfastes (rôle protecteur) lorsqu’il est administré avant le THC (en particulier l’anxiété, l’euphorie, les épisodes aigus et transitoires type bouffée délirante).
L’intérêt pour le CBD est croissant dans les troubles psychotiques. Les schizophrènes consommateurs de cannabis ayant un rapport CBD/THC plus élevé ont des symptômes positifs moins intenses et un meilleur score de fonctionnement global.1 Des résultats prometteurs en termes de réduction de l’insomnie et de meilleure gestion des affects négatifs4 ont aussi été décrits chez les personnes souffrant de troubles anxieux (phobies sociales par exemple) ou de syndrome de stress post-traumatique, qui auraient une disponibilité accrue des récepteurs aux cannabinoïdes.
Malgré cette littérature foisonnante, de nombreuses questions restent en suspens.
Risque de dépendance ?
Une des craintes principales est l’addiction. Les utilisateurs ont un risque de dépendance à long terme d’environ 9 %, ce qui est nettement inférieur à celui induit par les opiacés par exemple.
Selon 2 études transversales, dépression et troubles du sommeil seraient des facteurs prédisposant au développement d’un usage problématique.4 D’autres travaux suggèrent que le cannabis thérapeutique pourrait être « une drogue de sortie » en se substituant à d’autres substances plus nocives telles que l’alcool5 et les opiacés.6
En ce qui concerne le risque de développer une nouvelle dépendance, une étude suggère qu’il ne concernerait que des phénotypes de vulnérabilité (terrain, génétique, comorbidités psychiatriques) sous l’influence de facteurs environnementaux (difficultés sociales, événements stressants).
Selon 2 études transversales, dépression et troubles du sommeil seraient des facteurs prédisposant au développement d’un usage problématique.4 D’autres travaux suggèrent que le cannabis thérapeutique pourrait être « une drogue de sortie » en se substituant à d’autres substances plus nocives telles que l’alcool5 et les opiacés.6
En ce qui concerne le risque de développer une nouvelle dépendance, une étude suggère qu’il ne concernerait que des phénotypes de vulnérabilité (terrain, génétique, comorbidités psychiatriques) sous l’influence de facteurs environnementaux (difficultés sociales, événements stressants).
Effets cognitifs ?
Autre sujet préoccupant : les effets secondaires, notamment les troubles cognitifs et les syndromes amotivationnels après consommation prolongée. Deux méta-analyses concluent à des performances inférieures des usagers en termes de fonctionnement exécutif, mémoire épisodique, capacités d’apprentissage et habileté motrice. Néanmoins, la seule étude prospective s’intéressant au cannabis thérapeutique (à la dose de 2,5 g/j) incluant 200 participants n’a pas retrouvé de déficits cognitifs.7 Ces résultats sont à confirmer.
Quelle composition ?
C’est une des interrogations actuelles. Le cannabis sous forme de plante est-il plus bénéfique que les substances pures comme le dronabinol ou le nabilone (à base de THC synthétique) ?
L’intérêt actuel porte surtout sur le cannabis « naturel » : si les effets psychotropes sont liés à l’activation des récepteurs CB1 dans le cerveau, l’utilisation conjointe d’autres phytocannabinoïdes majeurs tels que le CBD semble les contrecarrer. Ainsi, des traitements comme le nabiximols (Sativex, association de CBD et THC en ratio 1:1) pourraient provoquer moins d’effets indésirables. De plus, le CBD aurait aussi une action anti- nociceptive. Néanmoins, avec 65 cibles moléculaires potentielles, son mécanisme d’action n’est pas encore complètement élucidé ; les nombreux autres phytocannabinoides sont encore peu étudiés.1
L’intérêt actuel porte surtout sur le cannabis « naturel » : si les effets psychotropes sont liés à l’activation des récepteurs CB1 dans le cerveau, l’utilisation conjointe d’autres phytocannabinoïdes majeurs tels que le CBD semble les contrecarrer. Ainsi, des traitements comme le nabiximols (Sativex, association de CBD et THC en ratio 1:1) pourraient provoquer moins d’effets indésirables. De plus, le CBD aurait aussi une action anti- nociceptive. Néanmoins, avec 65 cibles moléculaires potentielles, son mécanisme d’action n’est pas encore complètement élucidé ; les nombreux autres phytocannabinoides sont encore peu étudiés.1
Fumé, vaporisé ou ingéré ?
Avantages du cannabis fumé : un pic rapide et élevé et un effet durant environ 3 à 4 h. Cependant, il expose davantage au risque de toux et d’expectorations, de cancers et de BPCO. La vaporisation a la même cinétique d’action et, comme le cannabis fumé, rend possible la titration de la dose. L’ingestion a un impact retardé, avec des concentrations maximales obtenues en 3 h et un effet perdurant jusqu’à 6 h après la prise ; elle est toutefois associée à un risque plus élevé de surdosage.2 Il n’y a pas assez de données pour préférer une forme plutôt qu’une autre.Plusieurs autres voies d’administration sont actuellement en cours d’étude : rectale, sublinguale, transdermique, oculaire et intraveineuse.
Encadre
Indications potentielles
• Douleurs réfractaires aux thérapies accessibles (médicamenteuses ou non).
• Certaines formes d’épilepsie sévères et pharmacorésistantes.
• Soins de support en oncologie.
• Situations palliatives.
• Spasticité douloureuse de la SEP.
Références
1. Manseau MW, Goff DC. Cannabinoids and Schizophrenia: Risks and Therapeutic Potential. Neurotherapeutics 2015;12:816 824.
2. Miller RJ, Miller RE. Is cannabis an effective treatment for joint pain? Clin Exp Rheumatol 2017;35(Suppl 107): 59 67.
3. Katz D, Katz I, Porat-Katz BS, Shoenfeld Y. Medical cannabis: Another piece in the mosaic of autoimmunity? Clin Pharmacol Ther 2017;101:230-8.
4. Walsh Z, Gonzalez R, Crosby K, et al. Medical cannabis and mental health: A guided systematic review. Clin Psychol Rev 2017;51:15 29.
5. Mikuriya T. Cannabis as a Substitute for Alcohol: A Harm-Reduction Approach. J Cannabis Therapeutics 2004;4:79 93.
6. Lucas P. Cannabis as an adjunct to or substitute for opiates in the treatment of chronic pain. J Psychoactive Drugs 2012;44:125-33.
7. Ware MA, Wang T, Shapiro S, Collet JP; COMPASS study team. Cannabis for the Management of Pain: Assessment of Safety Study (COMPASS). J Pain 2015; 16:1233-42.
2. Miller RJ, Miller RE. Is cannabis an effective treatment for joint pain? Clin Exp Rheumatol 2017;35(Suppl 107): 59 67.
3. Katz D, Katz I, Porat-Katz BS, Shoenfeld Y. Medical cannabis: Another piece in the mosaic of autoimmunity? Clin Pharmacol Ther 2017;101:230-8.
4. Walsh Z, Gonzalez R, Crosby K, et al. Medical cannabis and mental health: A guided systematic review. Clin Psychol Rev 2017;51:15 29.
5. Mikuriya T. Cannabis as a Substitute for Alcohol: A Harm-Reduction Approach. J Cannabis Therapeutics 2004;4:79 93.
6. Lucas P. Cannabis as an adjunct to or substitute for opiates in the treatment of chronic pain. J Psychoactive Drugs 2012;44:125-33.
7. Ware MA, Wang T, Shapiro S, Collet JP; COMPASS study team. Cannabis for the Management of Pain: Assessment of Safety Study (COMPASS). J Pain 2015; 16:1233-42.

 Encadrés
Encadrés