Considérée comme une infection tropicale bénigne pendant 50 ans, cette arbovirose est à l’origine de nombreuses épidémies depuis 2014 dans le monde.
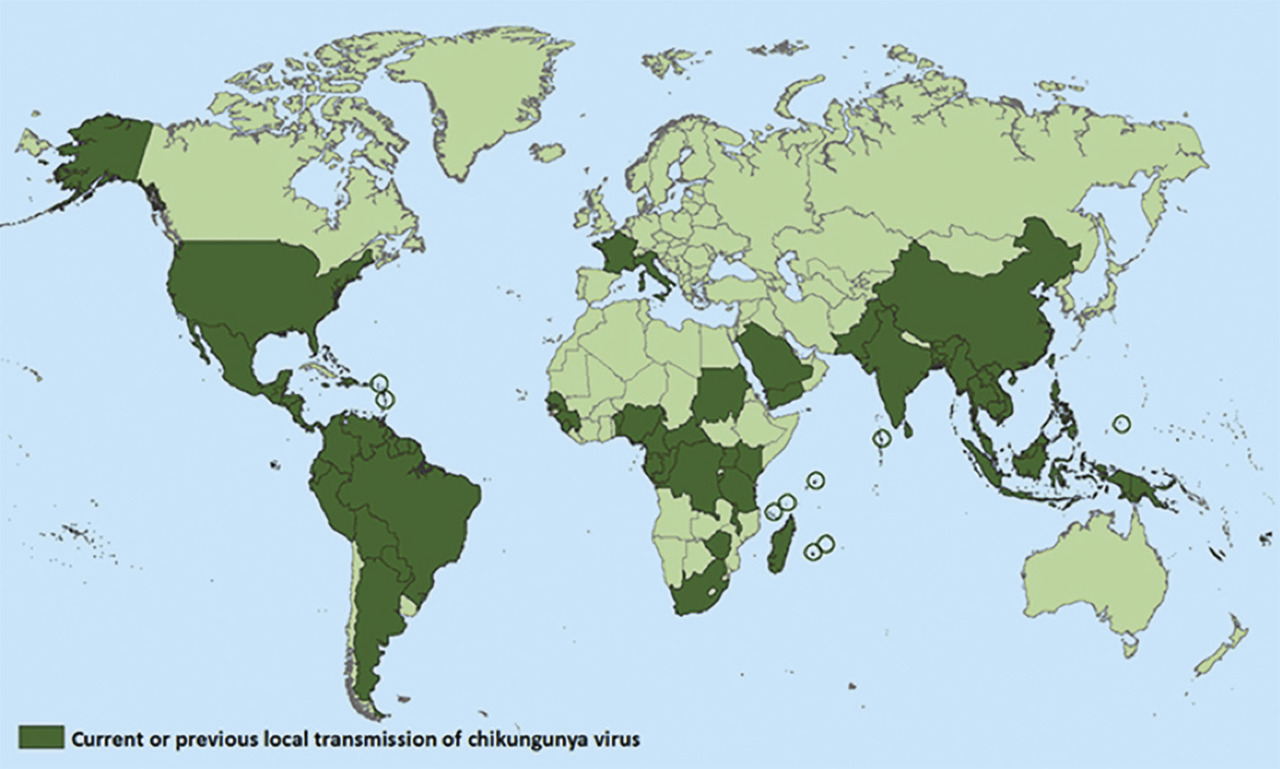
Le chikungunya, alphavirus arthrotrope transmis par la piqûre des moustiques Aedes spp., a infecté en 14 ans plus de 10 millions de personnes sur tous les continents : océan Indien (2004-2006), Asie du Sud-Est (endémo- épidémique), Pacifique (2011-2014), Amérique (depuis 2013) et Europe (circulation occasionnelle depuis 2007)1 [fig. 1 ]. La France a été particulièrement atteinte avec différents foyers de transmission autochtone depuis 2005. On estime que près de 500 000 Français ont été contaminés en outre-mer, en voyage et même ponctuellement dans le sud-est de l’Hexagone (2 cas à Fréjus à 2010, 11 à Montpellier en 2014, 17 au Cannet-des-Maures et à Taradeau en 2017).
Le chikungunya, alphavirus arthrotrope transmis par la piqûre des moustiques Aedes spp., a infecté en 14 ans plus de 10 millions de personnes sur tous les continents : océan Indien (2004-2006), Asie du Sud-Est (endémo- épidémique), Pacifique (2011-2014), Amérique (depuis 2013) et Europe (circulation occasionnelle depuis 2007)1 [
Une maladie mieux connue
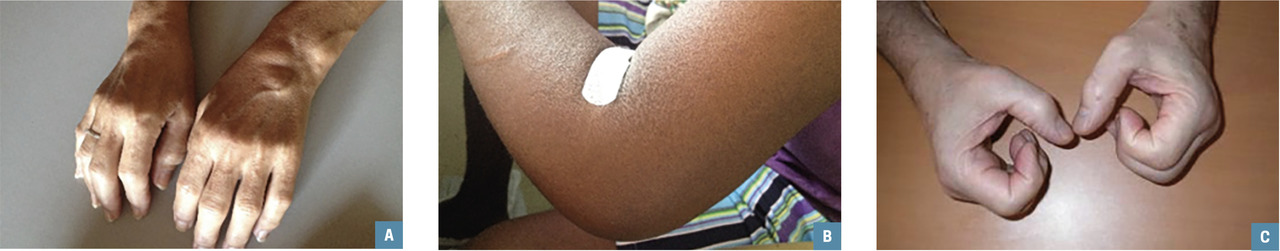
L’infection aiguë, symptomatique dans 60-80 % des cas chez l’adulte, est caractérisée par une fièvre éruptive (rash aspécifique) et des polyarthralgies, arthrites, œdèmes des extrémités, ténosynovites, bursites, enthésites (fig. 2 ). Les formes graves de l’adulte sont essentiellement liées à une décompensation des comorbidités, plus rarement à des atteintes spécifiques d’organes (méningo-encéphalites, myocardites, hépatites). La létalité est faible (0,1 à 1/1 000). La transmission materno-fœtale est possible si l’accouchement a lieu en période de virémie maternelle, qui dure 5 à 7 jours après le début des symptômes (allaitement alors contre-indiqué). Les formes congénitales et néonatales sont graves dans 1 cas sur 4. Il n’y a pas de surmorbidité décrite chez l’enfant de moins de 15 ans.2
Le stade post-aigu s’étend de la 4e semaine à la fin du 3e mois, chez plus de la moitié des patients : des douleurs articulaires prédominent aux pieds et aux mains, volontiers empâtées et enraidies. Puis, après une progressive diffusion centripète, les grosses articulations deviennent le siège de troubles musculo- squelettiques mécaniques (arthrose, tendinopathies, bursites…).
Au-delà de 3 mois, on parle de phase chronique, caractérisée par la persistance ou l’aggravation des douleurs, enraidissement, déconditionnement, altération de la qualité de vie, humeur dépressive et repli social. Elle peut durer plusieurs années.
Le stade post-aigu s’étend de la 4e semaine à la fin du 3e mois, chez plus de la moitié des patients : des douleurs articulaires prédominent aux pieds et aux mains, volontiers empâtées et enraidies. Puis, après une progressive diffusion centripète, les grosses articulations deviennent le siège de troubles musculo- squelettiques mécaniques (arthrose, tendinopathies, bursites…).
Au-delà de 3 mois, on parle de phase chronique, caractérisée par la persistance ou l’aggravation des douleurs, enraidissement, déconditionnement, altération de la qualité de vie, humeur dépressive et repli social. Elle peut durer plusieurs années.
Traiter les symptômes
En l’absence de thérapie efficace sur le virus, la prise en charge de la phase aiguë est symptomatique, en surveillant le risque iatrogène (surconsommation et automédication fréquentes, action délétère des corticoïdes à ce stade). On prescrit des antipyrétiques, des antalgiques de palier 1 à 3, voire des antidouleurs neuropathiques si score DN4 ≥ 4/10, l’hydratation et la médecine physique (autorééducation ciblée).
Les AINS ne sont introduits qu’à par-tir du 10e jour, en l’absence de contre- indication, à dose maximale (selon l’AMM) et poursuivis jusqu’au contrôle des symptômes. Une kinésithérapie est recommandée et souvent bénéfique (antalgie ; lutte contre le déconditionnement musculaire et l’enraidissement articulaire). Les corticoïdes (en cure courte, au maximum 20 mg/j) sont réservés aux atteintes polyarticulaires inflammatoires réfractaires aux AINS.3
La prise en charge au stade chronique est plus complexe. En ville : examen clinique de toutes les articulations ; tryptique antalgie-contrôle de l’inflammation-kinésithérapie. La suspicion précoce d’un authentique rhumatisme inflammatoire chronique révélé par le chikungunya fait orienter vers un spécialiste. Des signes articulaires inflammatoires persistant au-delà du 3e mois justifient des examens biologiques (IgG anti-vCHIK, CRP, VS, anti-CCP2, facteur rhumatoïde, acide urique, TSH, glycémie à jeun ± HLA-B27) et une imagerie ciblée (échographie articulaire pour la recherche de synovite, radiographies standard, voire IRM). Tout rhumatisme inflammatoire ainsi détecté relève d’un suivi spécialisé et d’un immunomodulateur (à instaurer sans délai ; méthotrexate en 1re intention).4
Le consensus d’experts publié en 2014 (accessible sur www.infectiologie.com) est peu connu des praticiens, y compris dans les départements français d’Amérique qui ont été meurtris par l’épidémie de 2013-2015. S’il n’est pas raisonnable de promettre à tous le retour à l’état « pré-chikungunya », il faut mettre en place un projet thérapeutique personnalisé visant à améliorer la qualité de vie. Ainsi, des consultations dédiées au post-chikungunya ont été créées comme à l’hôpital Laveran, Marseille (Pr Simon).
Les AINS ne sont introduits qu’à par-tir du 10e jour, en l’absence de contre- indication, à dose maximale (selon l’AMM) et poursuivis jusqu’au contrôle des symptômes. Une kinésithérapie est recommandée et souvent bénéfique (antalgie ; lutte contre le déconditionnement musculaire et l’enraidissement articulaire). Les corticoïdes (en cure courte, au maximum 20 mg/j) sont réservés aux atteintes polyarticulaires inflammatoires réfractaires aux AINS.3
La prise en charge au stade chronique est plus complexe. En ville : examen clinique de toutes les articulations ; tryptique antalgie-contrôle de l’inflammation-kinésithérapie. La suspicion précoce d’un authentique rhumatisme inflammatoire chronique révélé par le chikungunya fait orienter vers un spécialiste. Des signes articulaires inflammatoires persistant au-delà du 3e mois justifient des examens biologiques (IgG anti-vCHIK, CRP, VS, anti-CCP2, facteur rhumatoïde, acide urique, TSH, glycémie à jeun ± HLA-B27) et une imagerie ciblée (échographie articulaire pour la recherche de synovite, radiographies standard, voire IRM). Tout rhumatisme inflammatoire ainsi détecté relève d’un suivi spécialisé et d’un immunomodulateur (à instaurer sans délai ; méthotrexate en 1re intention).4
Le consensus d’experts publié en 2014 (accessible sur www.infectiologie.com) est peu connu des praticiens, y compris dans les départements français d’Amérique qui ont été meurtris par l’épidémie de 2013-2015. S’il n’est pas raisonnable de promettre à tous le retour à l’état « pré-chikungunya », il faut mettre en place un projet thérapeutique personnalisé visant à améliorer la qualité de vie. Ainsi, des consultations dédiées au post-chikungunya ont été créées comme à l’hôpital Laveran, Marseille (Pr Simon).
Menace d’émergence en France
Qu’il s’agisse de la France d’outre-mer ou hexagonale, l’origine d’une épidémie est identique. Un voyageur virémique se fait piquer par un moustique Aedes autochtone compétent pour transmettre le virus une semaine plus tard. Aux Antilles, une souche asiatique a été véhiculée par Aedes aegypti ; dans le Sud-Est, une souche africaine a été transmise par Aedes albopictus ou moustique tigre. Ce dernier, très invasif, a été identifié dans 42 départements en 2017 et devrait avoir colonisé la totalité du territoire métropolitain d’ici 2030.
Éviter toute nouvelle transmission autochtone à partir d’un cas importé est l’objectif du plan national antidissémination des arboviroses mis en place depuis 2006. Plusieurs actions : suspicion précoce des cas de CHIK importés ou autochtones (fièvre et arthralgies aiguës) ; isolement vectoriel de ces cas en phase aiguë (moustiquaire, répulsifs) ; confirmation précoce par le Centre national de référence (CNR) sur les arboviroses ; signalement à l’ARS (déclaration obligatoire, fiche de notification téléchargeable sur le site de l’ARS) ; lutte antivectorielle autour des cas suspects par les services de démoustication. Hors contexte épidémique, la confirmation biologique du diagnostic est impérative (imputabilité). Elle repose sur la RT-PCR entre J0 et J5 ; RT-PCR et sérologie entre J5 et J7 ; et sérologie seule au-delà de J7. Les IgM anti-vCHIK sont identifiés en moyenne à partir du 5e jour après l’apparition des signes cliniques et persistent 2 à 3 mois, tandis que les IgG se positivent entre le 7e et le 10e jour pour atteindre un maximum à J15. Les prélèvements sont adressés au CNR arbovirus avec une fiche de renseignements (http://cnr-arbovirus.fr).
Rôle du généraliste : prescription de la protection antivectorielle individuelle aux voyageurs dans les zones à risque (fig. 1 ), détection clinique au retour ou devant un tableau évocateur en zone non épidémique, coordination de la prise en charge standardisée des cas confirmés et orientation des patients complexes vers les spécialistes, éducation sanitaire sur la réalité du risque dans les régions colonisées par les moustiques Aedes.
Éviter toute nouvelle transmission autochtone à partir d’un cas importé est l’objectif du plan national antidissémination des arboviroses mis en place depuis 2006. Plusieurs actions : suspicion précoce des cas de CHIK importés ou autochtones (fièvre et arthralgies aiguës) ; isolement vectoriel de ces cas en phase aiguë (moustiquaire, répulsifs) ; confirmation précoce par le Centre national de référence (CNR) sur les arboviroses ; signalement à l’ARS (déclaration obligatoire, fiche de notification téléchargeable sur le site de l’ARS) ; lutte antivectorielle autour des cas suspects par les services de démoustication. Hors contexte épidémique, la confirmation biologique du diagnostic est impérative (imputabilité). Elle repose sur la RT-PCR entre J0 et J5 ; RT-PCR et sérologie entre J5 et J7 ; et sérologie seule au-delà de J7. Les IgM anti-vCHIK sont identifiés en moyenne à partir du 5e jour après l’apparition des signes cliniques et persistent 2 à 3 mois, tandis que les IgG se positivent entre le 7e et le 10e jour pour atteindre un maximum à J15. Les prélèvements sont adressés au CNR arbovirus avec une fiche de renseignements (http://cnr-arbovirus.fr).
Rôle du généraliste : prescription de la protection antivectorielle individuelle aux voyageurs dans les zones à risque (
Références
1. Petersen LR, Powers AM. Chikungunya: epidemiology. F1000Res 2016;5. pii: F1000.
2. Simon F, Javelle E, Cabie A, et al. French guidelines for the management of chikungunya (acute and persistent presentations). November 2014. Med Mal Infect 2015;45:243‑63.
3. Martí-Carvajal A, Ramon-Pardo P, Javelle E, et al. Interventions for treating patients with chikungunya virus infection-related rheumatic and musculo- skeletal disorders: A systematic review. PloS One 2017;12:e0179028.
4. Javelle E, Ribera A, Degasne I, et al. Specific management of post-chikungunya rheumatic disorders: a retrospective study of 159 cases in Reunion Island from 2006-2012. PLoS Negl Trop Dis 2015;9:e0003603.
2. Simon F, Javelle E, Cabie A, et al. French guidelines for the management of chikungunya (acute and persistent presentations). November 2014. Med Mal Infect 2015;45:243‑63.
3. Martí-Carvajal A, Ramon-Pardo P, Javelle E, et al. Interventions for treating patients with chikungunya virus infection-related rheumatic and musculo- skeletal disorders: A systematic review. PloS One 2017;12:e0179028.
4. Javelle E, Ribera A, Degasne I, et al. Specific management of post-chikungunya rheumatic disorders: a retrospective study of 159 cases in Reunion Island from 2006-2012. PLoS Negl Trop Dis 2015;9:e0003603.