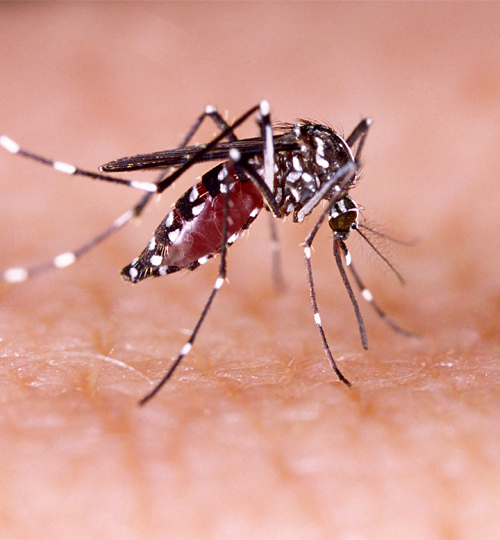
Le chikungunya est une maladie infectieuse causée par un virus à ARN simple brin positif du genre alphavirus. Ses moustiques vecteurs, Aedes aegypti et Aedes albopictus, sont en pleine progression en Europe et dans le continent américain dans le contexte du réchauffement climatique. Dans le monde, 5 millions d’infections par ce virus ont été rapportées lors des 15 dernières années, avec un taux de mortalité de 0,3 à 1 décès pour 1 000 malades et une infection persistante chez plus de la moitié des malades pouvant entraîner une polyarthrite invalidante.
Pour autant, aucune prophylaxie vaccinale n’existait jusqu’à présent contre cet agent viral. Les résultats du candidat-vaccin VLA1553 de Valneva viennent de paraître dans le Lancet. Constitué d’un virus atténué, en l’occurrence un virus dont une des protéines essentielles est tronquée et inactive, ce vaccin à dose unique est censé cibler toutes les souches circulantes du virus du chikungunya en entraînant une réponse immunitaire rapide et durable.
Afin de tester sa sécurité et son efficacité, des chercheurs autrichiens ont réalisé un essai de phase III multicentrique en double aveugle. Entre septembre 2020 et avril 2021, 4 128 volontaires sains ont été enrôlés et randomisés dans 43 sites de vaccination aux États-Unis suivant un ratio 3:1 entre groupe vacciné (une dose intramusculaire, N = 3 093) et groupe contrôle (injection de placebo, N = 1 035). Le critère de jugement principal était la proportion de participants ayant un niveau séroprotecteur d’anticorps anti-virus du chikungunya 28 jours après vaccination. L’analyse de l’immunogénicité a été menée sur 266 personnes du groupe vacciné et 96 personnes du groupe placebo.
Publiés en juin dans le Lancet, les résultats sont très encourageants : 28 jours après vaccination, la quasi-totalité des participants (263 sur 266) vaccinés étaient séroprotégés contre le virus du chikungunya, versus aucun des sujets contrôles. Le vaccin était bien toléré, avec 1,5 % d’effets secondaires graves sur 3 082 vaccinés analysés, contre 0,8 % d’effets secondaires graves dans le groupe placebo – soit une différence non significative.
Une demande d’autorisation de mise sur le marché fait actuellement l’objet d’un examen prioritaire par la Food and Drug Administration (FDA) aux États-Unis.
En outre, une étude clinique de VLA1553 chez les adolescents est également en cours au Brésil.
Stephenson KE. Live-attenuated Chikungunya vaccine: a possible new era. Lancet 2023;401(10394);P2090-1.
Bartholomeeusen K, Daniel M, LaBeaud DA, et al. Chikungunya fever. Nat Rev Dis Primers 6 avril 2023.
Martin Agudelo L. Chikungunya : bientôt en métropole ? Rev Prat (en ligne) 20 juin 2023.