Le diabète de type 1 (DT1) ou insulinodépendant a une incidence croissante chez les sujets jeunes. Il est lié à la destruction auto-immune des cellules bêtapancréatiques qui assurent à la fois la perception du niveau de glycémie et l’insulinosécrétion. L’étude du groupe de recherche DCCT (Diabetes Control and Complications Trial) a largement montré l’efficacité du contrôle glycémique sur la prévention des complications du DT1.1
Néanmoins, la diminution de l’hémoglobine glyquée (HbA1c) au cours du DT1 est fréquemment associée à la survenue d’hypoglycémies responsables non seulement d’une altération de la qualité de vie mais aussi d’une surmortalité. Cette dernière est liée à la perte progressive de la perception des hypoglycémies, associée à une grande variabilité glycémique conduisant à un diabète dit instable.2
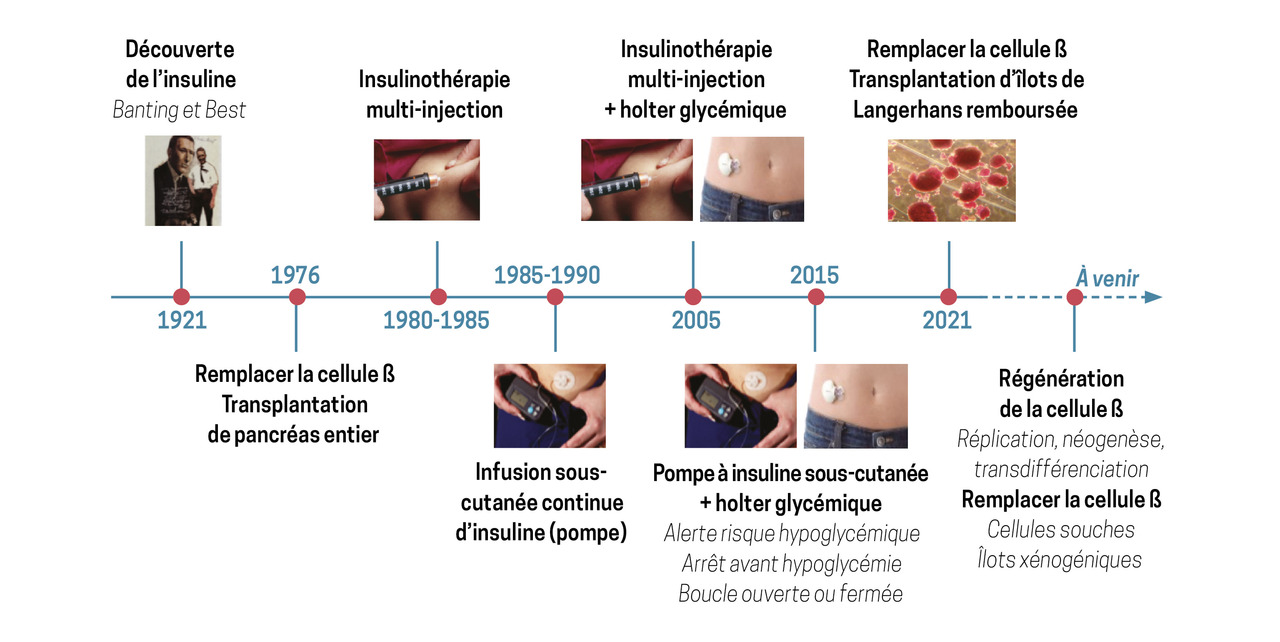
Bien que de nombreuses avancées scientifiques et technologiques aient été réalisées ces dernières années (
Ainsi, en cas de DT1 instable, avec échec des approches technologiques – quelle qu’en soit la raison –, la greffe d’îlots de Langerhans peut désormais être proposée en soins courants. Les essais cliniques ayant démontré sa faisabilité, sa sécurité, son efficacité supérieure à la pompe et des résultats durables et similaires à la greffe de pancréas à dix ans,3-5 elle est remboursée depuis 2021.
En quoi consiste la greffe d’îlots ?
La greffe d’îlots de Langerhans consiste à injecter des cellules pancréatiques endocrines, permettant de restaurer conjointement une insulinosécrétion endogène et la perception des hypoglycémies.6
Du donneur à l’isolement des îlots
Les îlots greffés sont actuellement issus du pancréas d’un donneur en état de mort cérébrale ou en arrêt de soins (cadre d’un prélèvement multi-organes). Le pancréas est attribué à un receveur sur liste d’attente par l’Agence de la biomédecine en fonction de différentes priorités, comme la compatibilité sanguine ABO et l’ancienneté de l’inscription.
L’isolement des îlots à partir du pancréas est réalisé par un laboratoire agréé. Le processus combine une digestion enzymatique et une purification du pancréas qui permet de séparer les cellules exocrines des cellules insulinosécrétrices tout en les maintenant groupées en unités fonctionnelles que sont les îlots.
Modalités d’administration
La préparation d’îlots prend alors la forme de suspension cellulaire conditionnée dans une poche de perfusion. Elle est infusée dans le foie via la veine porte, soit par abord radiologique sous anesthésie locale en ponctionnant la veine sous contrôle scopique, soit par mini-laparotomie sous anesthésie générale par un abord de Mc Burney.
Le choix de la voie d’abord est déterminé par l’expérience des centres greffeurs. La voie radiologique a un risque plus élevé de complications (hémorragies, thromboses), même si elle est moins invasive.
La masse insulaire extraite d’un seul pancréas permet de stabiliser les glycémies mais reste insuffisante pour obtenir une insulino-indépendance durable – objectif qui nécessite de répéter l’injection d’îlots une ou deux fois, idéalement sur une période de trois mois.
Simple à réaliser, mais pas anodine
En comparaison avec la greffe de pancréas entier, l’injection d’îlots est associée à une moindre morbidité chirurgicale, ce qui en fait un geste plus facile à proposer à des patients fragiles. Cependant, l’allogreffe nécessite une immunosuppression comportant deux étapes :
– une phase d’induction par un sérum antilymphocytaire ou un antirécepteur de l’interleukine 2 ;
– une phase de maintenance associant un inhibiteur des calcineurines (tacrolimus, le plus souvent) et du mycophénolate ou un inhibiteur de mToR.
Une surveillance étroite est de rigueur, car ce traitement est associé à un risque d’infections opportunistes et à une incidence accrue de cancers cutanés et de lymphomes. Le rapport bénéfices-risques doit donc être bien mesuré.
Le patient est avisé en amont de la greffe que la fréquence du suivi est hebdomadaire au centre de greffe pendant trois mois, puis mensuelle pendant neuf mois, et enfin trimestrielle au long cours.
Conditions de remboursement
Selon les recommandations de la Haute Autorité de santé (HAS), l’allogreffe d’îlots s’adresse à des patients diabétiques insulino-dépendants (le plus souvent de type 1) qui ont un diabète instable ou compliqué d’hypoglycémies non ressenties, ou déjà porteurs d’une greffe de rein.6,7
Autogreffe, en premier lieu
L’autogreffe d’îlots correspond au matériel cellulaire provenant du receveur lui-même, après une chirurgie pancréatique ou une pancréatite chronique hyperalgique. Elle est réalisée dans le but de prévenir un diabète insulinopénique et ne nécessite pas d’immunosuppression. En général, l’autogreffe est proposée directement par l’équipe de chirurgie.
Allogreffe pour les authentiques diabètes instables
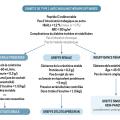
Actuellement, l’allogreffe d’îlots n’est pas proposée à tous les patients diabétiques de type 1 mais principalement en cas de diabète instable et/ou compliqué d’hypoglycémies nombreuses ou mal ressenties, en particulier en cas de greffe d’îlots seuls.8 Ces authentiques diabètes instables restent une situation assez rare, estimée à 3 cas pour 1 000 patients, se caractérisant par :
– la survenue imprévisible d’hypoglycémies nécessitant l’aide d’un tiers pour identifier la situation ou prendre son traitement ;
– l’impossibilité de maintenir la cible glycémique (0,7-1,8 g/L) au moins 50 % du temps pour les patients fragiles, 70 % pour les autres, avec un coefficient de variation important.
Option de la greffe après rein
La greffe d’îlots après rein est également proposée aux patients déjà porteurs d’une greffe rénale n’ayant pas pu bénéficier d’une greffe combinée rein-pancréas du fait de complications macro-angiopathiques sévères.
Quelles alternatives thérapeutiques à la greffe d’îlots ?
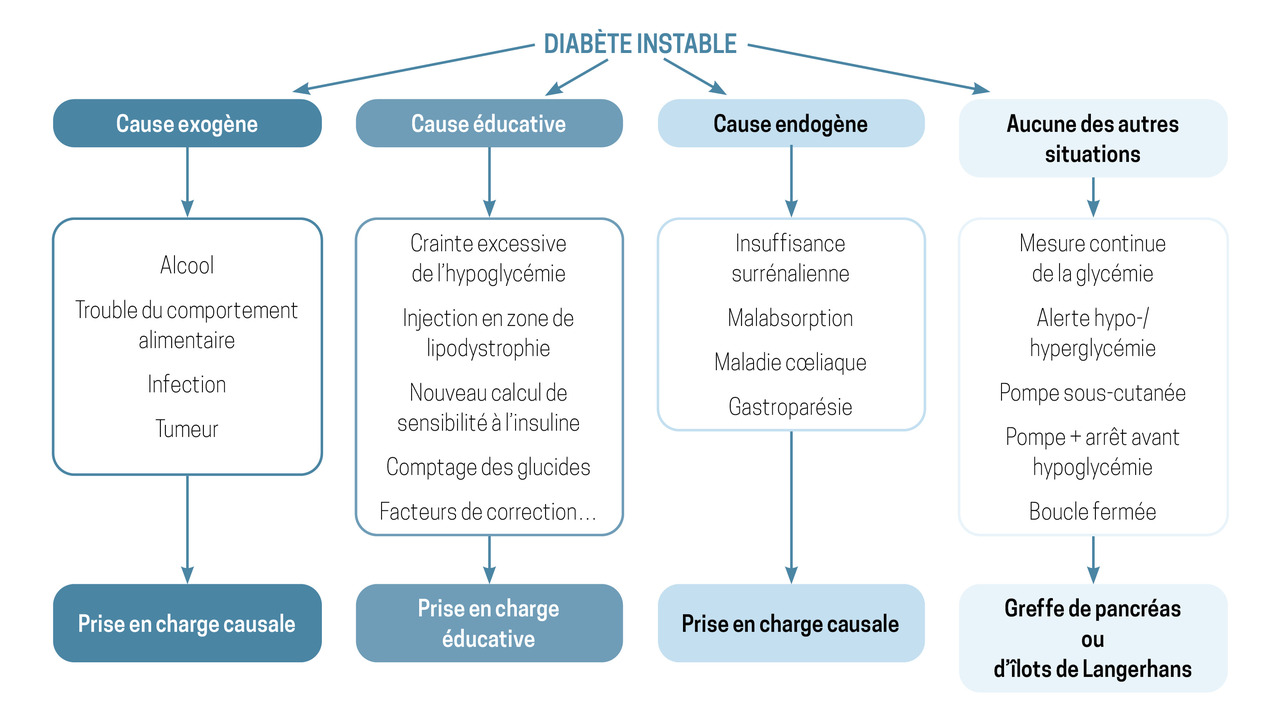
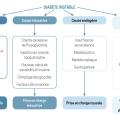
En cas d’instabilité glycémique, il convient de rechercher une cause organique ou comportementale (
En l’absence de ces causes, il est nécessaire de reprendre l’éducation thérapeutique et d’envisager l’administration d’insuline en pompe, avec capteurs, en boucle ouverte ou fermée. En cas d’échec, quelle qu’en soit la cause, une greffe d’îlots ou de pancréas peut être discutée.
La greffe de pancréas entier est une intervention lourde : elle est généralement combinée à une greffe de rein chez un patient de moins de 55 ans, d’indice de masse corporelle (IMC) inférieur à 30 kg/m2, sans complications macro-angiopathiques, mais avec une insuffisance rénale terminale.
Si le patient n’a pas d’insuffisance rénale terminale, une greffe de pancréas entier peut être discutée, mais la balance bénéfices-risques de cette chirurgie complexe est à prendre en compte.
Une greffe d’îlots seuls peut également être proposée chez des patients plus âgés (> 35-45 ans) avec un diabète instable insulino-dépendant depuis au moins cinq ans, en échec ou refus d’approches technologiques (
Quels résultats attendre de la greffe d’îlots ?
L’objectif principal de la greffe d’îlots est la restauration d’une insulinosécrétion et de la perception des hypoglycémies permettant l’arrêt de l’insulinothérapie exogène.
Elle améliore nettement l’équilibre et la variabilité glycémiques, ce qui permet d’obtenir un sevrage insulinique de plusieurs années lorsque la masse de cellules greffées est suffisante. Un quart des patients greffés restent insulino-indépendants au moins dix ans avec une HbA1c inférieure ou égale à 6,5 % ; la moitié gardent des îlots fonctionnels au moins une décennie, ce qui améliore la stabilité glycémique ; dans le quart restant, ils redeviennent insulino-dépendants en moyenne trois à dix ans après la greffe d’îlots.4
L’analyse des mesures continues du glucose a montré que la persistance d’un taux de peptide C, même faible, réduit significativement le temps en hypoglycémie (holter glycémique ou CGMS [continuous glucose monitoring system]), ce qui justifie de maintenir le traitement immunosuppresseur même en cas de reprise de l’insulinothérapie.8
Attention : le risque de mortalité par hypoglycémie chez le diabétique insulino-dépendant est toujours possible (évalué à 4 %, certes avant l’ère des capteurs). Le seul décès rapporté dans l’étude randomisée française a été observé dans le groupe non greffé, par hypoglycémie.3
Parcours de soins : quand et comment adresser le patient ?
Le médecin généraliste joue un rôle important dans la prise en charge du patient diabétique de type 1. L’indication d’une greffe d’îlots peut être évoquée par le médecin généraliste lui-même. Ce dernier peut également être amené à prodiguer des conseils au patient informé de ce traitement par le biais d’associations de patients, des médias ou du diabétologue.
Comprendre d’abord l’échec des autres traitements
Avant d’envisager une greffe d’îlots, il est nécessaire de connaître la qualité de l’équilibre glycémique du patient : l’HbA1c est-elle chroniquement élevée ? Les hypoglycémies sont-elles fréquentes ou mal ressenties ? Un coma hypoglycémique sévère est-il déjà survenu ? Autant de questions qui renseignent sur l’adhésion du patient à son traitement, à l’autosurveillance et aux règles d’hygiène de vie.
De multiples raisons peuvent être à l’origine d’un manque d’adhésion : des hypoglycémies répétées et/ou hyperglycémies chroniques affectant les capacités cognitives du patient ; la non-acceptation de la maladie ; un défaut d’éducation thérapeutique; une affection intercurrente ; des contraintes familiales et professionnelles laissant peu de temps au patient pour une bonne observance ; une hyperglycémie chronique maintenue par peur des hypoglycémies non ressenties ; un bon équilibre mais au prix d’un épuisement psychique altérant la qualité de vie.
Écouter pour convaincre
Un DT1 mal équilibré au long cours nécessite d’en référer au diabétologue afin d’éliminer les causes d’instabilité (
Même si l’indication de la greffe n’est pas tout à fait établie, discuter d’une proposition de stratégie thérapeutique sur le long terme – ce qui est déjà un acte thérapeutique – et connaître les avancées de la recherche peut être bénéfique pour le patient. Un avis extérieur peut aider celui-ci à « évoluer psychiquement » et accepter des contraintes thérapeutiques qui lui paraissaient autrefois intolérables.
Cette consultation, souvent nécessaire, permet au patient de percevoir que ses difficultés, son anxiété et sa souffrance sont reconnues et non pas seulement sanctionnées par la menace de complications.
Quels patients sont éligibles ?
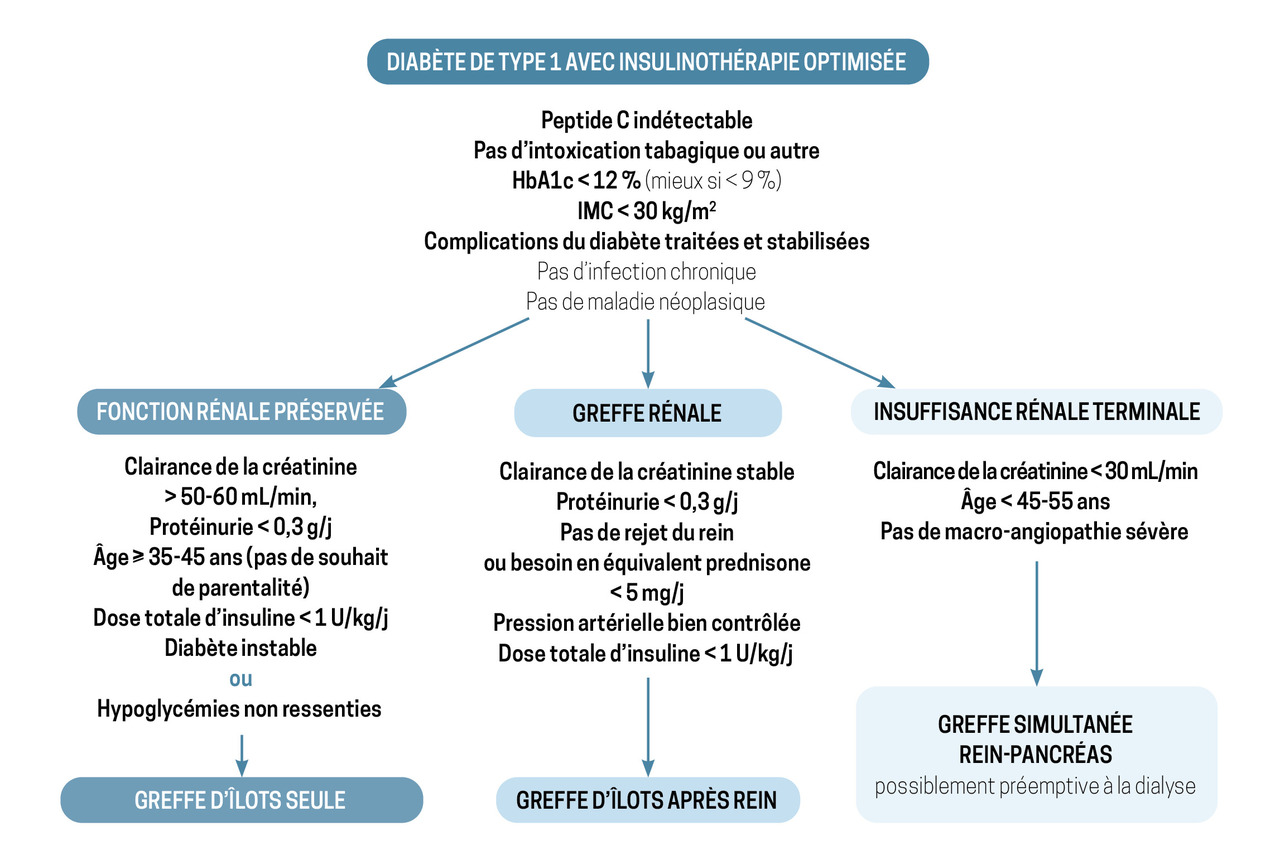
La greffe d’îlots est indiquée généralement chez les patients possédant le profil décrit dans le tableau. D’autres cas peuvent aussi être discutés.
La greffe d’îlots simultanée ou consécutive à la greffe de rein est souvent proposée par l’équipe de transplantation rénale, chez le patient DT1 de même profil que celui éligible à la greffe d’îlots seule.9
La greffe d’îlots simultanée à celle du rein est peu pratiquée mais permet de diminuer le nombre d’inductions puisque la première injection d’îlots est pratiquée, si l’isolement est bon, à partir du même donneur.
Généralement, le projet de greffe d’îlots après rein est antérieur à la greffe de rein après réfutation d’une double greffe rein-pancréas chez un patient fragile sur le plan vasculaire. Une greffe d’îlots peut également être proposée à la suite de la perte du greffon pancréatique lors d’une double greffe rein-pancréas.
La greffe d’îlots est réalisée idéalement dans les deux ans qui suivent la greffe de rein, sous réserve d’une fonction rénale satisfaisante, sans protéinurie, en l’absence d’épisodes de rejet, après sevrage de toute corticothérapie et adaptation éventuelle du traitement immunosuppresseur par le néphrologue.
Selon le profil du patient, le médecin généraliste peut adresser le patient au diabétologue référent avec lequel il travaille, parfois directement dans un centre d’évaluation, en vue d’une éventuelle greffe d’îlots. En attendant, le médecin généraliste peut informer le patient sur les alternatives thérapeutiques et leurs enjeux : insulinothérapie par pompe, capteurs, pompe avec arrêt automatique de l’insuline en cas d’hypoglycémie, boucle fermée, greffe de pancréas-organe.
Dans l’éventualité d’une greffe, le calendrier vaccinal du patient est vérifié, en particulier les vaccins contre le SARS-CoV-2 et le pneumocoque. Le sevrage tabagique est encouragé. Il convient d’orienter le patient vers le dentiste afin de dépister tout foyer infectieux et vers un cardiologue pour une échocardiographie et un dépistage de l’ischémie myocardique. En cas d’antécédent familial de cancer colique, une fibrocoloscopie est souhaitable. Enfin, une consultation gynécologique est indispensable chez les femmes, pour une mammographie et une contraception efficace.
Cellules souches, un espoir
La greffe d’îlots est donc une alternative à l’insulinothérapie optimisée en cas d’échec des approches technologiques dans le DT1 instable. Bien que son remboursement ait été obtenu en 2021, sa pratique se limite à quelques centres spécialisés en France et en Suisse. Elle est conditionnée à la prise d’un traitement immunosuppresseur, ce qui pour l’instant conduit à l’envisager plutôt chez des patients de plus de 40-45 ans.
Le développement de techniques à base de cellules souches devrait à l’avenir faciliter la disponibilité des greffons, néanmoins toujours au prix d’un traitement immunosuppresseur.10
Ce que le médecin généraliste doit savoir quand il suit un patient greffé d’îlots pancréatiques
Le médecin traitant doit appeler et/ou encourager le patient à appeler l’équipe de référence greffe disponible 24 h/24 pour tout événement intercurrent.
Il faut bannir toute corticothérapie (hyperglycémiante, même par voie inhalée ou percutanée).
Toute thérapeutique interférant avec le métabolisme des immunosuppresseurs (notamment les antifongiques imidazolés) est à exclure.
Le médecin doit rappeler au patient la nécessité d’éviter toute automédication (millepertuis) et la consommation de pamplemousse, qui interfèrent avec le métabolisme des immunosuppresseurs.
Le dosage des immunosuppresseurs se fait à jeun, avant la prise des médicaments (dosage résiduel).
En cas d’insuffisance rénale, le centre de greffe doit être averti car la dose des immunosuppresseurs est alors revue à la baisse, leur accumulation altérant la fonction rénale.
Le médecin traitant doit absolument veiller à ce que le patient n’arrête jamais son traitement immunosuppresseur.
Une antibiothérapie usuelle peut être prescrite en cas d’infection, mais il faut en référer au service de greffe si les symptômes persistent au-delà de 48 heures.
À l’apparition d’une aphtose buccale (qui peut être favorisée par le sirolimus), l’hémogramme doit être contrôlé : toute leucopénie doit faire réaliser une antigénémie vis-à-vis du cytomégalovirus.
La prévention de l’aphtose buccale repose sur une hygiène dentaire rigoureuse : brossage des dents 3 fois par jour et bains de bouche.
Que dire à vos patients
La greffe d’îlots pancréatiques est pratiquée dans les centres autorisés par l’Agence de biomédecine.
Elle est proposée en cas d’échec de l’insulinothérapie optimisée (multi-injections, pompe, pompe avec arrêt automatique avant hypoglycémie, boucle fermée) en raison d’hypoglycémies sévères et non ressenties.
Elle nécessite 2 à 3 injections de cellules sous anesthésie et un traitement immunosuppresseur après un bilan prégreffe soigneux.
Elle est indiquée en cas de diabète instable après échec des approches en pompe ou après greffe de rein.
Des sites d’information et d’association sur la greffe d’îlots sont disponibles :
– Fédération française des diabétiques : https://bit.ly/3FZfWMt
– Infos diabète : https://bit.ly/3Mwggoq
– Site de l’association TREPID : https://wp2.silvernet.fr/
Actuellement, les centres accueillant les patients pour greffe d’îlots sont Grenoble, Lille, Lyon, Montpellier, Strasbourg, Paris, Toulouse, Nantes et Nancy. Des informations supplémentaires peuvent être obtenues à la consultation de diabétologie ou de néphrologie de ces différents centres.
1. The Diabetes Control Complications Trial Research Group. The effect of intensive treatment of diabetes on the development and progression of long-term complications in insulin-dependent diabetes mellitus. N Engl J Med 1993;329(14):977-86.
2. Choudhary P, Rickels MR, Senior PA, et al. Evidence-informed clinical practice recommendations for treatment of type 1 diabetes complicated by problematic hypoglycemia. Diabetes Care 2015;38(6):1016-29.
3. Lablanche S, Vantyghem MC, Kessler L, et al. Islet transplantation versus insulin therapy in patients with type 1 diabetes with severe hypoglycaemia or poorly controlled glycaemia after kidney transplantation (TRIMECO): a multicentre, randomised controlled trial. Lancet Diabetes Endocrinol 2018;6(7):527-37.
4. Vantyghem MC, Chetboun M, Gmyr V, et al. Ten-Year Outcome of Islet Alone or Islet After Kidney Transplantation in Type 1 Diabetes: A Prospective Parallel-Arm Cohort Study. Diabetes Care 2019;42(11):2042-9.
5. Lablanche S, Borot S, Wojtusciszyn A, et al. Ten-year outcomes of islet transplantation in patients with type 1 diabetes: Data from the Swiss-French GRAGIL network. Am J Transplant 2021;21(11):3725-33.
6. Vantyghem MC, de Koning EJP, Pattou F, et al. Advances in ß-cell replacement therapy for the treatment of type 1 diabetes. Lancet 2019;394(10205):1274-85.
7. Wojtusciszyn A, Branchereau J, Esposito L, et al. Indications for islet or pancreatic transplantation: Statement of the TREPID working group on behalf of the Société francophone du diabète (SFD), Société française d’endocrinologie (SFE), Société francophone de transplantation (SFT) and Société francophone de nephrologie-dialyse-transplantation (SFNDT). Diabetes Metab 2019;45(3):224-37.
8. Chetboun M, Jannin A, Kerr-Conte J, et al. 1921-2021: From insulin discovery to islet transplantation in type 1 diabetes. Ann Endocrinol (Paris) 2021;82(2):74-7.
9. Kukla A, Ventura-Aguiar P, Cooper M, et al. Transplant Options for Patients With Diabetes and Advanced Kidney Disease: A Review. Am J Kidney Dis 2021;78(3):418-28.
10. Jones PM, Persaud SJ. Beta cell replacement therapy for type 1 diabetes: closer and closer. Diabet Med 2022;39(6):e14834.

 Encadrés
Encadrés