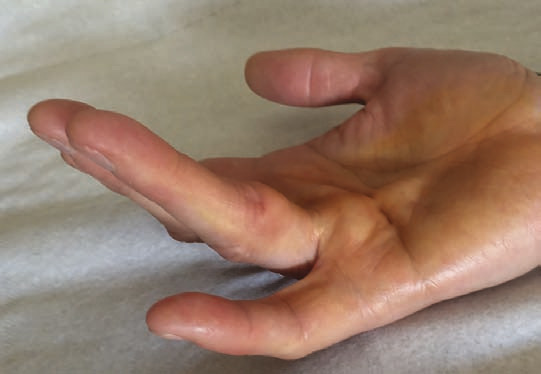
Cette maladie est liée à une rétraction fibreuse de l’aponévrose palmaire moyenne, pouvant entraîner une flexion progressive et irréductible d’un ou plusieurs doigts (surtout les 4e et 5e,figure 1). Elle touche environ 5 % de la population nord-européenne, essentiellement les hommes (80 %), avec un âge de début moyen autour de 50 ans. En France, sa fréquence est estimée entre 4 % et 10 % de la population générale.
C’est une affection génétique autosomique dominante, touchant surtout les personnes d’ascendance viking (jusqu’à 30 % des hommes en Islande). Diabète de type 1 et 2, consommation excessive d’alcool, prise d’antiépileptiques ou de certains antituberculeux, microtraumatismes répétés et travail mains fermées sont des facteurs de risque reconnus.
Le diagnostic est clinique : on retrouve des brides, digitales, palmaires ou digitopalmaires, des nodules durs et des dépressions en capiton dans la paume de la main. Il existe des formes avec des coussinets face dorsale en regard des articulations interphalangiennes proximales (diathèse de Dupuytren).
Comment évaluer la sévérité ?
Généralement indolore, cette maladie peut être néanmoins très handicapante. Les plaintes sont très variables : gêne uniquement esthétique ou fonctionnelle liée aux nodules ou cordes (attraper ou serrer des objets) ou à un flessum (difficultés pour serrer une main, pour se laver le visage…).
La sévérité est fonction de l’importance de l’angle d’ouverture des doigts. En pratique, ce qui distingue les formes graves des simples, c’est l’atteinte de plusieurs axes digitaux mais surtout une fibrose dans le doigt et l’association à un blocage articulaire des interphalangiennes.
Les formes très sévères sont rares, mais les facteurs de mauvais pronostic sont : début à un jeune âge, caractère très récidivant après traitement (quel qu’il soit), association avec d’autres pathologies fibrosantes (maladie de Ledderhose, de Lapeyronie, coussinets dorsaux des phalanges).
L’évolution se fait par poussées non prévisibles, à vitesse très variable d’un patient à l’autre et d’un doigt à un autre.
Quels traitements ?
Aujourd’hui : seulement pour les atteintes avancées
À l’heure actuelle, les techniques médicochirurgicales sont proposées lorsque le patient est véritablement gêné ou s’il ne peut plus poser la main à plat sur une table (test de la table). Leur choix est fonction de l’âge, de la localisation de la lésion, de la diffusion de la maladie, des antécédents de récidive. Ainsi, aucun traitement n’est à ce jour autorisé pour les stades débutants, sans flessum.
Dès que le flessum apparaît, l’aponévrotomie percutanée à l’aiguille ou les injections de collagénase peuvent être proposées. La première est une intervention non chirurgicale, ambulatoire et rapide, nécessitant une simple anesthésie locale : elle consiste à réaliser des perforations et sections des cordes aponévrotiques à travers la peau, à l’aide du biseau de l’aiguille utilisée pour l’injection de l’anesthésique. Les mouvements de va-et-vient de l’aiguille fragilisent la bride. Une extension du doigt complète la rupture de la fibrose. La deuxième est une injection de collagénase (Xiapex) au niveau de la corde aponévrotique rétractée (au maximum 3 points d’injection par corde). Une extension passive de l’articulation en flessum est réalisée par le médecin 24 heures après.
Pour les formes palmaires, on fait le test de la table : en cas d’impossibilité de mettre la main à plat, il y a déjà une indication à un geste local d’aponévrotomie percutanée. Dans les atteintes digitales, il faut traiter avant l’apparition d’un enraidissement articulaire.
Les formes sévères peuvent parfois être améliorées par une multi-aponévrotomie mais l’aponévrectomie chirurgicale est souvent la solution, surtout si les récidives sont fréquentes.
Un premier traitement pour les stades précoces ?
Un traitement pharmacologique pour les stades débutants de la maladie vient de faire ses preuves, pour la première fois, dans un essai randomisé en double aveugle contre placebo. L’étude, récemment parue dans le Lancet Rheumatology, a évalué l’efficacité de l’adalimumab dans cette indication : c’est un anticorps monoclonal anti-TNF-alpha utilisé dans certaines maladies inflammatoires comme la polyarthrite rhumatoïde, la spondylarthrite ankylosante, le psoriasis….
Entre février 2017 et janvier 2019, 140 patients ont été suivis (66 % d’hommes ; âge moyen : 59,7 ans). Ils étaient atteints de la maladie de Dupuytren, aux stades débutants, avec de nodules cliniquement observés et une histoire de progression dans les 6 mois précédents.
Les patients, répartis aléatoirement à parts égales, ont reçu soit des injections intranodulaires d’adalimumab (40 mg dans 0,4 mL), soit un placebo (solution saline, même volume), à 4 reprises : à l’inclusion, à 3 mois, 6 mois et à 9 mois. Ils ont été suivis à 12 et 18 mois.
À 12 mois, la dureté des nodules (critère principal, évalué sur 113 participants), évaluée à l’aide d’un duromètre, était moins importante dans le groupe traité par adalimumab que dans le bras contrôle (différence moyenne de plus de 4 points ; puis de 5 à 18 mois). La surface des nodules était également plus petite dans le groupe traité, à 12 mois (différence moyenne de 8,4 mm2), et encore plus à 18 mois (différence moyenne de 14,4 mm2). Aucune différence significative n’a été notée dans la hauteur des nodules entre les deux groupes à 12 mois, mais à 18 mois elle était diminuée de 1,1 mm dans le groupe traité par rapport au placebo.
Le traitement était sûr, aucun effet indésirable grave lié aux injections n’a été observé. Les effets indésirables locaux étaient des réactions mineures au site d’injection (démangeaisons, rougeurs, ecchymoses, hématomes), enregistrés à 25 reprises (placebo = 16, adalimumab = 9). Il n'y a pas eu de lésions nerveuses.
Des répercussions cliniques n’étaient pas observées parce que, aux stades précoces, la maladie a peu de conséquences fonctionnelles. Ainsi, au cours du suivi, il n’y a pas eu de changement significatif du déficit d’extension passive des articulations métacarpophalangiennes touchées, ni de la fonction préhensile. Cependant, un plus grand nombre de patients du groupe placebo ont vu leur maladie progresser ou étaient en attente d’une intervention chirurgicale, par rapport à ceux traités (mais les chiffres globaux étaient faibles : 10 et 3 respectivement).
C’est pourquoi, expliquent les auteurs, un suivi sur 10 ans est nécessaire, avec éventuellement d’autres injections si le nodule devait se réactiver, pour vérifier si la réduction dans la dureté et la taille des nodules induite par l’adalimumab a une incidence sur le développement des déformations des doigts et de la fonction de la main.
Lellouche H. Maladie de Dupuytren.Rev Prat Med Gen 2017;31(975):116-7.