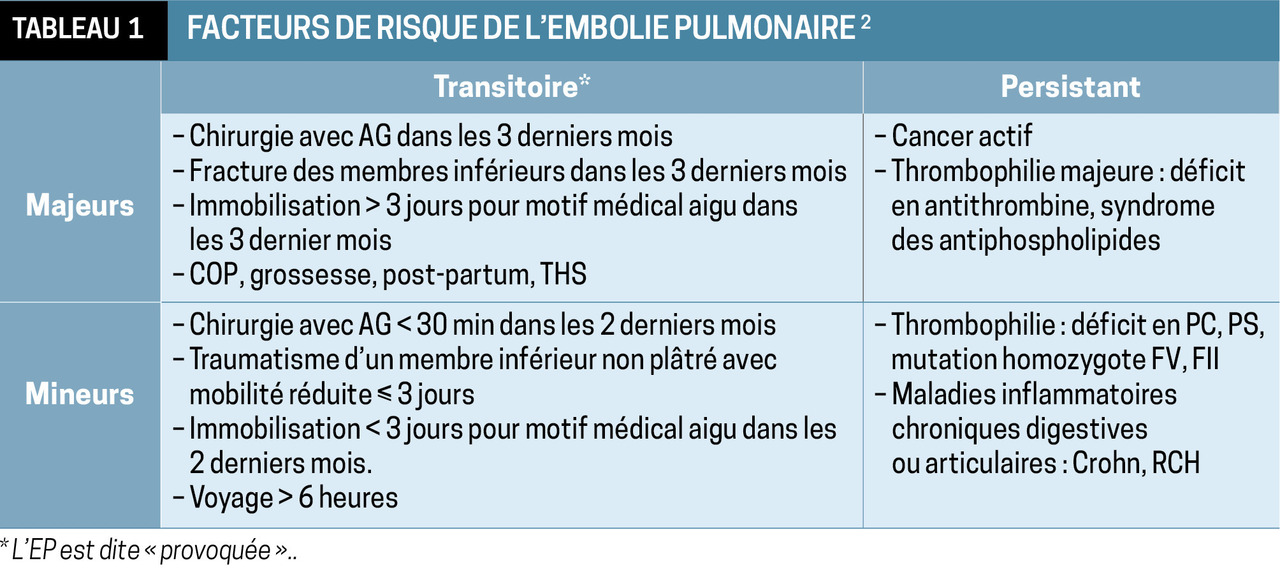
Facteurs de risque
Évaluer le risque de mortalité
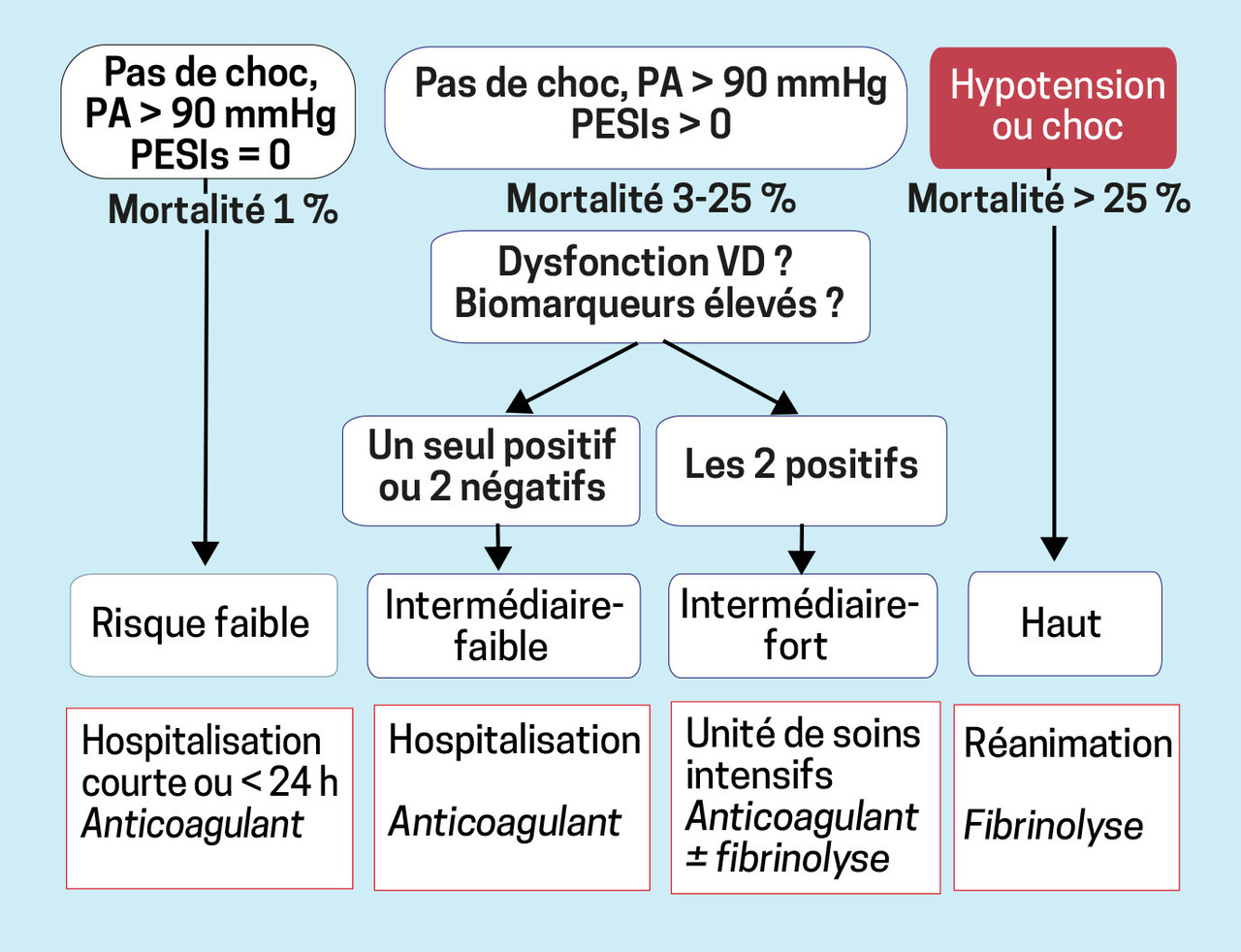
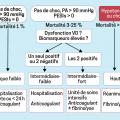
Première étape, on évalue la pression artérielle. Une PAS < 90 mmHg ou une baisse de la PA ≥ 40 mmHg sur 15 minutes signent un haut risque de décès, supérieur à 25 %. Une prise en charge spécifique en réanimation s’impose (5 % des EP). Outre les mesures symptomatiques (oxygénothérapie, remplissage vasculaire et catécholamines en cas de choc malgré le remplissage), héparinothérapie intraveineuse et thrombolyse sont rapidement nécessaires (
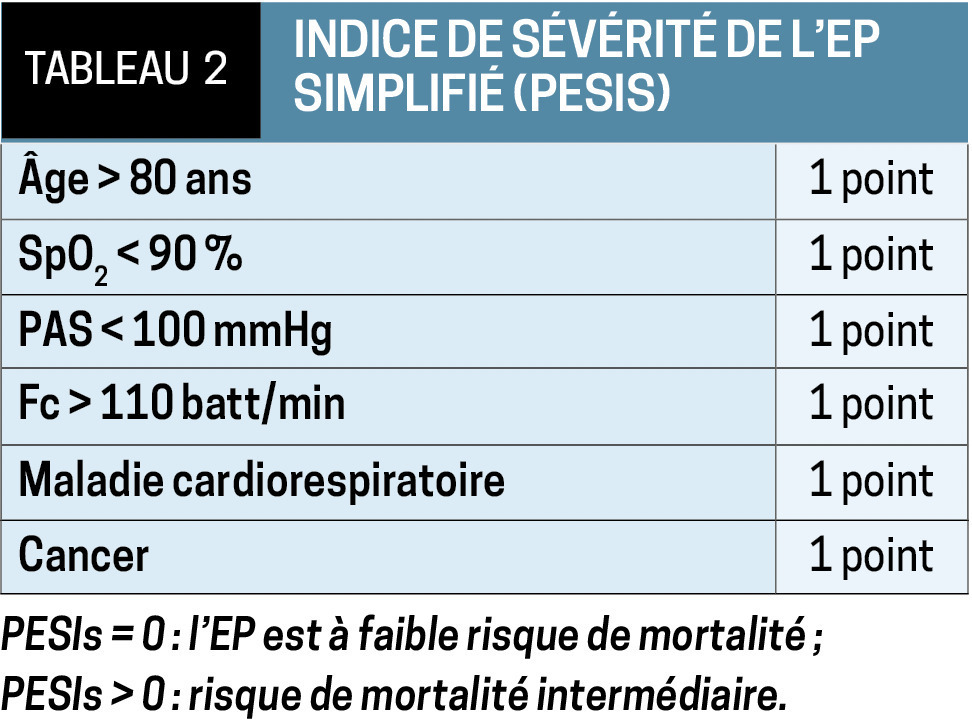
Deuxième étape, lorsque la PAS > 90 mmHg, on détermine le score PESIs (Pulmonary Embolism Severity Index simplified) afin d’évaluer le pronostic de ces patients stables hémodynamiquement. Ce score (tableau 2) les classe en 2 catégories : risque faible de mortalité (1 %) et risque intermédiaire (compris entre 3 et 25 %). Il est fondé sur des paramètres cliniques simples : l’âge, la fréquence cardiaque, la PAS, la saturation en oxygène en air ambiant, un cancer actif, une maladie cardiorespiratoire. Un PESIs à 0 reflète un faible risque, tandis que ≥ 1, il est intermédiaire.
Troisième étape, si l’EP est à risque intermédiaire, on évalue le retentissement cardiaque droit avec 2 paramètres : élévation des marqueurs cardiaques (BNP, NT-proBNP, troponine I ou T) et dilatation des cavités droites (rapport VD/VG > 1 au scanner ou > 0,9 à l’échographie cardiaque transthoracique). Si ces 2 paramètres sont présents, le risque de mortalité est intermédiaire élevé ; si un seul est noté, il est intermédiaire faible.
Lorsque le risque est intermédiaire élevé, une hospitalisation avec surveillance rapprochée dans une unité de soins intensifs avec monitorage continu s’impose compte tenu d’une éventuelle évolution défavorable.
Un traitement injectable (HNF ou HBPM) doit être instauré rapidement, et la thrombolyse doit être discutée en cas de dégradation de l’état clinique. Au décours des premiers jours sous héparinothérapie, un relais par antivitamine-K (AVK ; avec chevauchement) ou par AOD (sans chevauchement) doit être réalisé si le patient n’a plus de critères de gravité.
Qui traiter en ambulatoire ?
Si le risque est intermédiaire faible, elle peut être envisagée au cas par cas à l’aide du score HESTIA (encadré 1), fondé sur des critères très pragmatiques : contexte médico-social, grossesse, douleur thoracique nécessitant un antalgique…
Un score égal à 0 sélectionne les patients éligibles au traitement ambulatoire. Que le risque soit faible ou intermédiaire faible, l’anticoagulation est incontournable soit conventionnelle par héparinothérapie puis AVK, soit par un AOD d’emblée sans prétraitement héparinique (rivaroxaban, Xarelto, apixaban, Eliquis). Les AOD, plus maniables, sont à privilégier. En effet, leur non-infériorité par rapport aux AVK a été démontrée sur le risque de récidive.
En outre, ils induisent moins d’hémorragie grave, en particulier cérébrale.
Ce type de traitement impose une filière de soin spécifique dédiée à la MVTE et une structure d’accueil pour assurer une consultation précoce dans les jours qui suivent l’hospitalisation et/ou le passage aux urgences, en accord avec le patient et son médecin traitant. Cette filière optimise la prise en charge ultérieure. Objectifs de la consultation spécialisée précoce : débuter une enquête à la recherche de facteurs de risque d’événements thrombo-emboliques comme le cancer, adapter le choix thérapeutique initial, informer le patient et son entourage sur la MVTE et son traitement, s’assurer de la compréhension et de l’observance thérapeutique et organiser le suivi ultérieur. Débriefing abordant chacun de ces points, elle est souvent l’occasion d’une « dédramatisation » et d’une réassurance des patients parfois particulièrement stressés à leur sortie des urgences.
Anticoagulant : combien de temps ?
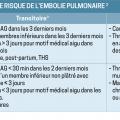
Le risque de récidive à l’arrêt des anticoagulants est faible si l’EP est provoquée par un facteur transitoire majeur (< 3 %/an) tandis qu’il est multiplié par 3 (> 9 % l’année suivant l’arrêt) s’il s’agit d’un épisode initial non provoqué ou associé à un cancer.
Si un traitement anticoagulant doit être prolongé, le risque hémorragique doit aussi être pris en compte. En effet, le risque de récidive thrombo-embolique est maximal la première année, puis décroît, tandis que le risque hémorragique augmente de façon linéaire avec l’âge. Ainsi, ce dernier peut devenir supérieur à celui de récidive sans traitement anticoagulant.
Une durée réduite à 4 ou 6 semaines comparée à 3 ou 6 mois est associée à 2 fois plus de récidives thrombo-emboliques. Par conséquent, la durée minimale est de 3 mois.
Prolonger le traitement 6 mois versus 3 mois ne s’accompagne pas d’une réduction de ce risque.5
Un essai randomisé multicentrique français PADIS EP, contrôlé, en double aveugle, a comparé un traitement prolongé de 18 mois par warfarine à un placebo chez 371 patients traités initialement 6 mois pour un premier épisode d’EP non provoquée.6 La poursuite de l’AVK était associée à une réduction du risque de récidive de 90 %. En revanche, dès l’arrêt de l’anticoagulant, le bénéfice n’était pas maintenu, et la fréquence des récidives n’était plus significativement différente entre les deux groupes.
Prolonger l’anticoagulant pendant 18 mois, après les 6 premiers mois, n’a pas d’impact durable sur le risque de récidive après l’arrêt.
Trois implications cliniques
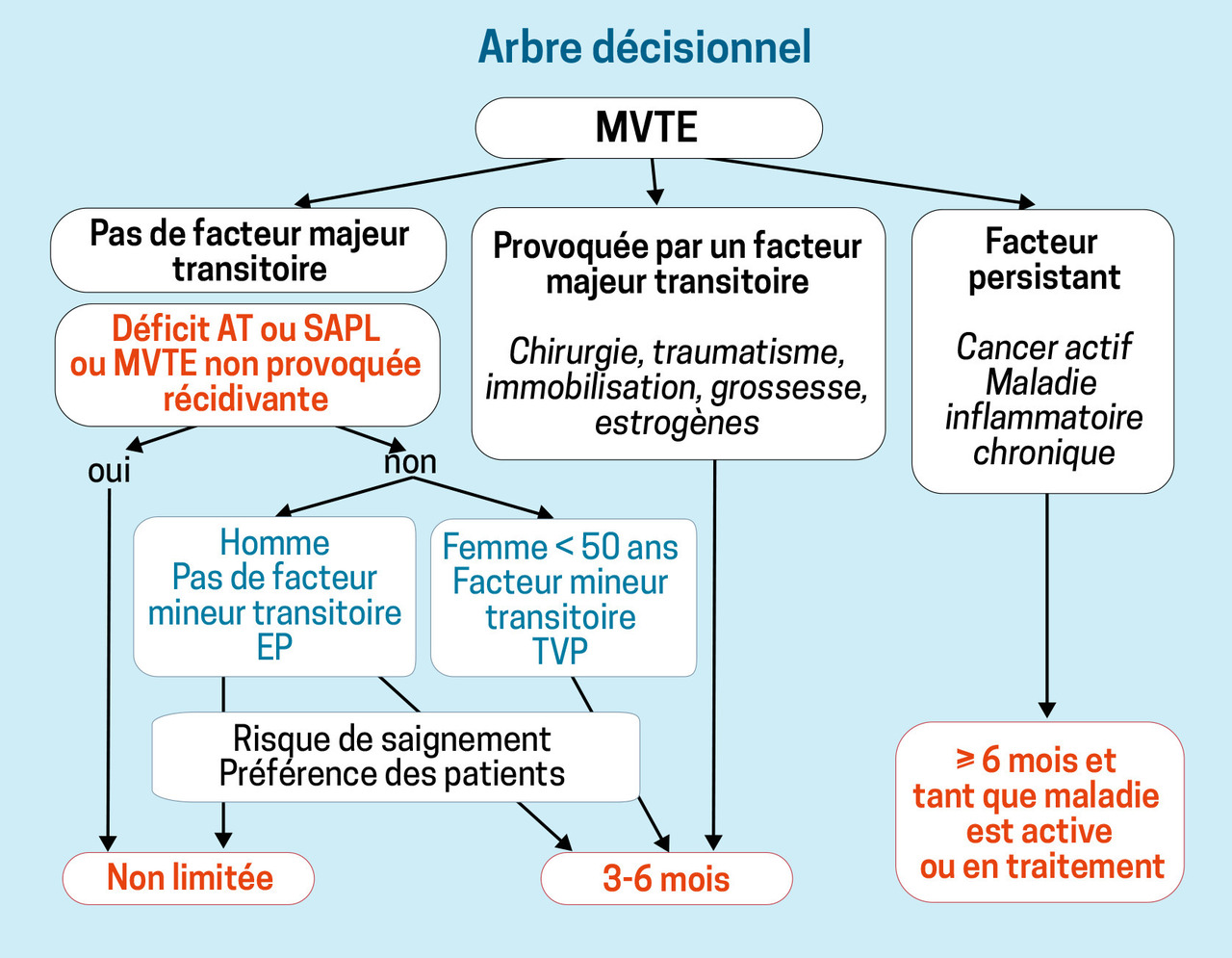
EP provoquée par un facteur majeur transitoire : 3 mois, voire 6 au maximum sont suffisants (faible risque de récidive).
Première EP non provoquée par un facteur majeur transitoire et non associée à un facteur persistant (absence de cancer essentiellement), 2 options : soit 3 à 6 mois au maximum, soit une durée non limitée (sans programmation de date d’arrêt).
EP associée à un cancer : on traite 6 mois au minimum et tant que le cancer est actif ou nécessite une thérapie anticancéreuse.
1. Score HESTIA
Le patient a-t-il une instabilité hémodynamique ?
Une thrombolyse ou embolectomie est-elle nécessaire ?
Le patient a-t-il une hémorragie active ou un risque élevé de saignement ?
A-t-il besoin ou eu besoin de plus de 24 heures d’oxygénothérapie pour maintenir une saturation en O2 > 90 % ?
L’embolie pulmonaire a-t-elle été diagnostiquée sous traitement anticoagulant ?
Le patient a-t-il une douleur intense nécessitant un antalgique intraveineux durant plus de 24 heures ?
Sa clairance de la créatinine est-elle < 30 mL/min ?
A-t-il une insuffisance hépatique sévère ?
La patiente est-elle enceinte ?
Antécédents documentés de thrombopénie induite par héparine ?
Autre raison médicale ou sociale motivant une hospitalisation de plus de 24 heures ?
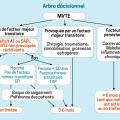
2. Première EP non provoquée : quelle durée traiter ?
Dans PADIS EP et d’autres études, environ 30 à 40 % des patients récidivent après un premier épisode d’EP non provoquée. Ainsi, l’objectif est d’identifier les patients à haut risque de récidive qui doivent bénéficier d’un anticoagulant pour une durée non limitée et ceux à faible risque chez qui 3 à 6 mois suffisent.
Des facteurs modulateurs peuvent aider. Ceux incitant à prolonger le traitement sont les thrombophilies héréditaires majeures : déficit en antithrombine, en protéine C ou S, combinées et homozygotes (facteur V Leiden ou mutation sur le gène de la prothrombine), filtre cave, maladie inflammatoire chronique digestive ou articulaire, sexe masculin, sévérité de l’EP (risque intermédiaire élevé ou risque fort) et préférence du patient.
En revanche, les jeunes femmes (< 50 ans) ont un faible risque de récidive thrombo-embolique après arrêt, et un traitement court est le plus souvent indiqué ; un facteur mineur (ex : trajet en avion de plus de 6 heures, entorse non plâtrée) incite aussi à un traitement court.4 Enfin, la décision de prolonger la durée doit prendre en compte les souhaits du patient pour une meilleure observance thérapeutique (fig. 2).
Actuellement, les modalités d’un traitement anticoagulant prolongé ne sont pas claires et font l’objet d’un protocole de recherche clinique d’initiative française (projet RENOVE, NCT03285438), dont le but est d’évaluer un AOD (apixaban ou rivaroxaban) à demi-dose versus pleine dose avec une durée non limitée.
2. Kearon C, Akl EA, Ornelas J, et al. Antithrombotic Therapy for VTE Disease: CHEST Guideline and Expert Panel Report. Chest 2016;149:315-52.
3. Konstantinides SV, Torbicki A, Agnelli G, et al. 2014 ESC guidelines on the diagnosis and management of acute pulmonary embolism. Eur Heart J 2014;35:3033-69, 69a-69k.
4. Rodger MA, Le Gal G, Anderson DR, Schmidt J, Pernod G, Kahn SR, et al. Validating the HERDOO2 rule to guide treatment duration for women with unprovoked venous thrombosis: multinational prospective cohort management study. BMJ 2017;356:j1065.
5. Boutitie F, Pinede L, Schulman S, et al. Influence of preceding length of anticoagulant treatment and initial presentation of venous thromboembolism on risk of recurrence after stopping treatment: analysis of individual participants’ data from seven trials. BMJ 2011;342:d3036.
6. Couturaud F, Sanchez O, Pernod G, et al. Six Months vs Extended Oral Anticoagulation After a First Episode of Pulmonary Embolism: The PADIS-PE Randomized Clinical Trial. JAMA 2015;314:31-40.

 Encadrés
Encadrés