L’encéphalopathie hépatique (EH), complication la plus fréquente de la cirrhose, a une expression clinique variable, allant de simples troubles neurocognitifs au coma. Elle peut engager le pronostic vital. Dépistage, au mieux à un stade précoce, et traitement sont donc cruciaux. Un facteur précipitant doit systématiquement être recherché et traité. On dispose de recommandations récentes de la Société française d’hépatologie (AFEF).1 Une attention particulière doit être portée aux diagnostics différentiels, notamment lorsque l’ammoniémie est normale.
De quoi parle-t-on ?
D’un ensemble des troubles neurologiques et neuropsychiatriques survenant au cours des maladies du foie ou chez des patients ayant des shunts porto-systémiques.2 Nous ne décrirons que l’EH au cours de la cirrhose, dite de type C.
Trente à 45 % des patients atteints de cirrhose auront une EH clinique au cours de l’évolution. La forme minime – examen normal et altérations détectées aux tests neurocognitifs – peut, quant à elle, toucher jusqu’à 85 % des sujets dans certaines séries.
Ces 10 dernières années, la pose d’un TIPS (Transjugular Intrahepatic Portosystemic Shunt) est souvent discutée devant une hémorragie digestive par rupture de varices ou une ascite réfractaire. Après TIPS, l’EH survient chez environ 35 % des patients.
Trente à 45 % des patients atteints de cirrhose auront une EH clinique au cours de l’évolution. La forme minime – examen normal et altérations détectées aux tests neurocognitifs – peut, quant à elle, toucher jusqu’à 85 % des sujets dans certaines séries.
Ces 10 dernières années, la pose d’un TIPS (Transjugular Intrahepatic Portosystemic Shunt) est souvent discutée devant une hémorragie digestive par rupture de varices ou une ascite réfractaire. Après TIPS, l’EH survient chez environ 35 % des patients.
Physiopathologie
Elle est incomplètement comprise. L’hyperammoniémie joue un rôle central. De récents travaux ont montré une synergie entre cette dernière et l’inflammation systémique. Au cours de la cirrhose, la production d’ammoniaque par les entérocytes est accrue, et son élimination moindre, en raison de l’insuffisance hépatique (dysfonctionnement du cycle de l’urée au niveau hépatique) ou des shunts porto-systémiques limitant le premier passage hépatique. Dans ces conditions, seules les cellules musculaires striées et les astrocytes peuvent métaboliser l’ammoniaque en glutamine. Ceci explique probablement pourquoi l’EH est plus fréquente chez les patients sarcopéniques.
Clinique : de l’astérixis au coma
Les symptômes les plus fréquents sont l’astérixis et le ralentissement psychomoteur, non pathognomoniques de l’EH clinique. Viennent ensuite léthargie, syndrome extrapyramidal, crises convulsives ou coma. Ces manifestations varient au cours du temps…
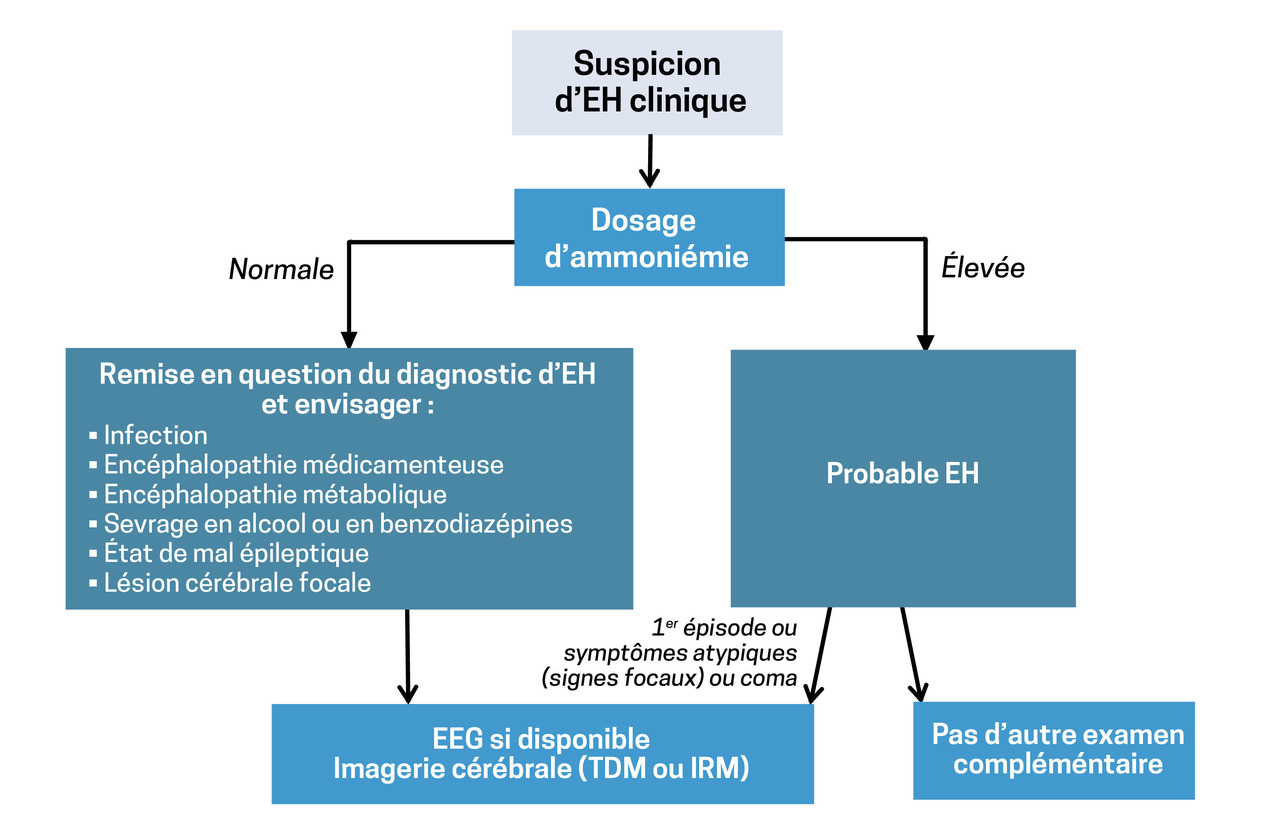
Ammoniémie, EEG et imagerie contribuent au diagnostic. Étant donné le rôle central de l’hyperammoniémie, son absence (< 50 μmol/L) remet en cause le diagnostic. À l’inverse, elle ne traduit pas obligatoirement une EH. L’EEG montre typiquement un tracé ralenti avec des ondes lentes triphasiques. Enfin, l’imagerie cérébrale en coupe, scanner ou au mieux IRM cérébrale, aide à éliminer des diagnostics différentiels. Des techniques plus sophistiquées telles que l’IRM cérébrale avec spectro-IRM étayent le diag- nostic.
Divers diagnostics différentiels sont à connaître (tableau ). En l’absence de signes neurologiques focaux, il faut éliminer les autres encéphalopathies métaboliques (urémique, hypercapnique, septique), le sevrage en alcool et l’état de mal non convulsivant.
Ammoniémie, EEG et imagerie contribuent au diagnostic. Étant donné le rôle central de l’hyperammoniémie, son absence (< 50 μmol/L) remet en cause le diagnostic. À l’inverse, elle ne traduit pas obligatoirement une EH. L’EEG montre typiquement un tracé ralenti avec des ondes lentes triphasiques. Enfin, l’imagerie cérébrale en coupe, scanner ou au mieux IRM cérébrale, aide à éliminer des diagnostics différentiels. Des techniques plus sophistiquées telles que l’IRM cérébrale avec spectro-IRM étayent le diag- nostic.
Divers diagnostics différentiels sont à connaître (
EH minime : difficile à détecter
En effet, pas de critère simple disponible en routine. Par ailleurs, là encore, les symptômes sont fluctuants. Certains patients ne se rendent pas compte des troubles ou, au contraire, les cachent. L’entourage a un rôle capital en rapportant notamment des modifications subtiles du comportement et/ou des performances. Sont évocatrices des anomalies des tests neurocognitifs tels que le PHES (psychometric hepatic encephalopathy score). Cependant, chronophage (30 minutes environ), il est peu utilisé en pratique.
L’EH minime engage le pronostic car elle favorise l’EH clinique, altérant la qualité de vie. Il faut la dépister chez tous les patients atteints de cirrhose. Récemment, un test simple dit de dénomination des animaux (nombres d’animaux cités en 60 secondes) a été recommandé par l’AFEF.1
Il est parfois difficile de la différencier d’une affection neurodégénérative. Dans ces circonstances, les symptômes fluctuent peu. Deux attitudes : bilan complet auprès d’un centre spécialisé ou traitement d’épreuve (cf. infra).
L’EH minime engage le pronostic car elle favorise l’EH clinique, altérant la qualité de vie. Il faut la dépister chez tous les patients atteints de cirrhose. Récemment, un test simple dit de dénomination des animaux (nombres d’animaux cités en 60 secondes) a été recommandé par l’AFEF.1
Il est parfois difficile de la différencier d’une affection neurodégénérative. Dans ces circonstances, les symptômes fluctuent peu. Deux attitudes : bilan complet auprès d’un centre spécialisé ou traitement d’épreuve (cf. infra).
Étapes de la prise en charge
Après exclusion des diagnostics différentiels : évaluer la sévérité qui peut motiver un passage en soins intensifs ; identifier et éradiquer les facteurs précipitants ; traiter l’hypoammoniémie ; prévenir la récidive.
Sont précipitants : hémorragie digestive, infection, déshydratation/dysnatrémie/ insuffisance rénale, constipation et médicaments sédatifs ou non. Ils peuvent précéder l’EH ou être contemporains. Leur traitement l’améliore dans 90 % des cas. De plus, leur éviction peut être préventive.
Étant donné l’association entre IPP et EH, leur prescription doit être limitée aux strictes indications. Tous les sédatifs (benzodiazépines) sont contre- indiqués au cours de la cirrhose. Sauf si surviennent crise convulsive ou delirium tremens.
Les hypoammoniémiants disponibles et ayant l’AMM en France sont les disaccharides non absorbables (lactulose, Duphalac ; lactitol, Importal). Le lactulose doit être prescrit en première intention dans le traitement de la crise (proposer 1 à 6 sachets par jour afin d’obtenir 2 à 3 selles par jour), en prophylaxie secondaire chez tous les patients et primaire chez ceux hospitalisés pour une hémorragie digestive haute.3
Mais, hormis la diarrhée, il provoque des flatulences. S’assurer de l’observance est important : son défaut participe pour beaucoup à l’échec de la prise en charge.
La rifaximine, antibiotique à large spectre à prescription hospitalière, qui réduit la production d’ammoniaque, a l’AMM en prévention secondaire après échec du lactulose en monothérapie et permet de diminuer le risque de récidive de l’EH de moitié. Elle ne doit être utilisée qu’en association avec ce dernier ou seule s’il est mal toléré.
Mesures associées : alimentation à teneur protéique normale et exercice physique régulier pour lutter contre la sarcopénie, qui participe au défaut d’épuration de l’ammoniaque.
Sont précipitants : hémorragie digestive, infection, déshydratation/dysnatrémie/ insuffisance rénale, constipation et médicaments sédatifs ou non. Ils peuvent précéder l’EH ou être contemporains. Leur traitement l’améliore dans 90 % des cas. De plus, leur éviction peut être préventive.
Étant donné l’association entre IPP et EH, leur prescription doit être limitée aux strictes indications. Tous les sédatifs (benzodiazépines) sont contre- indiqués au cours de la cirrhose. Sauf si surviennent crise convulsive ou delirium tremens.
Les hypoammoniémiants disponibles et ayant l’AMM en France sont les disaccharides non absorbables (lactulose, Duphalac ; lactitol, Importal). Le lactulose doit être prescrit en première intention dans le traitement de la crise (proposer 1 à 6 sachets par jour afin d’obtenir 2 à 3 selles par jour), en prophylaxie secondaire chez tous les patients et primaire chez ceux hospitalisés pour une hémorragie digestive haute.3
Mais, hormis la diarrhée, il provoque des flatulences. S’assurer de l’observance est important : son défaut participe pour beaucoup à l’échec de la prise en charge.
La rifaximine, antibiotique à large spectre à prescription hospitalière, qui réduit la production d’ammoniaque, a l’AMM en prévention secondaire après échec du lactulose en monothérapie et permet de diminuer le risque de récidive de l’EH de moitié. Elle ne doit être utilisée qu’en association avec ce dernier ou seule s’il est mal toléré.
Mesures associées : alimentation à teneur protéique normale et exercice physique régulier pour lutter contre la sarcopénie, qui participe au défaut d’épuration de l’ammoniaque.
Perspectives
La rifaximine administrée 15 jours avant le TIPS, puis 6 mois après, a un intérêt en prévention chez des sujets bien sélectionnés. À l’avenir, elle pourrait être recommandée systématiquement.4
La surveillance à distance par télémédecine de patients cirrhotiques ayant un antécédent d’EH fait baisser le taux de réadmission à l’hôpital. D’autres travaux semblent nécessaires pour développer davantage cette modalité.
La surveillance à distance par télémédecine de patients cirrhotiques ayant un antécédent d’EH fait baisser le taux de réadmission à l’hôpital. D’autres travaux semblent nécessaires pour développer davantage cette modalité.
Encadre
Qui adresser à un hépatologue hospitalier ?
Tous les malades atteints de cirrhose ayant des troubles neurologiques, en raison du pronostic de l’EH, de la nécessité d’éliminer les diagnostics différentiels, et de discuter de greffe hépatique dans les cas les plus sévères, faisant intervenir une équipe multidisciplinaire. Dans cette logique, un groupe unique a été créé à La Pitié-Salpêtrière, le Brain Liver Pitié-Salpêtrière (B-LIPS) group.Il peut être sollicité pour des bilans neurologiques et neurocognitifs.
Références
1. AFEF. Recommandations formalisées d’experts. Diagnostic et prise en charge de l’encéphalopathie hépatique sur cirrhose. AFEF. Octobre 2019. https://bit.ly/39Vo80E
2. Vilstrup H, Amodio P, Bajaj J, et al. Hepatic encephalopathy in chronic liver disease: 2014 Practice Guideline by the American Association for the Study of Liver Diseases and the European Association for the Study of the Liver. Hepatology 2014;60:715-35.
3. Gluud LL, Vilstrup H, Morgan MY. Nonabsorbable disaccharides for hepatic encephalopathy: A systematic review and meta-analysis. Hepatology 2016;64:908-22.
4. Bureau C, Jézéquel C, Thabut D, et al. Rifaximin reduces hepatic encephalopathy risk after TIPS. Hepatology 2019;70(S1):10A.
5. Rudler M, Bouzbib C, Weiss N, Thabut D. Diagnosis and management of hepatic encephalopathy. Clinics in Liver Disease 2021(sous presse).
2. Vilstrup H, Amodio P, Bajaj J, et al. Hepatic encephalopathy in chronic liver disease: 2014 Practice Guideline by the American Association for the Study of Liver Diseases and the European Association for the Study of the Liver. Hepatology 2014;60:715-35.
3. Gluud LL, Vilstrup H, Morgan MY. Nonabsorbable disaccharides for hepatic encephalopathy: A systematic review and meta-analysis. Hepatology 2016;64:908-22.
4. Bureau C, Jézéquel C, Thabut D, et al. Rifaximin reduces hepatic encephalopathy risk after TIPS. Hepatology 2019;70(S1):10A.
5. Rudler M, Bouzbib C, Weiss N, Thabut D. Diagnosis and management of hepatic encephalopathy. Clinics in Liver Disease 2021(sous presse).

 Encadrés
Encadrés