Le psoriasis est une dermatose inflammatoire chronique très fréquente dont la prévalence augmente d’autant qu’on s’éloigne de l’Équateur, allant de 0,91 % aux États-Unis à 8,5 % en Norvège.1 En France, la prévalence du psoriasis a été estimée à 3,6 % de la population.2
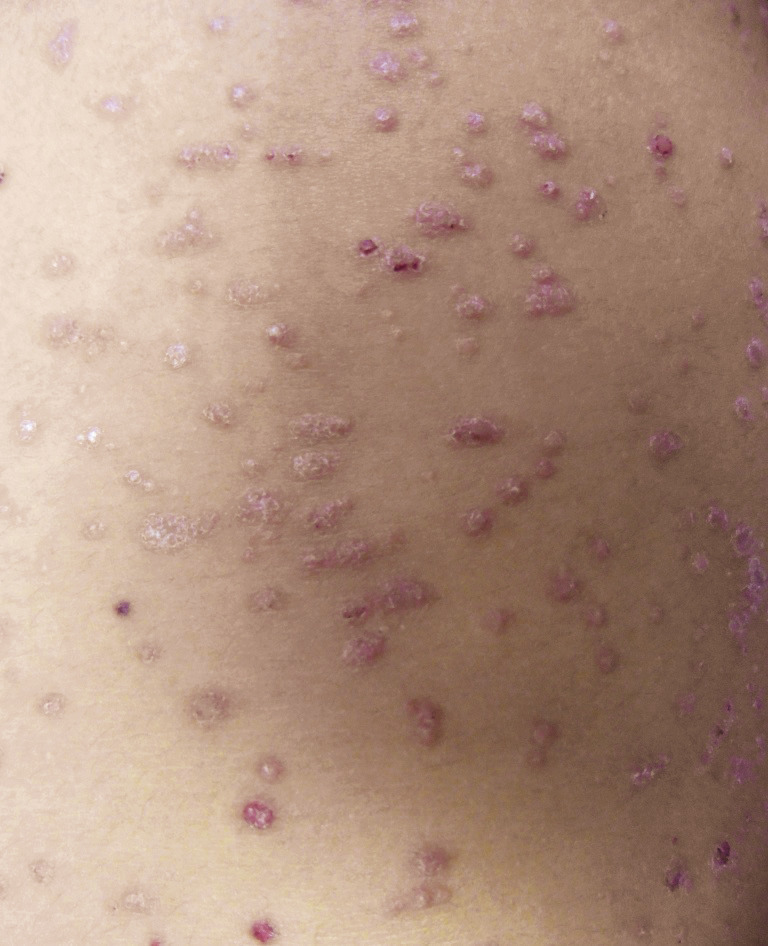
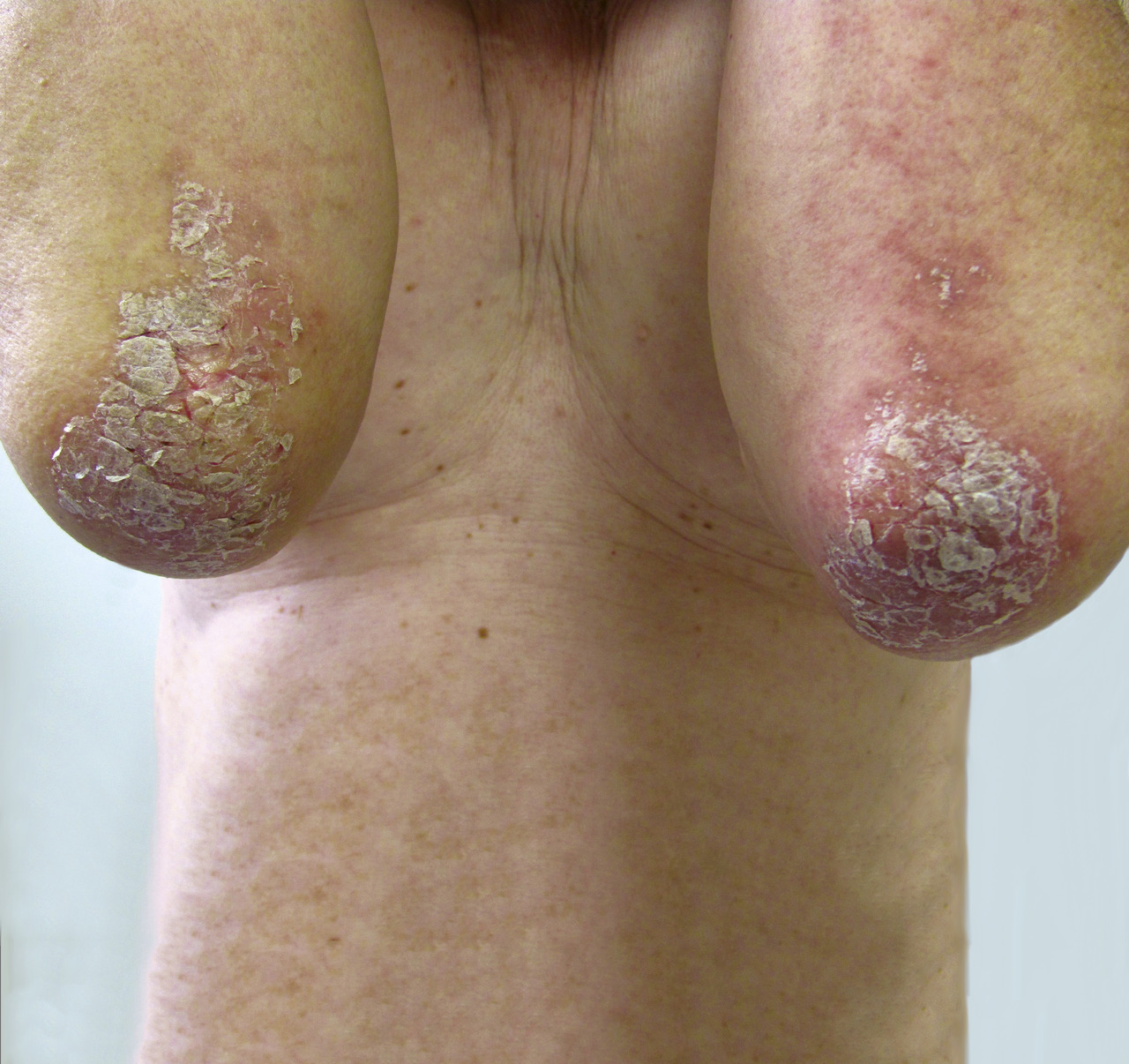
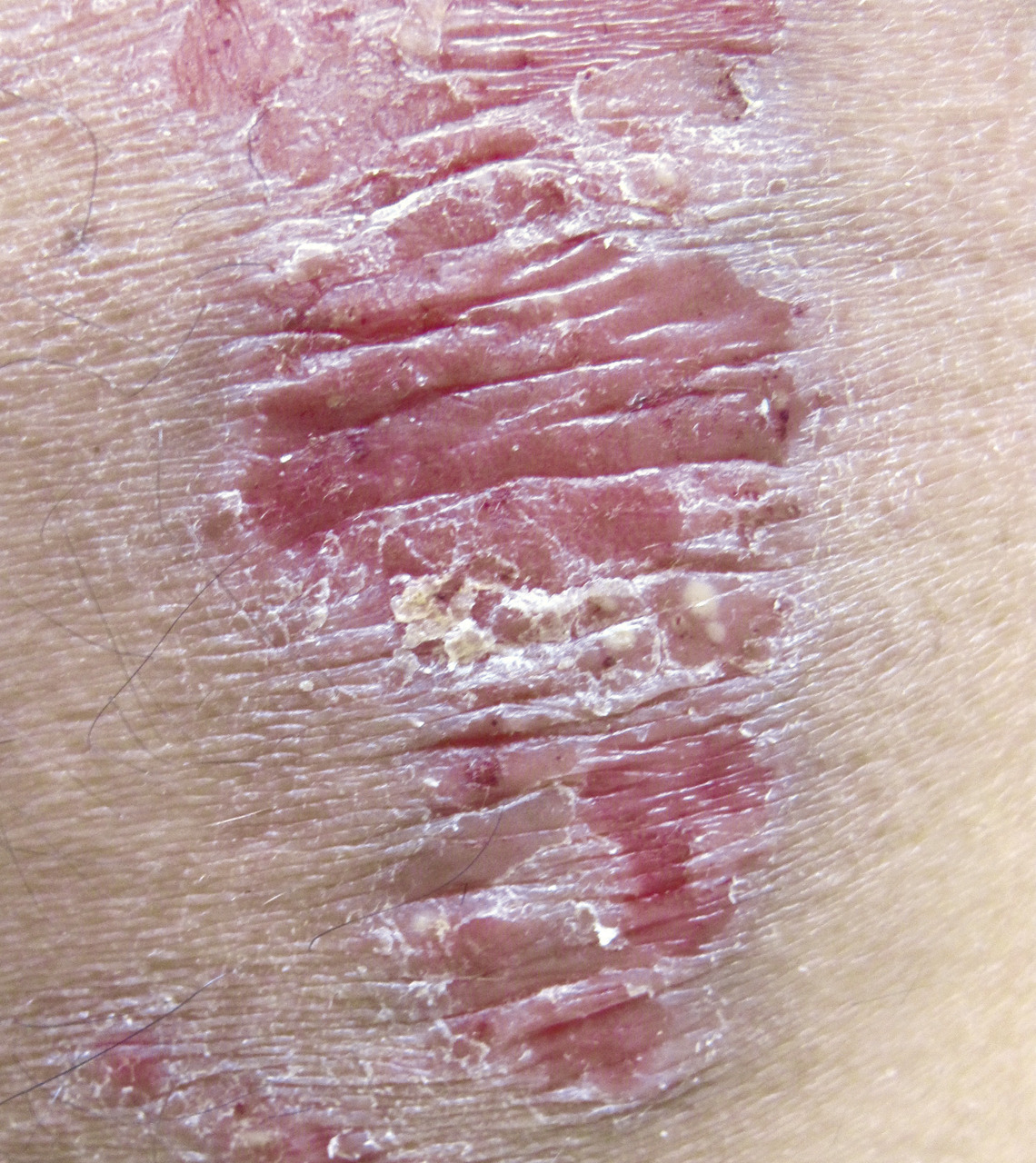
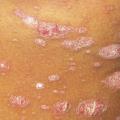
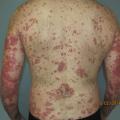
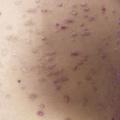
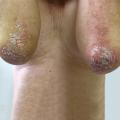
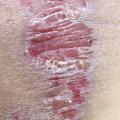
Le psoriasis ne pose en général pas de problème diagnostique, les plaques étant le plus souvent typiques, érythémato-squameuses, bien limitées, siégeant préférentiellement sur les zones « bastion » que sont les coudes et les genoux, le cuir chevelu, l’ombilic et les ongles.
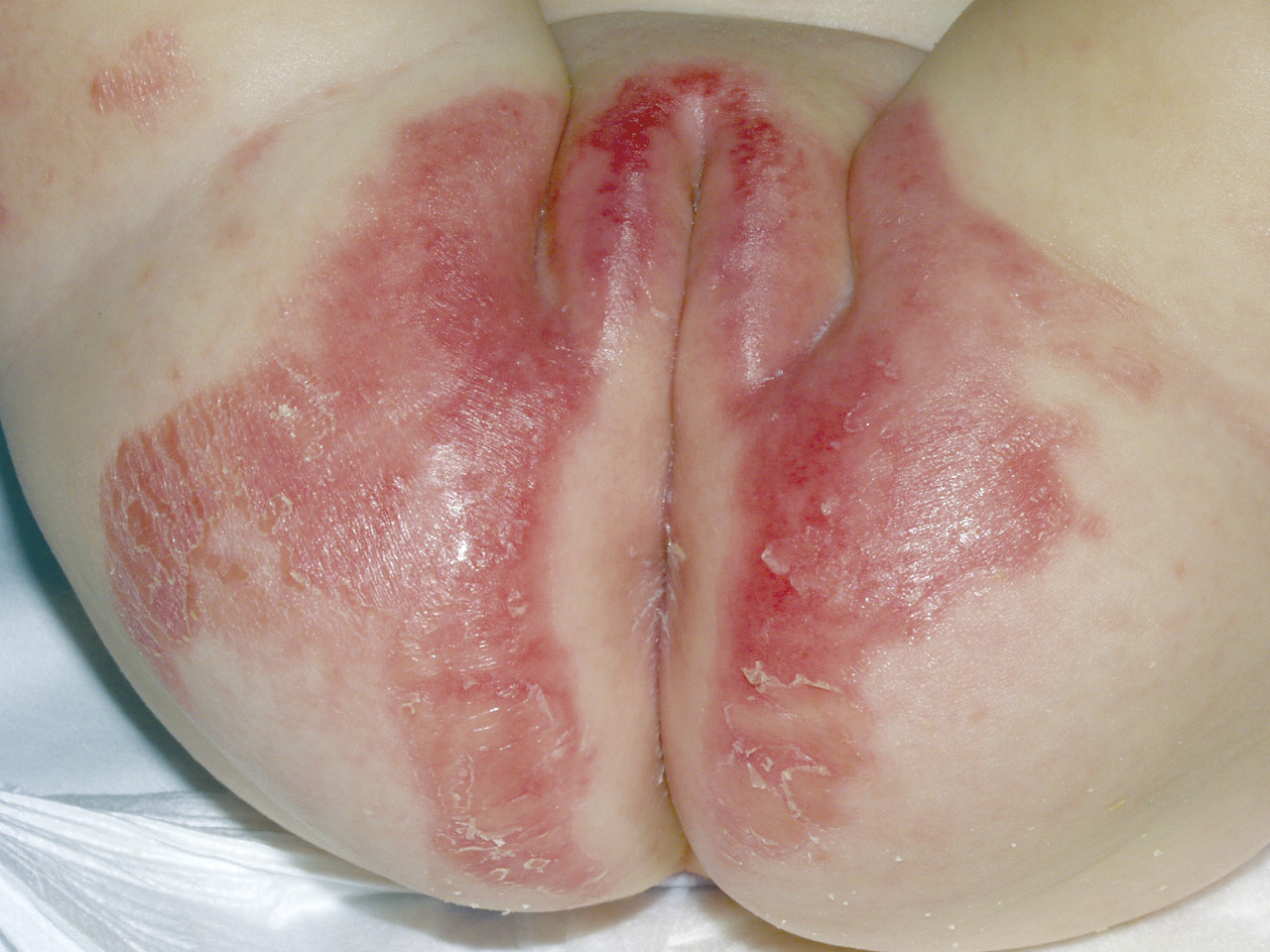
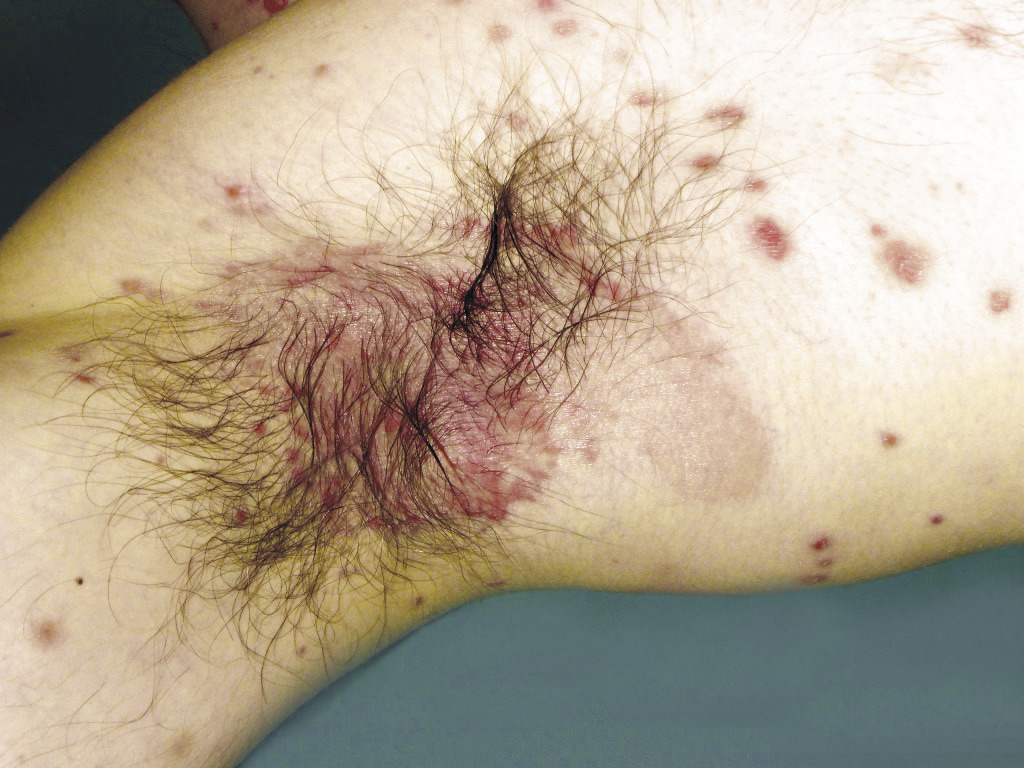
Le psoriasis en goutte ou le psoriasis inversé des plis sont d’autres formes de psoriasis assez fréquentes.
Évaluer pour mieux traiter
Bien que le pronostic vital ne soit jamais engagé, la gravité de la maladie doit être soigneusement appréciée afin de définir au mieux avec le patient les objectifs thérapeutiques. En effet, la présence ou non d’un rhumatisme psoriasique et/ou de comorbidités telles qu’un syndrome métabolique va influencer la décision thérapeutique.
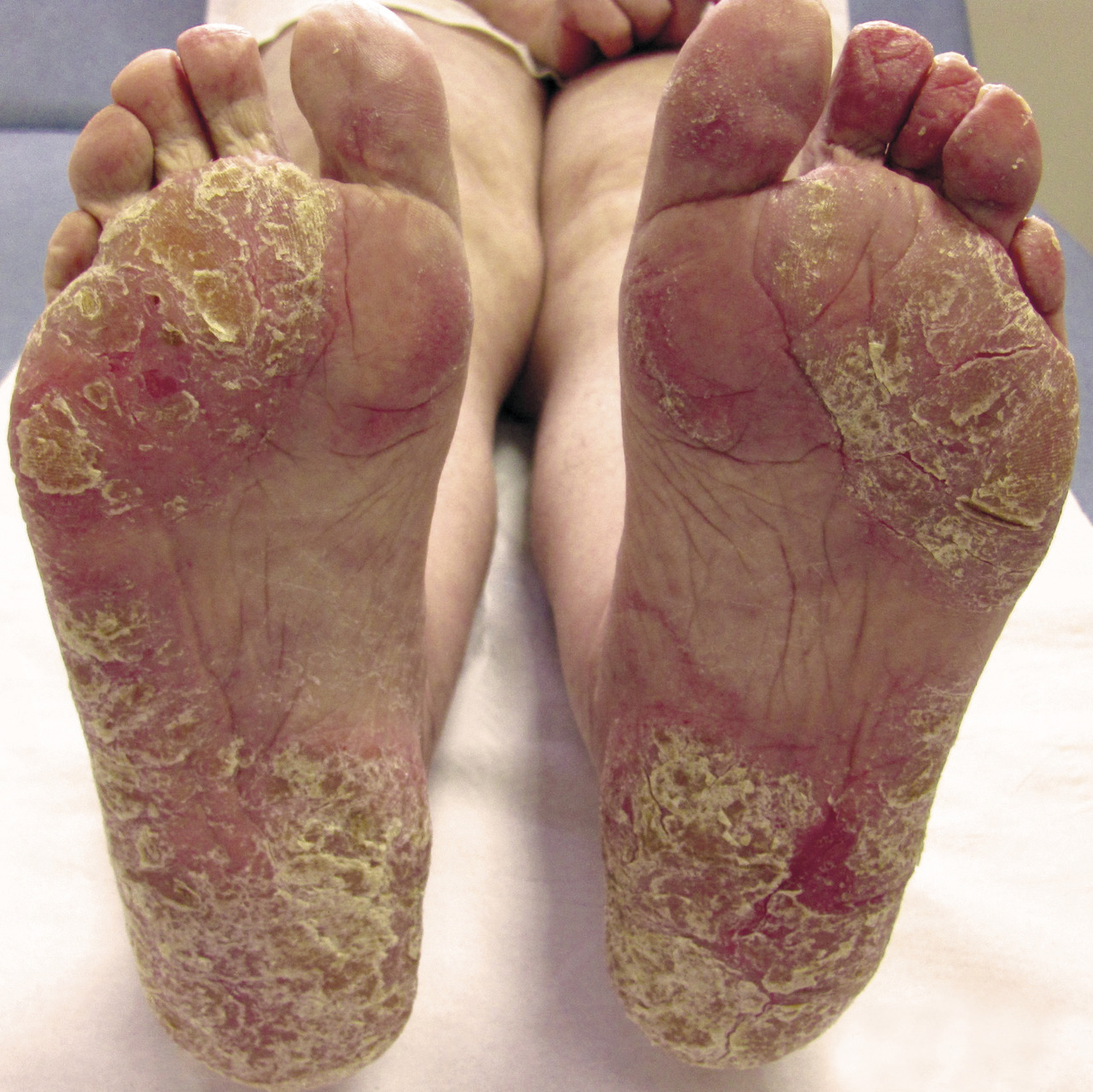
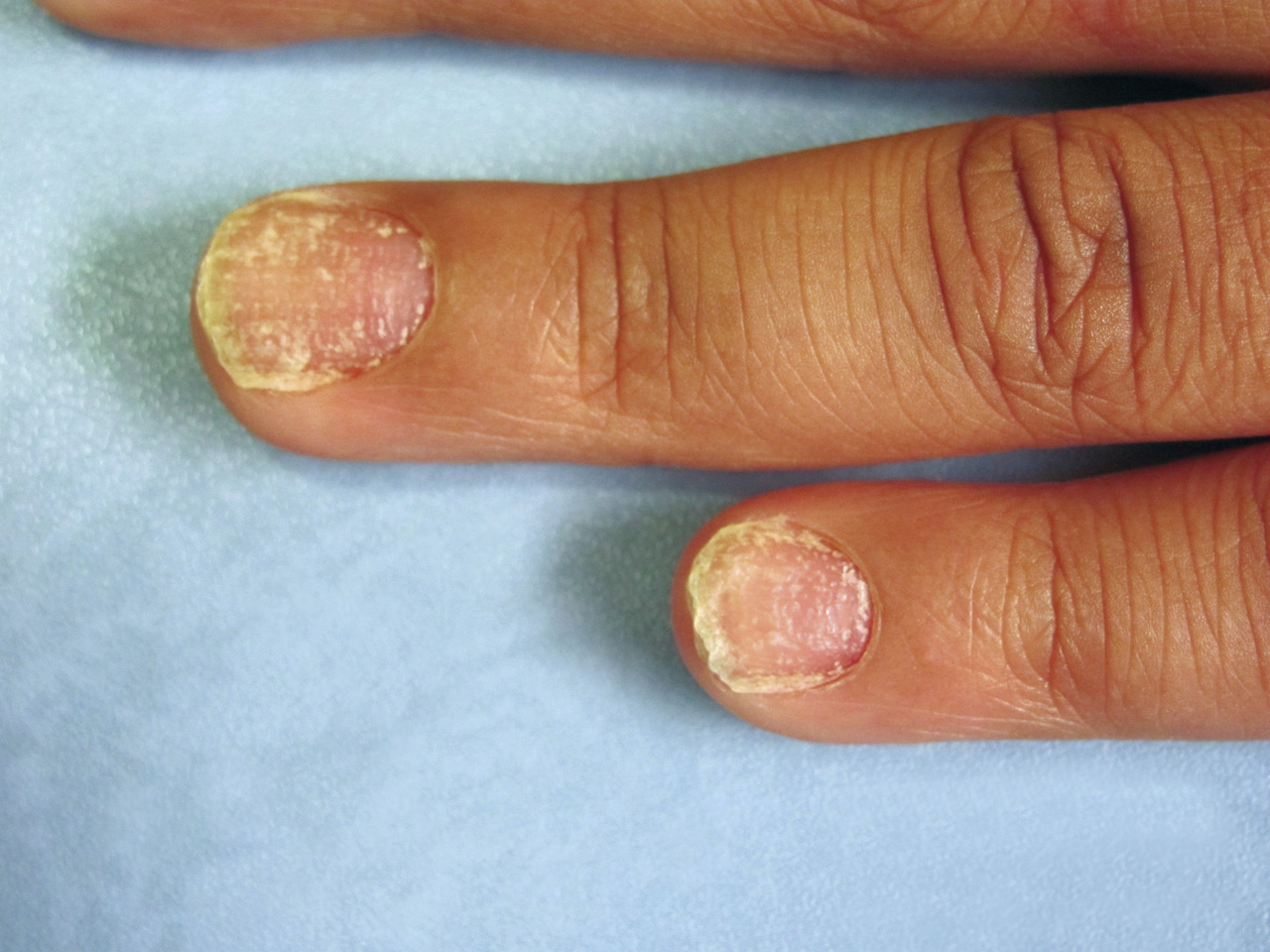
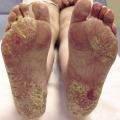
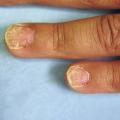
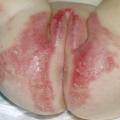
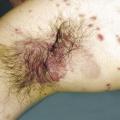
L’évaluation clinique d’un patient atteint est complexe car, comme pour toute dermatose affichante, ce n’est pas tant la quantité de surface corporelle atteinte que la « qualité » des zones atteintes qui importe pour le patient. Un psoriasis étendu mais camouflable sous les vêtements a moins de retentissement sur le quotidien du sujet qu’un psoriasis atteignant les zones visibles (dos des mains, ongles, visage, desquamation du cuir chevelu) ou les zones entraînant une gêne fonctionnelle (plantes des pieds ou paumes des mains avec crevasses, pulpite des doigts, onychodystrophie, organes génitaux). La présence ou non d’un prurit est également un élément à prendre en compte.
Qu’il y ait ou non une atteinte génitale, on ne doit pas négliger de s’intéresser au retentissement de la maladie sur la vie intime du patient, sujet difficilement abordé par le ou la patiente, et souvent évité par le médecin. De plus en plus de données épidémiologiques confirment le lien entre cette maladie inflammatoire et un certain nombre de comorbidités métaboliques et cardiovasculaires qu’il faut rechercher et/ou prévenir, pour une prise en charge globale optimale du patient.
La définition d’un psoriasis modéré à sévère, nécessitant un traitement systémique, tient compte à la fois d’une évaluation objective par le médecin (surface corporelle atteinte [SCA] ; évaluation globale par le médecin ou physician’s global assessment [PGA] ; indice de sévérité du psoriasis rapporté aux surfaces atteintes ou psoriasis area and severity index [PASI]) et d’une mesure de l’impact sur la qualité de vie (dermatology life quality index [DLQI]) dont le questionnaire est rempli par le patient.
La reproductibilité intra- et inter-examinateur de ces scores a été évaluée et elle semble supérieure pour le PASI. C’est ce dernier qui est validé et le plus souvent retenu dans les études cliniques, mais sa réalisation est plus longue que celle des autres scores.3, 4
Les différents scores
Il a été reconnu qu’une surface corporelle atteinte supérieure à 10 % ou un indice PASI supérieur à 10 et un résultat au questionnaire DLQI supérieur à 10 permettaient de définir un psoriasis modéré à sévère, nécessitant un traitement systémique. Mais certaines atteintes limitées mais très handicapantes comme celles des ongles ou des régions palmo-plantaires grèvent la qualité de vie des patients de façon majeure alors que les scores objectifs restent bas. Par conséquent, un résultat élevé même isolé au DLQI doit inciter à opter pour des thérapeutiques efficaces.5
Les différents tableaux détaillent le fonctionnement des scores disponibles les plus utilisés ainsi que leurs avantages et leurs inconvénients.
Surface corporelle atteinte (score SCA)
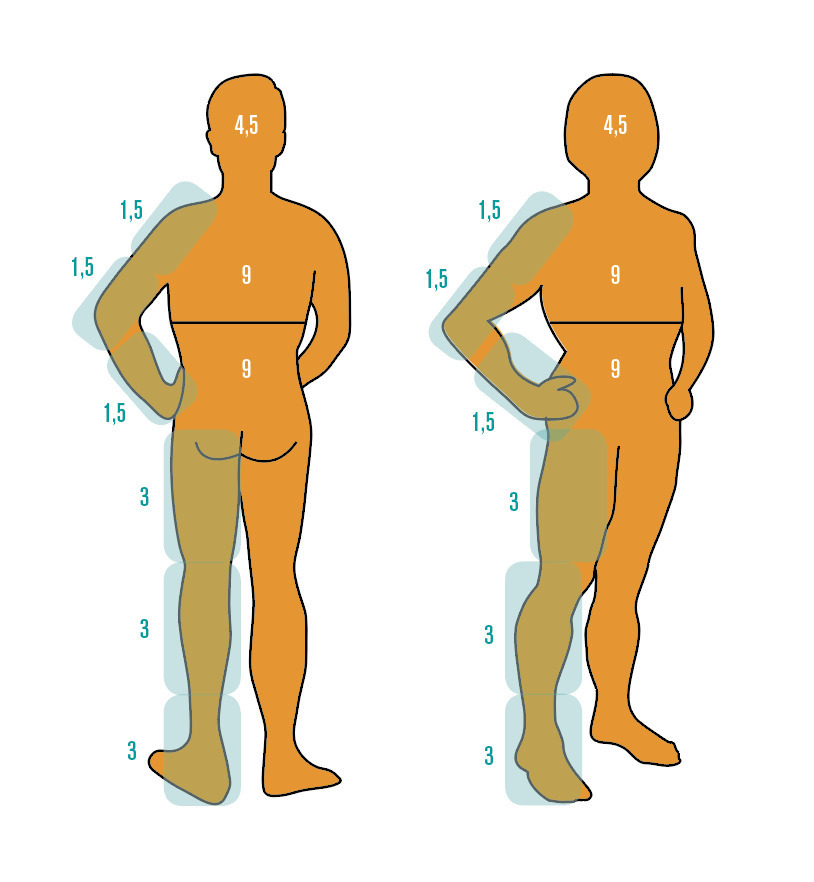
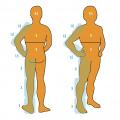
Sans préjuger de l’intensité ni de l’épaisseur des plaques, ce score permet de mesurer le psoriasis comme d’autres dermatoses, en fonction de la surface cutanée atteinte (v. figure) selon la règle habituelle des 9.
Évaluation globale par le médecin (score PGA)
Le score PGA (tableau 1) mesure de 0 à 5 l’intensité d’une plaque typique à un instant donné. Intuitif et rapide à réaliser, il ne tient toutefois pas compte de la surface cutanée atteinte.
Indice de sévérité du psoriasis rapporté aux surfaces atteintes (score PASI)
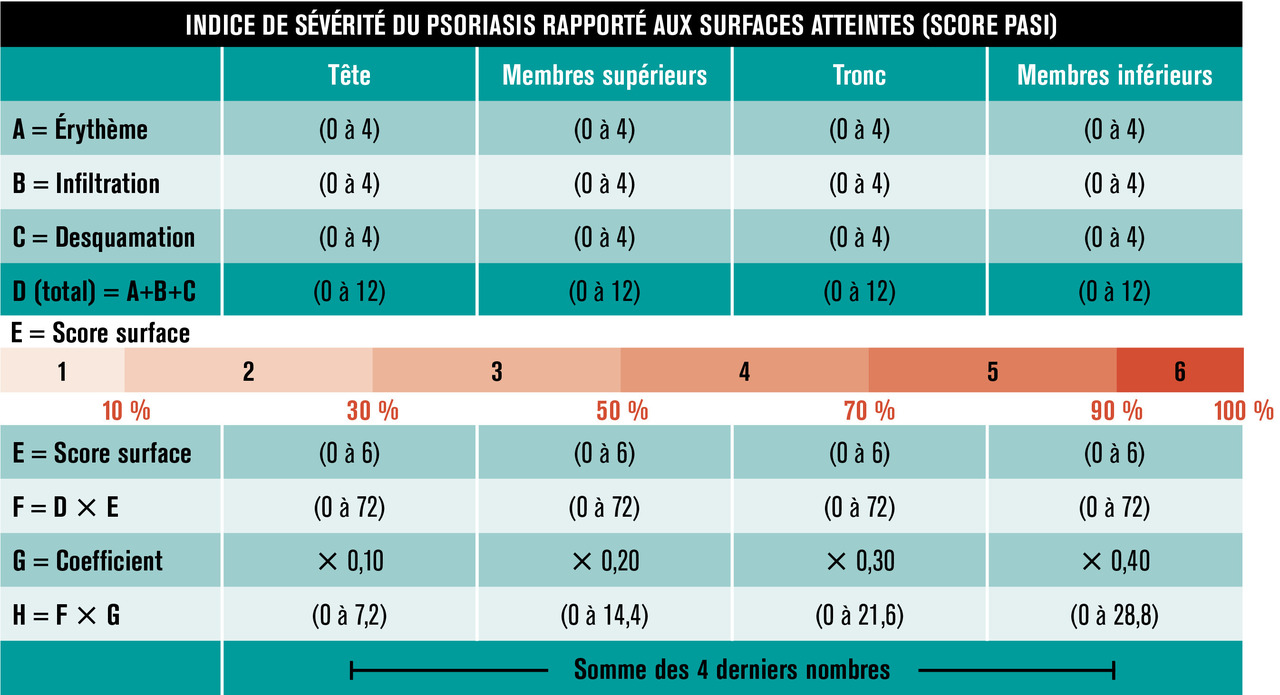
Ce score composite mesure successivement sur quatre zones du corps (tête, membres supérieurs, tronc et membres inférieurs) les trois caractéristiques des lésions : l’érythème, l’épaisseur de la plaque (infiltration) et la desquamation (tableau 2).
La somme des trois notes est ensuite multipliée par un chiffre allant de 0 à 6 correspondant au pourcentage de surface atteinte sur chaque segment du corps (par exemple, si 30 à 50 % du tronc est atteint on multiplie par 3 la somme des mesures cliniques obtenues sur le tronc, si 70 à 90 % de la surface sont atteints on multiplie par 5).
Ensuite, chaque segment du corps est pondéré en fonction de sa surface relative, la tête comptant pour 0,1, les membres supérieurs pour 0,2, le tronc pour 0,3 et les membres inférieurs pour 0,4 (total = 1). Le score PASI est obtenu par la somme des chiffres obtenus en bas de chacune des quatre colonnes.
Ainsi, si l’érythème était intense, quasi violine, l’infiltration majeure, supérieure à 2 mm et la squame blanche compacte et épaisse, sur toute la surface corporelle, le PASI s’élèverait à 72, mais ce chiffre n’est jamais atteint. On note aussi que l’atteinte des membres inférieurs avec sa pondération à 0,4 fait rapidement monter les scores, alors qu’une atteinte de tout le cuir chevelu, même épaisse, représentera moins de 70 % de la surface de la tête et n’est pondérée qu’à 0,1. Elle pèse donc peu sur le score PASI malgré une gêne souvent plus importante pour le patient qu’une atteinte des jambes ou des cuisses.
Un PASI supérieur à 10 représente un psoriasis modéré et justifie un traitement systémique.
Dans les essais thérapeutiques, l’objectif principal est l’atteinte du score PASI 75 ou 90. Cela se traduit par le pourcentage de patients dont le score PASI s’améliore de 75 % (ou de 90 %) sous traitement.
Ce type de score composite a été décliné pour les ongles (nail psoriasis severity index [NAPSI]).
Score de qualité de vie dermatologique
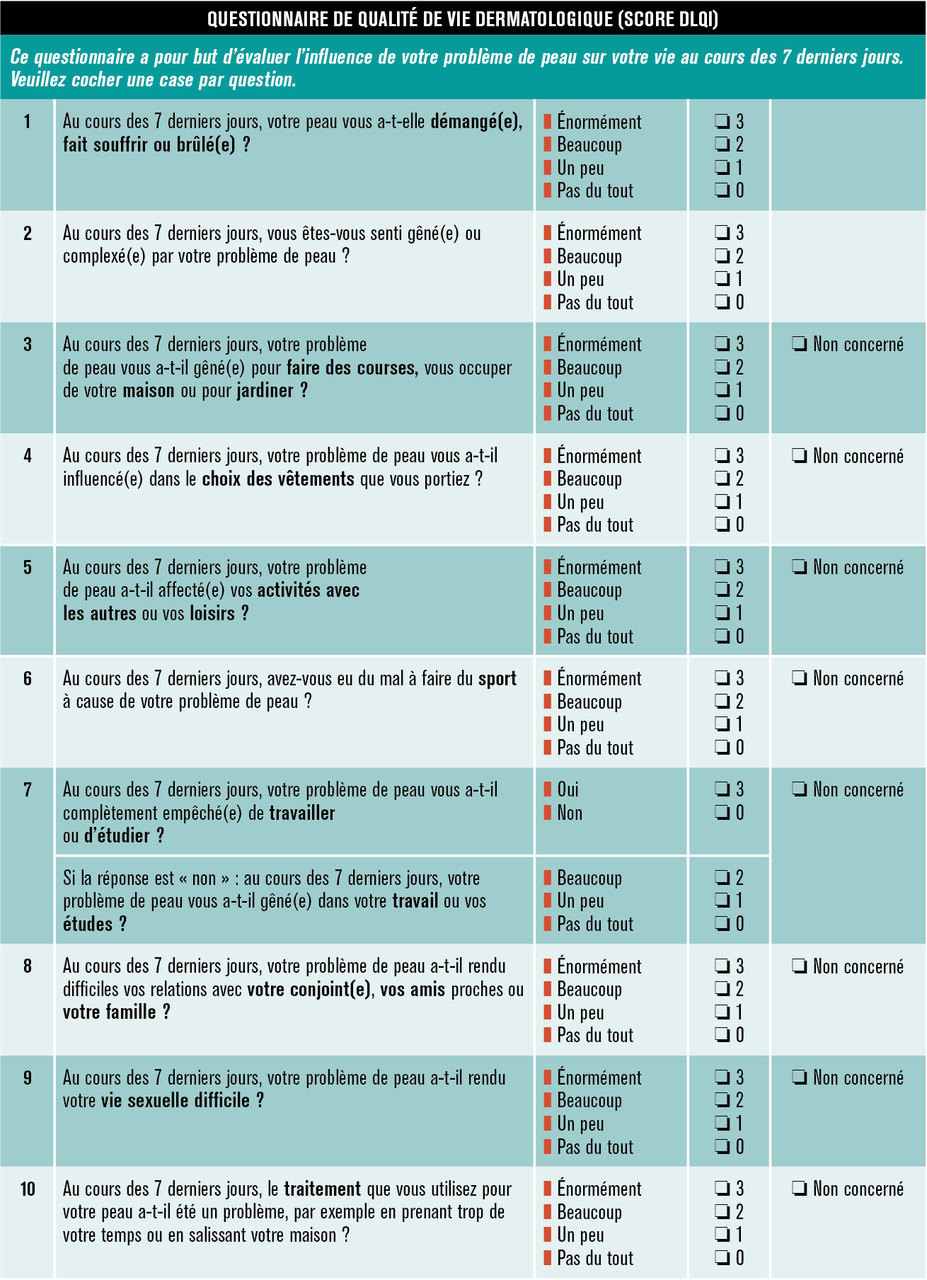
Le DLQI est un autoquestionnaire de qualité de vie standardisé et validé, rempli par le patient, idéalement sans influence du médecin, avant la consultation et mesurant l’impact de la dermatose lors des 7 jours précédents (tableau 3).
Il intègre plusieurs dimensions de mesure :
– une dimension physique, autonomie, capacité physique, capacité à réaliser les tâches quotidiennes ;
– une dimension psychologique, émotivité, anxiété, dépression et bien-être ;
– une dimension sociale, rapport à l’environnement familial, amical, professionnel, aux activités sociales et aux loisirs ;
– une dimension somatique, symptômes liés à la maladie et au traitement ;
– et d’autres dimensions telles que des douleurs, des troubles du sommeil, de l’alimentation, de la sexualité.
Chaque réponse est cotée de 0 (pas du tout ou non concerné) à 3 (énormément). La qualité de vie est considérée peu ou pas altérée si le score DLQI est inférieur ou égal à 5, altérée s’il est entre 5 et 10 et très altérée s’il est supérieur à 10.6 Le total maximal s'élève à 30.
Recherche des comorbidités associées
L’évaluation clinique d’un patient ayant un psoriasis ne se limite pas à la mesure de l’atteinte de la peau ou de la qualité de vie. Il faut rechercher de façon répétée la présence de signes débutants de rhumatisme inflammatoire, qui peuvent s’associer à un psoriasis cutané dans 7 à 26 % des cas.7 La survenue du rhumatisme est plus souvent secondaire au début de la maladie cutanée, même si celle-ci n’est pas très étendue. Les localisations au cuir chevelu, aux plis inguinaux ou interfessiers et aux ongles sont associées de façon significative à un rhumatisme psoriasique.8
Qu’il soit associé ou non à un rhumatisme, le psoriasis est une maladie inflammatoire chronique systémique s’associant de manière significative à un risque accru de comorbidités, dont le syndrome métabolique (v. encadré) est emblématique.
Il a été démontré un risque accru d’infarctus du myocarde, d’autant plus élevé que le psoriasis est sévère et que le patient est jeune (risque relatif : 3,10 ; intervalle de confiance à 95 % : 1,98-4,86).9
D’autres associations épidémiologiques commencent à être reconnues en dehors des maladies cardio-métaboliques : maladies gastro-intestinales, rénales, troubles de l’humeur… dont la pathogénie chez ces patients reste mal expliquée.10
UN FORT IMPACT SUR LA SANTÉ ET LE BIEN-ÊTRE
Le psoriasis est une maladie inflammatoire chronique ne se limitant pas à la peau, et ayant un fort impact sur la santé et le bien-être du patient. Le plus souvent, ce dernier ne formule pas le poids que représente sa maladie en consultation. Les échelles de mesure à notre disposition permettent d’évaluer la maladie de façon objective (surface atteinte, intensité des lésions) mais aussi de façon subjective (questionnaire de qualité de vie dermatologique). Il arrive fréquemment que les scores ne soient pas corrélés, et la décision thérapeutique doit tenir compte de tous ces aspects afin d’améliorer au mieux le quotidien des malades.
Tableau 2. Une note entre 0 et 4 est attribuée pour mesurer l’érythème, l’infiltration et la desquamation, sur chacune des quatre zones du corps.
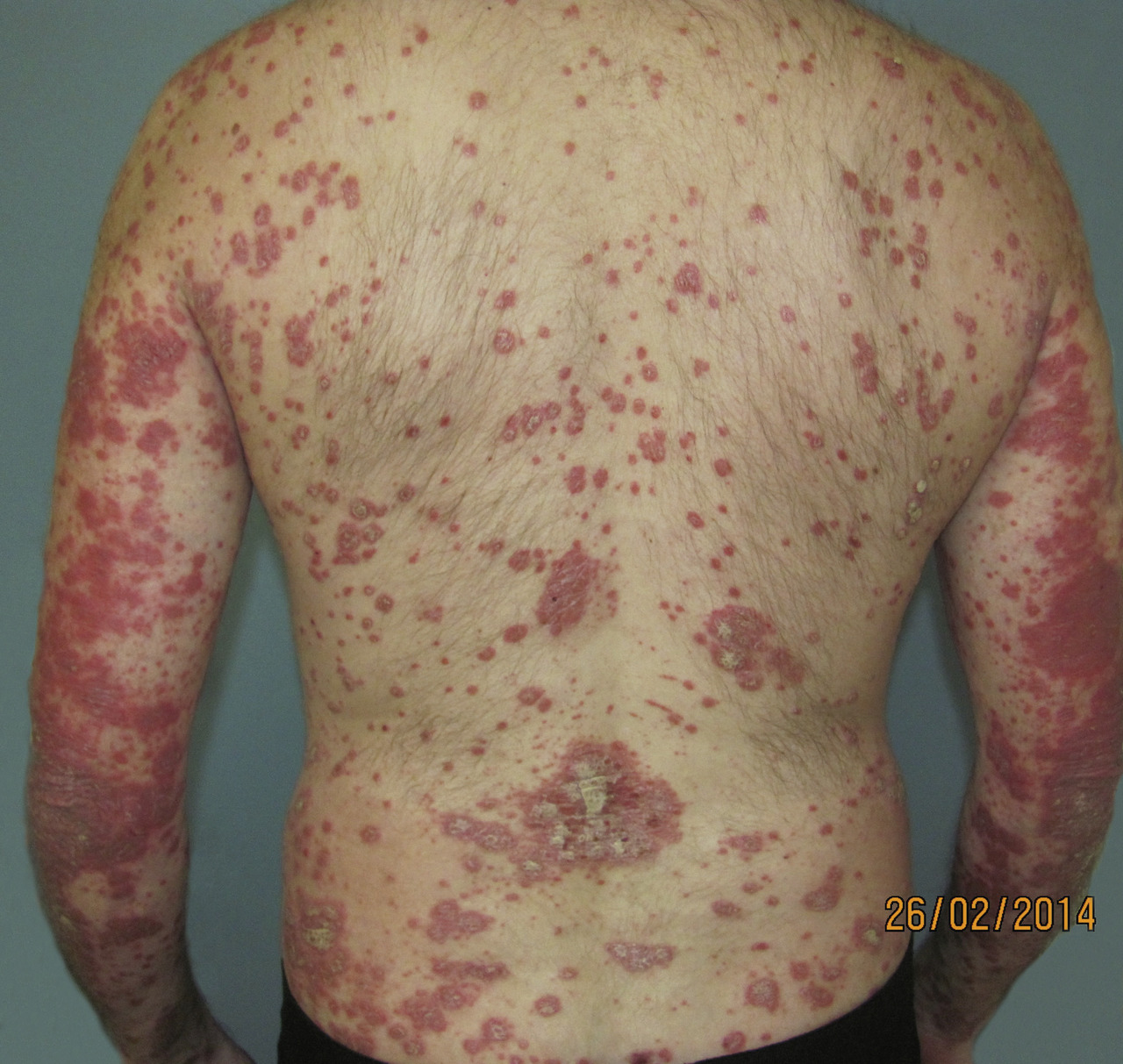
Remerciements au Dr Emmanuel Mahé pour son autorisation de publication des photographies ci-contre. (Tournier A, Mahé E. Psoriasis. Rev Prat 2018;68:e205-9)
Définition du syndrome métabolique
Tour de taille > 94 cm chez l’homme et 80 cm chez la femme
+ 2 critères parmi les suivants :
triglycérides > 1,50 g/L
cholestérol lié aux lipoprotéines de haute densité < 0,40 g/L chez l’homme et 0,50 g/L chez la femme
pression artérielle ≥ 130/85 mmHg
glycémie à jeûn > 1 g/L ou diabète
1. Parisi R, Symmons DP, Griffiths CE, Ashcroft DM; Identification and Management of Psoriasis and Associated ComorbidiTy (IMPACT). Global epidemiology of psoriasis: a systematic review of incidence and prevalence. J Invest Dermatol 2013;133:377-85.
2. Wolkenstein P, Grob JJ, Bastuji-Garin S, Ruszczynski S, Roujeau JC, Revuz J; Société française de dermatologie. French people and skin diseases: results of a survey using a representative sample. Arch Dermatol 2003;139:1614-9.
3. Berth-Jones J, Grotzinger K, Rainville C, et al. A study examining inter- and intrarater reliability of three scales for measuring severity of psoriasis: Psoriasis Area and Severity Index, Physician's Global Assessment and Lattice System Physician's Global Assessment. Br J Dermatol 2006;155:707-13.
4. Puzenat E, Bronsard V, Prey S, et al. What are the best outcome measures for assessing plaque psoriasis severity? A systematic review of the literature. J Eur Acad Dermatol Venereol 2010;24(Suppl 2):10-6.
5. Mrowietz U, Kragballe K, Reich K, et al. Definition of treatment goals for moderate to severe psoriasis: a European consensus. Arch Dermatol Res 2011;303:1-10.
6. Finlay AY, Khan GK. Dermatology Life Quality Index (DLQI)- a simple practical measure for routine clinical use. Clin Exp Dermatol 1994;19:210-6.
7. Prey S, Paul C, Bronsard V, et al. Assessment of risk of psoriatic arthritis in patients with plaque psoriasis: a systematic review of the literature. J Eur Acad Dermatol Venereol 2010;24(Suppl 2):31-5.
8. Wilson FC, Icen M, Crowson CS, McEvoy MT, Gabriel SE, Kremers HM. Incidence and clinical predictors of psoriatic arthritis in patients with psoriasis: a population-based study. Arthritis Rheum 2009;61:233-9.
9. Gelfand JM, Neimann AL, Shin DB, Wang X, Margolis DJ, Troxel AB. Risk of myocardial infarction in patients with psoriasis. JAMA 2006;296:1735-41.
10. Takeshita J, Grewal S, Langan SM, et al. Psoriasis and comorbid diseases: epidemiology. J Am Acad Dermatol 2017;76:377-90.

 Encadrés
Encadrés