La FMF est une pathologie auto-inflammatoire touchant les populations du pourtour méditerranéen. Le diagnostic n’est pas aisé. Le traitement est efficace, mais certaines précautions sont de mise. La HAS a mis en ligne des recos sur la conduite à tenir en pratique clinique courante devant des symptômes évocateurs, et lors des crises. Synthèse à destination des généralistes.
La fièvre méditerranéenne familiale est (FMF) une maladie génétique rare qui touche principalement les patients originaires du pourtour méditerranéen, en particulier les Turcs, Arméniens, Juifs sépharades et Maghrébins, Libanais, Kurdes, Italiens et Grecs. Il s’agit d’une maladie autosomique récessive (anciennement appelée maladie périodique), liée à des mutations du gène MEFV, qui code la protéine pyrine/marénostrine, impliquée dans la régulation de la sécrétion de l’interleukine 1β (IL1β). Les cytokines pro-inflammatoires sécrétées induisent la synthèse de protéines de l’inflammation (CRP notamment) par le foie. S’agissant d’une maladie autosomique récessive, pour être symptomatiques les patients doivent avoir deux variants pathogènes de MEFV.
Clinique : accès récidivants de fièvre + inflammation des séreuses
La FMF débute habituellement tôt dans la vie (90 % des cas avant l’âge de 20 ans), mais elle est souvent diagnostiquée à l’âge adulte, dans des contextes variés. Elle évolue par crises qui durent en moyenne de 24 à 72 heures, survenant à intervalles variables, de début et de fin brutaux, précédées dans 50 % des cas de prodromes. Le patient est asymptomatique entre les crises.
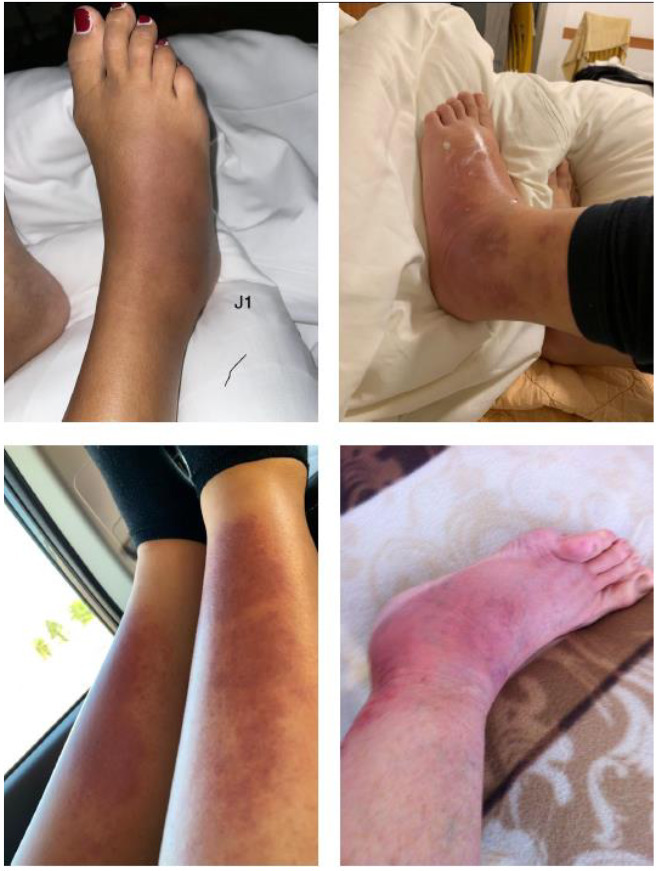
Il faut l’évoquer devant des accès récidivants defièvre entre 38,5 et 40 °C accompagnés d’une inflammation des séreuses à l’origine des symptômes : péritonite et douleurs abdominales parfois « pseudo-chirurgicales » pouvant s’associer à des vomissements et des troubles du transit (diarrhée ou constipation), pleurésie et douleurs thoraciques, synovite et arthralgies, voire arthrites des moyennes et grosses articulations (surtout genoux et chevilles) et, plus rarement, atteinte de la vaginale testiculaire (orchite) et péricardite. Diverses lésions cutanées peuvent survenir, la plus fréquente étant l’érythème érysipéloïde ou « pseudo-érysipèle » (fig. 1), œdème inflammatoire de la cheville avec un aspect érythémateux et luisant de la peau en regard ;bien quepeu fréquent, il est quasi-pathognomonique de la FMF chez un enfant appartenant à une ethnie à risque et peut être confondu avec un érysipèle.
Chez le petit enfant, le diagnostic est difficile car la fièvre peut être rapportée à une cause infectieuse : c’est la répétition des accès fébriles stéréotypés non accompagnés de signe infectieux ORL ou digestifs qui doit alerter.
Les crises sont favorisées par le stress, la fatigue, les menstruations.
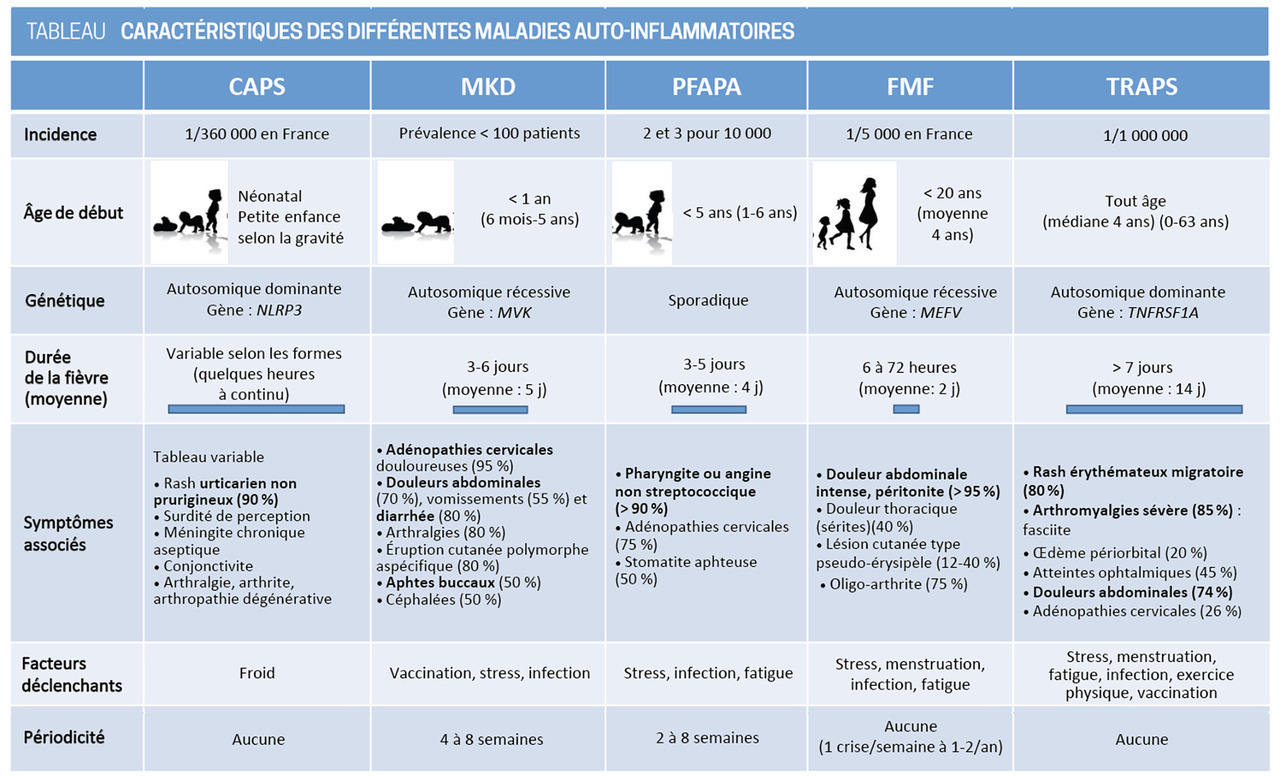
Les diagnostics différentiels sont nombreux (tableau 1 et fig. 2)
Quelles complications ?
En cas d’évolution de la FMF sans traitement durant plusieurs années, l’inflammation chronique non maîtrisée peut provoquer une amylose inflammatoire dont l’expression est surtout rénale (syndrome néphrotique pouvant conduire à une insuffisance rénale pouvant nécessiter une dialyse).
Chez les femmes enceintes, un accès aigu en début de grossesse peut déclencher une fausse couche.
Confirmer le diagnostic
Le diagnostic, évoqué devant une répétition de poussées inflammatoires et stéréotypées avec CRP élevée, est conforté par la recherche de mutations du gène MEFV. Cependant, leur absence alors que des signes cliniques et biologiques sont évocateurs ne permet pas d’éliminer le diagnostic. Un test à la colchicine (3 à 6 mois) peut alors être utile pour trancher.
Traitement de fond : colchicine à vie
Le traitement de fond repose sur la colchicine, à débuter à 1 mg/j (0,5 mg/j chez l’enfant de moins de 5 ans, les insuffisants rénaux ou hépatiques et les sujets très âgés). Il est adapté à la persistance ou non des crises et à la CRP intercritique qui doit être inférieure à la norme du laboratoire. La dose maximale quotidienne est de 2,5 mg/j chez l’adulte. Ce traitement à vie est efficace dans plus de 95 % des cas pour prévenir ou, à défaut, diminuer la fréquence et l’intensité des crises. Il s’agit du seul traitement qui a démontré une efficacité dans la prévention de l’amylose AA. Le respect strict de l’ordonnance est impératif et doit être expliqué au patient : l’effet préventif de la colchicine sur la survenue des crises ne sera observé que si le traitement est pris tous les jours, si possible à heures régulières et à une posologie suffisante fondée sur la réponse clinique et biologique.
Attention : le patient doit informer son médecin traitant de la prise de colchicine pour éviter les interactions médicamenteuses lors de prescriptions associées. En raison de leurs effets sur la P-glycoprotéine et le CYP3A4 – cytochromes métabolisant la colchicine –, de nombreuses molécules peuvent concourir à son accumulation intracellulaire et donc à ses effets secondaires : macrolides (clarithromycine, azithromycine), cyclosporine, kétoconazole, ritonavir, inhibiteurs des canaux calciques (vérapamil, diltiazem) [tableau 2].
La colchicine n’a pas d’impact négatif sur la croissance staturale chez l’enfant, la puberté, la fertilité. Contrairement à ce qui est écrit sur les boîtes de médicament, elle doit être continuée au cours de la grossesse et de l’allaitement (prendre le médicament au moment d’une tétée, le pic du passage de celui-ci dans le lait étant 2 heures après la prise par la mère). Une décision d’arrêt de la colchicine doit se prendre en concertation avec le médecin expert.
En cas de réponse insuffisante et/ou de toxicité ou d’intolérance à la colchicine, d’autres molécules telles que des biothérapies peuvent être proposées par des centres experts.
Traitement de la crise
En première intention, associer antalgiques-antipyrétiques (type paracétamol) avec des AINS :
- Enfant : paracétamol : 15 mg/kg (possibilité de dose de charge lors de la 1re prise = 30 mg/kg) toutes les 6 h sans dépasser les posologies maximales adultes, en association aux AINS, par exemple ibuprofène 8 mg/kg/6 h sans dépasser les doses maximales adultes.
- Adulte : paracétamol (1 g/6 h) en alternance avec un AINS type kétoprofène 100 mg, 1 cp x 2/j. En cas d’atteinte rénale, le recours aux AINS doit rester prudent.
Si la douleur n’est pas calmée, utiliser des antalgiques de palier 2 voire 3 :
- Enfant :
- Tramadol : 1 mg/kg x 4/j sans dépasser 400 mg/j.
- Morphine :
- voie IV : dose de charge, faire un bolus de 50 microgrammes/kg puis des bolus de 25 microgrammes/kg à administrer en fonction de la douleur au maximum 8 bolus toutes les 4 h ;
- voie intrarectale : 0,3 mg/kg toutes les 3 à 6 h.
- Adulte : tramadol ou association tramadol-paracétamol ou paracétamol-codéine, voire morphine en injections discontinues par voie IV ou SC en fonction de l’évolution de la douleur.
HAS. Fièvre méditerranéenne familiale (FMF). 12 décembre 2022.
Stankovic Stojanovic K. Fièvre méditerranéenne familiale. Rev Prat Med Gen 2014;28(930):768-9.
Dusser P, Koné-Paut I. Fièvres récurrentes chez l’enfant. Rev Prat Med Gen 2020;34(1046);616-8.
Richette P. Colchicine : attention aux surdosages. Rev Prat Med Gen 2020;34(1035);113.
Nobile C. Colchicine : attention aux surdosages (alerte ANSM). Rev Prat (en ligne) 1 juillet 2022.
Georgin-Lavialle S. 6 minutes de la filière : la fièvre méditerranéenne familiale. Fai2r 15 janvier 2021.