Argumenter l’attitude thérapeutique et planifier le suivi du patient.
Goitre
Définition
Les goitres peuvent être congénitaux ou acquis, diffus ou localisés, normo-, hypo- ou hyperfonctionnels, bénins ou malins.
On convient de parler de goitre :
cliniquement lorsqu’à la palpation la surface de chacun des lobes excède celle de la dernière phalange du pouce du sujet examiné ;
en échographie lorsque le volume thyroïdien (évalué par la somme du volume de chacun des lobes : hauteur × largeur × épaisseur x 0,52) excède 16 cm3 chez l’adolescent, 18 cm3 chez la femme adulte, 20 cm3 chez l’homme.
Évaluation
Clinique
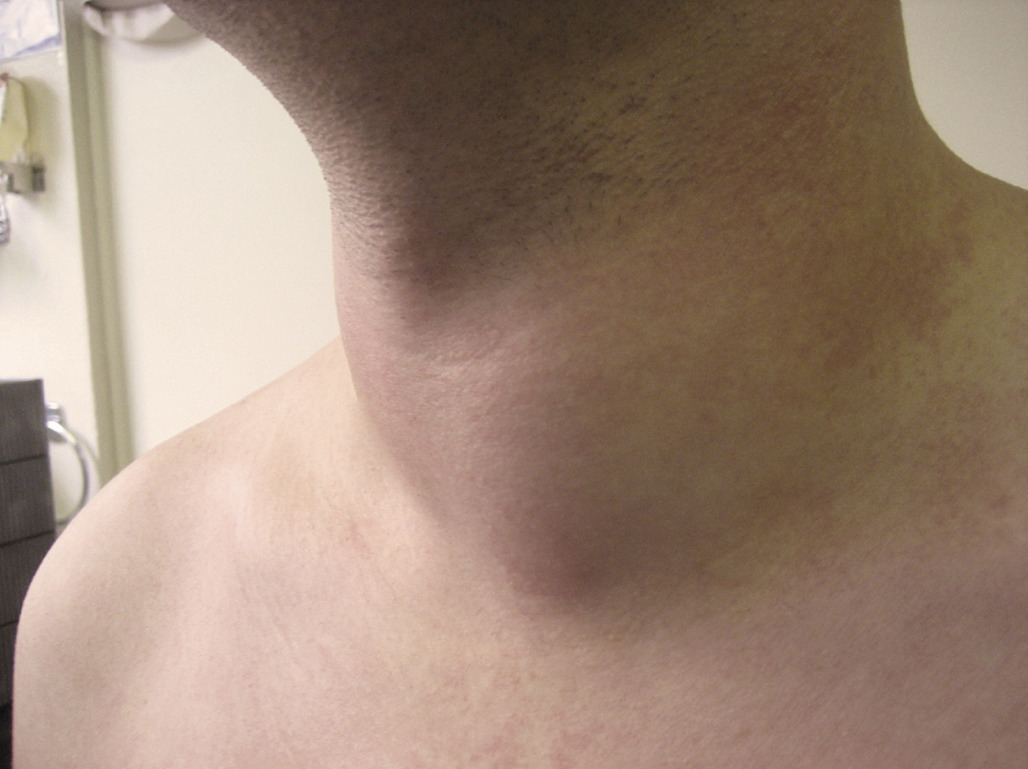
Cliniquement, les goitres sont remarqués par le patient ou l’entourage, ou découverts lors de la consultation. On précise l’ancienneté des signes, les antécédents familiaux de maladie thyroïdienne.L’hypertrophie est de degré variable :
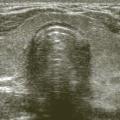
hypertrophie simplement palpable, mobile lors de mouvements de déglutition (fig. 1) ;
hypertrophie visible lorsque le cou est en extension ;
hypertrophie visible à distance.
On recherche :
une gêne fonctionnelle ;
des signes de compression : trachéale, récurrentielle, œsophagienne, veineuse (cf. infra) ;
des signes de dysfonction thyroïdienne ;
des adénopathies palpables.
Biologie
La mesure de la TSH est l’examen indispensable, à réaliser avant toute autre investigation :sa valeur normale conforte l’impression clinique d’euthyroïdie ;
une valeur accrue suggère un déficit de la production thyroïdienne ;
une valeur basse est en faveur d’une imprégnation excessive par les hormones thyroïdiennes.
Les autres explorations :
en cas d’anomalie de TSH, la mesure de T4 libre quantifie l’importance de la dysfonction hormonale ;
en cas d’accroissement de TSH se justifie la détection d’une auto-immunité antithyroïdienne par la mesure d’anticorps antithyropéroxydase (anti-TPO). La détermination du titre des anticorps antithyroglobuline (anti-Tg) est à réaliser en cas de négativité des anti-TPO ;
la mesure de la thyroglobuline est ici sans intérêt et ne doit pas être effectuée : sa valeur est accrue du seul fait de l’augmentation du volume thyroïdien et de l’éventuelle dysfonction, mais ne constitue nullement un argument en faveur du cancer.
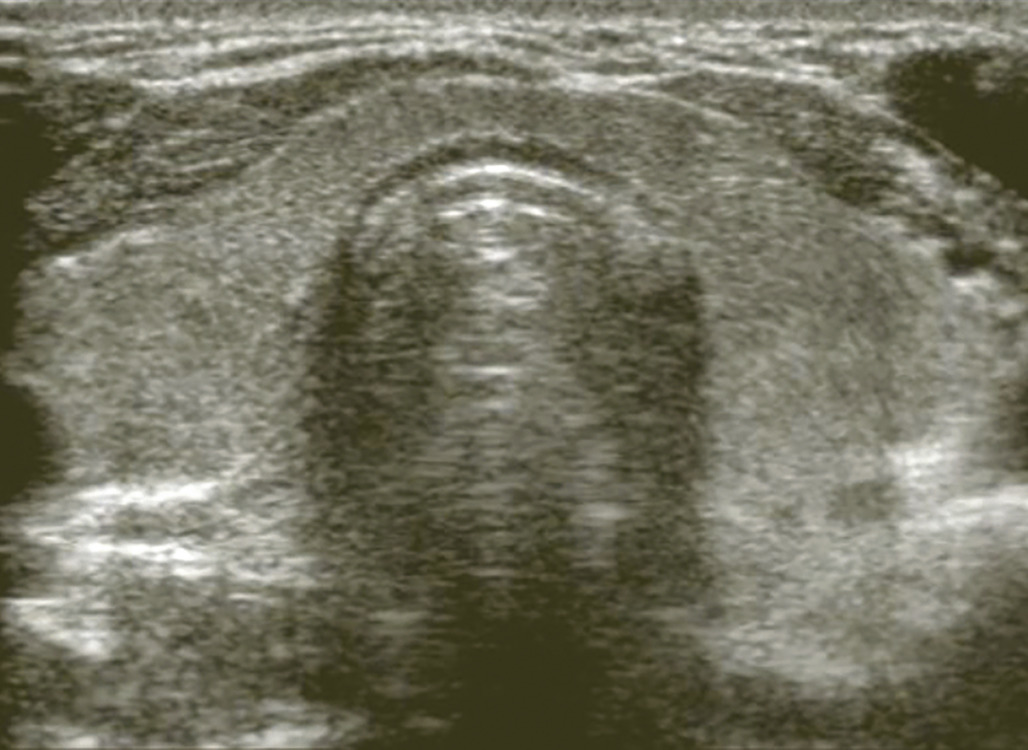
échographie de la thyroïde
Elle quantifie les dimensions de chacun des lobes et de l’isthme, ce qui permet le calcul du volume.Elle précise l’aspect ordinairement isoéchogène du parenchyme (
Elle autorise une description précise des éventuels nodules (
Elle contribue à la surveillance.
Goitre simple et goitre plurinodulaire
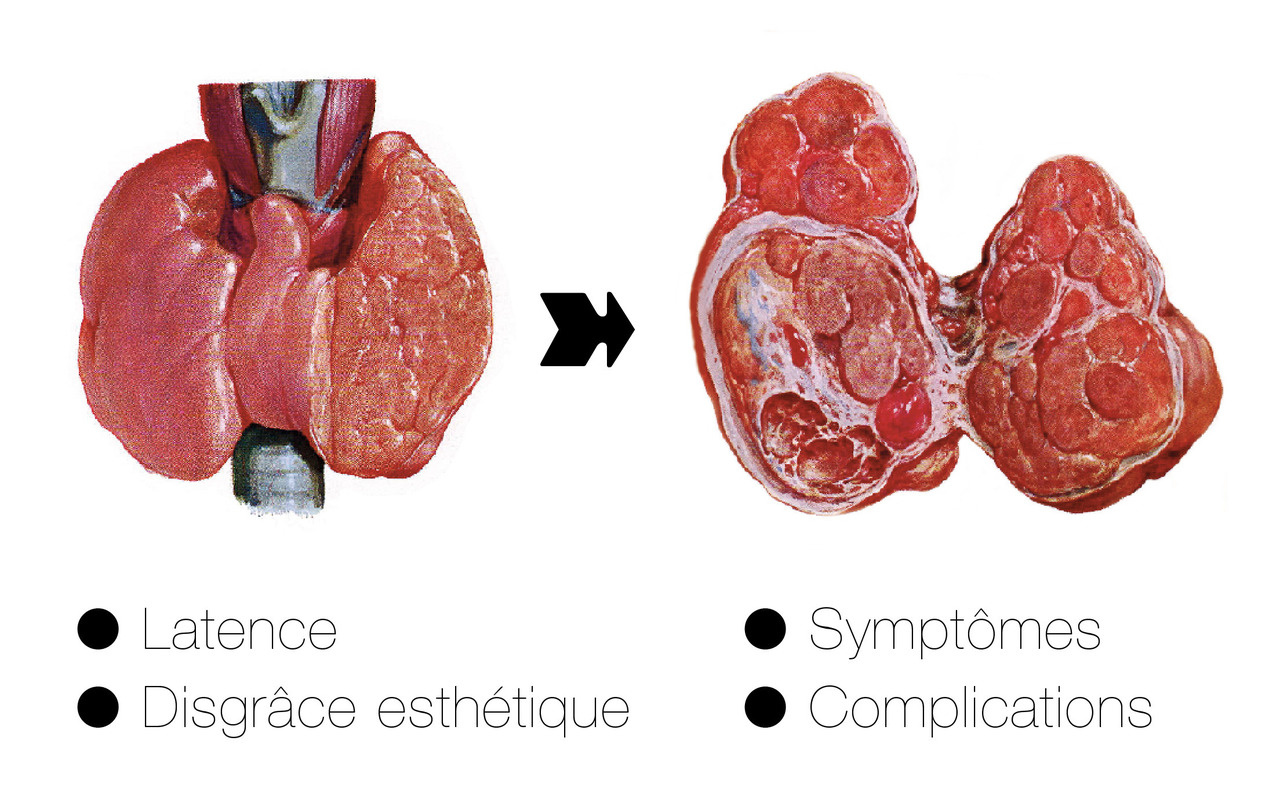
Initialement, l’hypertrophie est diffuse et homogène. Cependant, au fil des années et des décennies, le goitre se remanie par l’apparition de nodules ; certains (de l’ordre de 10 %) sont fonctionnels, captant les isotopes, et peuvent finir par devenir responsables d’hyperthyroïdie, notamment lorsque leur taille excède 2 cm ; d’autres (environ 4-5 %) correspondent à des cancers, souvent longtemps latents, malgré tout parfois rapidement évolutifs, notamment dans les formes peu différenciées des sujets âgés. C’est seulement au stade de goitre plurinodulaire qu’apparaît le risque de complications (
Les goitres sont d’une grande fréquence, affectant près de 10 % de la population adulte. Cependant, le goitre est plus rare chez l’enfant (moins de 5 %). C’est pourquoi l’Europe occidentale n’est pas considérée comme une zone de goitre endémique.
Physiopathologie
Facteurs constitutionnels : les goitres prédominent dans certaines familles, en liaison avec des mutations de différents gènes : Tg, TPO, MNG1… Comme il est habituel dans les maladies fréquentes et multifactorielles, leur détection n’a pas d’utilité pratique et n’a pas lieu d’être envisagée.La présence de récepteurs d’estrogènes sur les cellules vésiculaires explique la large prédominance féminine, la révélation fréquente en période pubertaire ou à l’occasion des grossesses. La parité contribue à la goitrogenèse et au remaniement nodulaire des goitres.
Facteurs environnementaux : la carence iodée a longtemps constitué le facteur principal, impliqué dans l’endémie goitreuse. Le déficit en iode augmente en effet la sensibilité du parenchyme thyroïdien à l’effet trophique de la TSH, ce que favorisent des modifications de facteurs intrathyroïdiens de la croissance épithéliale. De gros efforts ont été conduits partout dans le monde pour optimiser l’apport iodé des populations, surtout par l’iodation du sel alimentaire. La supplémentation iodée des femmes enceintes est cependant encore insuffisamment assurée. L’amélioration de l’apport iodé n’a pas fait disparaître les goitres, qui restent présents chez 10 % de la population adulte.
Le tabac, qui contient du thiocyanate, est goitrogène, comme certains aliments (chou, radis, manioc) et médicaments (lithium, certains tuberculostatiques, pommades à la résorcine…).
Histoire naturelle et évaluation
Les goitres simples se constituent fréquemment à l’adolescence, s’accentuent et s’organisent progressivement en nodules au fil des années et des décennies. Les grossesses, les stress de la vie courante contribuent à leur développement.Au stade initial, l’hypertrophie thyroïdienne est diffuse et homogène. Elle est cliniquement latente, parfois responsable d’une légère déformation cervicale. Le parenchyme est souple, régulier. On peut à ce stade vérifier la normalité du taux de la TSH (une valeur basse orienterait plutôt vers la maladie de Basedow, une valeur élevée vers la thyroïdite de Hashimoto). On peut aussi quantifier en échographie le volume thyroïdien, sans s’alarmer de l’éventuelle caractérisation fortuite d’un ou plusieurs nodules occultes de petites dimensions (< 1 cm de diamètre). La scintigraphie est à ce stade inutile.
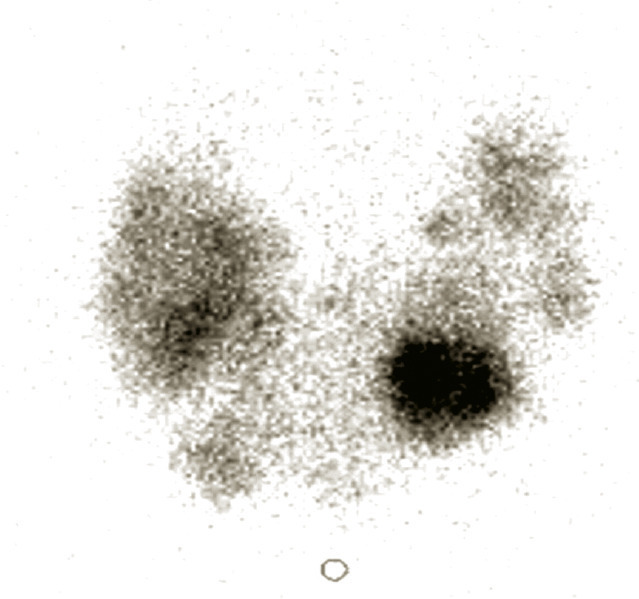
Progressivement, à l’âge adulte, l’hypertrophie thyroïdienne apparaît moins régulière, bosselée, déformée par des nodules dont on précisera les caractéristiques. À ce stade de goitre plurinodulaire de l’adulte, l’apparition d’une gêne cervicale, par exemple lors de la déglutition, est possible. On évalue le taux de la TSH, les données échographiques, sans négliger la ponction pour étude cytologique des nodules cliniquement ou échographiquement plus suspects (durs, rapidement évolutifs, EU-TIRADS 3 de plus de 2 cm, 4 ou 5). En scintigraphie au technétium ou à l’iode 123, la fixation apparaît à ce stade ordinairement hétérogène (
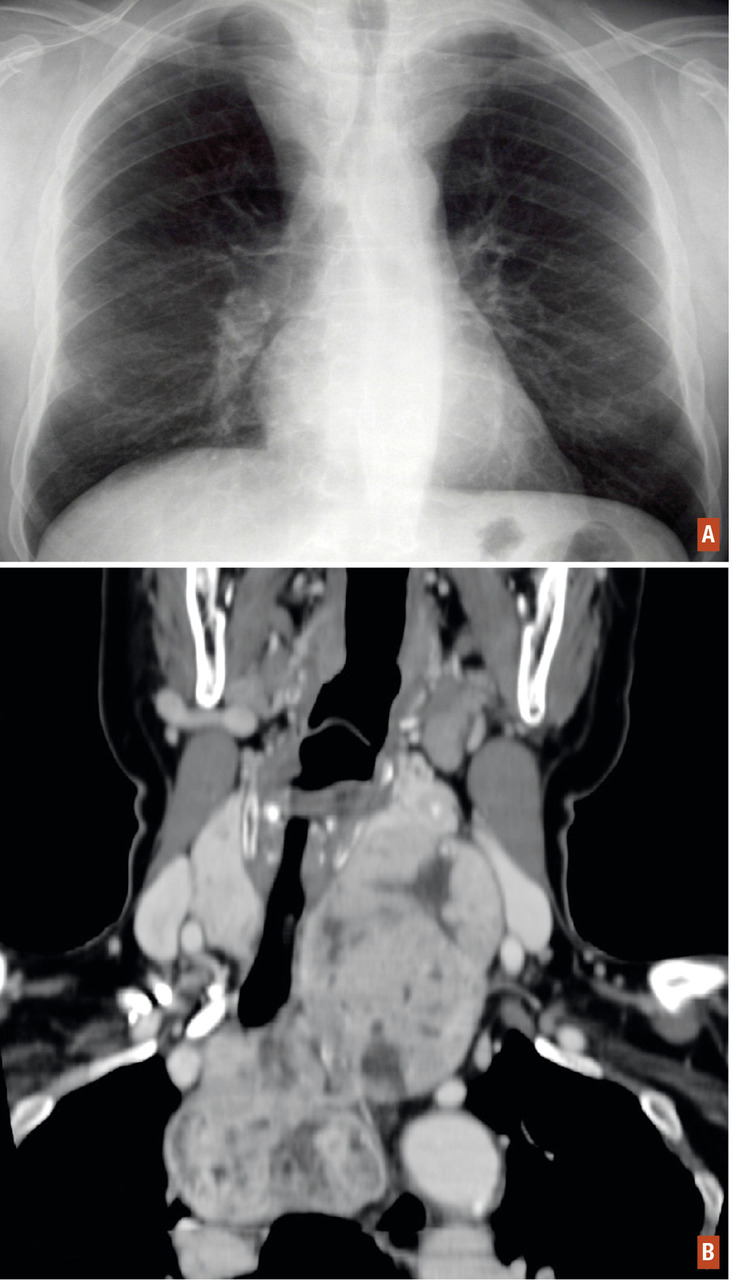
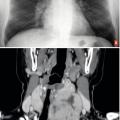
Il faut rechercher le caractère plongeant du goitre que l’on suspecte si n’est pas perçu le pôle inférieur des lobes lors de la déglutition, s’il existe une matité à la percussion et une circulation collatérale de la partie haute de la paroi thoracique. En cas de doute, la radiographie de thorax de face et de profil authentifie le prolongement endothoracique : opacité rétromanubriale, élargissant le médiastin antérosupérieur, refoulant ou laminant l’axe trachéal (
C’est au stade de goitre plurinodulaire que peuvent survenir les complications des goitres :
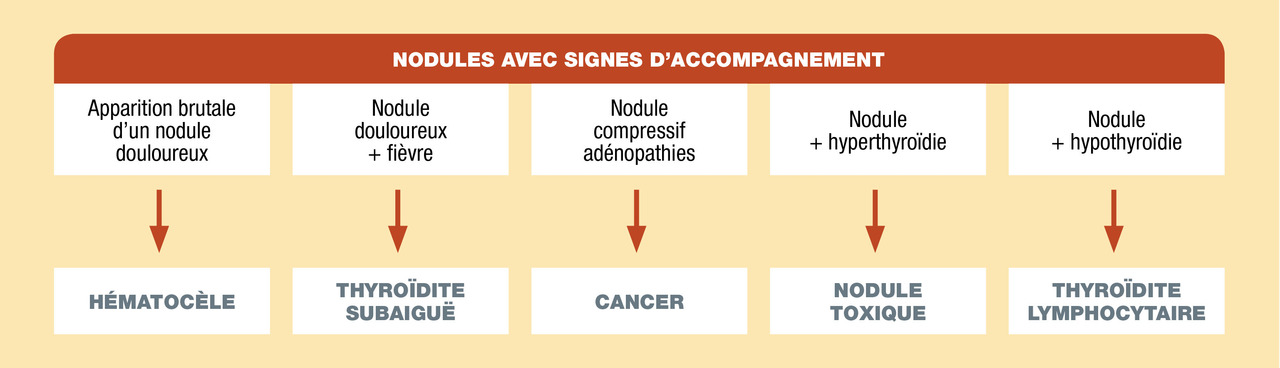
hémorragie (hématocèle) ;
infection (strumite) ;
hyperthyroïdie. Elle est annoncée par la baisse de TSH, puis responsable de signes thyrotoxiques, notamment cardiaques, et contribuant à la raréfaction osseuse ;
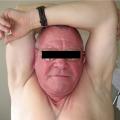
compression des organes de voisinage. Elle se marque par des troubles de la déglutition, une gêne respiratoire, des signes de compression veineuse : turgescence jugulaire, circulation collatérale, érythrose du visage démasquée par la manœuvre de Pemberton (bras levés collés contre les oreilles durant 1 mn) [fig. 6] ;
révélation d’un cancer. Les cancers sont présents dans 4-5 % des goitres plurinodulaires (soit une proportion analogue à celle constatée en cas de nodule solitaire). Ils sont longtemps latents au stade de tumeur différenciée, sous formes de nodules occultes, découverts lors de l’évaluation échographique ou de l’étude histopathologique de la pièce opératoire, puis cliniquement apparents. Certaines formes apparaissent dramatiquement évolutives, compressives et métastatiques, surtout en cas de dédifférenciation tumorale chez le sujet âgé.
Prise en charge thérapeutique
Elle est imparfaitement codifiée.En dépit de la latence clinique des stades initiaux, surtout dans les familles où se constituent des goitres, est ordinairement recommandée l’éradication médicamenteuse des petits goitres simples de l’adolescent qui font le lit des goitres multinodulaires de l’adulte. À ce stade, on peut obtenir la réduction de l’hypertrophie thyroïdienne par la prise de lévothyroxine (1 à 1,5 µg/kg/j), prescrite jusqu’à normalisation du volume thyroïdien, ordinairement après quelques mois.
On peut vérifier sous traitement médical que la TSH est réduite à une valeur proche de la limite inférieure de la normale (0,3-0,7 mU/L), et n’apparaît pas infranormale afin d’éviter tout inconfort et risque de surdosage thérapeutique. Le traitement peut être repris en cas de nouvelle poussée évolutive et de grossesse, ou maintenu au long cours dans les familles à risque si n’a pas été obtenue la normalisation du volume thyroïdien. L’apport d’iodure (100-200 µg/j), isolément ou en association avec l’hormone thyroïdienne, a également démontré son efficacité, mais n’est pas commodément disponible en France.
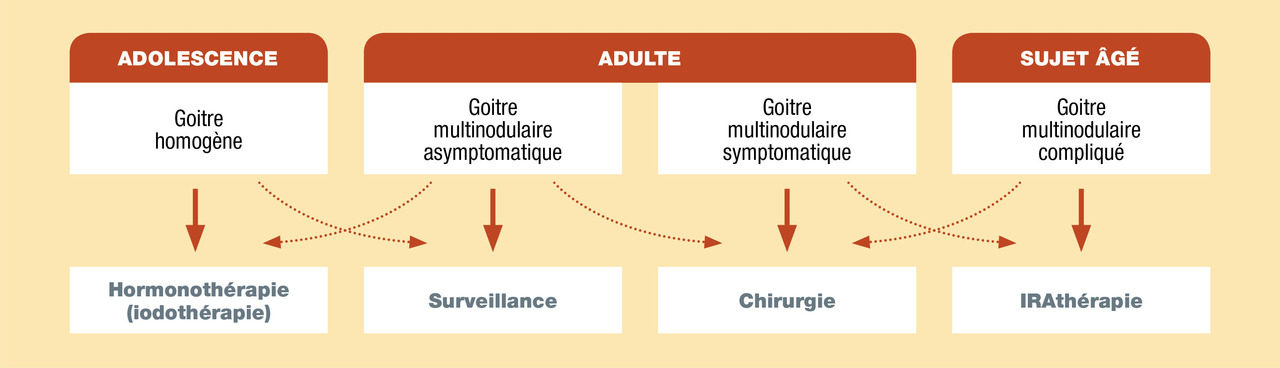
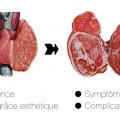
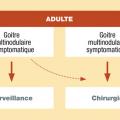
Chez l’adulte ou le sujet âgé, les goitres multinodulaires asymptomatiques, euthyroïdiens (sans abaissement de la TSH) et non suspects de malignité (cliniquement, en échographie et s’il est besoin en cytologie) bénéficient ordinairement de la seule surveillance. À ce stade, la thérapeutique médicale se révèle en effet ordinairement peu efficace ou mal tolérée, ce qu’explique la présence de nodules fonctionnels, captants, mal freinables par l’hormone thyroïdienne. L’intervention chirurgicale préventive peut également se discuter, en soulignant que celle-ci ne constitue pas un geste anodin, grevé d’un risque d’atteinte récurrentielle ou parathyroïdienne estimé à moins de 1 % dans les meilleures mains. Entre aussi en compte dans le choix des patients l’interrogation sur l’apparence future de la cicatrice.
Il est habituel de recommander l’exérèse chirurgicale consistant en la thyroïdectomie totale, dès que les goitres deviennent symptomatiques : gêne à la déglutition, à la phonation, disgrâce esthétique, circulation collatérale, TSH basse. À ce stade évolutif, la balance bénéfice-risques plaide alors authentiquement en faveur de la chirurgie. Bien sûr, l’intervention est aussi indispensable en cas de formation nodulaire suspecte de malignité.
Chez les sujets âgés, au stade de goitre ancien, négligé, lorsque l’état cardiaque ou général condui t à mettre en doute l’innocuité de la chirurgie, peut s’envisager l’administration d’une dose thérapeutique d’iode 131. L’IRAthérapie est susceptible d’obtenir une réduction rapide du volume du goitre (d’environ 30-40 % en 6 mois), l’atténuation des signes compressifs et l’éradication d’une éventuelle hyperthyroïdie. Des doses thérapeutiques complémentaires sont possibles, s’il apparaît nécessaire. L’iode 131 ne contre-indique pas le recours un jour ou l’autre à la chirurgie.
Les diverses possibilités de prise en charge thérapeutique ou de surveillance sont à présenter au patient, et doivent être discutées en vue d’un choix thérapeutique éclairé (
En définitive, l’évaluation diagnostique et les prises en charge des goitres simples diffèrent profondément en fonction du stade évolutif de la maladie. Chez tous les individus, et tout particulièrement dans les familles à risque de pathologie thyroïdienne, il est recommandé d’augmenter la charge en iode : consommation des produits de la mer, utilisation d’un sel enrichi en iode, prise de compléments alimentaires supplémentés en iodure (de l’ordre de 150 µg/j) avant la conception, tout au long de la grossesse et la période de lactation.
Autres pathologies thyroïdiennes responsables de goitre
Maladie de Basedow (v. chapitre Hyperthyroïdies)
Thyroïdites
La thyroïdite de Hashimoto constitue la forme hypertrophique des thyroïdites chroniques. Elle est responsable d’un goitre très ferme (de la consistance d’un pneu d’automobile), reproduisant exactement la morphologie de la glande au point qu’on palpe la pyramide de Lalouette. Elle expose à l’hypothyroïdie, ce qu’annonce l’accroissement de la TSH. Elle se marque biologiquement par des titres très élevés d’anticorps anti-TPO, en échographie par un aspect de goitre diffus, globalement hypoéchogène, légèrement hypervasculaire, finement hétérogène ou remanié par des formations nodulaires ou pseudonodulaires.Sans parler ici des formes atrophiques, toutes les autres thyroïdites (thyroïdites silencieuses d’origine auto-immune développées notamment dans le post-partum, thyroïdites subaiguës de De Quervain réactionnelles à une maladie virale, thyroïdite chronique fibreuse de Riedel) déterminent un goitre (
Rarement chez l’adulte, le goitre est la conséquence d’un trouble de l’hormonosynthèse en relation avec diverses anomalies moléculaires (transporteur de l’iode, TPO, déshalogénase, pendrine, Tg) et responsable d’hypothyroïdie congénitale. Le goitre s’observe aussi dans les états de sécrétion inappropriée de TSH, liés aux adénomes thyrotropes ou aux résistances aux iodothyronines.
Nodule thyroïdien
La majorité des nodules thyroïdiens sont bénins, et constituent la première manifestation d’une dystrophie plurinodulaire dont le développement s’affirmera au fil des années et des décennies. Un certain nombre d’entre eux (de l’ordre de 5 %) correspondent à des cancers, ordinairement de très bon pronostic lorsqu’ils sont reconnus, pris en charge et traités à ce stade nodulaire.
Épidémiologie
Les nodules sont 2 à 3 fois plus fréquents dans le sexe féminin. La grossesse, la déficience en iode, l’irradiation cervicale constituent des facteurs favorisants.
Évaluation
Plus communément, les nodules sont en apparence isolés. La majorité d’entre eux sont bénins, mais il importe de ne pas méconnaître un cancer. Concourent à la reconnaissance diagnostique un certain nombre d’arguments cliniques, biologiques, échographiques, cytologiques et évolutifs, qui seront ici précisés.
Primauté est donnée à la valeur de la TSH, qui guide la conduite des explorations :
une concentration sanguine accrue de TSH oriente vers un contexte de thyroïdite lymphocytaire, justifiant alors seulement la recherche des anticorps anti-TPO ; en cas des de négativité, la détermination est complétée par celle d’anti-TG. Dans les thyroïdites lymphocytaires, le problème difficile est de préciser la signification du nodule : soit nodule de thyroïdite, soit nodule épithéliomateux (3-4 % des cas) associé à la thyroïdite dont la nature peut être reconnue par les examens échographiques et cytologiques, soit nodule « vicariant » correspondant à un parenchyme normal épargné par le processus de thyroïdite, fixant les isotopes (Tc ou iode 123) et dont l’hypertrophie a été favorisée par l’accroissement de la TSH ;
une valeur basse de TSH est d’abord suggestive d’un nodule fonctionnel, producteur d’hormone thyroïdienne. La scintigraphie thyroïdienne à l’iode 123 ou au technétium révèle alors une fixation élective en regard du nodule palpé, extinctive vis-à-vis du reste du parenchyme. L’évaluation en échographie doppler couleur est susceptible de fournir aussi des aspects évocateurs.
Clinique (tableau 1)
Il faut prendre avec plus de prudence les nodules survenant dans le sexe masculin, dans le jeune âge (avant 16 ans) ou chez les sujets âgés (plus de 65 ans), et surtout après irradiation cervicale (la prévalence des nodules et la proportion de nodules malins sont alors 2 à 3 fois plus élevées). Le caractère très ferme ou dur, irrégulier, la présence de signes compressifs ou d’adénopathies sont suspects. L’évolutivité et la taille ne constituent pas isolément des arguments en faveur de la malignité. Cependant, il est prudent de se méfier particulièrement des nodules de plus de 3 ou 4 cm de diamètre, car le pronostic des cancers de grande taille est plus réservé. De même, n’est suspecte qu’une augmentation rapide de la taille du nodule : de plus de 20 % du volume ou de 2 mm de grand axe en un an.Biologie
Le dosage seul de la TSH est à réaliser en première intention.La mesure de la thyroglobuline n’a aucune place dans la reconnaissance du caractère bénin ou malin d’un nodule thyroïdien. Elle aura une utilité seulement dans la surveillance des cancers thyroïdiens opérés.
Le dosage de la calcitonine (CT) est recommandé, notamment avant toute intervention chirurgicale : chez un sujet porteur d’un nodule thyroïdien, un taux de calcitonine très élevé, supérieur à 100 pg/mL constitue un argument solide en faveur du cancer médullaire de la thyroïde (CMT), même si certaines tumeurs non thyroïdiennes (bronchiques, pulmonaires, pancréatiques, phéochromocytomes…) accroissent parfois le taux de calcitonine, modérément ou plus fortement. En cas de cancer médullaire de la thyroïde, la thyroïdectomie et le curage lymphatique par un chirurgien très spécialisé sont indispensables. Des accroissements modestes de calcitonine (20-50 pg/mL) s’observent dans des cancers médullaires de la thyroïde de petites dimensions mais aussi dans des hyperplasies des cellules C qu’on constate notamment chez les hommes, obèses et tabagiques, en cas de thyroïdite auto-immune ; une hypercalcitoninémie est possible aussi chez l’insuffisant rénal, dans les gastrites atrophiques, sous inhibiteur de la pompe à protons.
Échographie
L’échographie apporte des informations très précieuses sur les caractéristiques du nodule et du reste du parenchyme thyroïdien. Les nodules, notamment isolés, tissulaires hypoéchogènes, aux contours irréguliers, hypervasculaires, sans halo hypoéchogène complet en périphérie, sont particulièrement suspects. La présence de microcalcifications est suggestive des calcosphérites, caractéristique des cancers papillaires. L’examen peut détecter d’éventuelles adénopathies satellites.La classification EU-TIRADS quantifie le risque pronostique échographique de malignité des nodules (
Cytologie
L’étude cytologique du matériel cellulaire recueilli au niveau du nodule par ponction à l’aiguille fine est l’examen le plus sensible. L’examen est indispensable pour tous les nodules cliniquement suspects, aussi pour les nodules échographiquement plus suspects ; EU-TIRADS 3 de plus de 2 cm, EU-TIRADS 4 de plus de 15 mm, EU-TIRADS 5 de plus de 10 mm.La présentation des résultats de l’examen cytologique est maintenant codifiée en fonction du référentiel de Bethesda. Chaque classe fournit une orientation pronostique (tableau 3). 3 à 20 % des examens sont dits « ininterprétables » du fait de l’insuffisance du recueil du matériel (Bethesda 1), et doivent être répétées. 60 à 80 % des examens sont en faveur de la bénignité (Bethesda 2), ne justifiant pas la chirurgie. Une proportion plus faible de nodules sont cytologiquement « indéterminés » (Bethesda 3 et 4 surtout), majoritairement bénins, malins dans 6 à 40 % des cas, incitant à la prolongation des examens et de la surveillance. Les cytologies de classes 5 et 6 suspectes ou malignes relèvent de la chirurgie.
Scintigraphie et nodule thyroïdien
En présence d’une TSH normale, la scintigraphie de principe est un examen désuet : 90 % des nodules sont hypofixants, et seuls 5 à 10 % d’entre eux sont malins. Seul possède une signification le caractère fixant du nodule en faveur globalement de sa bonne différenciation. Le risque évolutif est un jour ou l’autre l’évolution vers l’hyperthyroïdie, qui apparaît ordinairement lorsque la taille du nodule fonctionnel excède 2,5 cm.On recommande la scintigraphie en cas de nodule cytologiquement à deux reprises ininterprétable (Bethesda 1) ou cytologiquement indéterminé (Bethesda 3 ou 4), de contre-indication ou de non-accessibilité à la ponction (traitement anticoagulant, altération des fonctions d’hémostase, nodule plongeant).
Stratégies thérapeutiques
Chirurgie
La chirurgie s’impose pour tous les nodules cliniquement, échographiquement et/ou cytologiquement suspects, ou lorsque la calcitonine est franchement accrue.La lobectomie-isthmectomie, éventuellement élargie en thyroïdectomie totale en fonction des résultats de l’étude anatomopathologique extemporanée du nodule, constitue un procédé thérapeutique traditionnel. Elle est inadaptée si en définitive le nodule apparaît malin lors de l’étude anatomopathologique définitive de la pièce opératoire. Elle n’était pas utile, et grevée d’un taux de récidive controlatérale de 30 à 40 % si le nodule est bénin.
Compte tenu des progrès de la chirurgie endocrinienne, les indications de la thyroïdectomie totale s’élargissent dès que le nodule apparaît suspect et qu’existe une dystrophie controlatérale.
Certains nodules, bénins et disgracieux, peuvent bénéficier d’une intervention par voie axillaire, robot-assistée.
Surveillance
La surveillance constitue une alternative à la chirurgie pour les nodules non suspects. Elle s’effectue au plan clinique, échographique, souvent complétée par un nouvel examen cytologique soit de principe après 6 mois, soit plus souvent lorsque l’évolution morphologique ultérieure le justifie (accroissement rapide du volume, aggravation du stade EU-TIRADS).Pour éviter une médicalisation excessive de nodules apparemment bénins, est recommandée une surveillance progressivement espacée : par exemple, après 6 mois, 1 an, 2 ans, 5 ans, 10 ans. Pour les formations nodulaires correctement évaluées, et initialement considérées non suspectes cliniquement, échographiquement et cytologiquement, l’évidence secondaire de malignité est possible mais rare, estimée à moins de 2 %.
Traitement hormonal
Le traitement hormonal frénateur par l’hormone thyroïdienne ne constitue pas un procédé diagnostique. Il a seulement pour intention de prévenir l’augmentation complémentaire de la taille du nodule et de la dystrophie périnodulaire. Il est particulièrement envisagé en cas de nodule bénin dans les familles où se constituent des goitres plurinodulaires. Il est à éviter chez les sujets de plus de 50 ans. Si dans ces circonstances, il est utilisé, il faut maintenir un taux de la TSH proche de la limite inférieure des normes pour éviter tout surdosage thérapeutique.Alcoolisation, thermoablation
La destruction de nodules cytologiquement bénins par des injections répétées d’alcool absolu ou par thermoablation (par les ultrasons, la radiofréquence ou le laser) fait l’objet d’études et d’évaluations.Situations particulières
Formations kystiques
Les kystes et hématocèles purs se présentent sous forme de formations anéchogènes. Celles-ci peuvent bénéficier de la ponction évacuatrice, éventuellement de l’hormonothérapie frénatrice et de l’alcoolisation en cas de récidive.Les formations mixtes à contenu liquide justifient éventuellement le dosage de Tg et de PTH dans le liquide de ponction (pour vérifier l’origine thyroïdienne ou parathyroïdienne des formations), surtout la ponction pour étude cytologique de la portion charnue. En cas de nodule mixte, il faut se méfier des liquides hémorragiques rapidement récidivants après ponction, qui peuvent correspondre à des cystadénocarcinomes papillaires.
Nodule thyroïdien et grossesse
Lorsqu’ils sont cliniquement, échographiquement ou cytologiquement suspects, les nodules peuvent être opérés au 2e trimestre de la grossesse, ou au-delà de l’accouchement.Nodule occulte
La majorité des nodules occultes et non palpables sont de petites dimensions, de moins de 1 cm de diamètre. Ils sont parfois plus volumineux (jusqu’à 2 à 3 cm), méconnus du fait de leur situation postérieure, ou lorsque la palpation cervicale est mal commode chez le sujet âgé, voûté ou obèse.
Les nodules occultes sont fortuitement découverts à l’occasion d’une évaluation au doppler de la circulation carotidienne, d’un examen échographique des parathyroïdes, d’une exploration tomodensitométrique cervicale ou thoracique, voire actuellement d’un examen par tomographie d’émission de positons (TEP).
Le risque que ces formations nodulaires occultes correspondent à un cancer est proche de 5 %. La très grande majorité de ces formations malignes correspondent à des microcancers papillaires (d’un diamètre < 1 cm) dont le pouvoir agressif est très faible.
En cas de nodule occulte incitent cependant à la prudence les observations suivantes :
la présence d’adénopathies cervicales ou d’une paralysie récurrentielle ;
une hérédité de cancer médullaire de la thyroïde (30 % de formes familiales), ou papillaire (près de 5 % sont familiaux affectant plus de 2 membres de la famille) ;
certaines caractéristiques échographiques : nodules fortement hypoéchogènes, hypervasculaires, à contours irréguliers, microcalcifications (EU-TIRADS 5) ;
la découverte par une fixation lors d’un examen par TEP.
La ponction à l’aiguille fine sous contrôle échographique en vue de l’examen cytologique est ordinairement réservée aux formations nodulaires solides hypoéchogènes de plus de 10 mm de diamètre, les seules à risque de morbidité.
Seules de rares situations justifient l’intervention chirurgicale, la surveillance échographique ou cytologique. La majorité des nodules occultes, fortuitement découverts, peuvent bénéficier de la simple surveillance clinique par la palpation occasionnelle de la loge thyroïdienne.
En définitive, le nodule thyroïdien ne constitue pas une urgence diagnostique. La lobectomie-isthmectomie ne constitue pas la meilleure approche diagnostique et thérapeutique. Statistiquement, un nodule thyroïdien est a priori bénin et constitue la première manifestation d’un goitre plurinodulaire. Le principe de bénignité est à remettre en cause lorsque les données cliniques, ou les données échographiques, ou les données cytologiques, ou enfin les données évolutives ne sont pas suffisamment rassurantes
.
Cancers thyroïdiens
La présentation des cancers s’est beaucoup modifiée durant ces dernières décennies. 40 % d’entre eux sont reconnus au stade de microcarcinome (< 10 mm), souvent fortuitement à l’occasion d’examens échographiques, ou lors de l’analyse anatomopathologique de goitres opérés.
Les problématiques actuelles sont constituées d’une part par le « surdiagnostic », correspondant à la reconnaissance et à la prise en charge de microcancers qui n’auraient jamais déterminé de morbidité. D’autre part, sont entrepris de gros efforts pour améliorer le pronostic de formes non guéries par la chirurgie et inaccessibles au traitement radio-isotopique (« tumeurs thyroïdiennes réfractaires ») pour lesquelles se développent des thérapeutiques nouvelles (comme les inhibiteurs de la tyrosine kinase) dont l’efficacité et la tolérance font l’objet d’évaluations.
Variétés anatomopathologiques
Les carcinomes différenciés d’origine vésiculaire se constituent à partir de l’épithélium des follicules thyroïdiens. Ils constituent plus de 90 % des cas et comportent :
les carcinomes papillaires : environ 85 % des cas, apparaissant chez le sujet jeune (avant 40 ans), souvent plurifocaux, à extension surtout locorégionale responsable d’un envahissement lymphatique cervical puis médiastino-pulmonaire. Les métastases à distance sont rares. Accessibles au traitement chirurgical et radio-isotopique, ils jouissent d’un excellent pronostic (plus de 95 % de guérison). Certaines variétés (à cellules hautes, sclérosants diffus…) sont de moins bon pronostic ;
les carcinomes vésiculaires : 5-10 % des cas, survenant un peu plus tardivement, peu lymphophile, à dissémination surtout hématogène, ce qui explique la possibilité de métastases pulmonaires, osseuses, cérébrales mais pratiquement jamais hépatiques. Les carcinomes vésiculaires encapsulés sont de très bon pronostic, les formes invasives ou à cellules oncocytaires ont un pronostic plus réservé ;
les carcinomes peu différenciés : 2-5 % (trabéculaires, insulaires…) sont de pronostic plus défavorable ;
les carcinomes anaplasiques (1 %) correspondent souvent à la dédifférenciation d’un cancer négligé, surviennent surtout chez le sujet âgé. Responsables d’un envahissement cervical rapidement dramatique et de métastases, ils sont très péjoratifs, le plus souvent responsables du décès en moins d’un an.
Les carcinomes médullaires sont développés aux dépens des cellules C de siège parafolliculaire et productrices de calcitonine. Ils constituent environ 7 % des cancers thyroïdiens. Ils sont de pronostic plus sévère, en raison de leur diffusion à la fois par voie lymphatique et sanguine, et de leur inaccessibilité au traitement radio-isotopique et à l’hormonothérapie thyroïdienne frénatrice. 30 % d’entre eux sont familiaux, liés à des mutations du gène RET, entrent souvent dans le cadre des néoplasies endocriniennes multiples de type 2 où s’observent aussi des phéochromocytomes et tardivement des adénomes parathyroïdiens (NEM2).
Rarement (1 % des cas) existent des lymphomes, des carcinomes épidermoïdes, des sarcomes, des paragangliomes ou des métastases thyroïdiennes (lcancer du rein à cellules claires).
Circonstances de découverte
Plus rarement, le cancer thyroïdien se révèle par une adénopathie cervicale, des signes de compression (comme une paralysie récurrentielle), des flushs ou une diarrhée motrice en lien avec un cancer médullaire, des métastases.
La découverte anatomopathologique de microcancers sur la pièce de thyroïdectomie d’un goitre ou lié à la maladie de Basedow est commune.
Facteurs pronostiques
Le risque de rechute et de décès des cancers différenciés de souche vésiculaire est accru en raison :
de l’âge : moins de 16 ans, plus de 45 ans ;
de la taille tumorale : plus de 2 ou 4 cm ;
de l’extension au-delà de la capsule thyroïdienne, de l’extension ganglionnaire massive, de métastases ;
du type histologique : formes papillaires à cellules hautes, sclérosant diffus, vésiculaire invasif ou peu différencié, oncocytaire ;
de la qualité de la prise en charge thérapeutique et de la surveillance.
Le pronostic de survie est traditionnellement défini par la classification TNM. Mais compte tenu de la très bonne survie de la majorité des patients est plutôt pris en compte le risque de récidive, comme dans la classification de l’ATA.
Prise en charge thérapeutique des cancers thyroïdiens différenciés de souche vésiculaire
Thyroïdectomie
La chirurgie est le traitement de 1re intention. Elle consiste, le plus souvent, en la thyroïdectomie totale, le curage ganglionnaire du compartiment central parfois latéral, indispensable en cas d’adénopathies malignes avérées. L’intérêt d’un curage prophylactique systématique en l’absence d’adénopathies décelables est controversé dans les cancers différenciés, recommandé dans les carcinomes thyroïdiens médullaires, les cancers de l’enfant et de l’adolescent. Dans certaines formes localisées de petites dimensions (moins de 2 cm), la lobectomie est parfois proposée.Les complications les plus habituelles sont l’hypoparathyroïdie et les paralysies récurrentielles (risque entre 1 et 5 %, lié à la sévérité de la maladie et l’expérience de l’équipe chirurgicale).
Traitement radiométabolique
Il consiste en l’administration d’une dose d’iode 131 (30 à 100 mCi = 3,7 GBq), à la faveur d’une brève hospitalisation en secteur radioprotégé. Il permet la destruction du tissu thyroïdien normal et d’éventuels foyers carcinomateux résiduels, la détection rare d’éventuelles localisations à distance. Il est réalisé en situation de défreinage de la TSH en l’absence d’hormonothérapie, ou plus souvent sous stimulation par TSH recombinante humaine exogène.On peut se dispenser du traitement radio-isotopique dans les formes localisées (< 2 cm de diamètre), de très bon pronostic.
Hormonothérapie
Elle est prescrite sous forme de lévothyroxine initialement à doses frénatrices (proche de 2 µg/kg/j) abaissant la TSH à une valeur proche de 0,1 mU/L. Secondairement, l’hormonothérapie est réduite à posologie substitutive (proche de 1,6-1,7 µg/kg/j) normalisant la TSH (entre 0, 3 et 2,5 mU/L) seulement si ont été obtenus les critères de rémission (cf. infra).Surveillance
Elle est fondée sur l’évaluation clinique : palpation de la loge thyroïdienne et des aires ganglionnaires, appréciation de la tolérance. Elle est complétée par la détermination de la concentration de la TSH, et celle de la thyroglobuline circulante (Tg) dont la valeur indétectable après thyroïdectomie totale et iode 131 n’est interprétable qu’en l’absence d’anticorps anti-Tg circulants. L’échographie cervicale permet de repérer d’éventuelles récidives locales et ganglionnaires, et de guider la cytoponction.La rémission est affirmée 6 à 12 mois après la chirurgie et l’administration d’iode 131, en l’absence de toute localisation échographique et en présence de valeurs indétectable de la Tg.
Les localisations résiduelles, les récidives et métastases peuvent bénéficier de réinterventions chirurgicales, de doses thérapeutiques itératives d’iode 131 (auxquelles sont sensibles 70 % des métastases). Dans les formes réfractaires, évolutives se discute l’opportunité de l’inclusion des patients dans des protocoles d’évaluation de thérapeutiques moléculaires ciblées.
Prise en charge des autres situations
Cancers peu différenciés et anaplasiques
Seules les formes intracapsulaires sont accessibles à la chirurgie. Dans les formes invasives, il n’y a pas d’indication à la chirurgie. Le confort de vie, sinon la survie, est améliorée par la radiothérapie intensive et si l’état du patient l’autorise à la chimiothérapie antimitotique.Cancer médullaire
Il justifie la thyroïdectomie totale, le curage ganglionnaire du compartiment central, souvent étendu aux compartiments latéraux. Il n’y a pas d’indication à l’iode 131. La lévothyroxine est donnée à posologie substitutive.La surveillance est exercée au plan clinique et échographique et par la mesure de la calcitonine circulante (CT), éventuellement complétée par celle de l’antigène carcino-embryonnaire (ACE). D’éventuelles localisations à distance peuvent justifier des interventions chirurgicales ou la radiothérapie. La chimiothérapie est envisagée pour des formes rapidement évolutives, ce que permet d’apprécier le temps de doublement de la calcitonine.
Le repérage des formes familiales est permis par la détection de mutations du gène RET. La pénétrance du gène est élevée, proche de 100 %, si bien que sa caractérisation conduit à des thyroïdectomies préventives précoces, dès le jeune âge (parfois dès 3-4 ans, selon le type de mutation).
En définitive, la prise en charge des cancers thyroïdiens dépend du type histologique de la tumeur et de son stade évolutif.
Goitre
Le remaniement nodulaire des goitres se constitue progressivement au fil des décennies.
C’est seulement au stade multinodulaire que les goitres deviennent symptomatiques et sont à risque de complications.
L’hormonothérapie, la simple surveillance, la chirurgie ou l’iode 131 constituent les possibilités de prise en charge des goitres en fonction de l’âge, des caractéristiques morphologiques et fonctionnelles de la pathologie thyroïdienne.
Nodule
Le dosage de la TSH est le premier examen à réaliser en cas de nodule thyroïdien.
Le risque carcinologique des nodules thyroïdiens est défini en échographie selon la classification EU-TIRADS, en cytologie selon la classification de Bethesda.
La majorité des nodules thyroïdiens peuvent bénéficier de la surveillance.
Cancer
Pour éviter le « surdiagnostic » de cancer et le « surtraitement », on convient de n’explorer que les nodules de plus de 8 à 10 mm de diamètre.
La thyroglobuline est un paramètre essentiel de la surveillance des cancers opérés.
Les tumeurs thyroïdiennes réfractaires à la chirurgie et l’iode 131 peuvent entrer dans le cadre de protocoles thérapeutiques par les inhibiteurs de tyrosine kinase.
La calcitonine constitue un marqueur diagnostique et pronostique des cancers médullaires de la thyroïde, familiaux dans un tiers des cas.
POINTS FORTS À RETENIR
Goitre
La correction de la déficience iodée n’a pas fait disparaître les goitres.
Le remaniement nodulaire des goitres se constitue progressivement au fil des décennies.
C’est seulement au stade multinodulaire que les goitres deviennent symptomatiques et sont à risque de complications.
L’hormonothérapie, la simple surveillance, la chirurgie ou l’iode 131 constituent les possibilités de prise en charge des goitres en fonction de l’âge, des caractéristiques morphologiques et fonctionnelles de la pathologie thyroïdienne.
Nodule
La très grande majorité des nodules thyroïdiens sont bénins, et surtout à risque d’évoluer vers un goitre multinodulaire.
Le dosage de la TSH est le premier examen à réaliser en cas de nodule thyroïdien.
Le risque carcinologique des nodules thyroïdiens est défini en échographie selon la classification EU-TIRADS, en cytologie selon la classification de Bethesda.
La majorité des nodules thyroïdiens peuvent bénéficier de la surveillance.
Cancer
Les cancers de souche vésiculaire sont ordinairement d’évolution lente et de bon pronostic, accessibles au traitement chirurgical, encore souvent complété par l’iode 131.
Pour éviter le « surdiagnostic » de cancer et le « surtraitement », on convient de n’explorer que les nodules de plus de 8 à 10 mm de diamètre.
La thyroglobuline est un paramètre essentiel de la surveillance des cancers opérés.
Les tumeurs thyroïdiennes réfractaires à la chirurgie et l’iode 131 peuvent entrer dans le cadre de protocoles thérapeutiques par les inhibiteurs de tyrosine kinase.
La calcitonine constitue un marqueur diagnostique et pronostique des cancers médullaires de la thyroïde, familiaux dans un tiers des cas.

 Encadrés
Encadrés