L’hémogramme, ou numération formule sanguine (NFS), est aujourd’hui l’examen biologique le plus prescrit en France. C’est un outil essentiel pour dépister, explorer ou suivre de nombreuses pathologies, bien au-delà du simple cadre des pathologies hématologiques.
Il est réalisé à partir d’un échantillon de sang prélevé par ponction veineuse et recueilli dans un tube contenant un anticoagulant de type EDTA (acide éthylène diamine tétra-acétique) – il n’est pas indispensable que le patient soit à jeun. Un prélèvement par microméthode au talon chez le nouveau-né ou au bout du doigt (capillaire) chez certains patients est possible.
Données quantitatives et qualitatives de l’hémogramme
- la mesure de la concentration en hémoglobine (Hb, en g/dL selon l’usage ou g/L) ;
- la numération des érythrocytes ou globules rouges (GR, en T/L ou 1012/L) ;
- le calcul de l’hématocrite (Ht, en %) correspondant au volume relatif occupé par les hématies par rapport au plasma (selon la formule : Ht = VGM × GR/10) ;
- les principales constantes érythrocytaires :
- volume globulaire moyen (VGM, en fL),
- concentration corpusculaire moyenne en hémoglobine (CCMH, en g/dL ; selon la formule : CCMH = Hb/Ht × 100),
- teneur corpusculaire moyenne en hémoglobine (TCMH, en pg/cellule ; selon la formule TCMH = Hb/GR × 10) ;
- la numération des plaquettes (PLT, en G/L ou 109/L) ;
- la numération des leucocytes (GB, en G/L ou 109/L) ;
- la formule leucocytaire (exprimée obligatoirement en valeur absolue).
Les valeurs normales de l’hémogramme chez l’adulte et le nouveau-né sont récapitulées dans les
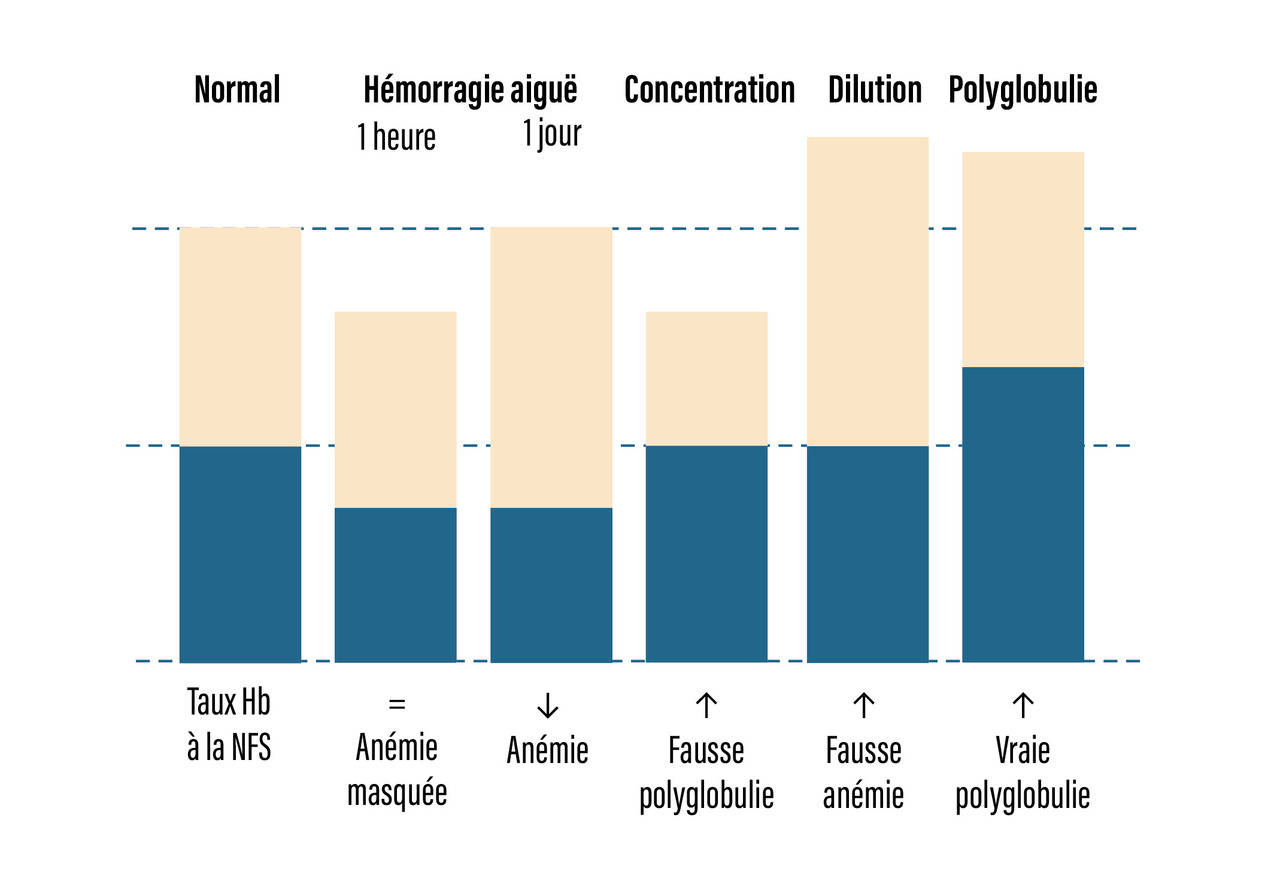
Il est important de noter que l’hémogramme donne des valeurs d’hémoglobine en concentration, la numération cellulaire tenant en effet compte des cellules et de leur contenant, le plasma. Les variations du plasma peuvent ainsi donner lieu à de fausses anémies par hémodilution ou à une pseudopolyglobulie par hémoconcentration (
L’analyse qualitative de l’hémogramme est assurée par l’examen du frottis sanguin. Il se fait après étalement d’une goutte de sang sur une lame et coloration de May-Grünwald Giemsa (MGG) ; il permet d’apprécier l’aspect cytologique des cellules et de détecter la présence de cellules anormales.
Indications d’un hémogramme (rang A)
Ainsi l’hémogramme doit être pratiqué devant :
- des signes d’appel évoquant une baisse d’une ou plusieurs lignées :
- syndrome anémique (pâleur, asthénie, dyspnée, tachycardie, souffle systolique…),
- syndrome hémorragique (hématome, purpura, ecchymose, saignement extériorisé…),
- syndrome infectieux, notamment inexpliqué, sévère, persistant ou récidivant,
- ictère ;
- des signes d’appel évoquant une augmentation d’une ou plusieurs lignées sanguines :
- syndrome d’hyperviscosité (érythrose cutanée, prurit aquagénique, acouphènes, vertiges…),
- syndrome tumoral, notamment ganglionnaire, hépatosplénomégalie,
- altération de l’état général (asthénie, amaigrissement, anorexie…),
- exploration d’une thrombose veineuse et/ou artérielle ;
- en dehors de toute symptomatologie, il fait partie du bilan :
- recommandé au 6e mois de grossesse,
- en médecine du travail ou de dépistage,
- en préopératoire,
- en préthérapeutique ou de suivi.
Indications d’une demande en urgence (rang A)
- un état de choc ;
- une pâleur intense ;
- une angine ulcéronécrotique ou résistante aux antibiotiques ;
- une hyperthermie après une prise médicamenteuse, notamment post-chimiothérapie cytotoxique ;
- un syndrome hémorragique, notamment un purpura pétéchial extensif, des bulles hémorragiques intrabuccales ;
- un purpura fébrile ;
- un syndrome tumoral ganglionnaire.
Indications du frottis sanguin et interprétation (rang A)
Les automates de laboratoire actuels sont de plus en plus performants pour détecter des anomalies quantitatives et qualitatives ; cependant, l’œil expert du biologiste reste indispensable pour une bonne interprétation cytologique.
Ainsi, l’automate génère une lame dans la plupart des anomalies de l’hémogramme, telles que :
- neutropénie, pour la recherche de signes de dysplasie, de cellules anormales, de lymphocytes à grains… ;
- hyperlymphocytose pour la recherche d’un aspect polymorphe ou monomorphe des lymphocytes, de lymphocytes atypiques ;
- monocytose, hyperbasocytose, hyperéosinophilie ;
- anémie normo- ou macrocytaire arégénérative, pour la recherche de signes de dysplasie, de carence vitaminique ;
- anémie hémolytique, pour la recherche d’anomalie des globules rouges (sphérocytose, drépanocytose, elliptocytose…) ;
- thrombopénie, pour la recherche de schizocytes, amas plaquettaires, anomalies constitutionnelles des plaquettes ;
- thrombocytose ;
- bicytopénie ou pancytopénie.
- un accès palustre (diagnostic d’espèce et parasitémie) ;
- un syndrome mononucléosique ;
- une suspicion de microangiopathie thrombotique (recherche de schizocytes) ;
- un syndrome tumoral ganglionnaire et/ou une splénomégalie ;
- en onco-hématologie pédiatrique.
Anomalies des différentes lignées et leurs principales causes (OIC-212-06-A)
- hémoglobinémie inférieure à 6 g/dL chez l’adulte et l’enfant, ou inférieure à 11 g/dL chez le nourrisson, ou toute anémie mal tolérée (dyspnée, douleur thoracique…) ;
- hématocrite supérieure à 60 % ;
- neutropénie sévère inférieure à 0,5 G/L, a fortiori agranulocytose avec un taux de polynucléaires neutrophiles (PNN) inférieur à 0,2 G/L (risque infectieux majeur) ;
- thrombopénie inférieure à 20 G/L, même en l’absence de syndrome hémorragique ;
- hyperleucocytose avec cellules immatures (blastes).
Anomalies de la lignée érythrocytaire
Anémie ( v . item 213)
Une anémie est définie par une baisse du taux d’hémoglobine, en fonction des valeurs seuils liées à l’âge et au sexe. Le taux d’hématocrite évolue parallèlement au taux d’hémoglobine, qu’il y ait hémoconcentration ou hémodilution ; cependant, ce paramètre n’intervient pas dans la définition de l’anémie, de même que le nombre de globules rouges.Cette définition peut être prise en défaut dans le cadre initial d’une hémorragie aiguë : la perte de sang ne modifie pas le ratio entre cellules sanguines et plasma. Cependant, la diminution du taux d’hémoglobine ne signifie pas toujours anémie. En cas d’hémodilution par augmentation du volume plasmatique, la concentration mesurée en hémoglobine est sous-estimée, source de fausse anémie. On peut retrouver cette situation lors de la grossesse (à partir du 2e trimestre), en cas de splénomégalie volumineuse, d’insuffisance cardiaque, d’hyperprotidémie.
La caractérisation de l’anémie est indispensable à la démarche diagnostique et se déduit des paramètres érythrocytaires (VGM, CCMH). Il est également essentiel de décrire son caractère régénératif ou non, sa profondeur, son caractère isolé ou associé à d’autres cytopénies et la présence d’éventuelles anomalies morphologiques.
Le volume globulaire moyen définit les anémies microcytaire (VGM inférieur à la norme), normocytaire (VGM normal) ou macrocytaire (VGM supérieur à la norme.)
La concentration corpusculaire moyenne en hémoglobine (CCMH) indique si l’anémie est normochrome (CCMH normal) ou hypochrome (CCMH inférieure à la norme). Il faut retenir qu’il n’existe pas de situation pathologique avec hyperchromie (CCMH supérieure à la norme). En effet, l’hyperchromie signe en général une erreur d’analyse de l’automate en lien avec la présence soit d’une agglutinine froide, soit d’une hyperbilirubinémie ou d’une hyperlipémie. Très rarement, on peut observer une vraie hyperchromie dans des sphérocytoses héréditaires, par déshydratation des globules rouges, faisant augmenter de manière modérée la CCMH.
Les anémies microcytaires (VGM < 80 fL chez l’adulte et < 70 fL chez l’enfant), pouvant être hypochromes ou normochromes, sont liées à un défaut de synthèse de l’hémoglobine. Elles doivent faire rechercher en première intention une carence en fer, ou sont souvent associées à un syndrome inflammatoire chronique. On retrouve, au second plan, des syndromes thalassémiques à explorer par une électrophorèse de l’hémoglobine, notamment si le bilan du métabolisme du fer et le bilan inflammatoire sont normaux.
Les anémies normocytaires (VGM compris entre 80 et 100 fL chez l’adulte, entre 70 et 95 fL chez l’enfant) nécessitent l’appréciation de la réponse médullaire par la numération des réticulocytes. On parle :
- d’anémie régénérative si les réticulocytes sont supérieurs à 120-150 G/L, orientant vers une cause périphérique telle une hémolyse, ou une phase de récupération érythrocytaire après une hémorragie aiguë, un syndrome inflammatoire prolongé, ou bien post-chimiothérapie cytotoxique ;
- d’anémie arégénérative si les réticulocytes sont inférieurs à 120 G/L, traduisant un défaut de production de la moelle osseuse (cause centrale). Après élimination d’une insuffisance rénale ou thyroïdienne, elle justifie une exploration médullaire.
Polyglobulie
La polyglobulie est définie par une élévation du taux d’hémoglobine et d’hématocrite, et ne tient pas compte du nombre de globules rouges. Dans la polyglobulie, l’hémoglobine et l’hématocrite augmentent de manière proportionnelle ; cependant, l’hématocrite est plus souvent utilisé car il est un reflet plus fidèle de l’augmentation de la masse sanguine.Le bilan étiologique doit d’emblée éliminer les fausses polyglobulies dans lesquelles l’augmentation de l’hématocrite, de l’hémoglobine et des globules rouges ne s’accompagnent pas d’une augmentation du volume globulaire total : sujets de grande taille et pléthoriques (syndrome de Gaisböck), hémoconcentration (déshydratation) par diminution du volume plasmatique, fausse polyglobulie microcytaire (augmentation des globules rouges mais pas de l’hémoglobine ni de l’hématocrite).
Anomalies morphologiques des globules rouges
Différentes anomalies morphologiques des globules rouges peuvent être décrites sur le frottis sanguin, plus ou moins spécifiques de certaines pathologies :- hématies en rouleaux, correspondant à des hématies empilées les unes sur les autres. Elles se retrouvent dans des dysglobulinémies (myélome) ou des états inflammatoires ;
- anisocytose, dans laquelle les hématies sont de diamètre variable. Cette anomalie n’est pas spécifique d’une pathologie ; elle est le simple témoin d’une dysérythropoïèse ;
- poïkilocytose, dans laquelle les hématies sont de forme différente. Cette anomalie a la même valeur non spécifique que l’anisocytose ;
- hématies en cible, c’est-à-dire avec la présence d’un halo central hémoglobinisé supplémentaire. Elles s’observent dans de nombreuses hémoglobinopathies, des hépatopathies avec ou sans ictère, la carence martiale ;
- dacryocytes, correspondant à des hématies en forme de larmes. Ils existent dans la myélofibrose, toutes les splénomégalies quelle qu’en soit l’origine, et des anémies carentielles sévères ;
- sphérocytes, qui sont des hématies sphériques et plus petites qu’attendu. Ils se voient dans la sphérocytose héréditaire et en cas d’anémie hémolytique ;
- schizocytes, qui sont des fragments d’hématies. Leur présence doit faire rechercher une microangiopathie thrombotique ;
- drépanocytes, qui correspondent à des hématies en forme de faucilles, signant une drépanocytose ;
- acanthocytes, qui sont des hématies avec quelques spicules à leur surface, signant une insuffisance hépatique/cirrhose ou une neuro-acanthocytose ;
- corps de Howell-Jolly, qui correspondent à un reliquat d’ADN intra-érythrocytaire. Ils se voient en cas d’asplénie fonctionnelle ou de splénectomie ;
- hématies ponctuées, avec des ponctuations basophiles intra-érythrocytaires. Elles ne sont pas spécifiques (infection, dysérythropoïèse, thalassémie, saturnisme…) ;
- corps de Pappenheimer, qui sont des granules sombres intra-érythrocytaires. Leur présence est peu spécifique (anémie sidéroblastique, thalassémie majeure, cirrhose…).
Anomalies de la lignée granulocytaire
Polynucléose neutrophilique
Elle correspond à un nombre de PNN supérieur à 7 G/L chez l’adulte et est le plus souvent d’origine réactionnelle : en premier lieu, à la suite d’une infection bactérienne généralisée ou localisée. À noter que les infections virales n’entraînent en général pas d’augmentation des neutrophiles, comme certaines infections bactériennes (typhoïde, tuberculose, brucellose).Certaines situations physiologiques doivent être éliminées :
- effort physique ;
- période post-prandiale ;
- fin de grossesse ;
- postopératoire ;
- nouveau-né.
- toxique (tabagisme) ou iatrogène (corticoïdes, lithium) ;
- maladie inflammatoire chronique ou cancer ;
- nécrose tissulaire (infarctus, pancréatite) ;
- cancer ou lymphome (lymphome de Hodgkin+++).
Neutropénie
La neutropénie est un facteur de risque infectieux majeur (bactérien et fongique), dès lors que les PNN sont inférieurs à 0,5 G/L. On parle d’agranulocytose si les PNN sont inférieurs à 0,2 G/L.Il est important de caractériser la neutropénie par sa profondeur, son ancienneté, si elle est permanente ou intermittente, et si elle est isolée ou associée à d’autres cytopénies.
Les neutropénies isolées et transitoires sont le plus souvent d’origine infectieuse ou médicamenteuse.
Les neutropénies d’aggravation progressive ou profonde doivent faire rechercher une hémopathie et adresser à un spécialiste.
Une neutropénie stable, modérée et isolée se retrouve fréquemment chez des sujets d’ethnie africaine par excès de margination (augmentation de l’adhésion des PNN aux cellules endothéliales).
Les causes principales des neutropénies sont :
- la prise de médicaments ;
- les infections : virales (hépatite, grippe, Covid, virus de l’immunodéficience humaine [VIH]…) mais aussi bactériennes (typhoïde, brucellose, septicémie sévère...) ou parasitaires (paludisme) ;
- les dysimmunités (syndrome de Felty, lupus) ;
- l’hypersplénisme (splénomégalie associée) ;
- les hémopathies malignes (leucémie aiguë, syndrome myélodysplasique, leucémie à grands lymphocytes granuleux [LGL]…) ;
- la prise de toxiques.
Myélémie
La myélémie correspond au passage dans la circulation sanguine de précurseurs immatures granuleux (métamyélocytes, myélocytes, promyélocytes, blastes). Il est important d’évaluer sa quantité (significative si supérieurs à 2 %) et son caractère équilibré (respect de la cascade de différenciation).Les principales causes sont :
- réactionnelles et transitoires : infection, maladie inflammatoire, anémie hémolytique, régénération médullaire (post-chimiothérapie) ;
- chroniques : syndrome myéloprolifératif, métastase osseuse de cancer solide.
Hyperéosinophilie
Le plus souvent, elle est liée à une infection parasitaire, une allergie, ou un médicament. Plus rarement, l’éosinophilie est satellite d’un cancer ou d’une maladie systémique.Elle peut se rencontrer fréquemment de manière transitoire chez le prématuré dans les deux premiers mois de vie.
Hyperbasophilie
L’hyperbasophilie peut s’observer de façon modérée lors de manifestations allergiques. Elle doit, sinon, faire penser à une leucémie myéloïde chronique.Hypermonocytose
L’excès de monocytes (supérieurs à 1 G/L) se voit le plus souvent de façon transitoire et est d’origine réactionnelle :- infection bactérienne (tuberculose, endocardite, typhoïde, brucellose…), parasitaire (paludisme, leishmaniose...) ;
- maladie inflammatoire ou néoplasie ;
- nécrose tissulaire ;
- régénération médullaire après une agranulocytose.
Une monocytopénie doit faire rechercher une leucémie à tricholeucocytes.
Hyperlymphocytose
Une analyse du frottis sanguin pour apprécier la morphologie des lymphocytes et la présence de cellules mononucléées hyperbasophiles est fondamentale dans l’orientation diagnostique. De plus, le seuil et l’origine d’une hyperlymphocytose dépendent grandement de l’âge :- chez l’enfant, elle est réactionnelle à une infection bénigne (virose, coqueluche) ;
- chez l’adolescent, elle est associée à un syndrome mononucléosique (voir item 217) ;
- chez l’adulte, elle est le plus souvent en lien avec un syndrome lymphoprolifératif, ou réactionnelle chez les patients tabagiques.
Lymphopénie
Inférieure à 2 G/L dans les premières années de vie et inférieure à 1 G/L ensuite, une lymphopénie est souvent associée à :- une infection virale (tous virus, notamment VIH) ;
- une hémopathie lymphoïde ;
- la prise de médicaments (corticothérapie, immunosuppresseur, chimiothérapie) ;
- une maladie dysimmunitaire ou inflammatoire (lupus, sarcoïdose…) ;
- un déficit immunitaire primitif ;
- une insuffisance rénale chronique.
Anomalies de la lignée mégacaryocytaire
Thrombocytose
La thrombocytose est le plus souvent d’origine réactionnelle (taux inférieur à 800 G/L) et doit faire rechercher :- un stress (chirurgie, accouchement…) ;
- une carence martiale ;
- un syndrome inflammatoire ;
- une splénectomie.
Thrombopénie
Elle est définie par un taux de plaquettes inférieur à 150 G/L, confirmé après vérification impérative sur lame pour éliminer un artefact dû à l’agglutination des plaquettes (induite par l’EDTA ou la coagulation du prélèvement). Les causes sont nombreuses et de deux types :- centrales (mégacaryocytes absents ou dysplasiques) dans le cadre d’aplasie médullaire, d’envahissement médullaire malin ;
- périphériques (moelle riche en mégacaryocytes normaux, sans cellules anormales dans la moelle osseuse) telles que le purpura thrombopénique immunologique (PTI), la coagulation intravasculaire disséminée (CIVD), les microangiopathies thrombotiques (MAT)…
Par ailleurs, une thrombopénie par séquestration splénique est fréquente en cas de splénomégalie.
Hémogramme chez l’enfant (OIC-212-07 et 08-A)
POINTS FORTS À RETENIR
L’hémogramme est l’examen le plus prescrit en France.
Les valeurs normales de l’hémogramme varient selon l’âge, le sexe et l’origine ethnique.
De façon générale, l’hémogramme est indiqué pour confirmer une donnée clinique, pour rechercher une possible anomalie devant un tableau clinique peu parlant ou pour quantifier une anomalie connue.
L’interprétation de l’hémogramme prend en compte des données quantitatives à interpréter en valeur absolue, et des données qualitatives.
L’hémogramme doit être réalisé avant toute thérapeutique, pouvant en modifier les données ou l’interprétation.
Hémogramme chez l’adulte et l’enfant : indications et interprétations
L’hémogramme est un examen tellement courant et transversal qu’il peut faire partie de tous les dossiers des ECN, toutes spécialités confondues. Une ou plusieurs questions sont d’ailleurs quasiment posées chaque année.
ECN 2016 – Patient de 29 ans présentant un lupus systémique. L’hémogramme à décrire montrait une anémie arégénérative, une thrombopénie et une lymphopénie.
ECN 2020 – Patient de 40 ans consultant pour une asthénie récente et une bulle hémorragique intrabuccale. Il était demandé de mentionner les examens à réaliser en urgence, notamment l’hémogramme ; et de décrire par la suite les résultats de cet examen : neutropénie, anémie normochrome et thrombopénie, orientant vers une leucémie aiguë.
ECN 2021 – Patient de 67 ans adressé aux urgences pour une pneumonie aiguë communautaire à pneumocoque. Il était demandé d’interpréter l’hémogramme retrouvant une anémie, une thrombopénie, une polynucléose neutrophile et une hyperlymphocytose. L’aspect morphologique devait faire évoquer une leucémie lymphoïde chronique.
Dans cet article
- Données quantitatives et qualitatives de l’hémogramme
- Indications d’un hémogramme (rang A)
- Indications d’une demande en urgence (rang A)
- Indications du frottis sanguin et interprétation (rang A)
- Anomalies des différentes lignées et leurs principales causes (OIC-212-06-A)
- Hémogramme chez l’enfant (OIC-212-07 et 08-A)

 Encadrés
Encadrés