Connaître les modes de transmission des différentes hépatites virales et les modalités de leur prévention.
Prescrire et interpréter les examens sérologiques utiles au diagnostic.
Connaître les grands principes du traitement et de la surveillance des hépatites chroniques B et C
Connaître les modalités de prévention.
Identifier les situations d’urgence et planifier leur prise en charge.
Généralités
Histoire naturelle des hépatites virales
Hépatites aiguës
Le bilan de première intention comporte : immunoglobulines (IgM) anti-VHA et anti-VHE, antigène (Ag) HBs et IgM anti-HBc, anticorps (Ac) anti-VHC. Lorsqu’il existe un contexte épidémiologique particulier (exposition sexuelle ou sanguine (usage de drogue ou exposition nosocomiale), voyage en pays de forte endémie, contexte épidémique), des tests de biologie moléculaire (recherche du génome viral par polymerase chain reaction [PCR]) peuvent être réalisés rapidement si les sérologies sont négatives en particulier pour les virus de l’hépatite C (VHC) et de l’hépatite E (VHE) pour lesquels les anticorps peuvent n’apparaître qu’après les manifestations cliniques ou biologiques. Les hépatites virales aiguës peuvent évoluer vers une guérison spontanée sans traitement ou, pour les hépatites B, C et rarement E vers une hépatite chronique. Au stade aigu, il existe de rares formes d’hépatites fulminantes qui entraînent une destruction hépatique massive et rapide et dont l’évolution est le plus souvent fatale en l’absence de transplantation hépatique.
Hépatites chroniques
Même si, dans le cas de l’hépatite A, des formes prolongées ou à rechute ont été décrites, il n’existe pas d’hépatite chronique liée au virus de l’hépatite A (VHA). En revanche, il a été montré que, dans certaines situations d’immunodépression, des infections chroniques par le VHE sont observées et peuvent être responsables d’hépatites chroniques.
Conduite à tenir face à une hépatite aiguë
Rechercher des signes de gravité et surveiller l’évolution
Le taux de prothrombine doit être réalisé de façon systématique et être répété au moins deux fois par semaine tant que la cytolyse est importante. Chez les patients traités par antivitamine K, il doit être remplacé par la mesure du facteur V. Une chute du taux de prothrombine en dessous de 50 % signe une hépatite sévère et justifie une hospitalisation rapide dans un service spécialisé.
La surveillance clinique doit rechercher l’apparition de signes d’encéphalopathie hépatique. L’apparition d’une somnolence, d’une inversion du rythme nycthéméral, d’un astérixis ou de troubles de conscience fait suspecter une hépatite fulminante qui nécessite une hospitalisation en urgence dans un service de réanimation à proximité d’un centre de transplantation hépatique.
Mesures à prendre
Aucun régime alimentaire spécifique n’est nécessaire mais la consommation d’alcool est contre-indiquée.
Des mesures d’hygiène spécifiques ne sont nécessaires que pour les hépatites A et E, en particulier si les malades restent à domicile. Dans cette situation, une recherche de la source de contamination doit être réalisée.
Une enquête familiale doit être systématiquement proposée, en particulier dans le cas des hépatites B, afin de pouvoir proposer une prise en charge précoce ou une vaccination de l’entourage.
L’hépatite B aiguë symptomatique et l’hépatite A sont des maladies à déclaration obligatoire.
Hépatite B
Introduction
Épidémiologie
Modes de transmission
- la transmission verticale est la transmission de la mère à l’enfant lors de l’accouchement, le risque est d’autant plus important que la charge virale maternelle est élevée ;
- la transmission horizontale est la transmission au sein d’un même foyer par des contacts rapprochés, surtout pour les enfants non vaccinés nés de parents infectés par le VHB ;
- les autres modes de contamination sont les rapports sexuels non protégés, l’utilisation de matériel infecté (usagers de drogues, tatouages, piercing…) ou le contact avec du sang ou des dérivés de sang infectés (transfusions sanguines avant les années 1990 en France, chirurgie, hémodialyse…).
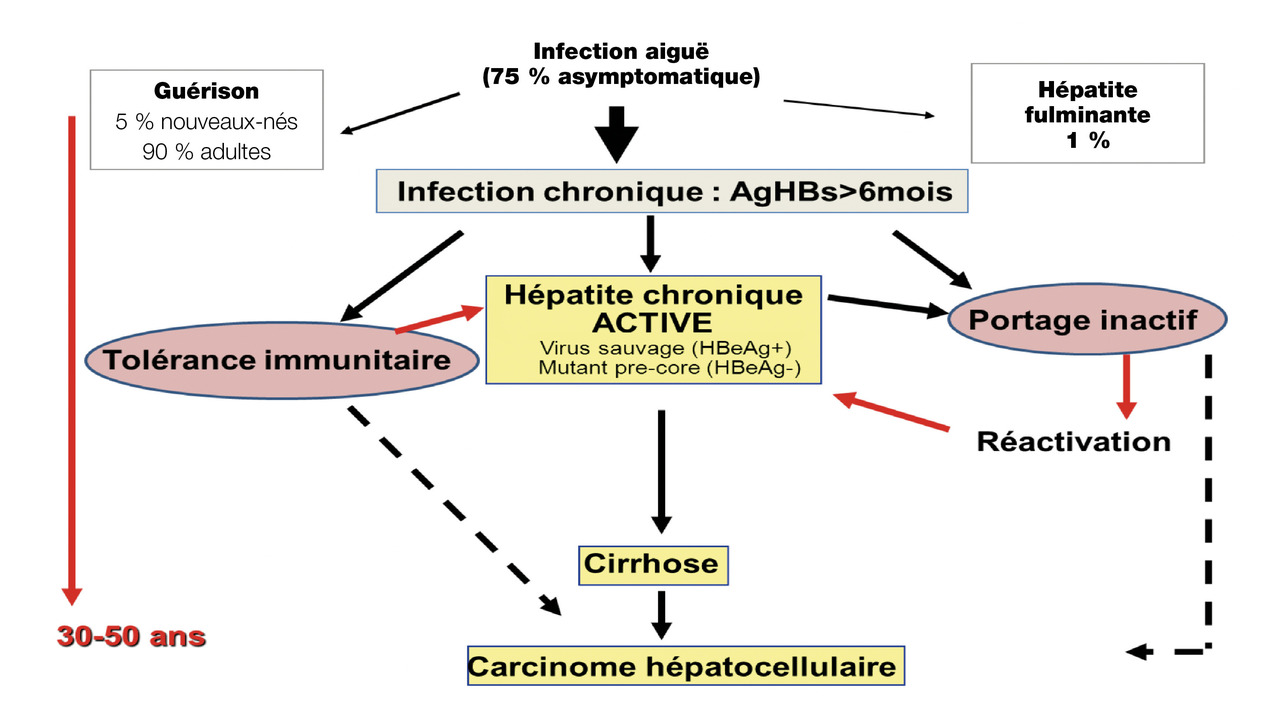
Histoire naturelle de l’infection par le VHB (fig. 1)
Hépatite aiguë
Après une incubation de 1 à 4 mois, elle est souvent asymptomatique, surtout chez l’enfant. Les symptômes cliniques et biologiques sont non spécifiques (v. Généralités). L’hépatite aiguë peut aboutir à la guérison (90-95 % des cas chez l’adulte non immunodéprimé, 10 % chez l’enfant) ou alors à une hépatite chronique. La présence d’IgM anti-HBc est caractéristique d’une infection aiguë.Une co-infection avec le virus de l’hépatite Delta augmente le risque d’hépatite fulminante.
Hépatite chronique
L’infection chronique par le VHB est définie par la persistance de l’Ag HBs au-delà de 6 mois.On distingue 4 phases d’infection chronique (tolérance immune, hépatite B chronique à virus sauvage, hépatite B chronique à mutant pré-C, portage inactif) dont les caractéristiques biologiques sont détaillées dans le
Risques évolutifs
Une surinfection par le virus de l’hépatite Delta aggrave l’hépatite B chronique et augmente le risque de progression vers la cirrhose et le carcinome hépatocellulaire.
Une réactivation virale peut survenir chez des patients au stade portage inactif ou de guérison sérologique en cas d’immunodépression sévère (sida, traitement immunodépresseur, chimiothérapie anticancéreuse) ; un dépistage de l’infection par le VHB est nécessaire dans ces situations et pourra justifier d’un traitement antiviral prophylactique.
Prise en charge d’une hépatite B
Hépatite B aiguë
Les indications de traitement sont rares : elles concernent les patients présentant une hépatite fulminante ou sévère. Les analogues nucléosidique ou nucléotidiques (voir plus loin), de préférence avec une haute barrière de résistance, sont les seules molécules utilisables.Il s’agit d’une maladie à déclaration obligatoire.
Hépatite B chronique
Le bilan initial est décrit dans leL’hépatite B chronique fait partie des affections de longue durée et une demande de prise en charge à 100 % est à réaliser.
Les indications classiques de traitement concernent les patients avec une hépatite chronique active (avec un Ag HBe positif ou négatif). Avant la mise en place d’un traitement, la réalisation d’une biopsie de foie est recommandée.
La biopsie se réalise chez tous les patients présentant une charge virale > 2 000 UI/mL et/ou une cytolyse (sauf dans la tolérance immune). Si la biopsie de foie retrouve un score d’activité (A) et/ou de fibrose (F) ≥ 2 selon le score Metavir, un traitement est indiqué.
Les traitements approuvés sont l’interféron pégylé (Peg-IFN), les analogues nucléosidiques (entécavir, telbivudine et lamivudine) et les analogues nucléotidiques (adéfovir, ténofovir et sa prodrogue, le ténofovir alafénamide [TAF]).
L’interféron est un traitement immunomodulateur reposant sur 1 injection sous-cutanée hebdomadaire pendant 12 mois. Les inconvénients du traitement par Peg-IFN sont les effets secondaires nombreux et son efficacité modérée. Il permet d’obtenir une séroconversion HBe pour 30 % des patients positifs pour l’Ag HBe. Son efficacité sur la charge virale et la cytolyse hépatique est limitée.2
Les analogues nucléos(t)idiques (NUC), administrés par voie orale, permettent d’obtenir une charge virale indétectable (virosuppression) dans plus 95 % des cas. Leur inconvénient est une durée de traitement indéterminée, le plus souvent « à vie » et le risque de sélection de souche virale résistante aux NUC. Les molécules indiquées en première intention du fait de leur barrière génétique de résistance élevée sont l’entécavir et le ténofovir.2 La telbivudine, la lamivudine et l’adéfovir ne sont quasiment plus utilisés en France en raison d’une moins bonne efficacité liée à un taux élevé de résistance. Le TAF est une prodrogue du ténofovir développée pour diminuer les concentrations plasmatiques de ténofovir afin d’améliorer la toxicité rénale et osseuse observées avec le ténofovir disoproxil fumarate. Malgré une efficacité comparable au ténofovir et une moindre toxicité rénale et osseuse, le TAF n’est actuellement pas remboursé en France dans l’indication du VHB. Une autorisation temporaire d’utilisation (ATU) est possible seulement dans les co-infections par le virus de l’immunodéficience humaine (VIH) et le VHB ou dans la mono-infection par le VIH, l’amélioration du service médical rendu par rapport au ténofovir n’ayant pas été jugé suffisant par la Haute Autorité de santé (HAS).
Pour le traitement de la co-infection VHB-VHD, le seul traitement actuellement sur le marché et ayant démontré une efficacité est le Peg-IFN. Les NUC seuls ou en combinaison avec le Peg-IFN n’apportent pas de bénéfice thérapeutique dans cette situation. Depuis fin 2018, le Myrcludex B est disponible en ATU en monothérapie ou en combinaison avec l’interféron pégylé. Il s’agit d’un inhibiteur d’entrée qui empêche le VHB et le VHD d’entrer dans l’hépatocyte et qui a démontré des résultats encourageants dans les études de phase 2 concernant la réplication du VHD. Les études de phase 3 sont en cours.
Situations particulières
Pour l’hépatite B certaines situations nécessitent la mise en place d’un traitement quels que soient le type d’hépatite chronique et l’importance de la charge virale : les patients cirrhotiques et les patients immunodéprimés doivent bénéficier d’un traitement par NUC pour prévenir le risque de progression de l’hépatopathie et de réactivation virale, respectivement.2Surveillance
En cas de diagnostic d’une hépatite B, un dépistage des maladies avec le même mode de transmission doit être réalisé (VIH, VHD, VHC…). Le patient doit être informé de la nécessité d’éviter les facteurs hépatotoxiques, notamment l’alcool. L’hépatite B chronique fait partie des affections longue durée (ALD) et justifie une prise en charge à 100 %.
Prévention de la transmission du VHB
Vaccination
Le vaccin contre l’hépatite B est d’autant plus efficace (95 %) qu’il est réalisé tôt dans la vie. Le schéma classique chez l’adulte comprend 2 injections à 1 mois d’intervalle et un rappel à 6 mois. Selon les recommandations de la HAS 2014, la vaccination contre le VHB est recommandée pour tous les nourrissons et enfants de moins de 16 ans. Les populations à risque (vie en collectivité, professionnels de santé, patients dialysés, pathologies hépatiques chroniques…) doivent être vaccinées.Prévention de la transmission materno-fœtale
La prévention de la transmission materno-fœtale repose sur le dépistage de l’Ag HBs au premier trimestre de la grossesse. Chez des enfants de porteurs chroniques l’immunoprophylaxie par injection d’immunoglobulines anti-HBs au nouveau-né et sa vaccination dès la naissance sont le standard en cas de charge virale faible de la mère (< 200 000 UI/mL). Les mères ayant une charge virale élevée (> 200 000 UI/mL) lors du premier trimestre de la grossesse doivent en plus recevoir un traitement antiviral (lamivudine, telbivudine et ténofovir autorisés) pour diminuer le taux d’échappement à la sérovaccination chez le nouveau-né (entre 9 et 15 % selon les études). En pratique, le ténofovir est utilisé de préférence pour son profil de haute barrière de résistance, sa bonne tolérance et les données cliniques disponibles chez les femmes enceintes.Hépatite C
Introduction
Dans le monde, on estime qu’environ 1-3 % de la population serait porteuse du VHC. En France, la prévalence était estimée à 0,84 %, soit 370 000 personnes porteuses d’Ac anti-VHC dont deux tiers sont virémiques. Seulement la moitié des patients connaît son statut virologique.
L’hépatite C est l’une des causes principales de cirrhose, de carcinome hépatocellulaire et de transplantation hépatique. L’évolution de la maladie est souvent silencieuse et le dépistage souvent tardif par rapport au moment de la contamination.
Depuis 2014, les nouveaux antiviraux directs permettant de traiter facilement l’hépatite C et de guérir la quasi-totalité des personnes ont été mis en place progressivement. L’objectif d’éradication du virus de l’hépatite C en France semble réalisable mais nécessite une amélioration et une optimisation des stratégies de dépistage et des parcours de prise en charge.
Mode de contamination
La transmission materno-fœtale lors de la grossesse et de l’accouchement est estimée entre 3 et 4 %. Ce risque est plus élevé en cas de co-infection VHC/VIH.
Diagnostic
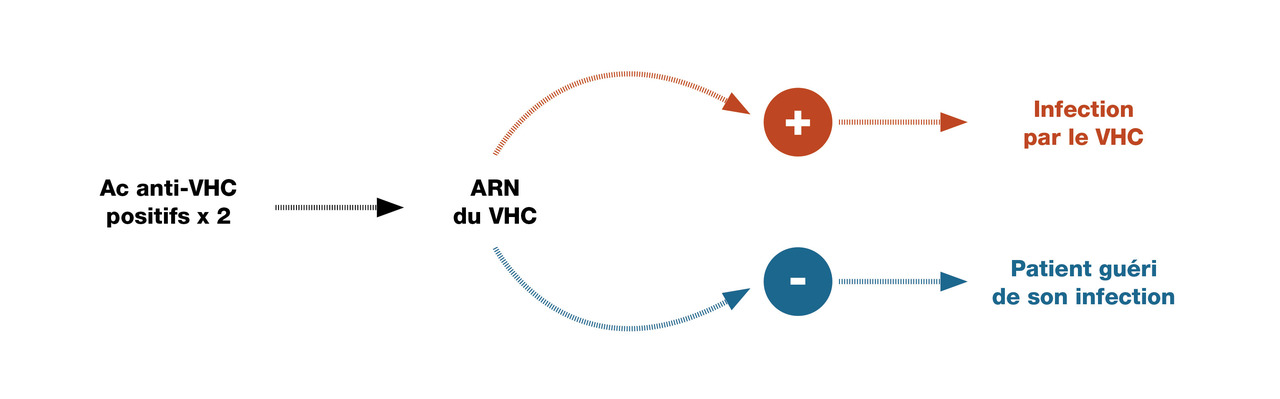
Le marqueur le plus précoce de l’infection aiguë est l’ARN du VHC qui devient positif dès la première semaine après la contamination. Les Ac anti-VHC peuvent apparaître plus tardivement, mais sont souvent positifs dans les premières semaines après contamination.
Le dépistage est conseillé en cas de notion de :
- transfusion de tout produit sanguin, dialyse ou soin hospitalier majeur (chirurgie lourde) avant 1992 ;
- toxicomanie active ou ancienne ;
- tatouage ou acupuncture ;
- incarcération ;
- sérologie VIH ou VHB positive ;
- porteur d’hépatite C dans l’entourage ;
- cytolyse chronique, d’asthénie inexpliquée.
Histoire naturelle et clinique
Hépatite C aiguë
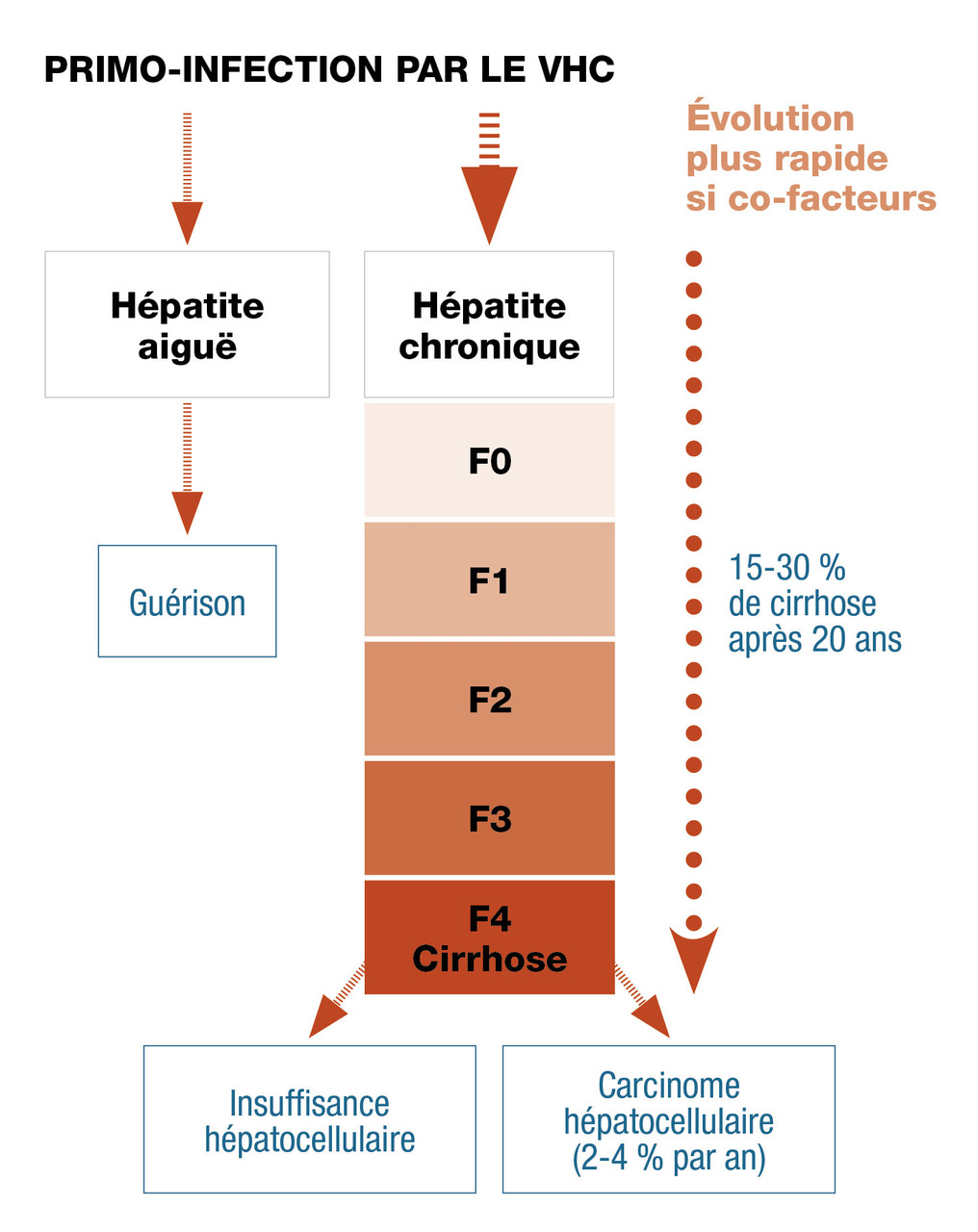
Dans 55-85 % des cas l’hépatite C devient chronique après la contamination (Hépatite C chronique
L’hépatite C est considérée chronique si la virémie persiste au-delà de 6 mois d’évolution. Elle est souvent asymptomatique ou associée à des symptômes aspécifiques (asthénie, troubles thymiques, myalgies, arthralgies chroniques, prurit). Les transaminases peuvent être normales, ou bien modérément élevées et, dans ce cas, souvent fluctuantes. Des complications extra-hépatiques, liées à la présence d’une cryoglobulinémie, sont possibles mais rares (glomérulonéphrite, polyneuropathie périphérique, vascularite, lymphome viro-induit) et peuvent représenter les premiers symptômes cliniques de l’infection.Au cours des hépatites C chroniques, l’évolution de la fibrose hépatique est progressive et souvent linéaire dans le temps. Le risque de cirrhose est estimé entre 15 et 30 % après 20 ans d’évolution et peut être aggravé par des cofacteurs comme la consommation d’alcool, de cannabis, et la co-infection avec le VIH.
Bilan initial
Évaluation de la sévérité de l’hépatopathie
L’évaluation du degré de fibrose est essentielle pour l’évaluation de la sévérité de la maladie et l’indication de traitement. Le score le plus utilisé en France est le score Metavir qui se base sur les stades histologiques (F0 : pas de fibrose, F1 : fibrose minime, F2 : fibrose modérée, F3 : fibrose extensive, F4 : fibrose sévère [L’évaluation de la sévérité de l’hépatopathie nécessite la réalisation d’une échographie abdominale pour rechercher des signes de dysmorphie hépatique ou d’hypertension portale et dépister un carcinome hépatocellulaire.
Bilan complémentaire
Il comprendra :- le génotype viral, car il peut influencer a durée du traitement et le choix des antiviraux ;
- la recherche de manifestations extra-hépatiques liées à une cryoglobulinémie ;
- la recherche de cofacteurs de fibrose (consommation d’alcool, diabète, co-infection par le VIH et/ou le VHB) ;
- la liste des traitements en cours pour éviter des interactions médicamenteuses avec les antiviraux.
Traitement
Hépatite C aiguë
Les recommandations ont récemment changé et toutes les hépatites C aiguës chez des personnes à haut risque de transmission (usager de drogue, HSH) nécessitent un traitement antiviral à la phase aiguë. Ce traitement suit le même schéma qu’un traitement à la phase chronique.Hépatite C chronique
Le traitement antiviral est maintenant indiqué pour toute personne infectée par le virus de l’hépatite C quel que soit le stade de la maladie. La prescription du traitement a été élargie aux médecins généralistes en raison de sa simplicité, sa bonne tolérance et sa haute efficacité dans le but d’éradiquer l’hépatite C en France dans les 5 prochaines années.La tolérance des traitements est excellente. L’observance du traitement sans modification de sa posologie est essentielle à son succès, ce qui doit être précisé au patient. Aucun suivi clinique ou biologique n’est nécessaire en l’absence de cirrhose décompensée. La guérison est à confirmer avec un dosage de l’ARN du VHC à 12 semaines après l’arrêt du traitement antiviral.
Pour faciliter la prescription aux généralistes l’AFEF a mis en ligne une présentation détaillée intitulée « Recommandations pour l’élimination de l’infection par le VHC en France » : https://afef.asso.fr/recommandations/recommandations-afef/
Mesures générales :
- il est important d’informer les patients et leurs proches sur les mesures à prendre pour éviter la transmission ;
- l’hépatite C chronique fait partie des affections de longue durée et une demande de prise en charge à 100 % est à réaliser ;
- le dépistage des cofacteurs de fibrose (alcool, certains médicaments, syndrome métabolique, VIH) et leur correction peut éviter la progression de la fibrose ;
- il est recommandé de vacciner les patients contre l’hépatite A et l’hépatite B.
Surveillance
Prévention
La transmission par les proches et notamment dans le couple est rare, mais il faut respecter les consignes suivantes :
- ne jamais partager les objets coupants (rasoir, coupe ongle) et brosses à dent ;
- éviter le contact direct avec le sang (portage de gants en cas de soins) ;
- éviter les rapports sexuels traumatisants et port de préservatif conseillé en cas de rapports pendant les règles ou en cas de plaie génitale.
Hépatite A
Caractéristiques virologiques
Le VHA est connu pour sa résistance aux agents physiques et chimiques qui lui confère une survie prolongée dans le milieu extérieur. Il résiste relativement à la chaleur et reste infectieux de plusieurs jours à plusieurs mois dans l’environnement. La virémie est faible et brève. Des particules virales sont éliminées dans les selles pendant une dizaine de jours.
Épidémiologie
Histoire naturelle
Manifestations cliniques
Bilan biologique
Évolution
Les formes plus rares sont :
- les formes prolongées (15 % des cas) sur plusieurs semaines ou mois, mais pas d’évolution vers la chronicité ;
- les formes à rechute (1-2 %) après guérison d’apparence complète. La rechute est unique le plus souvent, apparaissant moins d’un mois après la guérison apparente ;
- les formes fulminantes (< 1 %). L’atteinte est plus sévère chez le patient de plus de 60 ans et/ou présentant une maladie chronique du foie.
Diagnostique sérologique
Les IgG apparaissent rapidement après les IgM et persistent de nombreuses années témoignant du contact viral. L’immunité est solide et durable.
Prise en charge
Des mesures d’hygiène renforcées (avec isolement en cas d’hospitalisation) sont à mettre en place au cours des 8 semaines suivant les symptômes. L’arrêt de travail ou l’éviction scolaire dure 10 jours après les symptômes. Une vaccination de l’entourage est mise en place sans sérologie préalable dans un délai de 14 jours.
Prévention
La vaccination est recommandée pour les personnes exposées professionnellement (collectivités, traitement des eaux usées, restauration collective), les voyageurs en pays d’endémie, les patients porteurs d’une maladie chronique du foie, les homosexuels masculins, les personnes vivant en institution.
Deux vaccins entiers atténués sont disponibles (Havrix et Avaxim). Le schéma comporte une dose avec rappel 6 à 12 mois plus tard. Il est possible de faire un rappel 20 ans plus tard (en cas de perte des anticorps). Le taux de séroconversion est excellent (> 98 %).
Hépatite E
Caractéristiques virologiques
Épidémiologie
Histoire naturelle
Le patient immunodéprimé a des symptômes moins marqués mais peut présenter un passage à la chronicité.
Manifestations cliniques
Des manifestations extra-hépatiques sont possibles même si rares. Il s’agit d’atteintes neurologiques (atteinte centrale ou périphériques chez 5 % des patients), hématologiques (thrombopénie, anémie hémolytiques) et pancréatiques (pancréatite aiguë).
Bilan biologique
Évolution
Chez l’immunodéprimé, l’infection peut être chronique avec une persistance de la cytolyse et du VHE dans le sang ou les selles pendant plus de 6 mois.
Traitement
Aucun traitement n’est nécessaire chez les patients immunocompétents, l’évolution étant spontanément favorable.
Chez les patients immunodéprimés (transplantation rénale ou hépatique, par exemple) ou présentant une forme grave (sur hépatopathie chronique), un traitement par ribavirine à la dose de 800 mg par jour permet une guérison dans 66 % des cas à 3 mois, et une prolongation du traitement en cas d’échec permet dans la plupart des cas une clairance virale.
Prévention
POINTS FORTS À RETENIR
Elles sont responsables d’hépatite aiguë à transmission oro-fécale.
La prévention passe par la vaccination.
Leur transmission est verticale, sexuelle et parentérale.
Elles sont responsables d’hépatites aiguës et d’infections chroniques.
L’histoire naturelle des hépatites B chroniques est marquée par différentes phases, imposant une surveillance du patient au long cours.
Le principal risque est le développement d’une cirrhose et d’un carcinome hépatocellulaire.
La surinfection par le virus de l’hépatite Delta aggrave l’évolution de la maladie.
Il n’y a pas d’élimination virale complète, expliquant les cas de réactivation virale en cas d’immunosuppression.
Les traitements antiviraux prolongés permettent d’obtenir une virosuppression et une amélioration de l’histologie hépatique.
La prévention passe par la vaccination.
Leur transmission est principalement parentérale.
Elles sont responsables d’hépatites aiguës et d’infections chroniques.
L’histoire naturelle des hépatites C chroniques est généralement progressive avec un risque de développement d’une cirrhose 20-30 ans après la contamination, avec un risque ultérieur de carcinome hépatocellulaire.
La maladie peut se manifester par des symptômes extra-hépatiques (cryoglobulinémie).
Les traitements antiviraux permettent d’obtenir une élimination virale complète (guérison virologique) et une amélioration de l’histologie hépatique.
Il n’y a pas de vaccin pour la prévention qui passe donc par des mesures d’hygiène.
Elles sont responsables d’hépatite aiguë à transmission oro-fécale.
Des formes chroniques sont connues chez les patients immunodéprimés.
Il n’y a pas de vaccin disponible dans les pays occidentaux (vaccin disponible uniquement en Chine).

 Encadrés
Encadrés