L’hirsutisme correspond à une pilosité excessive développée dans des territoires masculins ou des zones androgéno-dépendantes comme le visage, le thorax, le dos, la ligne blanche, les creux inguinaux, les faces internes et postérieures des cuisses. Il est lié soit à une hypersécrétion d’androgènes provenant de l’ovaire ou de la surrénale, soit à une sensibilité cutanée accrue de la peau à des taux circulants normaux d’androgènes.
S’orienter par la clinique
L’ancienneté de l’hirsutisme, sa date d’apparition par rapport à la puberté et la présence de troubles du cycle sont des éléments à rechercher à l’interrogatoire. Une installation péripubertaire associée à des troubles primaires du cycle est en faveur d’un syndrome des ovaires polykystiques (SOPK) ou d’un déficit enzymatique surrénalien ; en revanche, un hirsutisme récent et évolutif doit alerter sur l’existence d’une pathologie tumorale.
Des signes en faveur d’un syndrome de Cushing (obésité, répartition facio-tronculaire de la masse grasse, bouffissures du visage, peau fine et fragile, hypertension artérielle, labilité émotionnelle, ecchymoses…) sont également à rechercher.
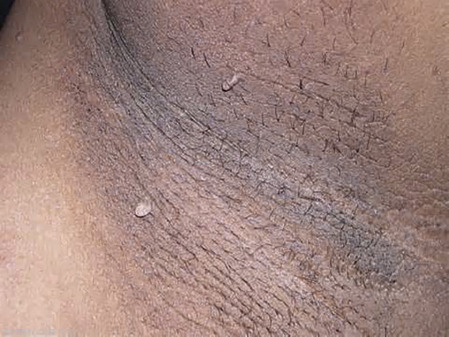
La présence d’un acanthosis nigricans (fig. 1), témoignant d’une résistance à l’insuline, oriente vers un SOPK.
La sévérité de l’hirsutisme est évaluée par le score modifié de Ferriman et Gallwey où, à chacune des neuf régions androgéno-sensibles, est assignée une cotation de 0 à 4 (fig. 2). Un score supérieur à 6 définit arbitrairement l’hirsutisme, mais son évaluation reste subjective.
Quels dosages hormonaux réaliser ?
La réalisation d’une évaluation hormonale est toujours indispensable.
En cas de menstruations, les examens doivent être pratiqués en début de cycle. Chez une femme en aménorrhée, les examens peuvent se faire à tout moment ou après une hémorragie de privation induite par un progestatif.
- Le dosage de la testostérone totale est recommandé en première intention, associé à celui de la sex hormone-binding globulin (SHBG), permettant de calculer un index de testostérone libre ou biodisponible.
- Le dosage de la 17-hydroxyprogestérone (17-OHP), en début de phase folliculaire, le matin, à distance de la prise de corticoïdes de base et après test au Synacthène permet le dépistage de l’hyperplasie congénitale des surrénales par déficit en 21-hydroxylase.
- Le dosage de la delta-4-androstènedione plasmatique est peu utile en pratique.
- Le dosage de la déhydroépiandrostérone (SDHEA) peut être utile en cas de suspicion clinique de syndrome de Cushing.
- Les dosages de l’hormone lutéinisante (LH), de l’hormone de stimulation folliculaire (FSH), de l’estradiol, de la prolactine et de la thyréostimuline (TSH) complètent le bilan. Ces dosages doivent être réalisés en l’absence de contraception hormonale ; celle-ci doit être arrêtée depuis au moins trois mois et remplacée par une contraception alternative non hormonale.
Des causes dominées par le SOPK
Le SOPK est responsable de l’hirsutisme dans 80 à 90 % des cas. L’hirsutisme idiopathique est un diagnostic d’élimination et les autres causes, certes rares, doivent donc être connues.
Syndrome des ovaires polykystiques
Le SOPK est une pathologie courante affectant entre 5 et 15 % des femmes ; il constitue la principale cause de troubles des règles et d’infertilité de la femme.
Son diagnostic repose sur les critères de Rotterdam :1
- existence d’une anomalie d’ovulation (oligo- ou anovulation) ;
- existence d’une hyperandrogénie clinique et/ou biologique ;
- présence d’ovaires polykystiques à l’échographie (par voie endovaginale, avec une sonde de plus de 8 MHz, présence d’au moins 20 follicules de 2 à 9 mm au sein de chaque ovaire et/ou augmentation du volume ovarien supérieure à 10 mL).
La confirmation de deux critères sur trois suffit à établir le diagnostic de SOPK, après exclusion d’autres affections. Cette pathologie survient fréquemment dans un contexte de surpoids ou d’obésité associées à une insulinorésistance : le dépistage du diabète de type 2 doit être systématique chez ces femmes.
Hyperplasie congénitale surrénalienne par déficit en 21-hydroxylase
Responsable de l’hirsutisme dans 2 à 4 % des cas, elle peut se manifester par une pubarche précoce, ou par un hirsutisme et/ou des troubles des règles – il s’agit alors de la forme dite « tardive » ou « non classique ».
Le diagnostic est suspecté sur le dosage de la 17-OHP avant et après injection de Synacthène, puis confirmé par l’analyse du gène CYP21A2.2
Tumeurs virilisantes de l’ovaire et de la corticosurrénale
Elles sont en cause dans 0,2 % des cas d’hirsutisme. Les symptômes sont d’apparition récente et soudaine, à distance de la puberté. Une concentration de testostérone deux fois supérieure à la normale fait suspecter le diagnostic de tumeur.
Syndrome de Cushing
Le tableau d’hypercortisolisme est alors souvent au premier plan.
Hirsutisme idiopathique
Ce diagnostic d’élimination représente 4 à 6 % des situations ; il se définit par une fonction ovarienne strictement normale et l’absence d’hyperandrogénie biologique.
Sur le plan clinique, l’hirsutisme est isolé et ancien, préexistant à la puberté mais souvent aggravé par celle-ci. Les antécédents familiaux sont fréquents.
Prise en charge : association de traitements généraux et locaux
Le traitement de l’hirsutisme repose sur l’utilisation de plusieurs types de médicaments visant à bloquer la production des androgènes ou leurs actions périphériques, associés à des traitements locaux. Ce traitement fait actuellement l’objet de recommandations publiées par la Société française d’endocrinologie.3
Hirsutisme modéré chez la femme non ménopausée
La contraception œstroprogestative (COP) est le traitement de première intention. À efficacité similaire, il est préférable de choisir une COP ayant le plus faible risque thrombo-embolique veineux (molécules de 2e génération).
En l’absence d’efficacité jugée suffisante, la Société française d’endocrinologie recommande d’associer la spironolactone à la COP (prescription actuellement hors autorisation de mise sur le marché [AMM]). La dose initiale habituellement utilisée est de 100 mg par jour, pouvant être augmentée jusqu’à 300 mg par jour, avec surveillance de l’ionogramme et de la créatininémie.
La spironolactone seule, sous couvert d’une contraception efficace, est le traitement de troisième intention en cas d’effets indésirables, de contre-indication et/ou d’absence d’efficacité de la COP.
Hirsutisme sévère invalidant de la femme non ménopausée
L’acétate de cyprotérone, associé à un estrogène, est le traitement de première intention. Du fait de l’augmentation du risque de méningiome associé à ce traitement, particulièrement s’il est prescrit à forte dose et pendant une longue durée, l’information et la surveillance ont été renforcées : deux documents sont à remettre aux patientes.4 La tolérance et l’efficacité du traitement doivent être évaluées à court terme, puis tous les ans par le prescripteur. La durée de traitement doit être la plus courte possible et à la posologie minimale efficace.
La spironolactone – sous couvert d’une contraception efficace – est le traitement de deuxième intention en cas d’effets indésirables, de contre-indication, de refus de la patiente ou d’absence d’efficacité de l’acétate de cyprotérone.
Traitements locaux en complément
La croissance du poil est un phénomène cyclique lent, nécessitant d’évaluer l’efficacité des traitements sur plusieurs mois et d’utiliser en parallèle des thérapeutiques symptomatiques.
L’épilation électrique ou laser est efficace, surtout sur peau claire avec des poils foncés. Son utilisation est limitée par son coût et l’absence de remboursement par la Sécurité sociale.
L’éflornithine (Vaniqa) est un topique ralentissant la croissance du poil. Ce traitement n’enlève pas les poils existants mais ralentit et prévient leur repousse. L’effet est observable après deux mois d’utilisation mais est réversible à l’arrêt du traitement. Son intérêt est également limité par son coût et l’absence de remboursement par la Sécurité sociale.
Teede HJ, Misso ML, Costello MF, et al. Recommendations from the international evidence-based guideline for the assessment and management of polycystic ovary syndrome. Hum Reprod 2018;33(9):1602-18.
Young J, Tardy V, de la Perrière AB, et al. Detection and management of late-onset 21-hydroxylase deficiency in women with hyperandrogenism. Ann Endocrinol (Paris) 2010;71(1):14-8.
Société française d’endocrinologie. Nouvelles recommandations pour le traitement des hyperandrogénies. Mai 2020. Disponible sur : http://bit.ly/3O70ZMk
ANSM. Androcur et ses génériques (acétate de cyprotérone, comprimés dosés à 50 ou 100 mg). Information pour les patients. Mai 2019. Disponible sur : http://bit.ly/3tuaoEs ; l’attestation d’information à remplir et signer par le médecin et le patient est disponible sur : http://bit.ly/3X2yrrG