Les accidents vasculaires cérébraux (AVC) représentent la deuxième cause de décès dans le monde, et la principale cause de handicap acquis chez l’adulte. En France, un AVC survient toutes les quatre minutes, soit environ 150 000 nouveaux cas par an. L’hypertension artérielle (HTA) est le principal facteur de risque modifiable des AVC, qu’ils soient ischémiques ou hémorragiques ; en effet, il existe une relation continue entre le niveau de pression artérielle et le risque d’AVC, sans véritable seuil : il a été estimé que chaque augmentation de pression artérielle systolique de 20 mmHg (ou de 10 mmHg de pression diastolique) double le risque de survenue d’AVC.1 La part de risque d’AVC attribuable à l’HTA est de presque 50 %.2
Si l’AVC est la complication neurologique la plus bruyante de l’HTA, il existe également un retentissement cérébral plus « chronique », que l’imagerie permet de visualiser : la maladie des petites artères cérébrales. Cette atteinte est responsable de troubles cognitifs et fonctionnels (troubles de la marche et de l’équilibre) importants.
HTA, principal facteur de risque d’Accident vasculaire cérébral
Manifestations ischémiques…
L’athérosclérose, les causes cardio-emboliques et la maladie des petites artères cérébrales sont responsables d’environ trois quarts des AVC ischémiques. Si l’HTA est un facteur de risque connu d’athérosclérose et de cardiopathie emboligène, elle est aussi directement responsable de la maladie des petites artères cérébrales. Par ailleurs, un antécédent d’HTA et la présence d’une pression artérielle élevée à la phase aiguë sont des facteurs de mauvais pronostic de l’AVC.3
… mais aussi hémorragiques
Les hémorragies cérébrales représentent 15 % des AVC dans les pays occidentaux et jusqu’à 50 % dans les pays en développement.4 La maladie des petites artères cérébrales liée à l’HTA est responsable à elle seule d’environ deux tiers des AVC hémorragiques.
Maladie des petites artères cérébrales
La maladie des petites artères cérébrales, très liée à l’HTA, est une artériosclérose des petits vaisseaux cérébraux (artérioles, capillaires et veinules). Pour résister à l’élévation de pression artérielle, les petits vaisseaux cérébraux perdent les cellules musculaires lisses de leur paroi, qui se durcit et s’épaissit jusqu’à entraîner l’occlusion du vaisseau. La densité en artérioles et en capillaires dans le tissu cérébral diminue, les échanges en oxygène et en glucose sont altérés, causant une souffrance du parenchyme cérébral.5 Ce sont les petites artères cérébrales perforantes vascularisant les régions profondes du cerveau qui sont particulièrement affectées.
Cette maladie des petites artères cérébrales est responsable d’AVC ischémiques « lacunaires », d’hémorragies cérébrales mais également d’une atteinte cérébrale plus « chronique ». Cette atteinte progressive du parenchyme cérébral se traduit par des troubles de la marche, de l’équilibre et par un déclin cognitif vasculaire avec une altération préférentielle des fonctions exécutives (attention, raisonnement, planification). Ces troubles cognitifs vasculaires peuvent aggraver ou déclencher des troubles cognitifs en lien avec une maladie dégénérative, comme la maladie d’Alzheimer.4
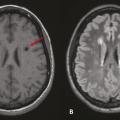
L’IRM permet de visualiser les stigmates de la maladie des petites artères cérébrales : anomalies de la substance blanche d’origine vasculaire présumée, lacunes et microsaignements cérébraux (microbleeds).
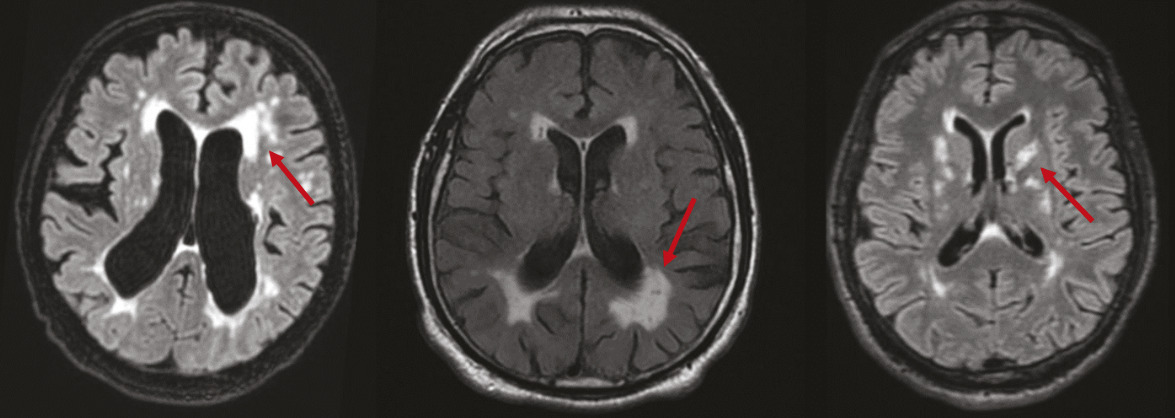
Anomalies de la substance blanche d’origine vasculaire présumée
Histologiquement, les anomalies de la substance blanche correspondent à un mélange hétérogène de démyélinisation, de micro-infarctus et de perte axonale. Présentes dans les régions sous-corticales et périventriculaires, elles sont visibles à l’IRM sous la forme d’hypersignaux en séquence T2 et iso- ou hyposignal en séquence T1 (
Des études épidémiologiques ont montré que la présence de ces anomalies de la substance blanche est associée à un risque trois fois plus important d’AVC et deux fois plus important de démence, mais aussi à un risque accru de troubles de l’équilibre et de troubles urinaires chez la personne âgée.4,6
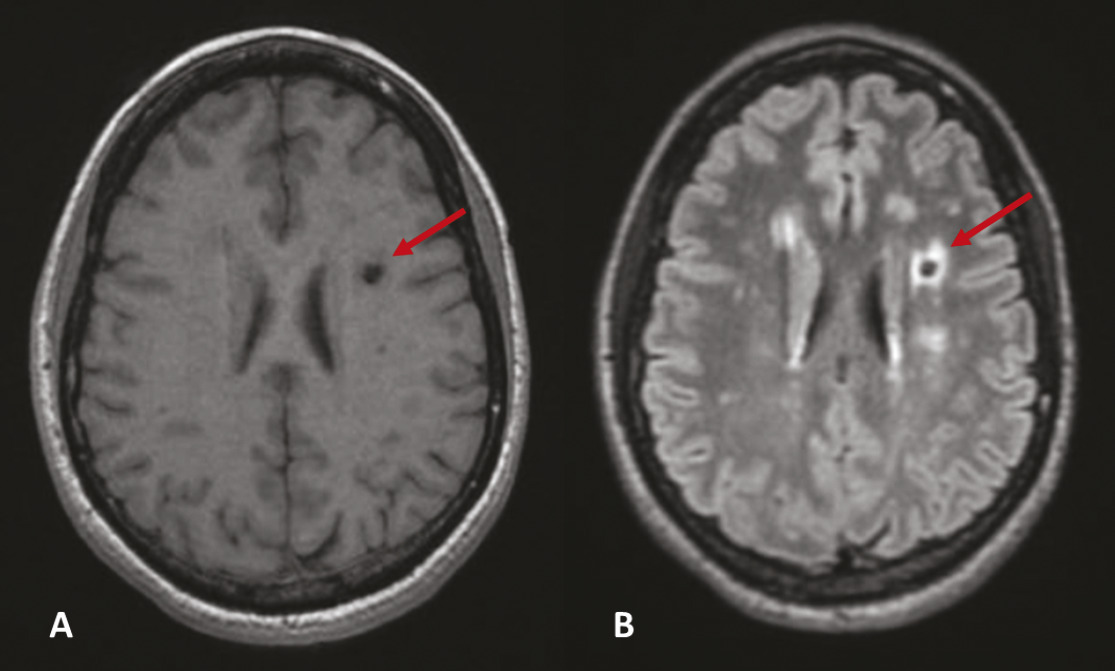
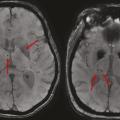
Lacunes, stigmates de lésions anciennes
Les lacunes sont des « trous » ovoïdes sous-corticaux, de 3 à 15 mm de diamètre, correspondant à une ancienne petite lésion ischémique ou hémorragique profonde dans le territoire d’une artère perforante, remplie de liquide céphalorachidien. La traduction à l’IRM cérébrale est une lésion en hyposignal T1 et T2, pouvant être entourée d’une couronne hyperintense en T2 FLAIR (
La présence de lacunes double le risque d’AVC et de démence. Elles sont également associées au risque de survenue de troubles de la marche et de l’équilibre.
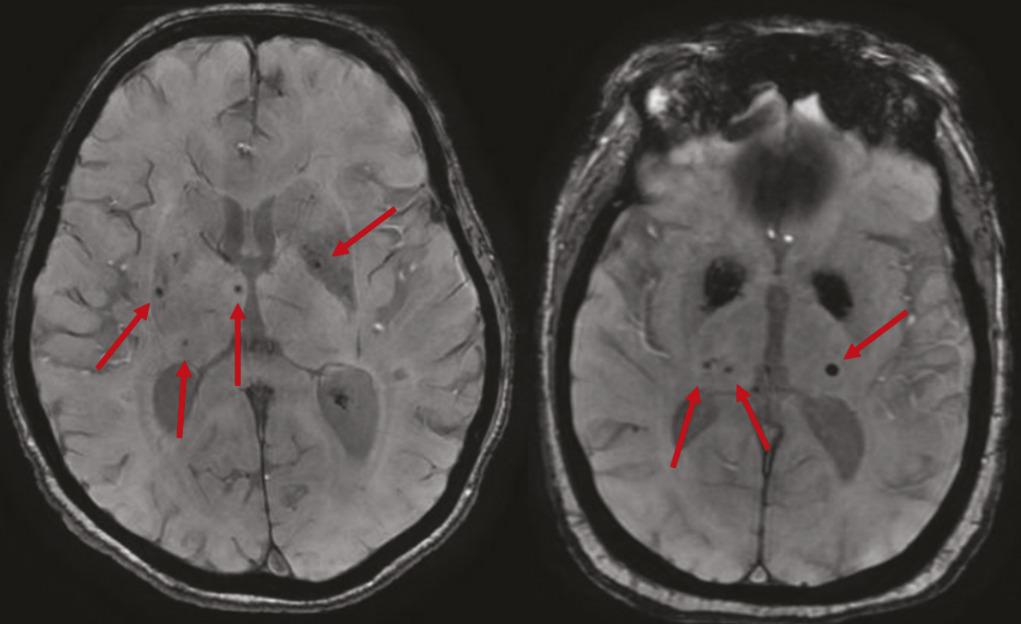
Microbleeds, en hausse avec l’âge
Les microbleeds sont des effractions de sang dans le parenchyme cérébral. À l’IRM, ce sont de petites lésions rondes de 2 à 5 mm, homogènes et très hypo-intenses en séquence de susceptibilité magnétique comme la séquence T2 écho de gradient (T2*) [
Leur prévalence augmente avec l’âge. Ils sont associés à un risque hémorragique mais également ischémique.
Ils sont à différencier des microbleeds lobaires périphériques, plutôt évoqués lors d’une angiopathie amyloïde cérébrale non liée à l’hypertension artérielle.
Objectif PA inférieur à 130/80 mmHg pour tous ?
Comme en prévention primaire, il existe une relation linéaire entre l’abaissement de la pression artérielle et la diminution du risque de récidive d’AVC.7 L’intérêt d’abaisser la pression artérielle en prévention secondaire des AVC a été montré par plusieurs essais cliniques randomisés. Ainsi, l’objectif désormais recommandé par l’American Heart Association et l’American Stroke Association est une pression artérielle inférieure à 130/80 mmHg chez la plupart des patients hypertendus après un AVC, pour réduire le risque de récidive d’AVC ou d’événement vasculaire.8
Les inhibiteurs de l’enzyme de conversion (IEC), les antagonistes du récepteur de l’angiotensine 2 (ARA2) et les diurétiques thiazidiques sont indiqués en première intention, mais le traitement doit être adapté aux comorbidités et aux préférences du patient pour une meilleure adhésion et davantage d’efficacité.8
La question non résolue est celle de l’existence d’un seuil de pression artérielle en deçà duquel il ne convient pas d’aller. En effet, certains patients avec d’autres comorbidités vasculaires associées pourraient moins bien tolérer cette diminution. La problématique est relativement similaire chez les patients ayant une maladie des petites artères cérébrales, où l’intérêt d’obtenir des chiffres bas de pression artérielle est discuté.9
Que dire aux patients ?
• L’HTA retentit sur plusieurs organes, et le cerveau en est une cible importante.
• Le bon contrôle tensionnel est primordial pour limiter le risque d’AVC mais aussi pour réduire le risque de survenue de troubles de la mémoire, de troubles de la marche ou de démence en vieillissant.
• Il existe de nombreux traitements antihypertenseurs, avec la possibilité de trouver un traitement adapté et bien toléré sans effet indésirable.
• La meilleure surveillance est l’automesure à domicile, avec des appareils simples.
• Un document « Hypertension artérielle et AVC », édité par la World Stroke Organization, est consultable sur le lien suivant : https://bit.ly/3U3RYG9
1. Lewington S, Clarke R, Qizilbash N, et al. Age-specific relevance of usual blood pressure to vascular mortality: a meta-analysis of individual data for one million adults in 61 prospective studies. Lancet 2002;360(9349):1903‑13.
2. O’Donnell MJ, Chin SL, Rangarajan S, et al. Global and regional effects of potentially modifiable risk factors associated with acute stroke in 32 countries (INTERSTROKE): a case-control study. Lancet 2016;388(10046):761‑75.
3. Cipolla MJ, Liebeskind DS, Chan SL. The importance of comorbidities in ischemic stroke: Impact of hypertension on the cerebral circulation. J Cereb Blood Flow Metab 2018;38(12):2129‑49.
4. Kelly DM, Rothwell PM. Blood pressure and the brain: the neurology of hypertension. Pract Neurol 2020;20(2):100‑8.
5. Wardlaw JM, Smith EE, Biessels GJ, et al. Neuroimaging standards for research into small vessel disease and its contribution to ageing and neurodegeneration. Lancet Neurol 2013;12(8):822‑38.
6. Meissner A. Hypertension and the Brain: A Risk Factor for More Than Heart Disease. Cerebrovasc Dis 2016;42(3‑4):255‑62.
7. Rahimi K, Bidel Z, Nazarzadeh M, et al. Pharmacological blood pressure lowering for primary and secondary prevention of cardiovascular disease across different levels of blood pressure: an individual participant-level data meta-analysis. Lancet 2021;397(10285):1625‑36.
8. Kleindorfer DO, Towfighi A, Chaturvedi S, et al. 2021 Guideline for the Prevention of Stroke in Patients With Stroke and Transient Ischemic Attack: A Guideline From the American Heart Association/American Stroke Association. Stroke 2021;52(7):e364-e467.
9. Yannoutsos A, Dreyfuss Tubiana C, Safar ME, et al. Optimal blood pressure target in stroke prevention. Curr Opin Neurol 2017;30(1):8‑14.

 Encadrés
Encadrés