L’imagerie est une étape indispensable dans la prise en charge des accidents vasculaires cérébraux (AVC) dans les 24 premières heures. Elle distingue les AVC hémorragiques des infarctus cérébraux, exclut les diagnostics différentiels et participe au bilan étiologique. Le bilan d’imagerie initial permet par ailleurs de guider l’indication des traitements de recanalisation à la phase aiguë.1
Infarctus cérébral
Diagnostic positif
Tomodensitométrie cérébrale et angio-TDM artérielle
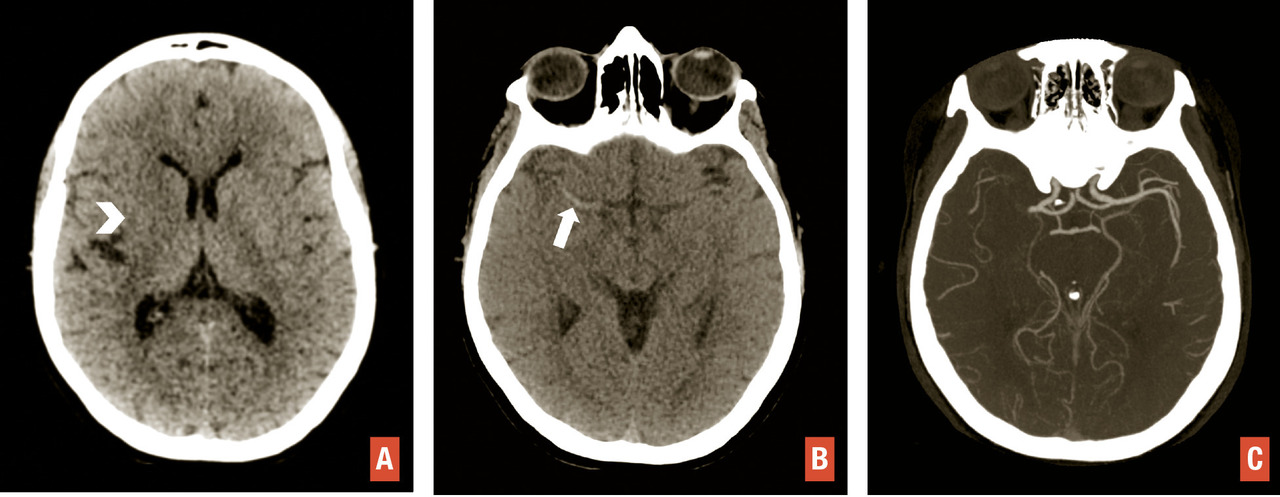
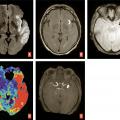
La tomodensitométrie (TDM) cérébrale garde une place centrale chez les patients suspects d’AVC, principalement en raison de sa large accessibilité, et en cas de contre-indication à l’imagerie par résonance magnétique (IRM). Sur le plan technique, elle est d’abord réalisée sans injection de produit de contraste, puis complétée par une angio-TDM des artères cervico-encéphaliques. La tomodensitométrie de perfusion peut venir compléter ces deux acquisitions, en cas de doute diagnostique ou pour guider la décision d’un traitement de recanalisation.2 En l’absence d’hématome, des signes d’infarctus peuvent exister sur une tomodensitométrie sans injection : dédifférenciation gris-blanc, effacement des sillons corticaux et hyperdensité spontanée de l’artère occluse (L’angio-TDM artérielle repose sur une acquisition lors du passage intra-artériel de produit de contraste iodé injecté par voie intraveineuse. Elle permet d’étudier les artères cervico-encéphaliques, à la recherche d’une sténose ou occlusion. L’angio-TDM dynamique (4D) renseigne également sur la qualité des collatérales suppléant le territoire ischémié.1
L’étude de la perfusion cérébrale repose sur des acquisitions séquentielles cérébrales itératives après injection d’un second bolus de produit de contraste iodé. Des logiciels dédiés permettent d’obtenir des cartographies de perfusion et d’estimer l’étendue respective de l’infarctus et de la zone de pénombre (hypoperfusée mais non encore infarcie). La présence d’une occlusion proximale permet d’orienter le patient vers un site de thrombectomie dans les 6 premières heures. Au-delà des premières heures, les images de perfusion sont essentielles pour guider la décision d’un traitement de recanalisation (thrombolyse intraveineuse après 4,5 heures, thrombectomie après 6 heures).1
IRM
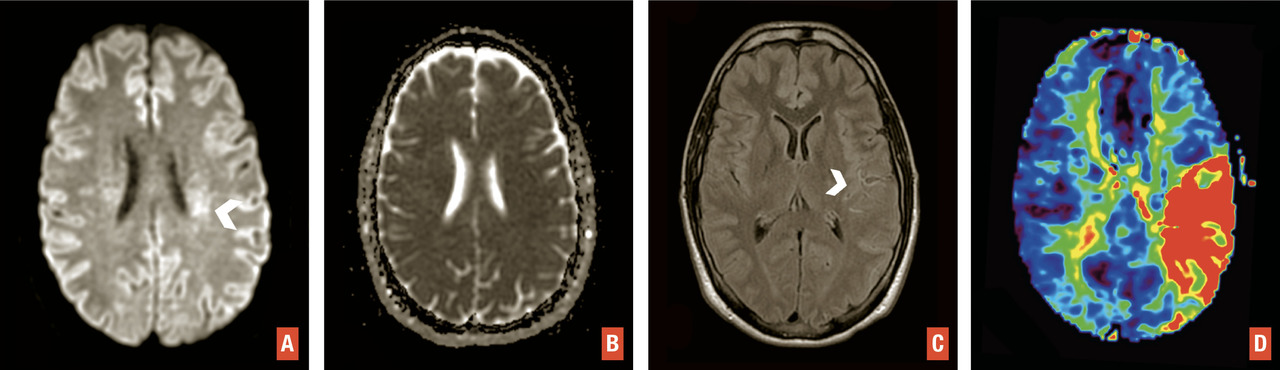
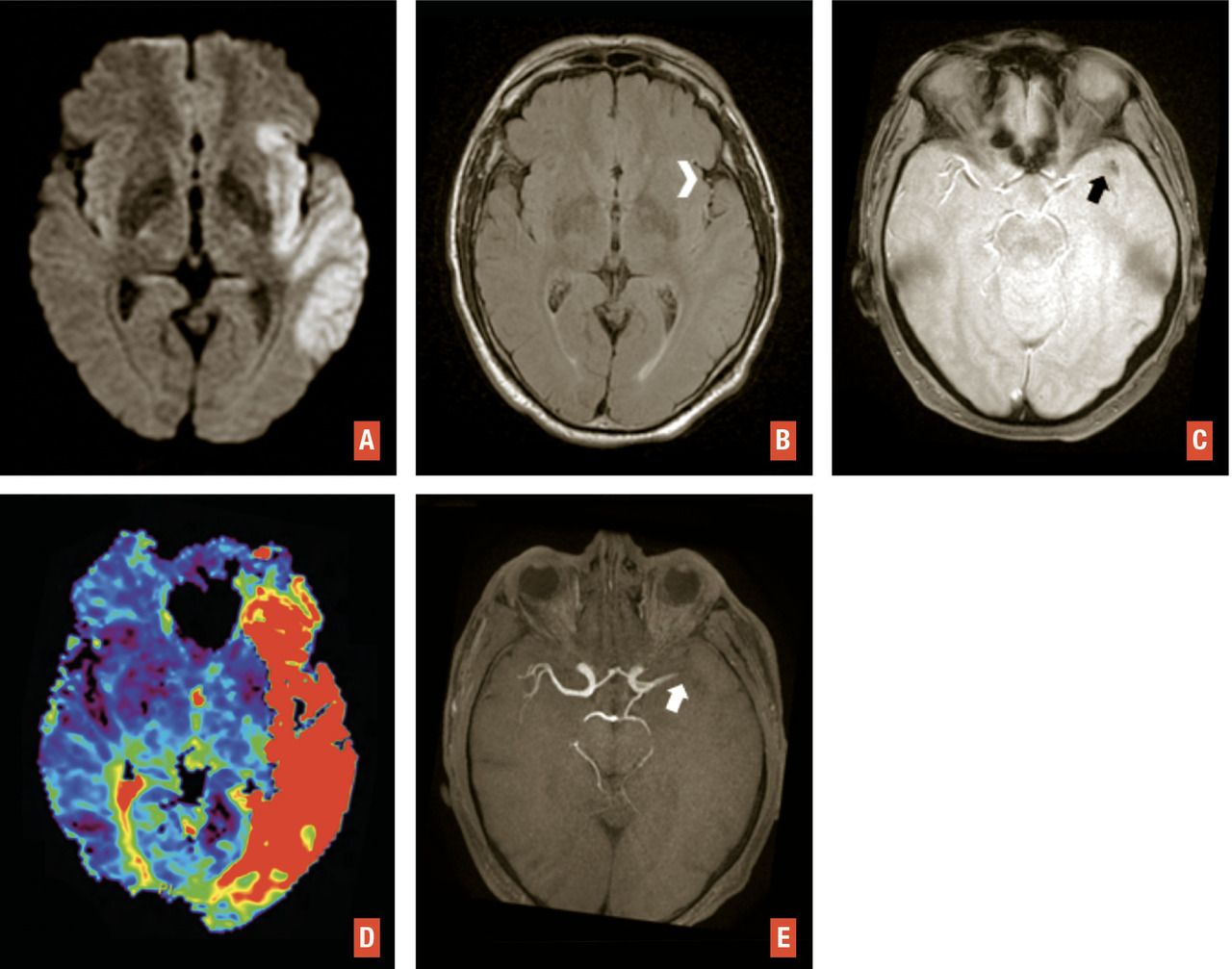
L’IRM est l’examen recommandé en France, si le plateau technique le permet sans retarder la prise en charge, et en dehors des contre-indications. Elle a une excellente sensibilité et spécificité pour détecter l’ischémie cérébrale aiguë. Un protocole standardisé est réalisable en moins de 10 minutes sans retarder la décision thérapeutique3 avec quatre séquences clés (– la séquence de diffusion pour détecter des lésions ischémiques récentes, en hypersignal avec baisse du coefficient apparent de diffusion, traduisant la restriction des mouvements des molécules d’eau secondaire à l’œdème cytotoxique. Bien que plus sensible que la tomodensitométrie, de rares faux négatifs peuvent s’observer en séquence diffusion en cas de lésion de petite taille, notamment de la fosse postérieure, d’examen très précoce ou de déficit transitoire ;
– la séquence de susceptibilité magnétique (T2* ou SWI) pour détecter un hématome,1 des séquelles hématiques ou une transformation hémorragique de lésions ischémiques, en particulier après traitement de recanalisation. Le thrombus artériel apparaît en hyposignal artériel linéaire ou curviligne en T2*, dont la sensibilité varie selon la composition du caillot, sa taille et le type de séquence utilisée ;
– la séquence FLAIR, qui permet d’apprécier l’étendue de la leucopathie vasculaire et les séquelles d’infarctus anciens, de dater l’infarctus (classiquement non visible avant 3 heures),1 de rechercher des hypersignaux vasculaires, en rapport avec des ralentissements vasculaires dans les artères collatérales en aval de l’occlusion ;
– l’angiographie par résonance magnétique (angio-IRM) 3D temps de vol du polygone de Willis (sans injection) afin de rechercher une occlusion ou une sténose des artères intracrâniennes. La séquence de perfusion T2* peut également être réalisée. Comme en tomodensitométrie, elle permet d’apprécier le risque d’extension de l’infarctus (« mismatch » perfusion-diffusion) et de décider d’un traitement de recanalisation dans des situations particulières (heure de début des symptômes inconnue, délai tardif)1 [
Diagnostics différentiels
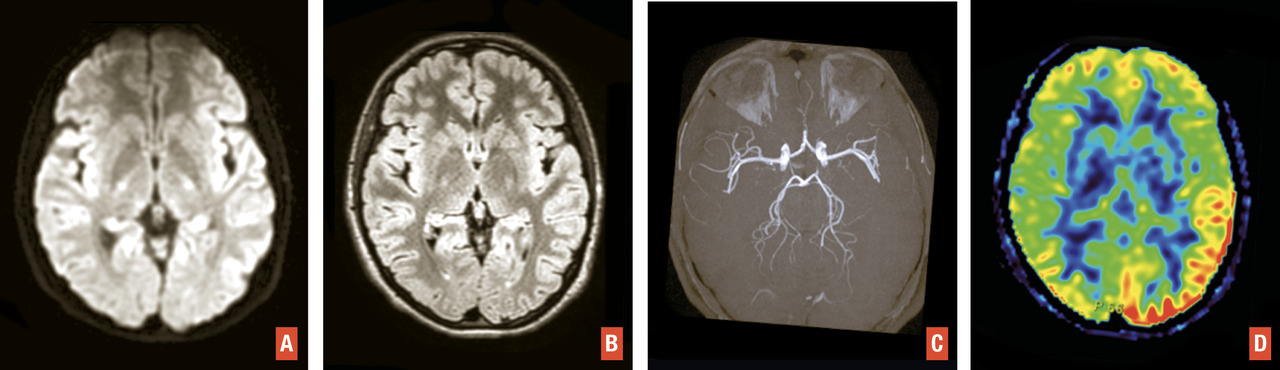
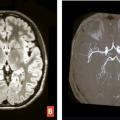
Ils représentent près de 20 % des suspicions cliniques d’AVC. L’IRM est plus performante que la tomodensitométrie pour distinguer un infarctus d’une pathologie non vasculaire. Les trois principaux diagnostics différentiels sont : déficits post-critiques, aura migraineuse, déficit « anorganiques » et, plus rarement, hypoglycémie, tumeurs cérébrales… En IRM, les anomalies ne sont pas systématisées à un territoire artériel et il n’existe pas d’occlusion artérielle.4 L’IRM permet d’orienter rapidement vers ces diagnostics différentiels et de proposer une prise en charge adaptée dès le stade aigu (fig. 4 ).
Diagnostic étiologique
L’imagerie oriente le diagnostic étiologique dès la phase aiguë. Le bilan repose sur les anomalies parenchymateuses et l’imagerie des artères cervico-encéphaliques. Les sténoses cervicales, le plus souvent en lien avec l’athérosclérose, sont recherchées par angio-IRM avec injection, angio-TDM ou ultrasonographie. Ces techniques permettent d’apprécier le degré de sténose et de guider une indication d’endartériectomie en cas de sténose serrée supérieure à 70 % selon les critères NASCET (North American Symptomatic Carotid Endarterectomy Trial Collaborators). Les marqueurs d’instabilité de la plaque sont recherchés par IRM de paroi (plaque hémorragique) et ultrasons.
La dissection cervicale, souvent suspectée cliniquement (âge jeune, cervicalgies, notion de traumatisme...), est confirmée après mise en évidence de l’hématome pariétal en IRM sur une séquence en pondération T1 avec saturation de la graisse.
L’origine cardio-embolique peut être suspectée face à des lésions ischémiques dans des territoires artériels différents. D’autres causes, beaucoup plus rares, telles que les vascularites, peuvent être évoquées sur les données IRM et en particulier de l’IRM de la paroi des artères.
La dissection cervicale, souvent suspectée cliniquement (âge jeune, cervicalgies, notion de traumatisme...), est confirmée après mise en évidence de l’hématome pariétal en IRM sur une séquence en pondération T1 avec saturation de la graisse.
L’origine cardio-embolique peut être suspectée face à des lésions ischémiques dans des territoires artériels différents. D’autres causes, beaucoup plus rares, telles que les vascularites, peuvent être évoquées sur les données IRM et en particulier de l’IRM de la paroi des artères.
Hémorragie cérébrale
Diagnostic positif
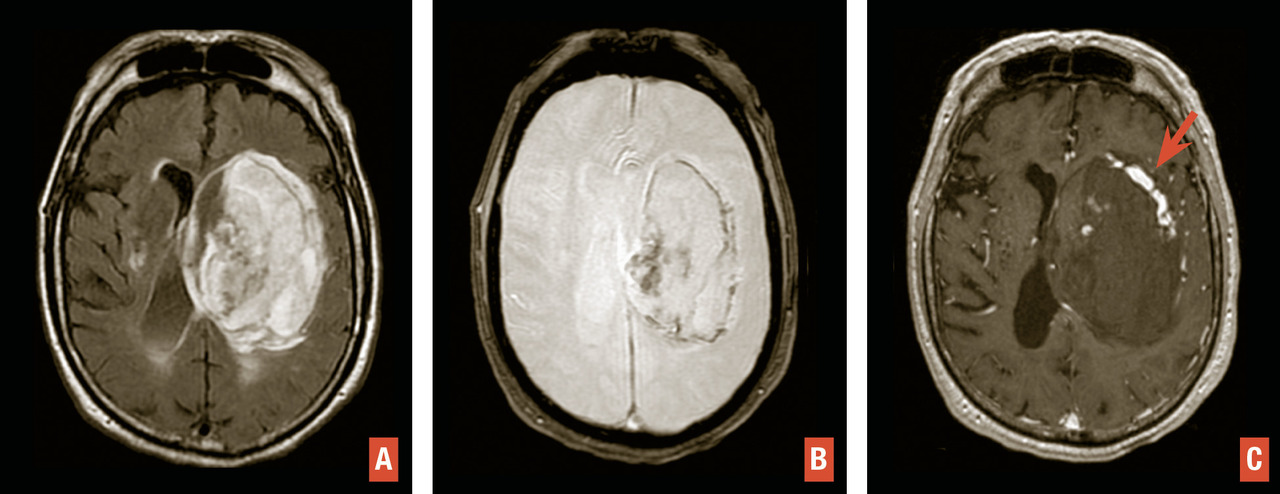
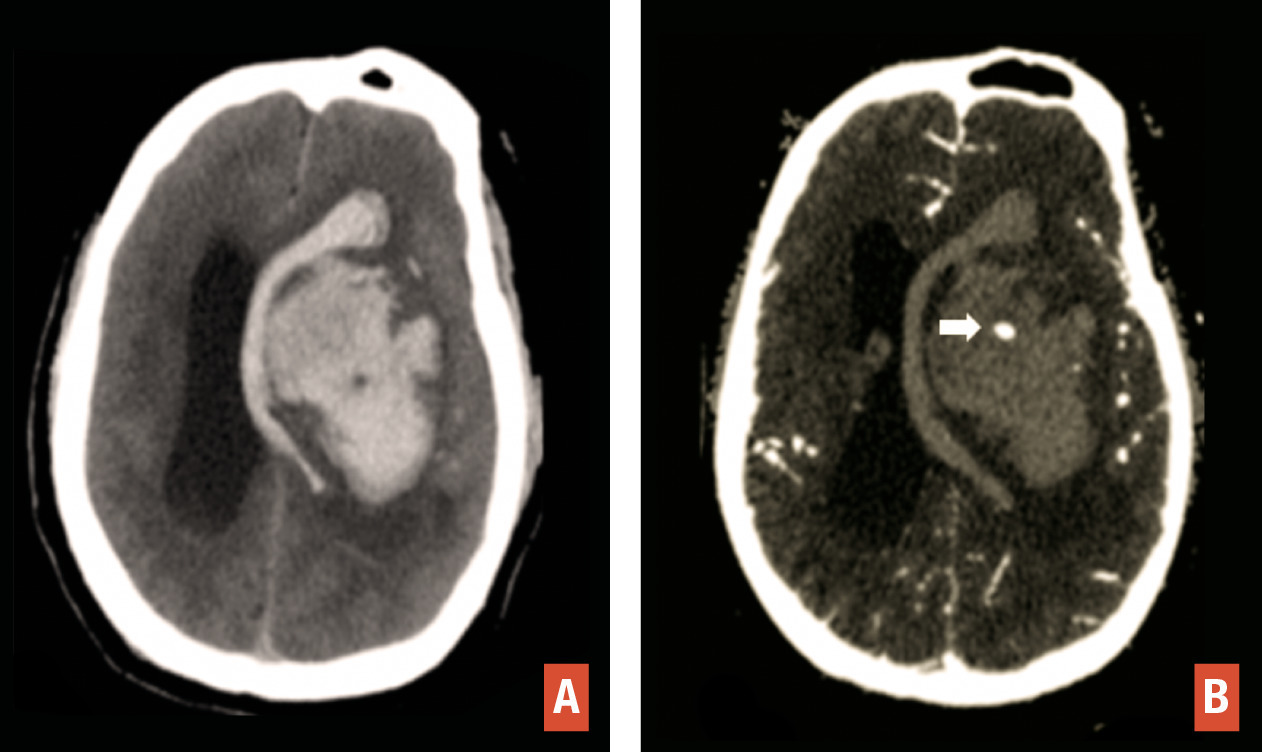
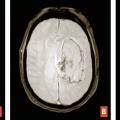
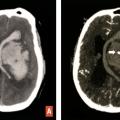
En TDM comme en IRM, l’hématome cérébral se traduit par une masse, de volume et de topographie variables, avec œdème périlésionnel. En tomodensitométrie, l’hématome aigu est hyperdense spontanément. En IRM, il est hyperintense en séquence T2/FLAIR avec hyposignaux le plus souvent périphériques en T2* (fig. 5 ). L’aspect hétérogène, la présence d’îlots hématiques satellites et le « spot sign » visible après injection traduisent un saignement actif avec risque de majoration rapide en volume (fig. 6 ).
Diagnostic étiologique
La cause la plus fréquente des hématomes cérébraux non traumatiques est la microangiopathie hypertensive. Les hématomes en lien avec cette cause sont le plus souvent profonds (noyaux gris centraux, protubérance) et s’associent volontiers à une leucopathie vasculaire, des lacunes et des micro-saignements profonds. Un bilan d’imagerie, à la recherche d’une autre origine, est réalisé en cas d’absence d’hypertension artérielle, d’âge jeune ou d’hématome lobaire.5 L’angio-TDM recherche une malformation vasculaire sous-jacente.
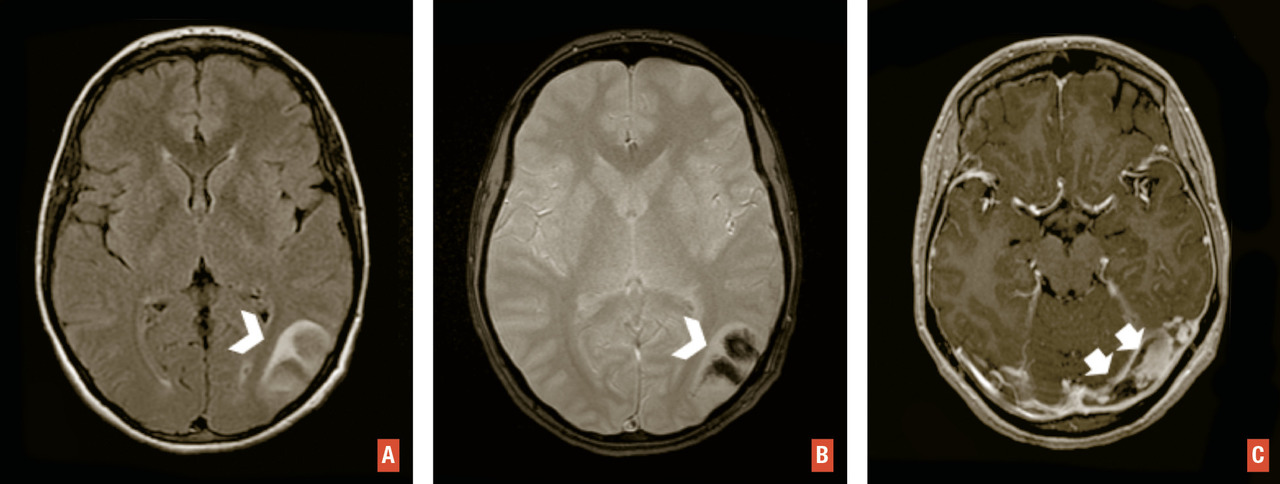
En IRM, le bilan comporte des séquences injectées dynamiques, une séquence de susceptibilité magnétique et une séquence volumique T1 sans et avec injection de gadolinium. L’injection dynamique permet une visualisation précoce des structures veineuses en cas de fistule ou de malformation artérioveineuse. Ce bilan peut être complété par une artériographie cérébrale en cas d’hématome lobaire non traumatique sans cause retrouvée en IRM. La séquence 3D T1 avec injection de gadolinium cherche à éliminer une tumeur sous-jacente et à s’assurer de la perméabilité des sinus veineux. Un thrombus veineux apparaît sous la forme d’un hyposignal linéaire sur les séquences de susceptibilité magnétique (T2* ou SWI) et d’un défaut de rehaussement d’un sinus veineux ou d’une veine corticale sur les séquences après injection (fig. 7 ). En cas d’hématome lobaire du sujet âgé, ces séquences recherchent des anomalies évocatrices d’angiopathie amyloïde telles que des microsaignements (« microbleeds ») de disposition périphérique, des séquelles d’hématomes et une sidérose corticale superficielle.
En IRM, le bilan comporte des séquences injectées dynamiques, une séquence de susceptibilité magnétique et une séquence volumique T1 sans et avec injection de gadolinium. L’injection dynamique permet une visualisation précoce des structures veineuses en cas de fistule ou de malformation artérioveineuse. Ce bilan peut être complété par une artériographie cérébrale en cas d’hématome lobaire non traumatique sans cause retrouvée en IRM. La séquence 3D T1 avec injection de gadolinium cherche à éliminer une tumeur sous-jacente et à s’assurer de la perméabilité des sinus veineux. Un thrombus veineux apparaît sous la forme d’un hyposignal linéaire sur les séquences de susceptibilité magnétique (T2* ou SWI) et d’un défaut de rehaussement d’un sinus veineux ou d’une veine corticale sur les séquences après injection (
Orienter le traitement immédiat
L’imagerie occupe une place centrale dans la prise en charge des accidents vasculaires cérebraux à la phase aiguë. L’IRM est privilégiée si elle est disponible. Elle oriente la décision thérapeutique immédiate, notamment les indications de thrombolyse et de thrombectomie mécanique, et participe au diagnostic étiologique des ischémies et des hématomes.
Références
1. Powers WJ, Rabinstein AA, Ackerson T, et al. Guidelines for the early management of patients with acute ischemic stroke: 2019 update to the 2018 guidelines for the early management of acute ischemic stroke: a guideline for healthcare professionals from the American Heart Association/American Stroke Association. Strok. 2019;50:e344-e418.
2. Jadhav AP, Desai SM, Liebeskind DS, Wechsler LR. Neuroimaging of acute stroke. Neurol Clin 2020;38:185-99.
3. Provost C, Soudant M, Legrand L, et al. Magnetic resonance imaging or computed tomography before treatment in acute ischemic stroke. Stroke 2019;50:659-64.
4. Daniere F, Edjlali-Goujon M, Mellerio C, et al. MR screening of candidates for thrombolysis: How to identify stroke mimics? J Neuroradiol 2014;41:283-95.
5. Kranz PG, Malinzak MD, Amrhein TJ. Approach to imaging in patients with spontaneous intracranial hemorrhage. Neuroimaging Clin N Am 2018;28:353-74.
2. Jadhav AP, Desai SM, Liebeskind DS, Wechsler LR. Neuroimaging of acute stroke. Neurol Clin 2020;38:185-99.
3. Provost C, Soudant M, Legrand L, et al. Magnetic resonance imaging or computed tomography before treatment in acute ischemic stroke. Stroke 2019;50:659-64.
4. Daniere F, Edjlali-Goujon M, Mellerio C, et al. MR screening of candidates for thrombolysis: How to identify stroke mimics? J Neuroradiol 2014;41:283-95.
5. Kranz PG, Malinzak MD, Amrhein TJ. Approach to imaging in patients with spontaneous intracranial hemorrhage. Neuroimaging Clin N Am 2018;28:353-74.