Ces nouvelles recommandations sont seulement applicables chez les sujets de moins de 18 ans, en Europe et en Amérique du Nord.3 Elles sont différentes des recommandations récemment publiées chez l’adulte qui proposent certains antibiotiques non autorisés en pédiatrie.
Quand diagnostiquer une infection à H. pylori ?
Cependant, en cas de suspicion d’une maladie organique à l’origine de douleurs abdominales récurrentes avec des signes d’alarme suggestifs d’une pathologie peptique, une endoscopie diagnostique doit être réalisée. Les méthodes non invasives de diagnostic de l’infection à H. pylori ne sont pas recommandées. Rechercher une infection à H. pylori chez l’enfant ayant des douleurs abdominales fonctionnelles ou en tant que cause d’une petite taille n’est pas recommandé.
Chez les enfants ayant une anémie par carence martiale réfractaire au traitement et pour lequel les autres causes ont été éliminées, la recherche d’une infection à H. pylori lors d’une endoscopie digestive peut être recommandée ; les tests non invasifs ne sont pas recommandés dans le bilan d’investigation initiale de l’anémie par carence martiale chez l’enfant.
Chez les patients avec un purpura thrombocytopénique immun chronique et une thrombocytopénie, des tests diagnostiques non invasifs (test respiratoire à l’urée marquée au 13C et/ou la recherche de l’antigène H. pylori dans les selles) peuvent être utilisés.
Si une infection à H. pylori est trouvée fortuitement au cours d’une endoscopie pratiquée pour une autre raison, un traitement peut être envisagé après avoir discuté avec les patients et/ou les parents des risques et des bénéfices du traitement de l’infection.
Comment diagnostiquer l’infection à H. pylori ?
La stratégie « test and treat » n’est pas recommandée chez l’enfant. Le but de l’investigation clinique est de détecter la cause des symptômes chez l’enfant. Cependant, les données actuelles indiquent que, en l’absence de la maladie peptique, l’infection à H. pylori n’entraîne pas de symptômes. De ce fait, la réalisation d’un test non invasif (test respiratoire à l’urée marquée au 13C et/ou recherche de l’antigène H. pylori dans les selles) pour détecter et traiter l’infection n’est pas indiquée.
Le diagnostic initial de l’infection doit être fondé sur le prélèvement des biopsies lors d’une endoscopie.
Des tests diagnostiques non invasifs d’H. pylori pourraient être préconisés uniquement lors de l’investigation des causes du purpura thrombocytopénique immun chronique.
Les tests fondés sur la détection des anticorps (immunoglobulines G et A) anti-H. pylori dans le sérum, les urines, et la salive ne sont pas recommandés en pratique clinique, ni pour la détection de l’infection ni pour le contrôle de l’éradication bactérienne après traitement chez les enfants et les adolescents.
Enfin, avant de rechercher et de contrôler l’éradication d’H. pylori, il convient d’arrêter le traitement par inhibiteur de la pompe à protons (IPP) au moins 2 semaines avant et par un antibiotique au moins 4 semaines avant d’effectuer le test.
Au cours de l’endoscopie digestive, six biopsies gastriques (antro-fundiques) doivent être réalisées pour établir le diagnostic de l’infection à H. pylori.
À partir de ces biopsies, sont effectués : une culture bactérienne (avec antibiogramme) et/ou une polymerase chain reaction (PCR) ; un examen histologique selon la classification de Sydney définissant sur les biopsies gastriques l’intensité des lésions suivantes, inflammation histologique, activité histologique, atrophie gastrique, métaplasie intestinale et détection d’H. pylori ; un test à l’uréase rapide. Le diagnostic de l’infection est retenu lorsque la culture (antibiogramme) et/ou la PCR sont positives, soit au moins deux autres tests invasifs l’histologie (gastrite à H. pylori) et le test à l’uréase rapide.
Si le traitement antiacide ne peut pas être arrêté pour 2 semaines en raison de la récidive des symptômes, il est préconisé de changer pour un anti-H2 avec une discontinuation du traitement 2 jours avant les tests.
Quand traiter l’infection à H. pylori ?
Résistances aux antibiotiques chez l’enfant
Comment traiter l’infection à H. pylori ?
En cas de prescription d’une quadruple thérapie fondée sur le bismuth chez les enfants de moins de 8 ans, il est souhaitable d’associer bismuth, IPP, amoxicilline et métronidazole tandis que chez les adolescents de plus de 18 ans, on préfère l’association bismuth, IPP, métronidazole et tétracycline (Pylera).
Le rôle des probiotiques serait de diminuer les effets indésirables et d’améliorer l’adhésion au traitement, ce qui augmenterait l’efficacité des différents traitements d’éradication.
Une monothérapie par un IPP doit être poursuivie après le traitement d’éradication pendant 2 à 4 semaines supplémentaires chez les patients ayant une maladie peptique.
Il est nécessaire que le médecin explique au patient et à sa famille l’importance de la bonne prise du traitement en raison du risque important d’échec en cas de manque d’adhésion. Un taux d’éradication élevé est atteint lorsque plus de 90 % du traitement prescrit a été ingéré. Il est aussi conseillé de donner au patient et à ses parents un livret individuel expliquant la nature de cette maladie et les différents médicaments à prendre en précisant leurs doses et la durée du traitement.
Contrôle de l’éradication bactérienne
Ce contrôle est réalisé par un des tests non invasifs : le test respiratoire 13C-TRU ou le test d’antigène monoclonal dans les selles (HpSA). La disparition des symptômes n’est pas un bon indicateur de la réussite du traitement.
Points essentiels
Les douleurs abdominales récurrentes ne sont pas spécifiques de l’infection à H. pylori chez les enfants.
La gastrite nodulaire est l’aspect endoscopique le plus fréquent chez l’enfant. L’infection à H. pylori est un facteur de risque de développer un ulcère duodénal, mais non d’ulcère gastrique chez les enfants dans les pays à faible prévalence d’infection.
Le but de l’investigation de symptômes gastro-intestinaux est d’en déterminer leur cause et selon les cas de rechercher la présence d’H. pylori.
Quand rechercher une infection à H. pylori chez l’enfant ?
lIndications directes :
– signes cliniques suggérant une maladie peptique
– anémie par carence martiale réfractaire au traitement habituel
– purpura thrombocytopénique immun chronique
lIndications indirectes :
– présence d’érosions et/ou ulcération gastriques et/ou duodénales (i.e. maladie peptique)
– présence d’une gastrique nodulaire
– présence de signes endoscopiques en faveur du lymphome du MALT chez les adolescents et les jeunes adultes.
Le diagnostic initial de l’infection à H. pylori est fondé sur l’endoscopie gastrique avec biopsies.
Un enfant ne doit être traité que sur des indications cliniques. La recherche de l’infection et son traitement doivent apporter un bénéfice clair et direct.
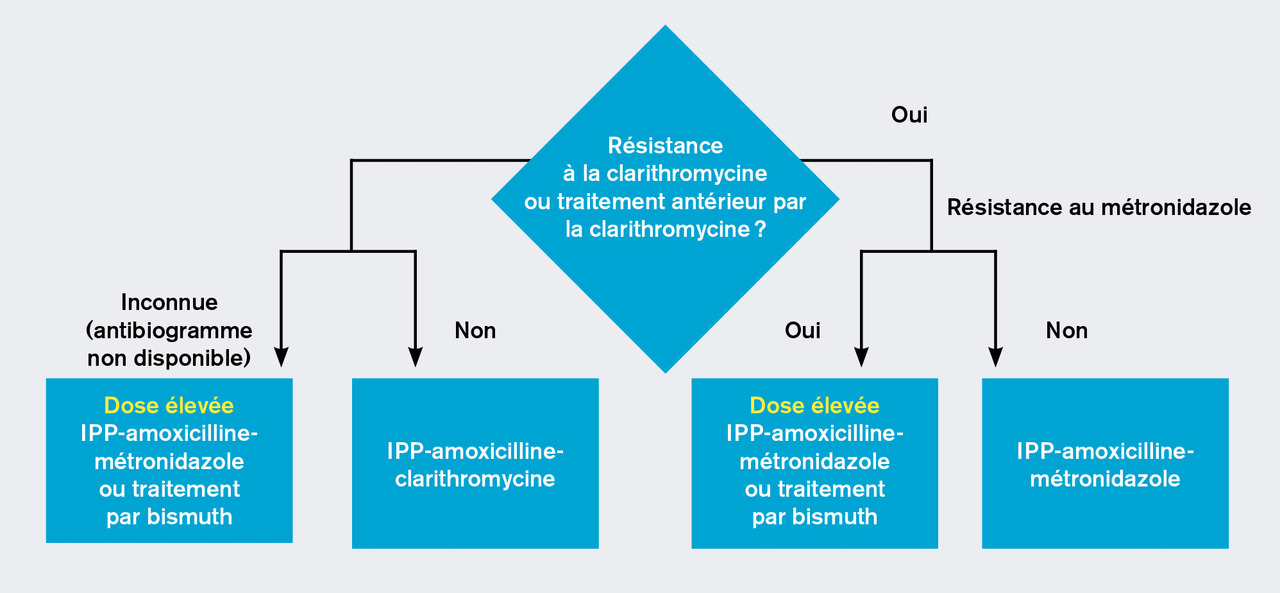
Le traitement d’éradication doit être adapté aux résultats de l’antibiogramme et/ou de la PCR.
Le traitement recommandé est une triple thérapie adaptée à l’antibiogramme d’une durée de 14 jours avec des fortes doses d’inhibiteur de la pompe à protons.
Le contrôle de l’éradication doit se faire par un 13C-TRU ou un test de détection d’antigènes bactériens dans les selles.
La relation entre les chances d’éradication et l’observance thérapeutique doit être expliquée à l’enfant et à ses parents.
2. Koletzko S, Jones NL, Goodman KJ, et al. Evidence-based guidelines from ESPGHAN and NASPGHAN for Helicobacter pylori infection in children. H. pylori Working Groups of ESPGHAN and NASPGHAN. J Pediatr Gastroenterol Nutr 2011;53:230-43.
3. Jones NL, Koletzko S, Goodman K, et al, on behalf of ESPGHAN, NASPGHAN. Joint ESPGHAN/ NASPGHAN guidelines for the management of Helicobacter pylori in children and adolescents (update 2016). J Pediatr Gastroenterol Nutr 2017;64:991-1003.
4. Kalach N, Bontems P, Raymond J. Helicobacter pylori infection in children. Helicobacter 2017;22(Suppl 1):e12414. https///doi.org/10111/hel.12414.
5. Kalach N, Serhal L, Asmar E, et al. Helicobacter pylori primary resistant strains over 11 years in French children. Diag Microbiol Infect Dis 2007;59:217-22.

 Encadrés
Encadrés