La prise en charge de la primo-infection maternelle par le cytomégalovirus (CMV) au premier trimestre de la grossesse a été révolutionnée par la validation de l’efficacité du traitement antiviral (valaciclovir) sur la transmission maternofœtale. De l’ère où la sérologie pendant la grossesse n’était pas recommandée en raison de l’absence de traitement validé, nous passons aujourd’hui à une ère où la sérologie devrait être de plus en plus souvent prescrite afin d’identifier les femmes enceintes qui pourraient bénéficier de cette nouvelle prise en charge. Les objectifs sont ici de mettre en lumière les enjeux de cette infection pendant la grossesse, les indications de la prescription de la sérologie, les moyens de prévention primaire (éviter l’infection maternelle) et secondaire (éviter la transmission du virus au fœtus en cas de primo-infection maternelle).
CMV : un virus au tropisme tissulaire étendu
L’infection par le CMV, virus de la famille des Herpesviridae, est fréquente. Des épisodes de réactivation et de réinfection sont possibles.
Cycle du CMV dans l’organisme
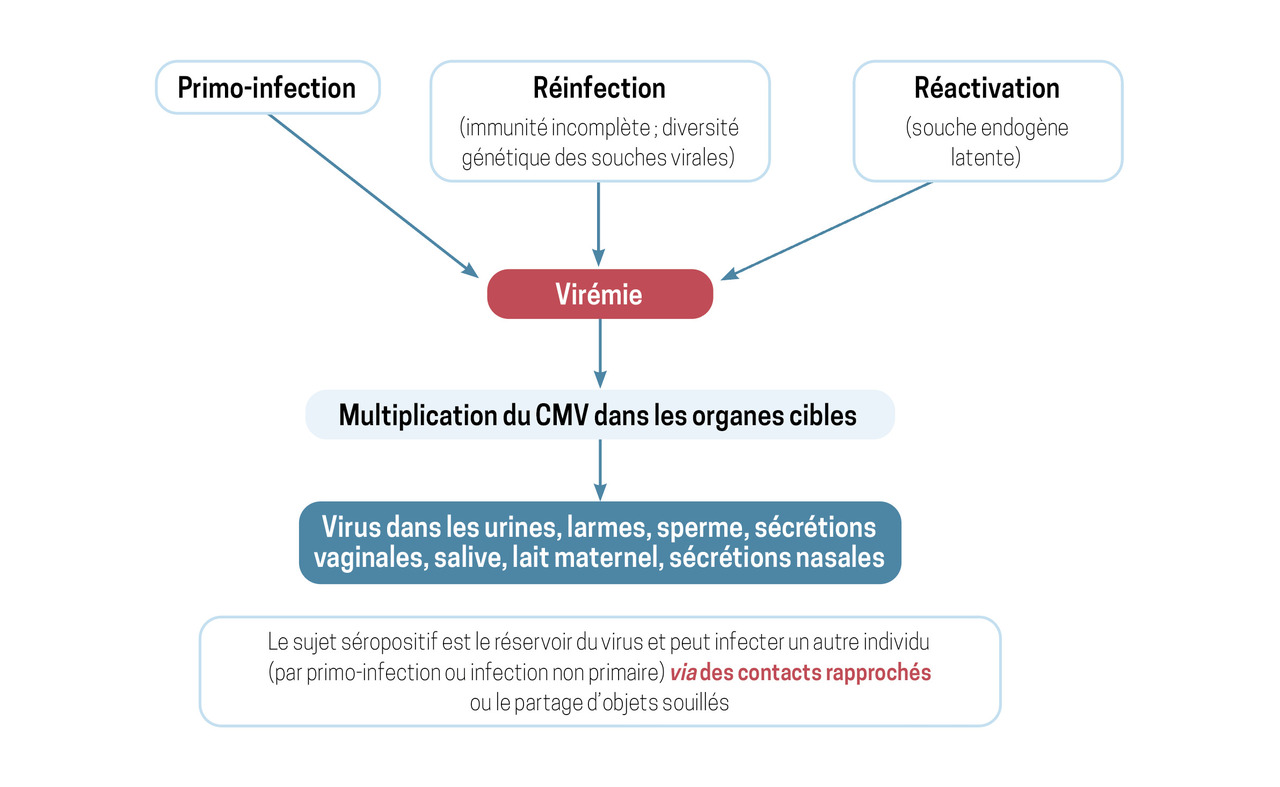
Lors de la primo-infection, le virus pénètre dans l’organisme par les muqueuses (oropharyngées, génitales) et s’y multiplie dans les cellules épithéliales, monocytaires ou endothéliales. Les monocytes infectés rejoignent la circulation sanguine (virémie) et le virus est transporté dans tous les organes cibles. Le tropisme tissulaire du virus est large : il se multiplie dans le foie, la rate, le rein, le cerveau, le système nerveux périphérique, le placenta, les glandes mammaires, les glandes salivaires et les épithéliums génitaux. Cette réplication virale très large se traduit par la présence du virus dans tous les liquides biologiques (
Le CMV, comme tous les virus de la famille des Herpesviridae, a développé des stratégies pour échapper au système immunitaire et ainsi persister dans l’organisme au décours de la primo-infection. Cette latence virale peut se compliquer d’épisodes de réactivation de la souche endogène. Par ailleurs, le génome du CMV ayant une variabilité génétique élevée et la réponse immunitaire acquise lors de la primo-infection ne conférant qu’une protection partielle, des réinfections sont possibles avec des souches génétiquement différentes.
L’infection par le CMV en quelques chiffres
L’infection par le CMV est fréquente, avec une séroprévalence dans la population générale mondiale de plus de 80 % et de 50 à 60 % en Europe.1
Dans les pays à hauts revenus, la séroprévalence est de l’ordre de 20 % à l’âge de 2 ans. La primo-infection des nourrissons peut avoir lieu dès les premiers jours de vie par contamination avec les sécrétions génitales lors de l’accouchement, par le lait maternel ou, plus tard, par contact avec d’autres nourrissons infectés, notamment au sein d’une crèche. Une augmentation progressive de la séroprévalence est observée : de 30 % chez l’adolescent à plus de 70 % chez le sujet adulte âgé. Chez l’adulte, la contamination se fait par contact rapproché avec un sujet séropositif (son partenaire ou son jeune enfant, notamment si celui-ci fréquente une collectivité).
Dans les autres pays, la contamination se fait plus tôt, et la séroprévalence à l’âge de 2 ans est proche de 80 %. De façon générale, un niveau socio-économique bas et un nombre élevé de personnes vivant au domicile sont des facteurs de risque d’acquisition précoce du CMV.
Infection congénitale par le CMV : fréquence, morbidité et facteurs de risque
Les données épidémiologiques permettent d’identifier les femmes à risque d’infection congénitale par le CMV et d’en prévenir la survenue.
Prévalence
La prévalence de l’infection congénitale par le CMV est de 0,7 % dans le monde et de 0,2 à 0,4 % en Europe.2 En France, dans une enquête portant sur une cohorte de 11 942 nouveau-nés dépistés en Île-de-France, la prévalence était de 0,37 %.3 Le CMV est la cause la plus fréquente de séquelles neurosensorielles d’origine congénitale.
L’infection du placenta et du fœtus a lieu au décours d’une infection maternelle, primaire ou non. En France, 55 % des infections fœtales sont dues à une primo-infection maternelle. Dans les pays du Sud où la séroprévalence chez les femmes enceintes est très élevée, presque la totalité des infections fœtales surviennent après une infection non primaire.
Morbidité
Deux catégories de symptômes sont décrites chez les enfants avec infection congénitale par le CMV (
- les symptômes néonataux liés à la primo-infection fœtale généralisée aiguë peuvent être présents quel que soit le terme de survenue de la primo-infection maternelle.4 Ils sont très largement dominés par le retard de croissance ; les autres signes sont moins fréquents ;
- les séquelles neurosensorielles peuvent être présentes dès la naissance, ou survenir de façon retardée. Contrairement aux symptômes d’infection aiguë, ces séquelles auditives ou neurologiques ne surviennent que chez les enfants infectés à la suite d’une infection maternelle du premier trimestre.4
La fréquence des séquelles après infection maternelle non primaire est moins bien étudiée mais semble similaire à celle décrite après une primo-infection maternelle.
Quelles sont les femmes à risque ?
La France et les autres pays d’Europe de l’Ouest ont la séroprévalence du CMV chez la femme enceinte la plus basse (entre 50 et 60 %), alors qu’elle atteint 70 à 80 % dans les pays d’Europe du Sud, 80 à 90 % dans les pays d’Afrique du Nord et est supérieure à 90 % en Asie du Sud-Est et en Afrique subsaharienne.1 Il y a donc, en France, un nombre important de femmes séronégatives à risque de primo-infection pendant leur grossesse ; la fréquence de la primo-infection est de 1,4 % tout au long de la grossesse et de 0,5 % au premier trimestre.5
Les femmes séronégatives lors de leur première grossesse et dont l’intervalle entre deux grossesses est d’un à deux ans constituent un groupe à très haut risque, avec 10 % de risque de primo-infection au premier trimestre, soit un risque 20 fois plus élevé que dans la population générale des femmes enceintes.
De façon schématique, la femme enceinte à risque de primo-infection est une femme née en France, qui travaille, ayant au moins un enfant et dont la dernière grossesse est récente.
Les facteurs de risque d’infection par le cytomégalovirus non primaire pendant la grossesse sont moins bien connus ; un niveau socio-économique bas et une comorbidité (diabète, dysthyroïdie) pourraient la favoriser, mais pas la parité.
Diagnostic des infections maternelles
Quels sont les outils et quelle démarche diagnostique entreprendre pour détecter une infection par le CMV aux stades pré- et périconceptionnels ?
Outils diagnostiques de la primo-infection maternelle
La primo-infection maternelle est le plus souvent symptomatique et se résume à un syndrome pseudogrippal non spécifique. Le diagnostic clinique est donc difficile ; une fièvre modérée prolongée associée à une cytolyse hépatique modérée est évocatrice.
Le diagnostic de l’infection maternelle est fondé sur la sérologie : une séroconversion des immunoglobulines G (IgG) confirme la primo-infection.
Lorsque la séroconversion ne peut pas être mise en évidence, le diagnostic repose sur la détection des IgG et d’IgM : la présence d’IgM n’est pas spécifique d’une primo-infection récente puisque ces anticorps peuvent persister durant plusieurs mois après une primo-infection ; leur présence peut aussi être liée à des réactions sérologiques croisées ou non spécifiques ; la mesure de l’avidité des IgG permettant de dater une infection est donc impérative en cas d’IgM positives. Le profil sérologique typique de la primo-infection associe des IgM élevées, des IgG basses et une avidité basse des IgG.
Dans les études de dépistage systématique au premier trimestre de la grossesse, 1 à 5 % des femmes ont des IgM positives, mais, dans 60 à 80 % des cas, la présence de ces IgM n’est pas liée à une primo-infection survenue pendant la grossesse : l’avidité des IgG étant forte, cela élimine une primo-infection datant de moins de trois mois.2
Peut-on diagnostiquer en routine une infection maternelle non primaire ?
Il n’existe pas d’outil validé pour identifier les femmes préimmunes, à risque d’accoucher d’un nouveau-né infecté. Ces femmes ont des sérologies sans particularité : IgG positives à taux stable, absence d’IgM et avidité des IgG élevée. Ainsi, nous conseillons de ne pas refaire la sérologie CMV à une femme enceinte connue comme séropositive.
Quand prescrire une sérologie CMV en médecine générale et pendant la grossesse ?
Les recommandations du Haut Conseil de la santé publique (HCSP) publiées en 2018 préconisent de ne pas réaliser le dépistage sérologique pendant la grossesse. Ces recommandations ont néanmoins été émises avant la publication des résultats de l’étude randomisée démontrant l’efficacité du traitement préventif par valaciclovir ; elles nécessiteraient donc d’être remises en question.
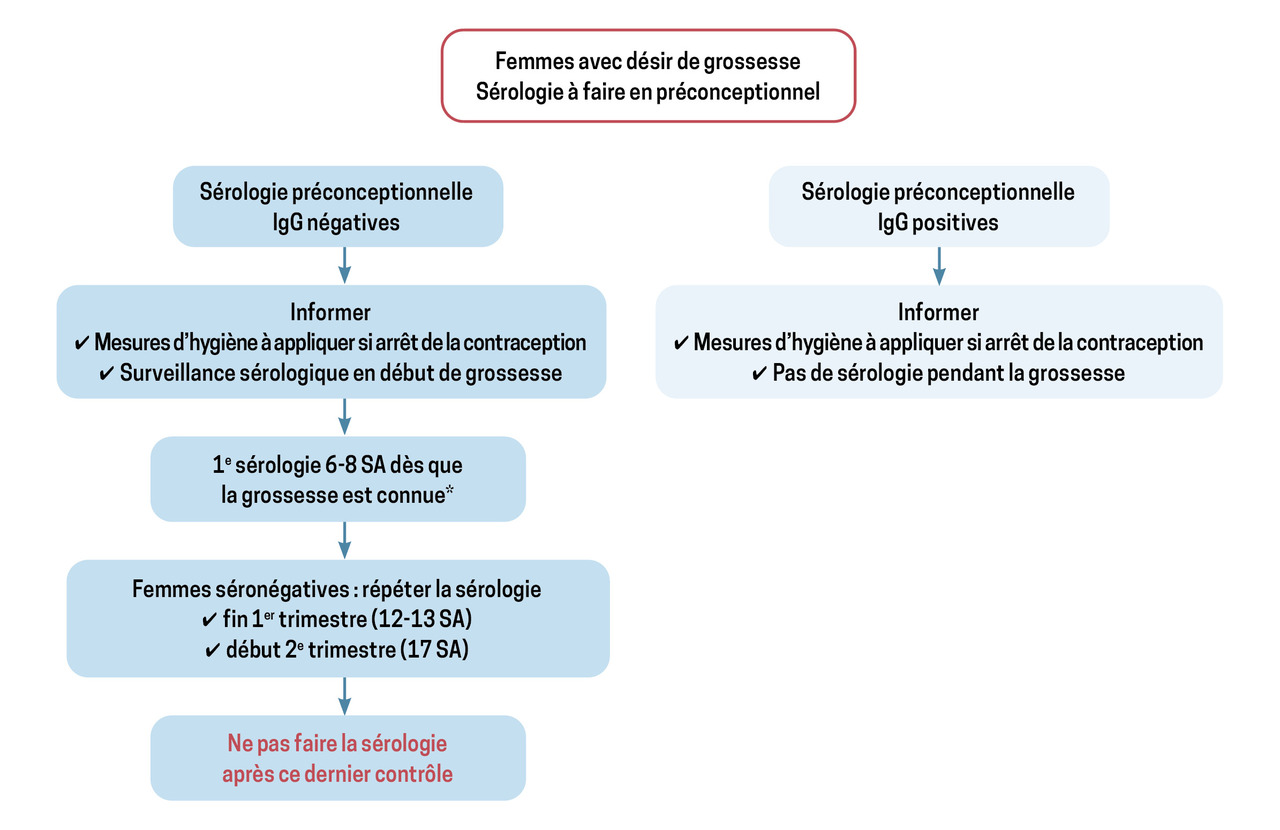
Ainsi, au même titre que la réalisation des sérologies rubéole et toxoplasmose avant la grossesse, nous conseillons de prescrire une sérologie CMV aux femmes ayant un désir de grossesse et de les informer des mesures d’hygiène à appliquer dès l’arrêt de la contraception :
- en cas de sérologie positive (IgG positives), il est inutile de répéter la sérologie pendant la grossesse ;
- dans le cas d’une sérologie négative, un contrôle doit être réalisé dès le début du premier trimestre, idéalement vers 6 à 8 semaines d’aménorrhée (SA), puis répété à 12-13 SA et une dernière fois au tout début du deuxième trimestre. En effet, les infections maternelles des deuxième et troisième trimestre n’étant pas responsables de séquelles, refaire la sérologie ultérieurement n’est pas utile (
Traitement préventif de l’infection maternofœtale
Les mesures d’hygiène avant et pendant la grossesse sont essentielles, et le médecin généraliste joue un rôle majeur dans la diffusion de ce message.
En cas de primo-infection, un traitement existe pour limiter la transmission maternofœtale du virus.
Prévenir l’infection maternelle du premier trimestre
Les mesures d’hygiène (tableau) consistent à éviter les échanges de fluides (salive, urines, sécrétions nasales, larmes) directs ou manuportés, notamment entre une femme enceinte et de jeunes enfants. Se laver les mains (après les soins apportés au nourrisson : change, mouchage…), éviter les échanges de cuillères et de linge de toilette et nettoyer régulièrement les jouets sont les trois mesures d’hygiène principales. Elles sont bien décrites dans les recommandations du HCSP de 2018,6 fondées sur les résultats d’une seule étude randomisée qui avait démontré l’efficacité des mesures hygiéniques sur le taux de primo-infections maternelles survenues au cours des deuxième et troisième trimestres.7
Il est important de noter qu’il n’existe aucune preuve de l’efficacité de ces conseils d’hygiène pour éviter les infections maternelles non primaires.
Cependant, pour que ces mesures soient efficaces et diminuer ainsi le risque de séquelles et de handicap chez l’enfant à naître, elles doivent être appliquées très tôt (avant même la conception) afin de couvrir les périodes à risque : périconceptionelle (2 mois précédents) et premier trimestre. Ainsi, informer sur ces mesures lors de la première consultation de maternité (généralement programmée à 11-12 semaines) est trop tardif : ces messages doivent être diffusés à toutes les femmes ayant un désir de grossesse ; le rôle des médecins généralistes est ici essentiel, dans le cadre d’une consultation préconceptionnelle, par exemple.
Un traitement antiviral pour prévenir la transmission maternofœtale en cas de primo-infection maternelle !
Plusieurs antiviraux actifs contre le CMV (ganciclovir, cidofovir et foscarnet) sont utilisés pour traiter les infections sévères chez des patients immunodéprimés. Cependant, ces médicaments, antagonistes de nucléotides, ont des effets tératogènes potentiels et une toxicité bien connue (effets indésirables hématologiques et rénaux), empêchant leur utilisation pendant la grossesse.
Le valaciclovir n’est pas le meilleur anti-CMV. Néanmoins, à doses élevées, il a démontré son efficacité pour prévenir l’infection par le CMV chez les patients transplantés. Par ailleurs, des données de pharmacovigilance très rassurantes existent concernant son utilisation durant la grossesse.8-10
Dans une étude non randomisée, 8 g/j de valaciclovir ont été administrés à des femmes dont le fœtus était infecté. Ce traitement a été associé à une proportion plus élevée de nouveau-nés asymptomatiques par rapport à une cohorte historique (82 vs 43 %), sans aucun effet indésirable notable rapporté ni chez le fœtus ni chez la mère.8 Cet essai a démontré la plausibilité de l’efficacité du valaciclovir dans ce contexte.
Sur la base de ces résultats encourageants, une équipe israélienne a réalisé un essai en double aveugle contre placebo, montrant l’efficacité du valaciclovir (8 g/j) sur la transmission verticale du CMV chez 100 femmes enceintes ayant eu une primo-infection au premier trimestre.9 Le valaciclovir a été administré du diagnostic de la primo-infection à l’amniocentèse. Ce traitement a permis d’obtenir une réduction de 70 % de la transmission verticale : transmission à 29 % dans le groupe placebo contre 11 % dans le groupe valaciclovir. Par ailleurs, dans cette étude, plus le délai entre la date présumée de la primo-infection et la date de l’initiation du traitement était court, plus le risque de transmission au fœtus était faible, témoignant de l’importance d’instaurer rapidement le traitement après le diagnostic.
À la suite de cet essai clinique dont les résultats ont été rendus publics en 2019, nous traitons systématiquement les patientes ayant une primo-infection du premier trimestre, dans notre centre. Nous avons comparé les issues de 65 grossesses traitées par valaciclovir avec des contrôles historiques. Nous avons montré une baisse significative de la transmission verticale de 29 à 12 %.10 Nos résultats reproduisent donc, dans une autre population, ceux obtenus par l’équipe israélienne, confortant l’intérêt de cette prise en charge thérapeutique.
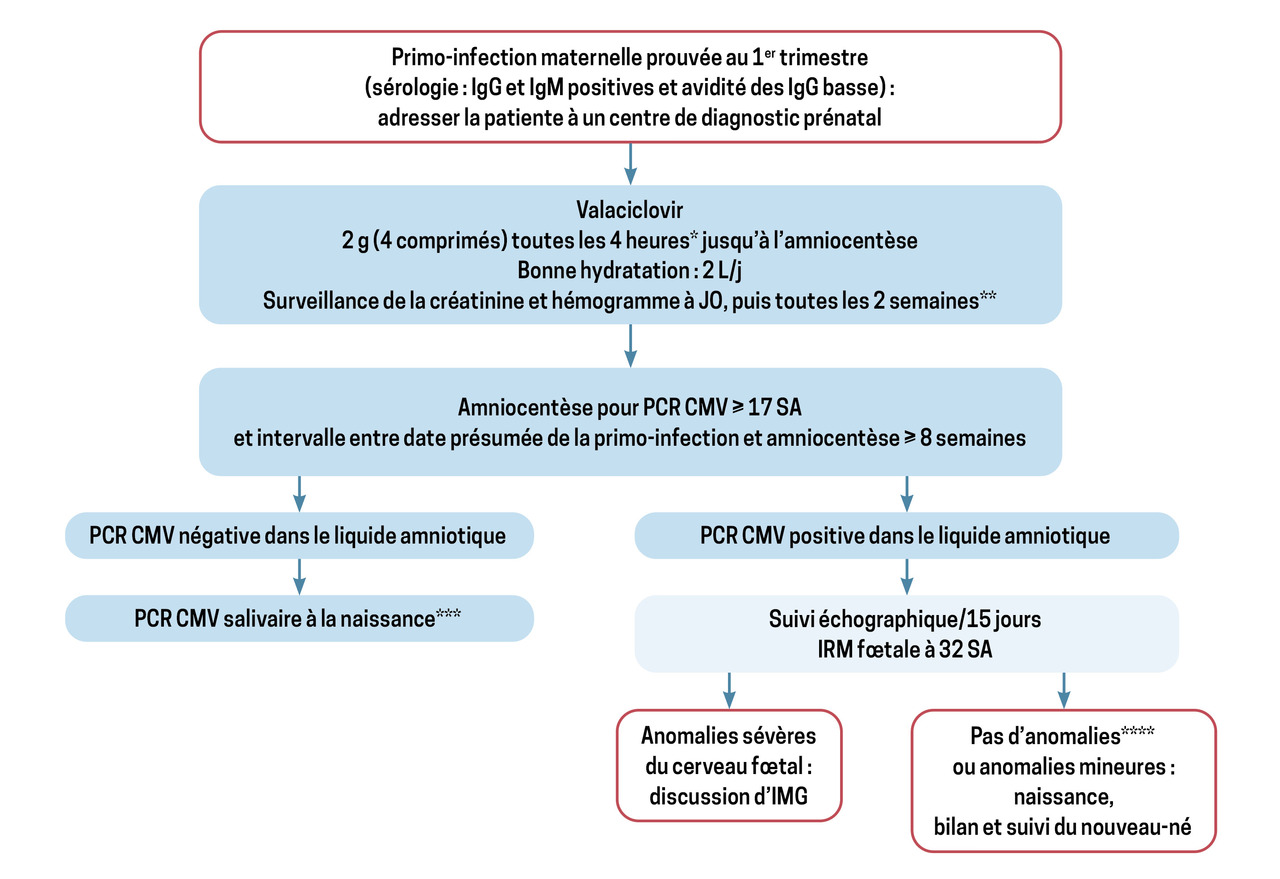
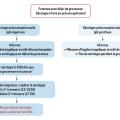
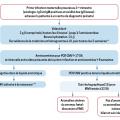
Les aspects pratiques de la prise en charge d’une primo-infection maternelle au premier trimestre de la grossesse peuvent être résumés sous forme d’un algorithme, suivi notamment dans les centres de diagnostic prénataux (
Que dire à vos patients ?
La primo-infection par le CMV est le plus souvent silencieuse et bénigne chez la femme enceinte, mais ce virus peut traverser le placenta et infecter le fœtus dans 30 à 40 % des cas.
L’infection du fœtus peut se compliquer de troubles de l’audition ou du développement neurologique lorsque l’infection de la mère est survenue au premier trimestre.
La sérologie avant la grossesse est utile ; si elle est négative, elle doit être refaite au cours du premier trimestre de grossesse pour identifier une éventuelle primo-infection.
La sérologie maternelle permet de détecter la primo-infection du premier trimestre. Si elle est avérée, un traitement par antiviral permet de diminuer à moins de 10 % le risque de transmission virale au fœtus.
Pour les femmes ayant un projet de grossesse ou déjà enceintes, il est recommandé de respecter des mesures d’hygiène lors des contacts avec les jeunes enfants, durant tout le premier trimestre de grossesse.
Les conseils de prévention sont à retrouver sur le site du Haut Conseil de la santé publique : https://bit.ly/3iorxwQ (tableau).
Il existe une association de parents ayant été confrontés à une infection par le CMV pendant la grossesse : https://stopcmv.fr/
1. Zuhair M, Smit GSA, Wallis G, et al. Estimation of the worldwide seroprevalence of cytomegalovirus: A systematic review and meta-analysis. Rev Med Virol 2019;29(3):e2034.
2. Leruez-Ville M, Foulon I, Pass R, et al. Cytomegalovirus infection during pregnancy: State of the science. Am J Obstet Gynecol 2020;223(3):330‑49.
3. Leruez-Ville M, Magny JF, Couderc S, et al. Risk Factors for Congenital Cytomegalovirus Infection Following Primary and Nonprimary Maternal Infection: A Prospective Neonatal Screening Study Using Polymerase Chain Reaction in Saliva. Clin Infect Dis Off Publ Infect Dis Soc Am 2017;65(3):398‑404.
4. Faure-Bardon V, Magny JF, Parodi M, et al. Sequelae of Congenital Cytomegalovirus Following Maternal Primary Infections Are Limited to Those Acquired in the First Trimester of Pregnancy. Clin Infect Dis Off Publ Infect Dis Soc Am 2019;69(9):1526‑32.
5. Gouarin S, Palmer P, Cointe D, et al. Congenital HCMV infection: A collaborative and comparative study of virus detection in amniotic fluid by culture and by PCR. J Clin Virol Off Publ Pan Am Soc Clin Virol 2001;21(1):47‑55.
6. Haut Conseil de la santé publique. La prévention de l’infection à cytomégalovirus chez la femme enceinte et chez le nouveau-né. Rapport 2018.
7. Revello MG, Lazzarotto T, Guerra B, et al. A randomized trial of hyperimmune globulin to prevent congenital cytomegalovirus. N Engl J Med 2014;370(14):1316‑26.
8. Leruez-Ville M, Ghout I, Bussières L, et al. In utero treatment of congenital cytomegalovirus infection with valacyclovir in a multicenter, open-label, phase II study. Am J Obstet Gynecol 2016;215(4):462.e1-462.e10.
9. Shahar-Nissan K, Pardo J, Peled O, et al. Valaciclovir to prevent vertical transmission of cytomegalovirus after maternal primary infection during pregnancy: A randomised, double-blind, placebo-controlled trial. Lancet 2020;396(10253):779‑85.
10. Faure-Bardon V, Fourgeaud J, Stirnemann J, et al. Secondary prevention of congenital CMV infection with valaciclovir following maternal primary infection in early pregnancy. Ultrasound Obstet Gynecol 2021;58(4):576-81.

 Encadrés
Encadrés