Informer et conseiller en matière de prévention de la transmission du VIH.
Connaître les situations justifiant la prescription d’une sérologie VIH. Interpréter les résultats d’une sérologie VIH et en annoncer le résultat.
Reconnaître une primo infection par le VIH.
Prévenir et reconnaître les principales complications infectieuses associées au VIH.
Connaître et savoir dépister les principales complications non infectieuses associées au VIH.
Connaître les grands principes du traitement antirétroviral, de son suivi et de son observance.
Dépister une infection à VIH au cours de la grossesse et en organiser la prise en charge.
Éléments de physiopathologie
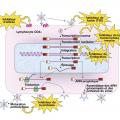
L’infection aboutit également à la constitution précoce, dès les premiers jours de la primo-infection, d’un réservoir ou sanctuaire viral, principalement au sein des lymphocytes T CD4 mémoires, notamment dans les structures lymphoïdes associées au tissu intestinal. Ce réservoir est peu diminué par les antirétroviraux. La longue durée de vie de ces cellules latentes ainsi que leur capacité proliférative sont la principale cause de la persistance virale dans l’organisme. En conséquence, le traitement antirétroviral n’a qu’un effet suspensif, son interruption conduit au bout de quelques jours à la reprise d’une réplication virale et donc de la destruction progressive du système immunitaire.
Prévention de la transmission sexuelle et sanguine du VIH
- de l’utilisation de mesures barrières (préservatif masculin ou féminin) au cours des rapports sexuels ;
- de la mise à disposition de kits d’injection à usage unique pour éviter l’échange de seringues lors de l’usage de drogues ;
- du dépistage précoce et du traitement des infections sexuellement transmissibles (IST) qui facilitent la transmission du VIH ;
- de mesures comportementales de réduction des rapports sexuels à risque, et de sevrage ou de substitution de l’usage de drogues injectées ;
- de la circoncision dans certains pays à faibles ressources, permettant une diminution du risque d’acquisition du VIH chez l’homme d’environ 50 % ;
- du traitement antirétroviral après exposition accidentelle aux liquides biologiques (
v. item 362 ) ;
- du traitement systématique des personnes vivant avec le VIH, qui a montré une grande efficacité dans la prévention de la transmission de l’infection par le VIH par voie sexuelle dans les couples hétérosexuels et homosexuels lorsque la charge virale VIH est indétectable depuis plus de 6 mois (traitement comme prévention de la transmission, ou tasp en anglais pour « treatment as prevention ») ; un dépistage précoce de l’infection par le VIH et la mise sous traitement immédiate quel que soit le taux de lymphocytes CD4 permettraient de fortement diminuer la chaîne de transmission de l’infection par le VIH ;
- de l’instauration d’une prophylaxie antirétrovirale pré-exposition (PREP) chez une personne prenant un risque d’infection alors qu’elle n’est pas infectée par le VIH par la combinaison de deux inhibiteurs de la transcriptase inverse (INTI), le ténofovir et l’emtricitabine, qui a démontré une efficacité importante dans la réduction du risque d’acquisition de l’infection par le VIH chez les hommes ayant des relations sexuelles avec des hommes (HSH) ; depuis 2016, en France, il est autorisé de prescrire une prophylaxie antirétrovirale pré-exposition par ténofovir-emtricitabine à certaines personnes à haut risque.
Indication du dépistage de l’infection à VIH
Le dépistage ciblé des populations clés, à haut risque d’infection, doit se faire à intervalles réguliers, tous les ans au moins, tous les trois mois pour les hommes ayant des relations sexuelles avec des hommes. Il concerne :
- les hommes ayant des relations sexuelles avec des hommes ;
- les personnes hétérosexuelles ayant eu plus d’un partenaire dans les douze derniers mois, notamment les personnes en situation de prostitution ;
- les personnes originaires de Guyane, des Caraïbes ou d’Afrique subsaharienne ;
- les usagers de drogues injectables ;
- les personnes incarcérées ;
- les partenaires sexuels des personnes vivant avec le VIH.
- symptômes évocateurs d’une complication du VIH dont cancer, tuberculose, fièvre prolongée, polyadénopathie, lymphopénie, thrombopénie, etc. ;
- suspicion ou diagnostic d’infection sexuellement transmise ou d’hépatite virale B ou C ;
- projet de grossesse et grossesse ;
- première prescription de contraception ;
- viol.
Diagnostic de l’infection à VIH
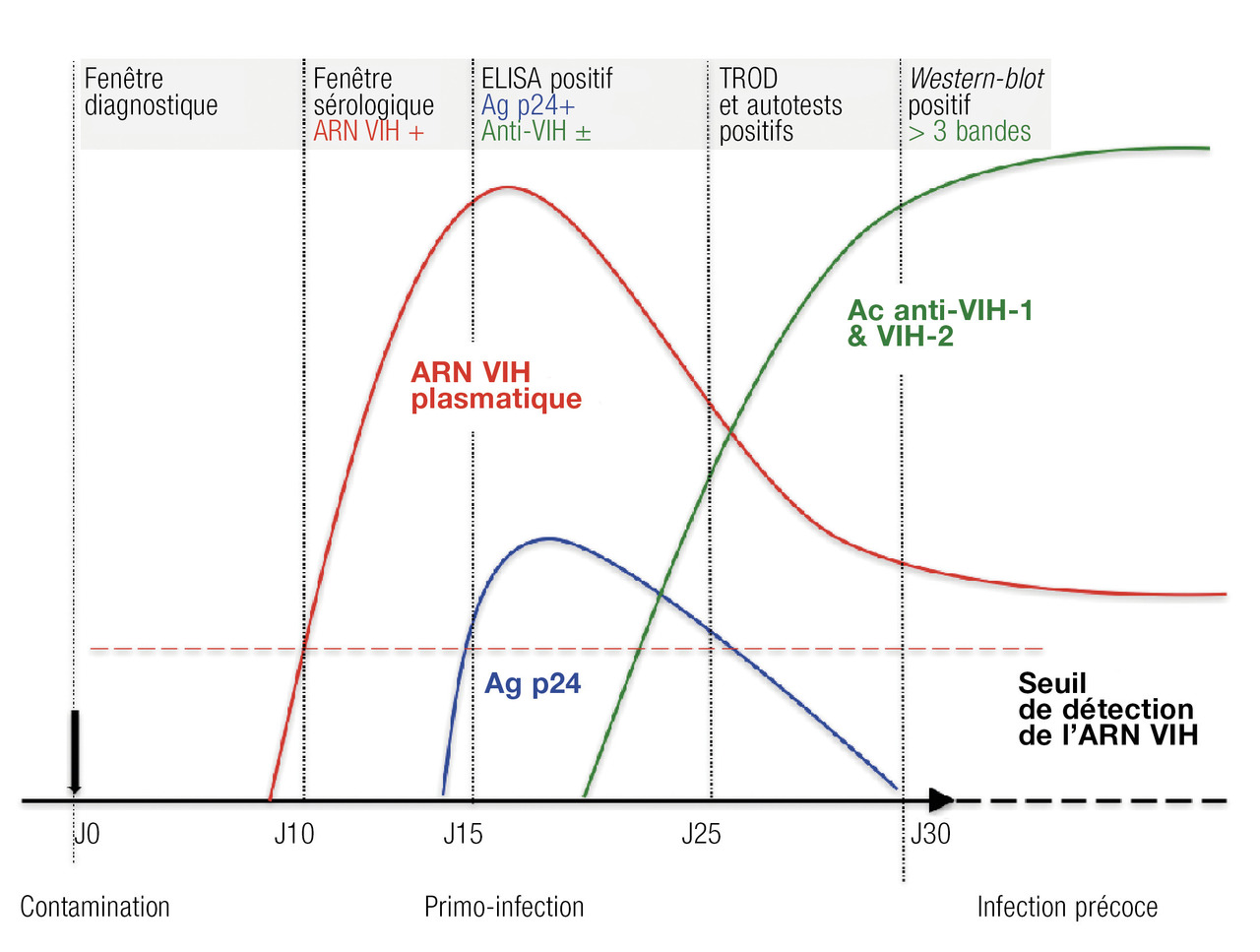
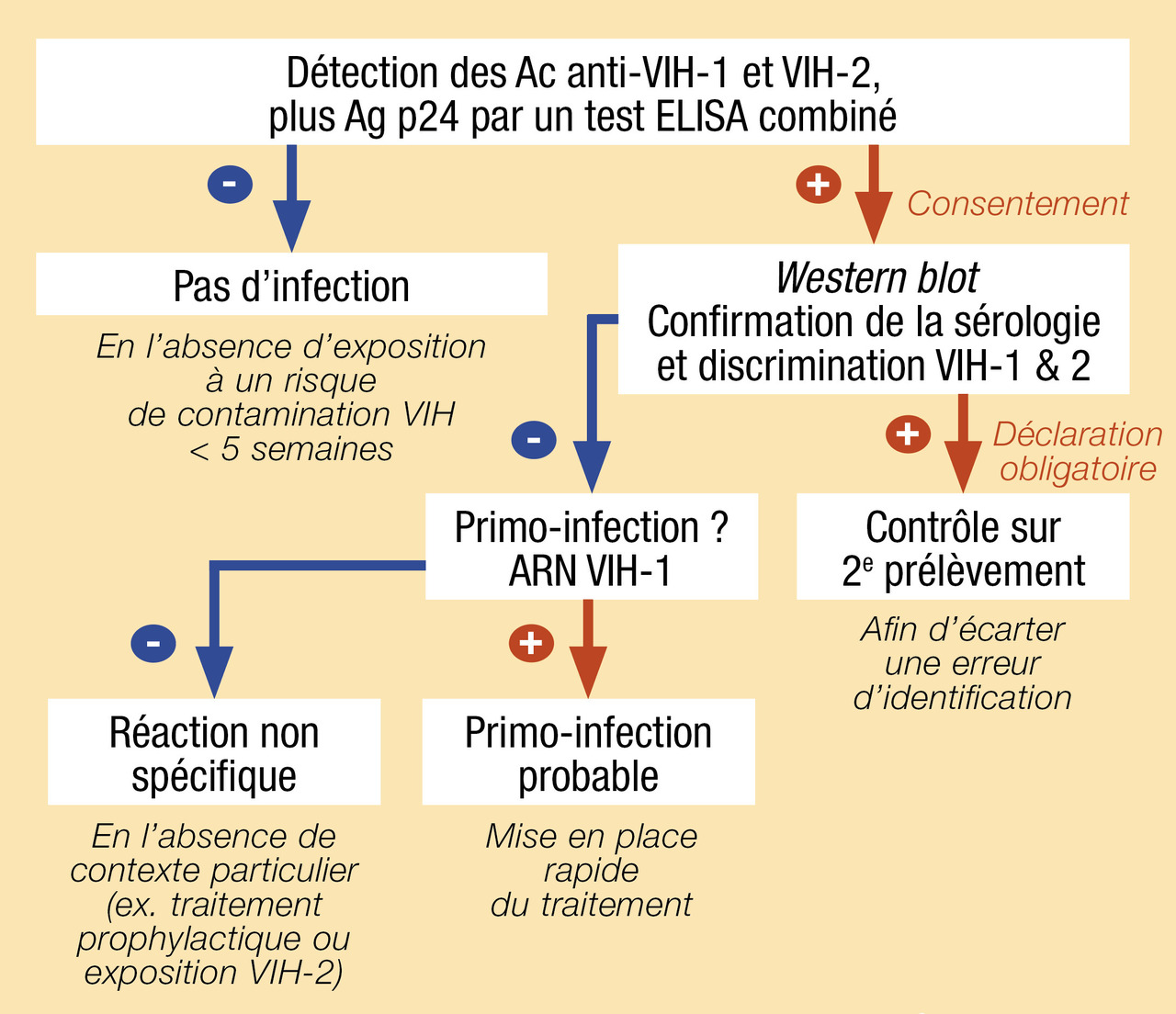
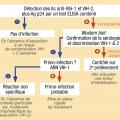
Le diagnostic biologique de l’infection par VIH repose en France sur un test immunologique mixte, combiné de type ELISA permettant la détection simultanée des anticorps anti-VIH-1 et anti- VIH-2 et de l’antigène (Ag) p24 du VIH-1. La détection de l’Ag p24 permet de réduire la fenêtre sérologique lors de la primo-infection. Les tests rapides d’orientation diagnostique et autotests réalisables en moins de 15 minutes sur sang veineux ou capillaire offrent une alternative aux tests de laboratoire. Les tests rapides d’orientation diagnostique et autotests détectent les anticorps anti-VIH-1 et anti- VIH-2 et sont équivalents en termes de performances aux tests ELISA combinés pour le diagnostic des infections en phase chronique mais leur sensibilité est très faible en situation de primo-infection en raison de l’absence de détection de l’Ag p24.
En cas de dépistage positif par ELISA, le diagnostic sérologique doit être confirmé par un test de type western blot ou immunoblot qui détecte des anticorps dirigés contre différentes protéines du VIH et se positive progressivement à partir du 25e jour après la contamination. Un western blot négatif signifie donc soit un faux positif du test ELISA, soit une primo-infection très récente. S’il y a des arguments cliniques ou épidémiologiques pour une primo-infection à VIH, les explorations doivent être complétées par une mesure de l’ARN VIH plasmatique. La confirmation par western blot permet également le plus souvent de différencier les infections VIH-1 et VIH-2. En cas de positivité du western blot, un contrôle sur un 2e prélèvement est requis pour écarter tout risque d’erreur d’identification des tubes de sang. La stratégie de diagnostic biologique de l’infection à VIH est décrite sur la
Un consentement éclairé de la personne testée est requis pour le dépistage de l’infection à VIH. L’obtention de l’accord verbal du patient est indispensable au dépistage sauf s’il y a urgence au diagnostic (accident d’exposition aux liquides biologiques ou suspicion de sida) et impossibilité physique pour le patient de donner son consentement (confusion ou coma). La proposition de dépistage doit s’accompagner d’une information sur le motif du dépistage (présence de facteurs de risque ou de symptômes), sur les mesures de prévention de l’infection à VIH et sur la prise en charge d’une éventuelle infection.
Lors du rendu d’un résultat négatif, le post-test counseling est l’occasion d’inscrire le consultant dans un processus de prévention et de réduction des risques. Il faut rappeler que ce résultat ne vaut que pour le jour où la prise de sang a été réalisée, que la sensibilité des tests n’est pas totale en cas de contamination datant moins de 5 semaines pour un dépistage par test ELISA combiné et de 3 mois par tests rapides d’orientation diagnostique, et renouveler l’information sur les mesures de prévention du VIH et des infections sexuellement transmissibles.
Le rendu d’un résultat positif doit s’accompagner d’informations sur :
- les modalités de suivi et le bon pronostic sous traitement antirétroviral ;
- les mesures de prévention vis-à-vis des partenaires sexuels ; il faut conseiller au sujet de les informer ; la préservation du secret médical et le respect de la confidentialité priment, les soignants ne peuvent informer eux-mêmes les partenaires sexuels de la personne ayant appris sa séropositivité sauf demande expresse de celle-ci et en sa présence ;
- les possibilités de procréation.
Il ne faut pas omettre le protocole de prise en charge en ALD (affection de longue durée) et la déclaration obligatoire anonyme aux agences régionales de santé qui transmettent ensuite les notifications à Santé publique France.
Primo-infection par le VIH
Tout tableau fébrile inexpliqué doit faire évoquer le diagnostic de primo-infection à VIH.
Le diagnostic de la primo-infection se fait par la sérologie mettant en évidence une positivité des tests de dépistage ELISA combinés et un western blot négatif ou incomplet. La quantification de l’ARN VIH plasmatique complète la démarche de diagnostic de la primo-infection (
Principales complications infectieuses associées au VIH. Diagnostic et prévention
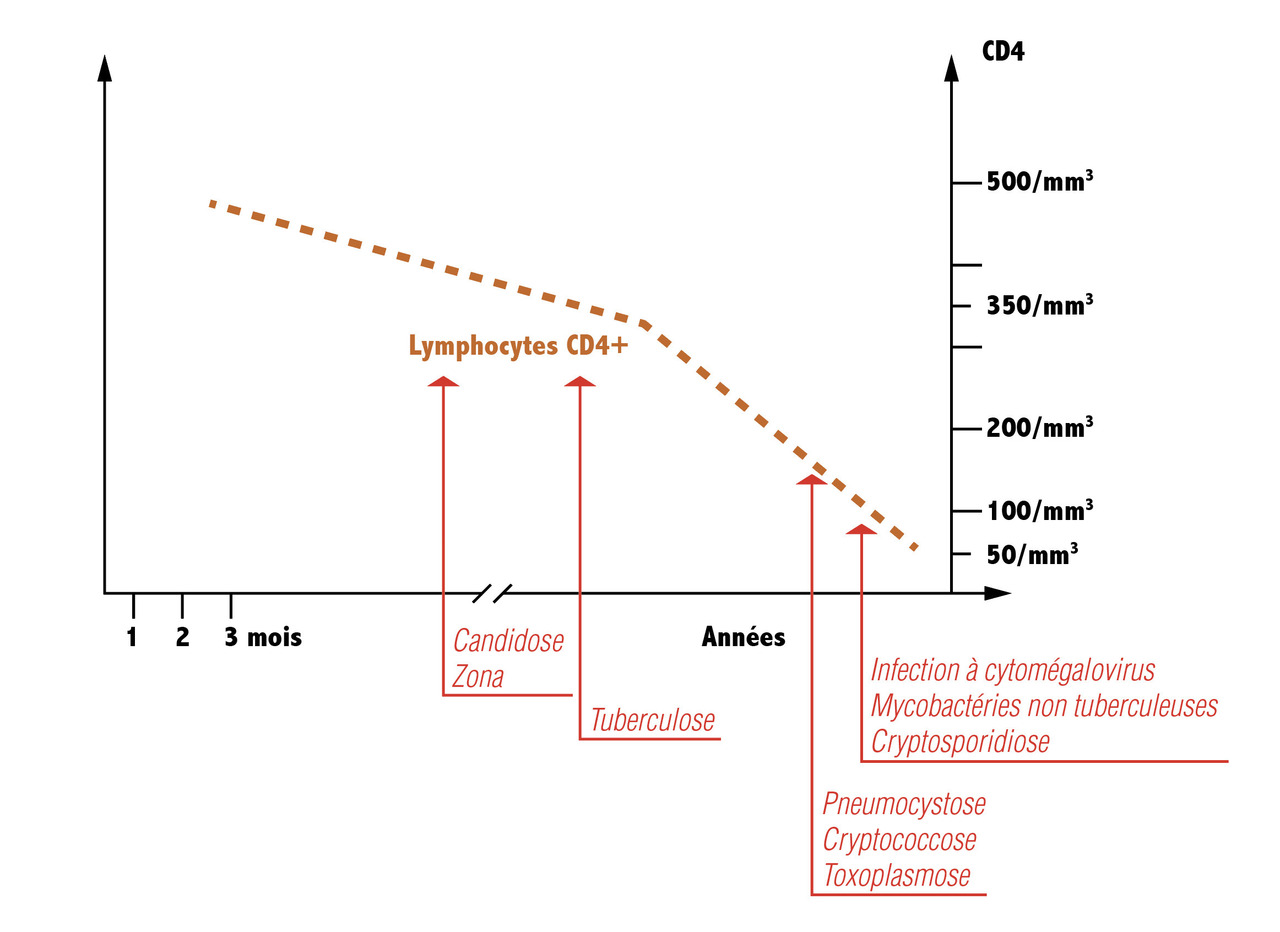
Infections opportunistes
Tuberculose (v. Item 155 )
Les signes et symptômes de la tuberculose maladie au cours de l’infection à VIH sont peu différents de ceux observés chez le sujet non infecté par le VIH. Elle peut survenir à des taux de CD4 élevés. Sa prévention primaire repose sur le dépistage et le traitement de l’infection tuberculeuse latenteCandidoses muqueuses
La candidose orale est fréquente, y compris à des taux de CD4 élevés. Sa présentation est le plus souvent celle d’un muguet. La candidose œsophagienne survient plus tardivement et se manifeste par l’association d’une candidose orale et d’une dysphagie basse souvent douloureuse. Le diagnostic est clinique, il peut être confirmé par l’aspect caractéristique et des biopsies lors d’une endoscopie digestive haute.Zona
Le zona est fréquent au cours de l’infection à VIH, souvent à des taux de CD4 élevés. La survenue d’un zona chez un sujet jeune doit faire proposer un test VIH. Sa présentation est parfois extensive avec une extension multimétamérique.Pneumocystose pulmonaire
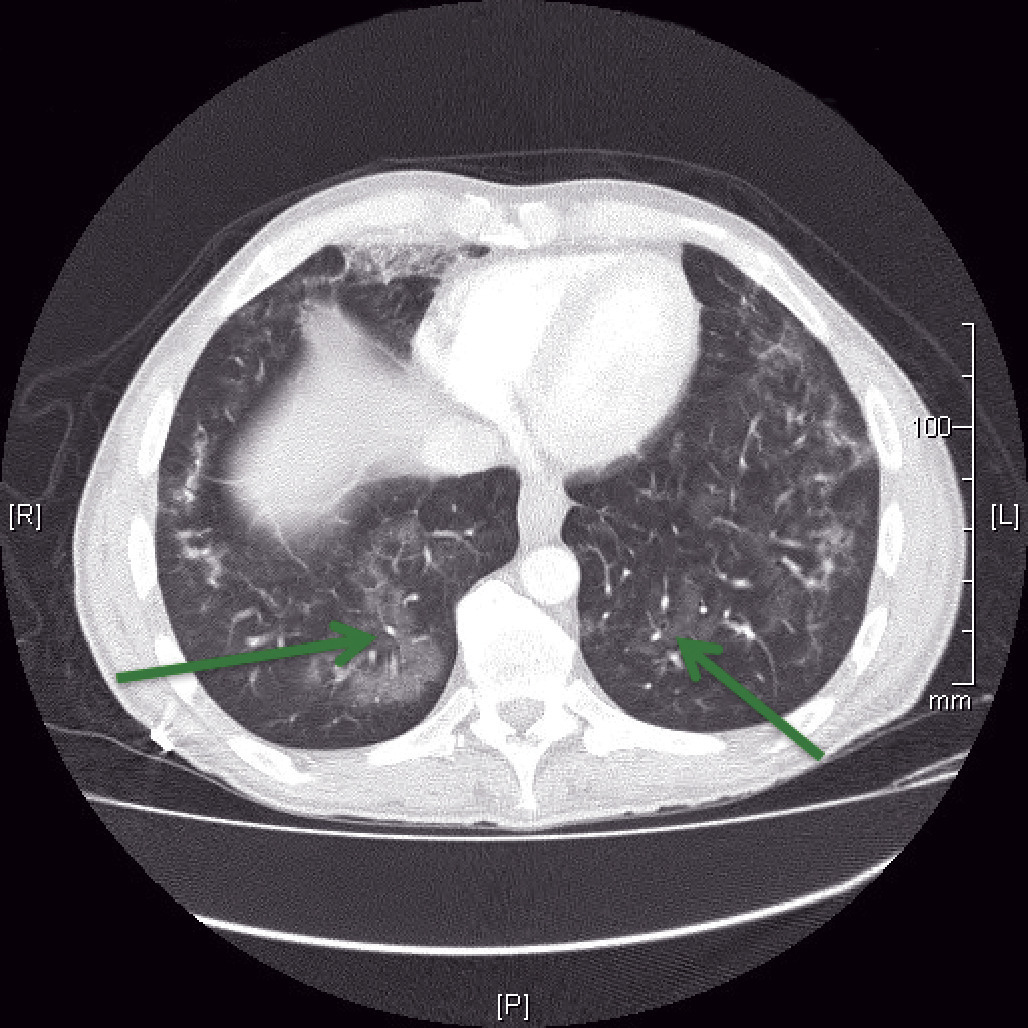
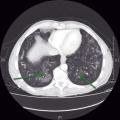
Sa présentation est celle d’une pneumopathie interstitielle d’installation progressive avec souvent une hypoxémie marquée au moment de la prise en charge. L’aspect tomodensitométrique est celui d’une pneumopathie diffuse avec aspect en verre dépoli (Toxoplasmose cérébrale
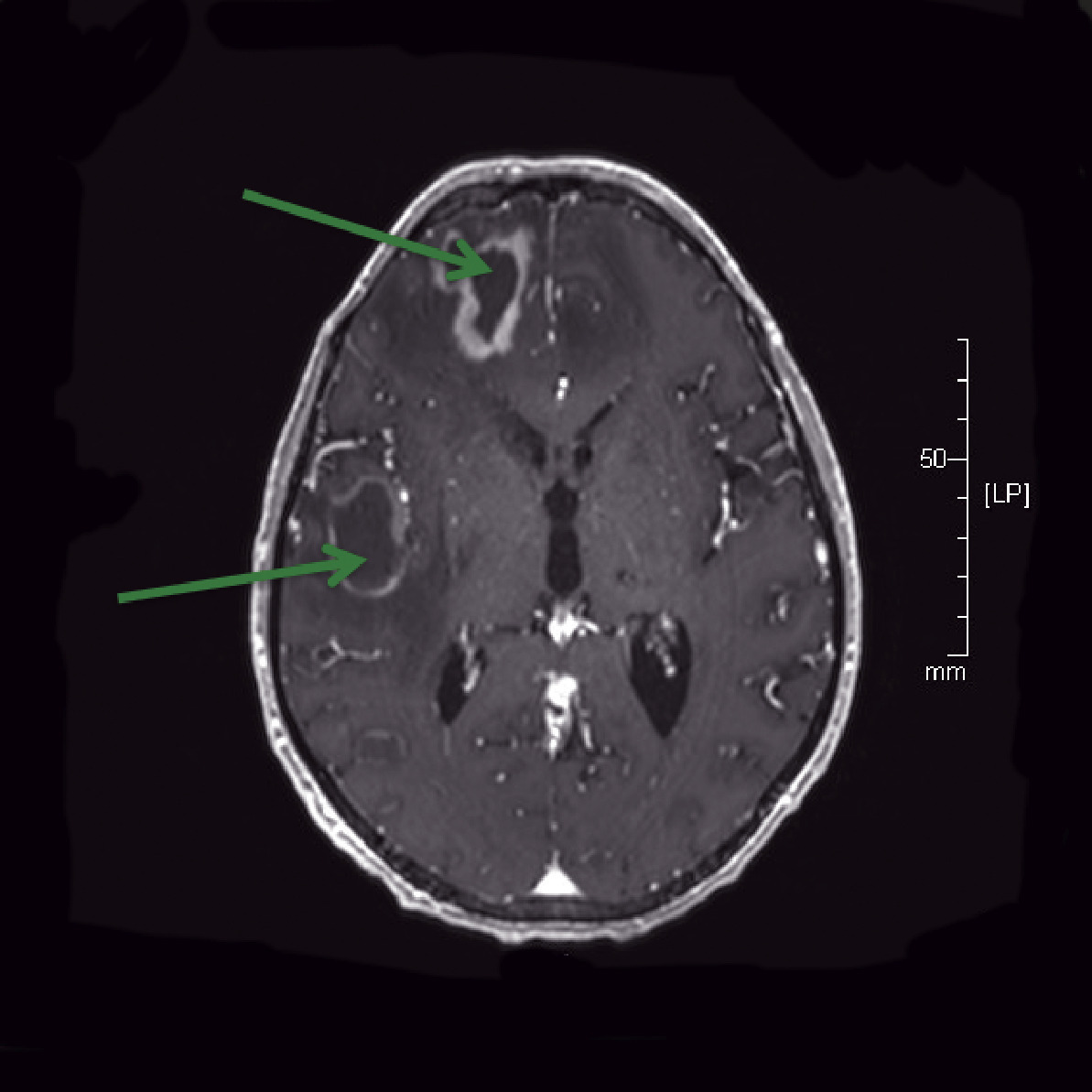
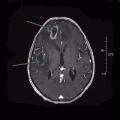
Les abcès cérébraux sont dus à la réactivation de kystes de Toxoplasma gondii acquis lors d’une primo-infection antérieure. La présentation clinique est celle d’une encéphalite avec des troubles neurologiques centraux, et fréquemment un déficit focalisé et/ou une confusion, fébrile. Le diagnostic est évoqué par l’imagerie cérébrale, de préférence par résonance magnétique, qui montre des lésions, le plus souvent multiples, en cocarde, avec une lésion de tonalité hydrique nécrotique centrale, une coque renforcée par l’injection de produit de contraste et un halo périphérique de densité hydrique lié à l’œdème (La confirmation diagnostique repose le plus souvent sur l’évolution favorable de l’imagerie sous traitement antiparasitaire, qui constitue un test thérapeutique. En l’absence d’amélioration à 3 semaines, une biopsie cérébrale stéréotaxique est indiquée. Si la ponction lombaire n’est pas contre-indiquée par l’effet de masse, on peut réaliser une PCR dans le liquide, très spécifique mais peu sensible.
Cryptococcose neuroméningée
Le tableau clinique est celui de céphalées souvent fébriles d’installation progressive, elles sont liées à l’hypertension intracrânienne qui fait toute la gravité de la maladie. Le diagnostic est confirmé par la positivité de l’antigène cryptococcique dans le sang et le liquide. Le champignon Cryptococcus neoformans, est mis en évidence à l’examen direct par la coloration à l’encre de Chine et par la recherche de l’antigène cryptococcique. La réaction cellulaire du liquide céphalo-rachidien est souvent modérée, voire absente.Autres infections
Pneumonies à pneumocoque
Les pneumonies à pneumocoque sont plus fréquentes au cours de l’infection VIH, y compris chez les patients ayant une restauration immunitaire sous traitement antirétroviral. Leur présentation ne présente pas de particularité liée au VIH (Infections sexuellement transmissibles et hépatite A
Du fait de modes de contamination communs, les infections sexuellement transmissibles et l’hépatite A sont plus fréquentes au cours de l’infection à VIH, notamment chez les hommes ayant des relations sexuelles avec des hommes. Leur dépistage systématique (sérologie syphilitique annuelle, PCR gonocoque et Chlamydia régulières) est recommandé en cas de conduites à risque. La vaccination contre l’hépatite A est souhaitable chez les hommes ayant des relations sexuelles avec des hommes.Hépatites virales B et C
Les co-infections par les virus des hépatites B (antigène HBs [AgHBs], anticorps anti-HBs et anti-HBc) et C (anticorps anti- HCV) doivent être recherchées dès le diagnostic de VIH car elles sont fréquentes (en France : antigène HBs positif : 7 % ; sérologie VHC positive 20 %) et modifient la prise en charge. La recherche de la co-infection par le virus delta est nécessaire en cas de positivité de l’AgHBs. En cas de co-infection VIH-VHB, le traitement antirétroviral doit comprendre du ténofovir, molécule active sur les deux virus.La prévention de l’hépatite B repose sur la vaccination qui doit être systématiquement proposée si la sérologie VHB est négative et repose sur un schéma renforcé à double dose.
L’incidence de l’hépatite C aiguë est actuellement élevée chez les hommes ayant des relations sexuelles avec des hommes infectés par le VIH du fait d’une transmission sexuelle ou par usage de drogues injectées. Elle doit être dépistée régulièrement dans cette population, par sérologie, ou par PCR si la sérologie est positive du fait d’un antécédent d’infection antérieure guérie qui ne protège pas contre le risque de réinfection.
Principales complications non infectieuses associées au VIH. Diagnostic et prévention
L’incidence de la plupart de ces complications non infectieuses diminue avec l’instauration de plus en plus précoce du traitement antirétroviral associée à une meilleure restauration de l’immunité cellulaire. De nombreuses complications cancéreuses et cardiovasculaires sont liées à des comportements à risque (tabac, alcool…) qu’il faut encourager à modifier.
Cancers
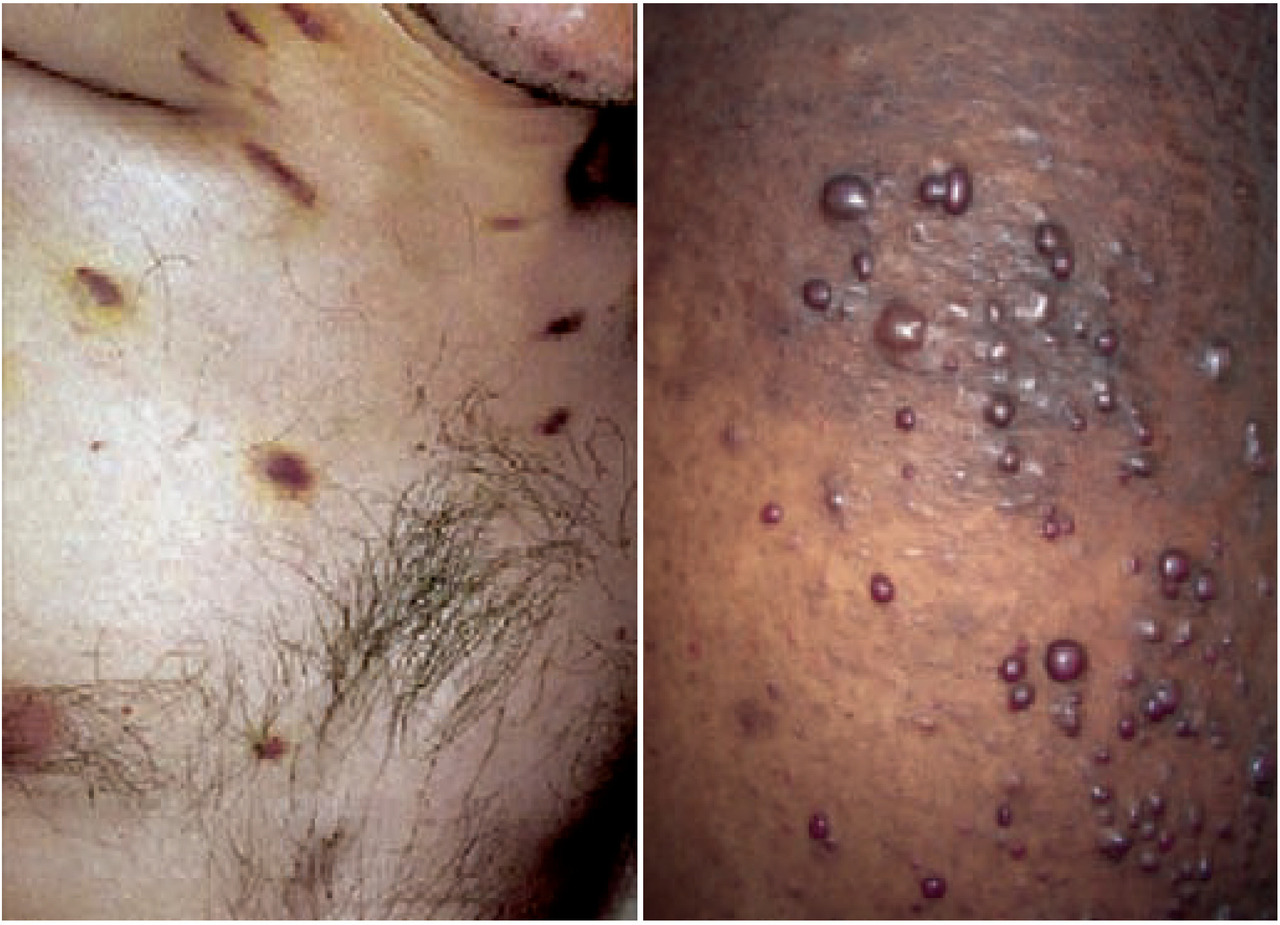
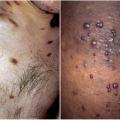
La maladie de Kaposi (MK) est liée au pouvoir oncogène du virus du groupe Herpès HHV-8, une prolifération de cellules endothéliales et de cellules fusiformes. Dans les pays riches, la maladie de Kaposi touche préférentiellement les hommes ayant des relations sexuelles avec des hommes, alors qu’en Afrique, toutes les personnes vivant avec le VIH peuvent être atteintes. Les formes cutanéo-muqueuses sont les plus fréquentes, réalisant des nodules ou des plaques, violacés, infiltrés (
Les lymphomes non hodgkiniens sont la deuxième cause de mortalité par cancer chez les personnes vivant avec le VIH en France. Il s’agit principalement de lymphomes B à grandes cellules, le plus souvent associés à la prolifération de lymphocytes B infectés par le virus d'Epstein-Barr (EBV). Les lymphomes de Burkitt surviennent habituellement à des taux de lymphocytes CD4 > 200/mm3. Les lymphomes cérébraux surviennent généralement à des taux de lymphocytes CD4 < 100/mm3. Pour les lymphomes à grandes cellules, les caractéristiques immunovirologiques des patients sont très variables, mais ils sont rares chez les personnes vivant avec le VIH traitées efficacement.
L’infection par les papillomavirus humains (HPV), en particulier à haut risque (principalement de génotype 16 ou 18), est responsable des lésions précancéreuses et du cancer du col de l’utérus. Ce cancer est plus fréquent chez les femmes vivant avec le VIH comparativement à la population générale. Il est recommandé de réaliser un frottis cervical annuel chez les femmes vivant avec le VIH (tous les 6 mois si le taux de lymphocytes TCD4 < 200/mm3).
Certains cancers non classant sida ont une incidence plus élevée chez les personnes vivant avec le VIH, en raison de la co- infection par des virus pro-oncogènes (par exemple HPV et cancer anal, EBV et lymphome de Hodgkin), ou de l’effet de l’immunodépression (cancer broncho-pulmonaire, mais le rôle du tabac est essentiel). Le cancer bronchopulmonaire est maintenant la première cause de décès par cancer chez les personnes vivant avec le VIH. Les lymphomes de Hodgkin, qui représentent 40 % des lymphomes chez les personnes vivant avec le VIH et sont liés à l’EBV dans 80 % des cas, ont un pic d’incidence pour les sujets avec un taux de lymphocytes CD4 autour de 200 cellules/mm3.
Autres complications non infectieuses
Le VIH lui-même peut être responsable de complications. Il s’agit de manifestations neurologiques (encéphalite, myélite et polynévrite sensitive), hématologiques (thrombopénie périphérique) ou rénales (néphropathie glomérulaire liée au VIH, qui est plus fréquente chez les personnes d’origine africaine).
Enfin, les manifestations du vieillissement apparaissent plus fréquentes ou plus précoces chez les personnes vivant avec le VIH, principalement celles qui ont été infectées dans les années 1980-90. Ces manifestations pourraient être la conséquence d’une activation immune prolongée. Il s’agit d’artériopathies, notamment coronariennes, d’ostéoporose et de troubles cognitifs
Grands principes du traitement antirétroviral, de son suivi et de son observance
Principes et modalités du traitement antirétroviral
- 2 inhibiteurs de la transcriptase inverse + 1 inhibiteur de protéase (IP) ;
- 2 inhibiteurs de la transcriptase inverse + 1 inhibiteur de l’intégrase (II) ;
- 2 inhibiteurs de la transcriptase inverse + 1 inhibiteur non nucléosidique de la transcriptase inverse (INNTI).
L’objectif du traitement antirétroviral est d’empêcher la progression vers le sida et le décès en maintenant ou en restaurant un nombre de CD4 > 500/mm3. Pour atteindre ce but, le traitement antirétroviral doit rendre la charge virale ARN VIH (CV) plasmatique indétectable (< 50 copies/mL) et la maintenir telle tout au long de la vie du patient. Le choix de la combinaison est pris en fonction du profil de résistance aux antirétroviraux sur le génotypage de résistance, de la fonction rénale (contre-indication du ténofovir en cas d’insuffisance rénale), de la présence de l’allèle HLA-B5701 (contre-indication de l’abacavir en raison d’un risque d’hypersensibilité grave), et de l’existence d’interactions médicamenteuses. Le choix doit être discuté avec le patient, et la place de l’éducation thérapeutique est essentielle. Les indications d’instauration du traitement sont énumérées dans le
Au cours des premiers mois de traitement, il convient de réaliser une mesure de la charge virale plasmatique :
- à M1, où elle doit avoir baissé d’au moins de 2 log copies/mL ;
- à M3, où elle doit être < 400 copies/mL ;
- à M6, où elle doit être < 50 copies/mL.
Gestion des risques liés au traitement antirétroviral
Le ténofovir peut induire une tubulopathie rénale qui peut être dépistée au cours du bilan de suivi (
La toxicité mitochondriale est liée à la classe des inhibiteurs de la transcriptase inverse qui ont une action inhibitrice sur la transcriptase inverse et sur la polymérase gamma de l’ADN mitochondrial de la cellule hôte. Il peut en résulter une pancréatite aiguë, des neuropathies périphériques et c’est l’un des mécanismes incriminés dans la lipodystrophie, une modification de la répartition du tissu adipeux corporel. Avec les inhibiteurs de la transcriptase inverse les plus récents, la survenue de cette complication est exceptionnelle, mais de nombreux patients traités dans les années 1990 conservent des séquelles d’expositions antérieures à des molécules plus toxiques.
Certains traitements, l’éfavirenz et le dolutégravir, ont été incriminés dans la survenue de troubles neuropsychiques, agitation, dépression, troubles du sommeil.
Infection par le VIH et grossesse
Il est recommandé de débuter le traitement antirétroviral avant conception ou dès le 1er trimestre en associant deux inhibiteurs de la transcriptase inverse et un inhibiteur de protéase. L’accouchement par voie basse est réalisé si la charge virale est < 50 copies/mL à 38 semaines d’aménorrhée (SA). Hors nécessités obstétricales, la césarienne est réservée aux femmes avec une charge virale > 400 copies/mL. Une prophylaxie pendant l’accouchement par zidovudine intraveineuse est indiquée si la charge virale est > 400 copies/mL au bilan des 34-36 SA. Cette prophylaxie est systématique quelle que soit la charge virale en cas de chorio-amniotite, d’hémorragies antepartum, et d’accouchement prématuré. Dans les pays riches, l’allaitement est contre-indiqué, même sous traitement antirétroviral.
Le nouveau-né reçoit un traitement antirétroviral post-exposition par névirapine pendant 2 semaines ou zidovudine pendant 4 semaines si le virus est résistant à la névirapine. Ce traitement est renforcé (zidovudine, lamivudine et névirapine ou lopinavir) en cas de charge virale > 400 copies/mL en fin de grossesse ou d’autre facteur associé à un risque élevé de transmission.
Le dépistage de l’infection par le VIH dans les populations clés, hommes ayant des relations sexuelles avec des hommes et personnes originaires d’Afrique subsaharienne, doit être réalisé à intervalles réguliers.
La prévention de l’infection par le VIH repose principalement sur les mesures barrières (préservatifs), la mise à disposition de matériel d’injection à usage unique pour les usagers de drogue et le traitement antirétroviral des personnes infectées et des personnes à haut risque d’infection (prophylaxie pré-exposition).
L’indication des antirétroviraux est universelle chez les personnes vivant avec le VIH.
Le traitement antirétroviral de première intention repose sur l’association de deux inhibiteurs nucléosidiques de la transcriptase inverse et d’un troisième agent qui est soit un inhibiteur non nucléosidique de la transcriptase inverse, soit un inhibiteur de protéase potentialisé par le ritonavir, soit un inhibiteur d’intégrase.
L’observance régulière du traitement est la principale clé du succès du traitement antirétroviral dont l’objectif est de rendre la charge virale ARN VIH plasmatique indétectable et de la maintenir telle tout au long de la vie.
L’effet du traitement antirétroviral est uniquement suspensif ; il ne permet pas la guérison de l’infection.
La pneumocystose pulmonaire, la tuberculose et la toxoplasmose cérébrale restent des infections opportunistes fréquentes que tout médecin doit savoir reconnaître rapidement.
Message de l'auteur
Un dossier de primo-infection par le VIH, diagnostics différentiels (autres primo-infections), difficultés du diagnostic biologique, prise en charge, mesures sociales (prise en charge en affection de longue durée, déclaration obligatoire anonyme), conseils vis-à-vis de l’entourage en respectant le secret médical.
Une situation requérant la proposition d’un dépistage de l’infection VIH, appartenance à une population clé, infection opportuniste, infection sexuellement transmise.
La prise en charge d’une personne chez qui on vient de diagnostiquer une infection VIH, indication et modalités du traitement antirétroviral (avec nécessité de connaître les principales molécules appartenant aux quatre principales familles d’antirétroviraux, inhibiteurs nucléosidiques de la transcriptase inverse, inhibiteurs non nucléosidiques de la transcriptase inverse, inhibiteurs de protéase, inhibiteurs d’intégrase), indication et modalités des préventions primaires et secondaires des principales infections, modalités de surveillance.
Les contre-indications à l’abacavir (phénotype HLA B57*01) et au ténofovir (insuffisance rénale).
Un dossier décrivant la présentation clinique habituelle d’une des principales infections opportunistes, pneumocystose pulmonaire, tuberculose pulmonaire, toxoplasmose cérébrale et cryptococcose neuroméningée et demandant la prise en charge diagnostique.
Un dossier de découverte de l’infection VIH chez une femme enceinte et demandant d’expliquer les risques de transmission du VIH à l’enfant et les moyens de la prévenir.
Dans cet article
- Éléments de physiopathologie
- Prévention de la transmission sexuelle et sanguine du VIH
- Indication du dépistage de l’infection à VIH
- Diagnostic de l’infection à VIH
- Primo-infection par le VIH
- Principales complications infectieuses associées au VIH. Diagnostic et prévention
- Principales complications non infectieuses associées au VIH. Diagnostic et prévention
- Grands principes du traitement antirétroviral, de son suivi et de son observance
- Infection par le VIH et grossesse

 Encadrés
Encadrés