FOCUS
L’insuffisance cardiaque (IC) à fraction d’éjection ventriculaire gauche (FEVG) préservée (IC-FEP) est un problème croissant du fait du vieillissement de la population et des progrès thérapeutiques. Elle concerne environ 50 % des insuffisants cardiaques. Elle associe symptômes et/ou signes d’IC, FEVG ≥ 50 %, élévation des peptides natriurétiques (BNP > 25 pg/mL ou NTproBNP > 125 pg/mL) et au moins 1 des 2 facteurs suivants : anomalie cardiaque structurale (hypertrophie myocardique et/ou dilatation de l’oreillette gauche) et/ou altération de la fonction diastolique.1 Elle répond à des mécanismes complexes d’adaptation systémique et cardiaque qui varient au cours du temps. Elle se manifeste par de multiples phénotypes cliniques et biologiques, et s’accompagne de nombreuses comorbidités, en particulier chez le sujet âgé. Cette grande variété explique pourquoi la thérapeutique est compliquée.2
L’insuffisance cardiaque (IC) à fraction d’éjection ventriculaire gauche (FEVG) préservée (IC-FEP) est un problème croissant du fait du vieillissement de la population et des progrès thérapeutiques. Elle concerne environ 50 % des insuffisants cardiaques. Elle associe symptômes et/ou signes d’IC, FEVG ≥ 50 %, élévation des peptides natriurétiques (BNP > 25 pg/mL ou NTproBNP > 125 pg/mL) et au moins 1 des 2 facteurs suivants : anomalie cardiaque structurale (hypertrophie myocardique et/ou dilatation de l’oreillette gauche) et/ou altération de la fonction diastolique.1 Elle répond à des mécanismes complexes d’adaptation systémique et cardiaque qui varient au cours du temps. Elle se manifeste par de multiples phénotypes cliniques et biologiques, et s’accompagne de nombreuses comorbidités, en particulier chez le sujet âgé. Cette grande variété explique pourquoi la thérapeutique est compliquée.2
Approches thérapeutiques
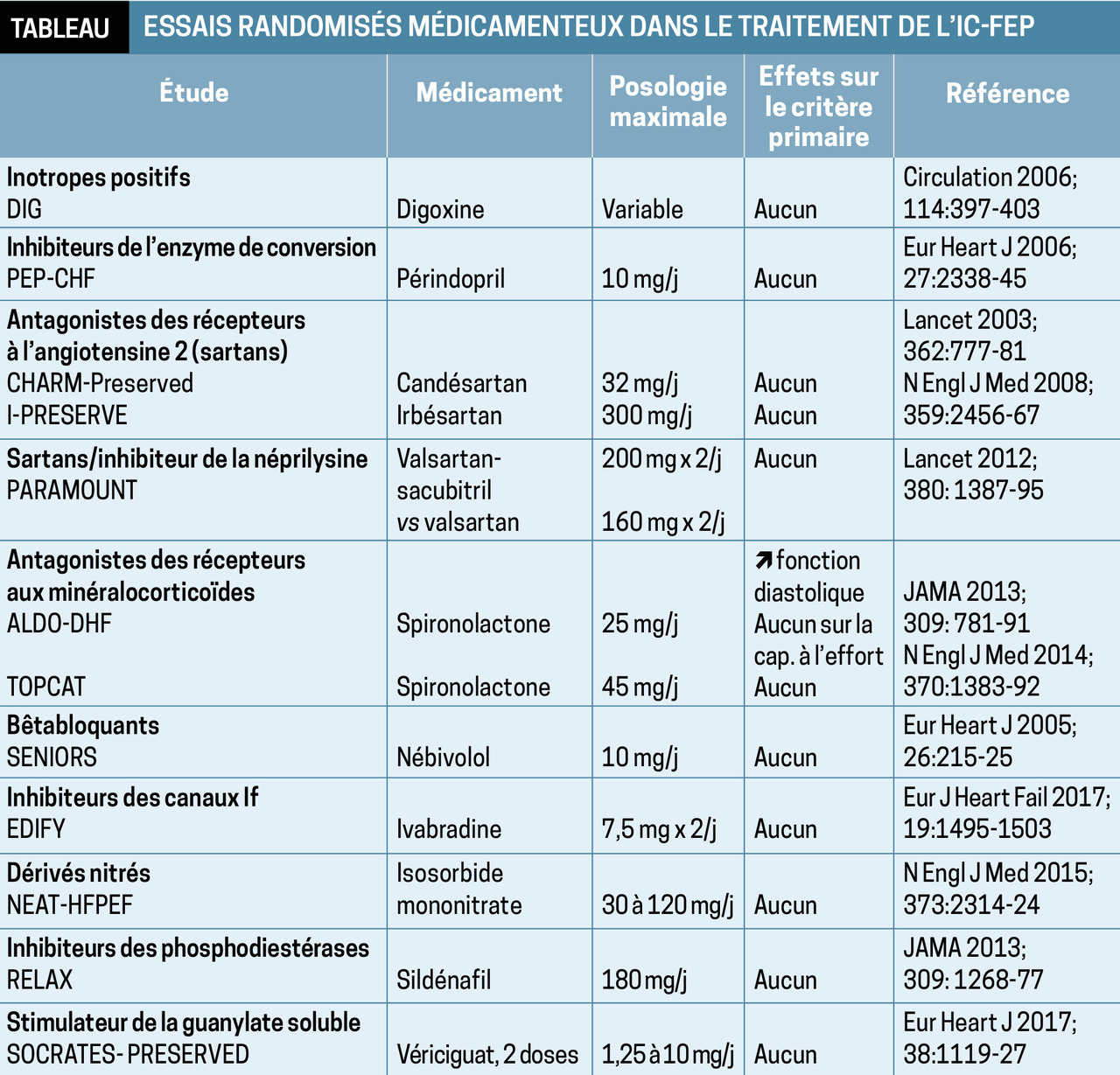
D’après diverses études épidémiologiques, l’évolution des traitements médicamenteux de l’IC au cours des dernières décennies n’a permis aucune amélioration du pronostic de l’IC-FEP, contrairement à celui de l’IC systolique.3 Or de grands essais ont testé les classes efficaces en termes de réduction de la morbi-mortalité dans l’IC systolique.
Malheureusement, tous se sont avérés négatifs (tableau ), ne montrant aucun gain sur les critères primaires. Ainsi, la digoxine, les inhibiteurs de l’enzyme de conversion (IEC), les antagonistes des récepteurs à l’angiotensine 2 (sartans), les bbloquants, les antagonistes des récepteurs aux minéralocorticoïdes, les inhibiteurs des canaux If ont connu des échecs retentissants, d’où l’absence de recommandations d’une quelconque classe hormis celle des diurétiques.
Des explications sont avancées : prises en charge variables selon les pays, différences dans le type et la fréquence des comorbidités associées mais également dans la sélection des malades (le diagnostic de certitude étant difficile), et dans l’organisation des systèmes de soins locaux pour ce type de pathologie. Il apparaît difficile de cibler avec précision les patients concernés du fait des comorbidités très variées, parfois multiples, notamment chez les sujets âgés. Ainsi les malades inclus dans les grands essais aux critères de sélection trop stricts pour des populations très hétérogènes ne seraient guère représentatifs de ceux de la vraie vie. Dans les analyses de cohortes observationnelles (méta-analyses ou analyses de propensité permettant de comparer les médicaments à partir de données de suivi), IEC et bbloquants ont des effets plutôt encourageants sur des critères durs de mortalité ou d’hospitalisations pour IC.
Ainsi, l’éducation thérapeutique prend toute sa place, elle a des résultats très positifs et doit être encouragée. Elle réduit la mortalité, indépendamment du traitement utilisé.4
La sédentarité et le manque d’activité physique sont responsables d’anomalies musculaires cardiaques et squelettiques induisant une dysfonction diastolique. Une activité physique modérée pourrait avoir un rôle protecteur vis-à-vis des déterminants physiopathologiques de l’IC-FEP.
Malheureusement, tous se sont avérés négatifs (
Des explications sont avancées : prises en charge variables selon les pays, différences dans le type et la fréquence des comorbidités associées mais également dans la sélection des malades (le diagnostic de certitude étant difficile), et dans l’organisation des systèmes de soins locaux pour ce type de pathologie. Il apparaît difficile de cibler avec précision les patients concernés du fait des comorbidités très variées, parfois multiples, notamment chez les sujets âgés. Ainsi les malades inclus dans les grands essais aux critères de sélection trop stricts pour des populations très hétérogènes ne seraient guère représentatifs de ceux de la vraie vie. Dans les analyses de cohortes observationnelles (méta-analyses ou analyses de propensité permettant de comparer les médicaments à partir de données de suivi), IEC et bbloquants ont des effets plutôt encourageants sur des critères durs de mortalité ou d’hospitalisations pour IC.
Ainsi, l’éducation thérapeutique prend toute sa place, elle a des résultats très positifs et doit être encouragée. Elle réduit la mortalité, indépendamment du traitement utilisé.4
La sédentarité et le manque d’activité physique sont responsables d’anomalies musculaires cardiaques et squelettiques induisant une dysfonction diastolique. Une activité physique modérée pourrait avoir un rôle protecteur vis-à-vis des déterminants physiopathologiques de l’IC-FEP.
Quelles recommandations ?
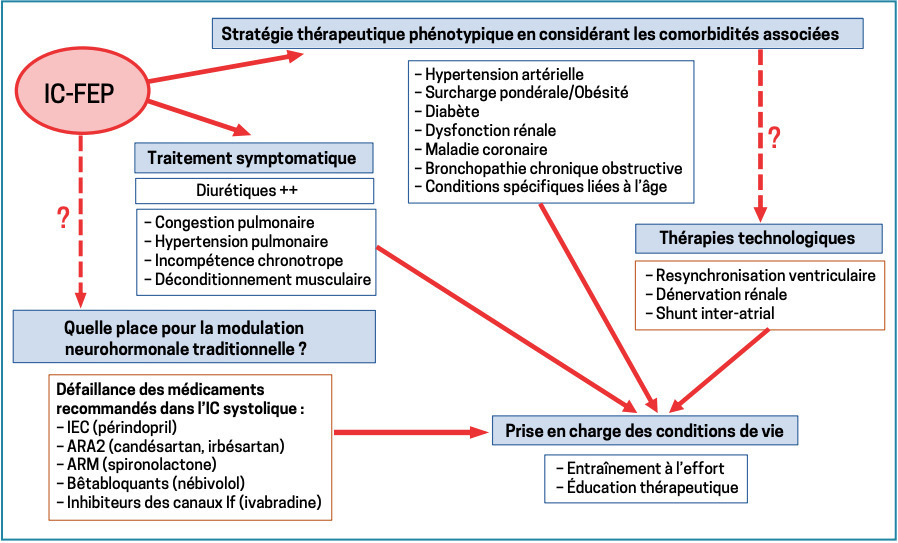
Compte tenu des nombreuses comorbidités et de la grande variété de mécanismes et voies biologiques impliquées, il est évident qu’une seule classe médicamenteuse ne peut être efficace. La thérapeutique doit prendre en compte les différentes entités contribuant à l’IC-FEP (figure ). Comme les patients sont souvent âgés et symptomatiques, avec une altération très significative de leur qualité de vie, le but principal du traitement doit être d’alléger les symptômes et d’améliorer le bien-être.1, 2
Les recommandations européennes proposent une stratégie simple.1 En cas de surcharge volumique, on doit prescrire des diurétiques (classe I, niveau de preuve B). Il faut ensuite traiter toutes les conditions pathologiques coexistantes séparément de façon appropriée (classe I, niveau de preuve C). Dans une troisième étape, il est crucial d’éduquer les patients à connaître leur maladie et sa gestion, en y associant un réentraînement à l’effort.
Les recommandations européennes proposent une stratégie simple.1 En cas de surcharge volumique, on doit prescrire des diurétiques (classe I, niveau de preuve B). Il faut ensuite traiter toutes les conditions pathologiques coexistantes séparément de façon appropriée (classe I, niveau de preuve C). Dans une troisième étape, il est crucial d’éduquer les patients à connaître leur maladie et sa gestion, en y associant un réentraînement à l’effort.
Espoirs futurs
De nouvelles approches sont testées : la voie des peptides natriurétiques (inhibiteurs de la néprilysine), la stimulation par l’oxyde nitrique, puissant vasodilatateur (dérivés nitrés, inhibiteurs des phosphodiestérases), ou bien d’autres voies prometteuses comme celle de l’inflammation systémique, la dysfonction endothéliale et microvasculaire, la signalisation de l’axe GMP cyclique- protéine kinase G (stimulateurs directs de la guanylate cyclase soluble).
Parmi les thérapeutiques non médicamenteuses, la prise en charge d’une désynchronisation électrique par un stimulateur triple chambre, le contrôle d’une HTA par dénervation rénale ont déjà été évalués. C’est peut-être surtout la prise en compte de l’intolérance à l’effort qui pourrait bénéficier de techniques invasives. Ainsi, il est possible de réduire l’augmentation de pression intra-auriculaire gauche à l’effort (décharge dans l’oreillette droite) par la création percutanée d’un shunt iatrogénique gauche-droit interatrial.5 Le suivi à 1 an est encourageant.
Pathologie complexe, elle est liée étroitement aux comorbidités.
Aucun médicament recommandé, à l’exception des diurétiques si surcharge volumique.
Privilégier l’éducation thérapeutique et l’activité physique.
Parmi les thérapeutiques non médicamenteuses, la prise en charge d’une désynchronisation électrique par un stimulateur triple chambre, le contrôle d’une HTA par dénervation rénale ont déjà été évalués. C’est peut-être surtout la prise en compte de l’intolérance à l’effort qui pourrait bénéficier de techniques invasives. Ainsi, il est possible de réduire l’augmentation de pression intra-auriculaire gauche à l’effort (décharge dans l’oreillette droite) par la création percutanée d’un shunt iatrogénique gauche-droit interatrial.5 Le suivi à 1 an est encourageant.
Pathologie complexe, elle est liée étroitement aux comorbidités.
Aucun médicament recommandé, à l’exception des diurétiques si surcharge volumique.
Privilégier l’éducation thérapeutique et l’activité physique.
Références
1. Ponikowski P, Voors AA, Anker SD, et al. Guidelines for the diagnosis and treatment of acute and chronic heart failure: The Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC) developed with the special contribution of the Heart Failure Association (HFA) of the ESC. Eur Heart J 2016;18:891-975.
2. Redfield MM. Heart failure with preserved ejection fraction. N Engl J Med 2016;375:1868-77.
3. Owan TE, Hodge DO, Herges RM, Jacobsen SJ, Roger VL, Redfield MM. Trends in prevalence and outcome of heart failure with preserved ejection fraction. N Engl J Med 2006;355:251-9.
4. Agrinier N, Schockmel M, Thilly N, et al. Effectiveness of a patient education programme in heart failure with preserved ejection fraction: Results from the ODIN cohort study using propensity score matching. Arch Cardiovasc Dis 2018;111:5-16.
5. Feldman T, Mauri L, Kahwash R, et al.; REDUCE LAP-HF I Investigators. Transcatheter interatrial shunt device for the treatment of heart failure with preserved ejection fraction (REDUCE LAP-HF I): a phase 2, randomized, sham-controlled trial. Circulation 2018;137:364-75.
2. Redfield MM. Heart failure with preserved ejection fraction. N Engl J Med 2016;375:1868-77.
3. Owan TE, Hodge DO, Herges RM, Jacobsen SJ, Roger VL, Redfield MM. Trends in prevalence and outcome of heart failure with preserved ejection fraction. N Engl J Med 2006;355:251-9.
4. Agrinier N, Schockmel M, Thilly N, et al. Effectiveness of a patient education programme in heart failure with preserved ejection fraction: Results from the ODIN cohort study using propensity score matching. Arch Cardiovasc Dis 2018;111:5-16.
5. Feldman T, Mauri L, Kahwash R, et al.; REDUCE LAP-HF I Investigators. Transcatheter interatrial shunt device for the treatment of heart failure with preserved ejection fraction (REDUCE LAP-HF I): a phase 2, randomized, sham-controlled trial. Circulation 2018;137:364-75.