De quoi parle-t-on ?
Les différents types d’ACM sont classés en systèmes de courte durée, adaptés aux situations cliniques aiguës (choc cardiogénique réfractaire) et en appareillage de longue durée, destinés à être implantés chez les patients insuffisants cardiaques chroniques avancés pour une période de plusieurs mois, voire de manière définitive.
Au sein des ACM longue durée, on distingue les mono-gauche utilisés en cas de défaillance monoventriculaire gauche, et les biventriculaires. Le cœur artificiel total implantable peut être envisagé si une cardiectomie est indiquée (infection, tumeur, thrombus mural étendu, CIV post-infarctus) en attente de transplantation.
Ces 10 dernières années, les améliorations techniques, et en particulier le développement des pompes à flux continu, plus petites et durables, ont élargi l’utilisation de l’ACM mono-gauche. En Europe, 2 000 pompes sont implantées annuellement (environ 200 par an en France). La survie à 1 an est supérieure à 80 %. Ces dispositifs améliorent également la qualité de vie.
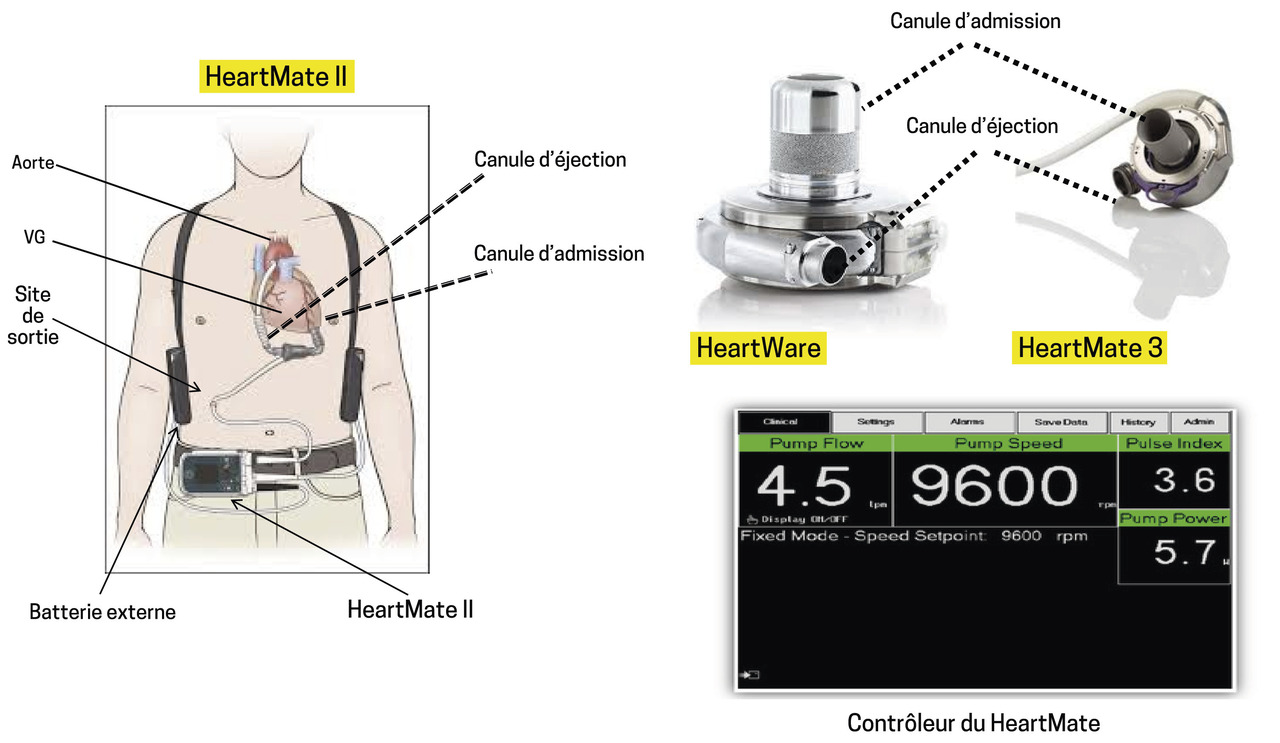
Actuellement, les 3 modèles les plus courants sont HeartWare HVAD (HeartWare International, Inc. Framingham, MA), HeartMate II et HeartMate 3 (Thoratec Corporation, Pleasanton, CA) [figure].
Comment ça marche ?
La pompe est reliée à l’apex du ventricule gauche par une canule d’admission et à l’aorte ascendante par une prothèse d’éjection en dacron. L’alimentation électrique est assurée par un câble tunnelisé sous la peau et relié à une console portative alimentée par des batteries.
Un certain nombre de paramètres sont visibles au niveau de la console ; vitesse de la pompe (pump speed), sa puissance (pump power), débit de l’assistance (pump flow) et indice de pulsatilité (pulse index) [figure].
Le câble percutané doit être fixé à la peau afin de minimiser les traumatismes et tensions au site de sortie et les infections de la machine. Le pansement est fait au moins 2 fois par semaine de manière stérile, toute zone inflammatoire doit être signalée au centre implanteur.
Les patients sous ACM mono-gauche doivent bénéficier d’un traitement anti- coagulant efficace par antivitamine K avec un objectif d’INR entre 2 et 3 et d’un antiagrégant plaquettaire, l’aspirine (81-325 mg/j). Par ailleurs, malgré l’absence de preuves scientifiques, ils reçoivent les médicaments classiques de l’IC : IEC (ou ARA II), bêtabloquants et anti-aldostérone.
Indications
On peut aussi l’envisager en cas de contre-indication potentiellement réversible à la transplantation, comme l’hypertension artérielle pulmonaire.
Idéalement, le malade doit être stabilisé, sans défaillance multiviscérale, conséquence d’un choc cardiogénique non contrôlé.
Pont à la récupération. Il s’agit d’un sujet ayant une cardiopathie avancée ischémique et/ou valvulaire, potentiellement réversible après chirurgie – par exemple, insuffisance mitrale ischémique avec coronaires pontables et zones de viabilité confirmée mais à haut risque opératoire compte tenu de l’altération de la fonction cardiaque. Le traitement chirurgical correcteur s’accompagne de la mise en place d’une ACM pour plusieurs mois, le temps que s’opère le remodelage du ventricule.
Implantation définitive ou alternative à la transplantation. Cette voie qui suscite l’enthousiasme et les recherches requiert de nombreuses innovations technologiques.
La fiabilité et la durabilité des assistances (certains patients ont été traités plus de 5 ans) ont justifié le concept d’implantation, alternative à la transplantation pour ceux ne pouvant être greffés en raison principalement d’un âge avancé, supérieur à 65 ans. Ainsi, le caractère de moins en moins invasif des ACM doit faire considérer comme candidat potentiel tout sujet ayant une contre-indication à la transplantation cardiaque.
Les contre-indications à l’ACM sont le plus souvent relatives : sepsis grave non contrôlé, défaillance multi-organes jugée irréversible, âge > 75 ans, cancer évolutif et troubles neurologiques graves.
Toute la difficulté devant une dysfonction d’organe est de déterminer si elle est potentiellement réversible après restauration d’une circulation efficace, ou si elle est irréversible, contre-indiquant l’ACM de quelque type que ce soit.
En pratique, l’intervention doit être programmée ou réalisée en urgence différée chez des malades stabilisés.
La classification INTERMACS (Interagency Registry for Mechanically Assisted Circulatory Support, registre de tous les patients américains avec ACM depuis 2006) stratifie le risque postopératoire des candidats à l’ACM [tableau]. Chaque stade, défini par la gravité clinique préopératoire, est corrélé au pronostic après implantation. Les patients INTERMACS 2, 3 et 4 sont des candidats idéals à l’assistance mécanique (alors que pour les profils 5, 6 et 7, un traitement médical est indiqué).
étant donné la mortalité importante associée au choc cardiogénique (> 50% à 1 mois) chez un sujet ayant une cardiopathie chronique avec une dysfonction VG sévère, un seul épisode de ce type suffit à envisager un bilan prétransplantation et/ou l’implantation d’une assistance de longue durée.
Bilan avant implantation : attention au ventricule droit
L’apparition d’une insuffisance ventriculaire droite après une assistance mono-gauche augmente la morbi-mortalité (19 à 43 %). Le choix du type d’assistance est important, car les patients recevant une assistance biventriculaire ou un cœur artificiel total ont un risque de décès de plus de 2 fois supérieur avant la greffe. Après celle-ci, leur survie est elle aussi diminuée comparée à celle des patients ayant un système monoventriculaire.
Les patients ayant une dysfonction globale et relevant d’une assistance biventriculaire ou d’un cœur artificiel total ne doivent pas être assistés s’ils n’ont pas de projet de greffe. Il faut leur proposer un traitement médical optimal (si échec : soins palliatifs).
La prédiction du risque d’insuffisance cardiaque droite après une assistance mono-gauche est difficile. L’évaluation du ventricule droit doit être réalisée dans la mesure du possible chez un malade stabilisé. Les critères sont cliniques, hémodynamiques et morphologiques (échographie, IRM).
2. Gustafsson F, Rogers JG. Left ventricular assist device therapy in advanced heart failure: patient selection and outcomes. Eur J Heart Fail 2017;19:595-602.
3. Aissaoui N, Morshuis M, Maoulida H, et al. Management of end-stage heart failure patients with or without ventricular assist device: an observational comparison of clinical and economic outcomes. Eur J Cardiothorac Surg 2018;53:170-7.
4. Mehra MR, Naka Y, Uriel N, et al.; MOMENTUM 3 Investigators. A Fully Magnetically Levitated Circulatory Pump for Advanced Heart Failure. N Engl J Med 2017;376:440-50.
5. Feldman D, Pamboukian SV, Teuteberg JJ, et al.; International Society for Heart and Lung Transplantation. The 2013 International Society for Heart and Lung Transplantation Guidelines for mechanical circulatory support: executive summary. J Heart Lung Transplant 2013;32:157-87.

 Encadrés
Encadrés