Diagnostiquer une insuffisance rénale aiguë (IRA) et une anurie.
Diagnostiquer une IRA fonctionnelle, obstructive et parenchymateuse. connaître les principales causes des IRA.
Argumenter les principes du traitement et la surveillance des IRA.
Définition de l’insuffisance rénale aiguë et de l’anurie
Nous allons retenir ici la définition la plus récente et consensuelle établie en 2012 par la Kidney Disease/Improving Global Outcome (KDIGO)
Par ailleurs, deux autres définitions plus anciennes utilisant ces deux mêmes paramètres peuvent être retrouvées dans d’autres études comme la classification RIFLE (Risk/Injury/Failure/Loss/ESRD) datant de 2004 et la classification AKIN (Acute Kidney Injury Network) datant de 2007.
Une notion essentielle est qu’en période de variation rapide de la fonction rénale (aggravation ou en récupération) il n’est pas possible d’estimer le débit de filtration glomérulaire en utilisant les formules se basant sur la créatinine plasmatique comme CKD-EPI, MDRD ou Cockcroft et Gault. On peut donc caractériser la sévérité de l’atteinte rénale, mais on ne peut pas estimer, en pratique clinique, le débit de filtration glomérulaire exact en cas d’insuffisance rénale aiguë.
L’anurie est l’absence de production d’urine par le rein et doit être distinguée d’une obstruction sur les voies urinaires.
Quelques limites peuvent être notées à cette définition actuelle de l’insuffisance rénale aiguë : la créatininémie de base n’est pas souvent disponible, le débit de diurèse est difficile à mesurer en dehors des patients porteurs d’une sonde urinaire, et la créatininémie est un marqueur tardif et peu sensible.
Même s’il existe une recherche active d’autres biomarqueurs d’insuffisance rénale aiguë plus sensibles et précoces, comme la cystatine C par exemple, la mesure de la créatinine plasmatique n’a pas été remplacée de nos jours en pratique clinique.
Physiopathologie de l’insuffisance rénale aiguë
Ainsi, dans la plupart des cas, c’est par la baisse de la pression hydrostatique (résultat de la baisse de la pression artérielle moyenne ou d’un déséquilibre de pression intraglomérulaire secondaire à des troubles de l’hémodynamique rénale) que baisse le débit de filtration glomérulaire.
En cas d’obstruction urinaire, c’est l’augmentation de la pression dans la chambre urinaire qui s’oppose à la Puf et diminue ou annule la filtration glomérulaire.
Déterminer le caractère aigu ou chronique de l’insuffisance rénale
La recherche de dosages antérieurs de créatininémie implique souvent de contacter la famille, le médecin traitant, voire les laboratoires, cliniques et hôpitaux où le patient aurait été soigné préalablement.
En l’absence de valeurs antérieures disponibles, les arguments (non spécifiques) qui font pencher le diagnostic vers une insuffisance rénale chronique plutôt que vers une insuffisance rénale aiguë sont :
- la notion de « maladie rénale » chez le patient ou dans sa famille, et ses comorbidités (diabète, hypertension artérielle) ;
- la présence d’une anémie normocytaire normochrome arégénérative, et d’une hypocalcémie ;
- la taille des reins, évaluée par un échographiste expérimenté ou sur un scanner (des reins de moins de 8 cm, dédifférenciés ou polykystiques permettent d’affirmer la chronicité).
Insuffisance rénale aiguë post-rénale (obstructive)
Les causes des insuffisances rénales obstructives (
L’insuffisance rénale aiguë obstructive est le plus souvent anurique, mais on peut observer des mictions par regorgement en cas d’obstacle sous-vésical (ex : adénome de la prostate), une diurèse conservée, voire une polyurie en raison d’un obstacle incomplet, ou encore une diurèse « résiduelle » si les reins natifs d’un patient greffé excrètent encore de l’urine. Il faut donc systématiquement chercher un globe vésical, des signes fonctionnels urinaires obstructifs (dysurie, mauvaise vidange vésicale) ou irritatifs (pollakiurie). Dans le doute et en l’absence de signes infectieux, un sondage vésical d’épreuve peut être indiqué. Dans tous les cas, il faut disposer d’une imagerie rénale à la recherche d’une dilatation des cavités pyélocalicielles par échographie (non irradiante), ou scanner abdomino-pelvien sans injection. Si les cavités sont dilatées de façon unilatérale, alors l’obstruction ne peut être responsable d’une insuffisance rénale aiguë qu’en cas de rein fonctionnel unique.
Une absence de dilatation n’élimine pas totalement une cause obstructive : si la présomption est très forte, il ne faut pas hésiter à répéter les imageries car la dilatation des cavités peut apparaître secondairement après rétablissement de la volémie. Enfin, la dilatation peut être absente en cas de fibrose rétropéritonéale, cause rare mais au cours de laquelle les uretères enserrés dans la fibrose ne peuvent pas se dilater.
En cas d’obstacle sous-vésical, le drainage des urines doit se faire par sondage vésical ou cathétérisme sus-pubien en cas de prostatite, sténose urétrale ou échec de sondage urétral.
En cas d’obstacle sus-vésical, le drainage consiste en la mise en place de sonde(s) urétérale(s) par voie endoscopique rétrograde ou en la mise en place de néphrostomie(s) percutanée(s).
Le drainage des urines est le plus souvent rapidement efficace et peut permettre d’éviter l’épuration extrarénale en l’absence de situations d’urgence vitale. Il peut toutefois se compliquer d’un syndrome de levée d’obstacle : c’est-à-dire d’une polyurie osmotique avec pertes ioniques importantes, qui impose une surveillance clinico-biologique très rapprochée afin de compenser les pertes dans les 48 premières heures. En cas de réascension de la créatinine, il faut évoquer une nouvelle obstruction ou une déshydratation par polyurie de levée d’obstacle (v. plus loin).
Insuffisance rénale aiguë fonctionnelle
Le contexte (troubles digestifs, pathologie de fond) et l’examen clinique (déshydratation en cas d’hypovolémie vraie, ou au contraire hyperhydratation en cas d’hypovolémie efficace) aident à poser le diagnostic. Le
Certains médicaments jouent un rôle aggravant au cours des insuffisances rénales aiguës fonctionnelles. En situation d’hypoperfusion rénale ; les anti-inflammatoires non stéroïdiens par leur effet antagoniste sur la vasodilatation de l’artériole afférente (médié par les prostaglandines) ; les inhibiteurs de l’enzyme de conversion et les antagonistes du récepteur de l’angiotensine 2 en inhibant la vasoconstriction de l’artériole efférente résultant de l’activation du système rénine-angiotensine paralysent les systèmes d’adaptation rénale à l’hypovolémie. Enfin, en bloquant un site de réabsorption du sodium, les diurétiques gênent la réponse rénale adaptée (le verrouillage de la natriurèse) à une hypovolémie. En pratique, ces médicaments sont souvent associés.
Le traitement de l’insuffisance rénale aiguë fonctionnelle consiste à restaurer la volémie vraie ou efficace.
Dans le cas d’une déshydratation par perte (digestive, rénale, cutanée), la rééquilibration hydro-électrolytique et notamment l’apport de solutés isotoniques (cristalloïdes en première intention, car les colloïdes ont une toxicité rénale très probable) est recommandée.
Les solutés « balancés » type Ringer Lactate peuvent être envisagés pour relayer le soluté salé isotonique indiqué en première intention et limiter l’acidose hyperchlorémique (mais il faut faire attention à l’apport en potassium qu’ils incluent). Si l’insuffisance rénale est peu sévère, une hydratation per os (eau, notamment gazeuse et alimentation salée) peut être préconisée avec suivi en ambulatoire et contrôle biologique. La réhydratation est déterminée et réévaluée au moins quotidiennement en fonction de la perte de poids supposée, de l’amélioration clinique du patient et de certains paramètres biologiques (hémoconcentration, déverrouillage de la natriurèse…).
Dans des situations plus spécifiques, les traitements adaptés doivent être envisagés :
- déplétion par diurétiques, cure de dobutamine, voire ultrafiltration dans le syndrome cardiorénal ;
- déplétion par diurétiques de l’anse, et traitement étiologique dans les syndromes néphrotiques ;
- remplissage vasculaire par de l’albumine et vasoconstricteurs (glypressine) dans le syndrome hépatorénal.
Insuffisance rénale aiguë parenchymateuse
En l’absence de signe extrarénal, a fortiori en cas d’hypotension récente (état de choc, chute de pression artérielle pendant une anesthésie générale, etc.) ou de prise de médicament néphrotoxique, il s’agit le plus souvent d’une nécrose tubulaire aiguë qui ne nécessite pas de biopsie rénale (le tube proximal ayant une consommation énergétique importante est situé dans une zone physiologiquement peu oxygénée, et est donc très sensible à l’hypoxie). Dans tous les autres cas, la biopsie rénale est discutée pour poser un diagnostic et établir une attitude thérapeutique.
Le
L’insuffisance rénale aiguë aux produits de contraste iodés est probablement secondaire à une toxicité tubulaire directe associée à une ischémie des tubules liée à une augmentation de la viscosité dans les vasa recta lors du passage du produit. L’iode en soi n’est pas néphrotoxique. L’incidence de cette pathologie a probablement été surestimée au cours des dernières années, et l’utilisation des nouveaux produits de contraste iodés a permis une baisse de son incidence. Les patients à risque sont les insuffisants rénaux chroniques principalement, mais d’autres facteurs de risque peuvent s’associer comme l’âge, le diabète, le myélome, l’injection artérielle ou le volume de produit de contraste injecté. La prise en charge est principalement préventive avec une hydratation par NaCl 0,9 % et comme suggéré par une étude l’administration d’oxygène aux lunettes lors de la procédure même si la saturation est correcte. Ces mesures s’ajoutent bien entendu à une juste indication des examens. Toutes les mesures au décours, et notamment l’hémodialyse, n’ont montré aucune efficacité. La perfusion de bicarbonate de sodium avant la procédure ou l’administration de N-acétyl-cystéine n’ont pas montré leur utilité sur des grandes études prospectives récentes. Si la toxicité survient, l’optimisation de la volémie (pas d’hyperhydratation) et les mesures symptomatiques sont indiquées.
La rhabdomyolyse aiguë que l’on rencontre en pratique le plus souvent en contexte de chute (personne âgée avec station au sol), de toxicité médicamenteuse (statines), d’infection (grippe saisonnière, leptospirose) ou de crise tonico-clonique généralisée se complique d’insuffisance rénale aiguë de mécanisme mixte ; d’une part fonctionnelle par vasoconstriction de l’artériole afférente (effet direct) et constitution d’un troisième secteur (œdème musculaire) puis d’autre part par précipitation intra-tubulaire de myoglobine avec la protéine de Tamm-Horsfall. Le tableau est celui d’une insuffisance rénale aiguë sévère (KDIGO III), parfois oligo-anurique, avec un aspect d’urines rouges (myoglobinurie) et une bandelette urinaire faussement positivée pour le sang par la myoglobine. Biologiquement, l’hyperkaliémie est de règle, associée à une hyperphosphorémie (lyse cellulaire) et une hypocalcémie (par précipitation avec le phosphore). Le traitement consiste principalement en une hydratation abondante par soluté salé isotonique ou bicarbonate de sodium en monitorant le pH urinaire (objectif > 6), qui ne doit pas être acide, et le risque de surcharge (notamment pulmonaire) chez des patients souvent anuriques.
Les insuffisances rénales aiguës médicamenteuses par toxicité tubulaire ou précipitation intra-tubulaire (sels de platine, amphotéricine B, antibiotiques, antiviraux…) sont principalement prévenues par l’adaptation des doses à la fonction rénale si celle-ci est anormale (www.sitegpr.com) et l’encadrement des cures par hydratation abondante, éventuellement lors d’une hospitalisation courte. La prise en charge si la toxicité survient peut consister en l’adaptation des doses (dosages médicamenteux, notamment en cas d’insuffisance rénale), la concession de dose ou le changement de molécule associés à une gestion symptomatique (troubles hydro-électrolytiques fréquents liés à la dysfonction tubulaire).
Les insuffisances rénales aiguës immuno-allergiques surviennent entre 2 et 4 semaines après l’introduction d’un traitement (délai potentiellement réduit si réintroduction ou s’il s’agit de rifampicine), à la suite d’une réaction d’hypersensibilité de type retardée (type IV de Gell et Coombs). Le tableau clinique est souvent fruste, mais peut inclure un rash cutané, ou une érythrodermie (DRESS syndrome) et des arthralgies. L’insuffisance rénale aiguë peut être d’intensité modérée à sévère, avec une protéinurie tubulaire de moins de 2 g/g, et une leucocyturie (éosinophilurie classique mais non constante). Le diagnostic est porté par le néphrologue, en milieu spécialisé, sur une biopsie rénale quand celle-ci peut être réalisée (infiltrat inflammatoire interstitiel riche en éosinophiles avec ou sans granulomes). Le traitement repose sur la corticothérapie, avec un niveau de preuve faible, et la récupération est inconstante. La prise en charge préventive est limitée puisqu’il s’agit d’événements accidentels, mais repose en pratique principalement sur la juste prescription des inhibiteurs de la pompe à protons (IPP) et des antivitamine-K (éviter la fluindione).
Les autres causes parenchymateuses d’insuffisance rénale aiguë seront traitées dans les chapitres correspondants (glomérulopathies, néphropathies vasculaires, myélome…).
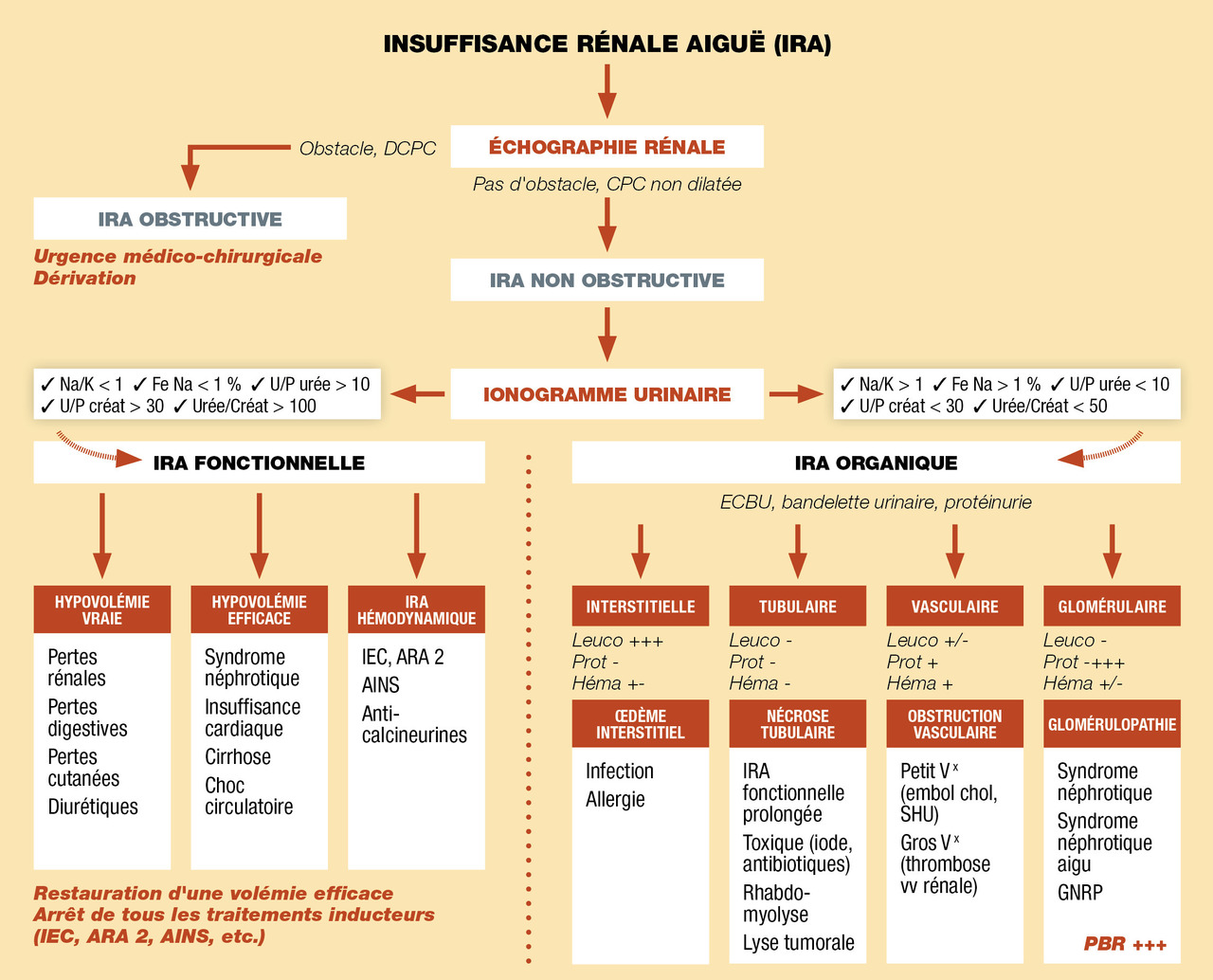
La démarche diagnostique générale devant une insuffisance rénale aiguë est synthétisée dans la
Principes de traitement et surveillance
Les principales complications de l’insuffisance rénale aiguë sont métaboliques, comme l’acidose et l’hyperkaliémie mais aussi volémiques, avec l’œdème pulmonaire de surcharge, et s’associent à la dénutrition. Enfin, il existe un risque accru d’infections nosocomiales et d’hémorragie digestive.
Les facteurs de pronostic rénal en cas d’atteinte aiguë sont : la fonction rénale antérieure et le type d’insuffisance rénale. En effet, dans le cas des insuffisance rénale aiguë parenchymateuses, la nécrose tubulaire aiguë a un meilleur pronostic, avec une récupération classique après une phase de quelques jours à 3 semaines. Cependant, une surveillance après l’épisode d’insuffisance rénale aiguë est nécessaire car une séquelle est possible, et l’évolution vers l’insuffisance rénale chronique est plus fréquente.
Les facteurs associés au pronostic vital du patient sont l’existence d’un choc septique, le nombre de défaillances d’organe, les complications et le terrain sur lequel survient l’insuffisance rénale aiguë.
Gérer l’urgence néphrologique
- hyperkaliémie (K+ > 5,5 mmol/L) : par administration per os ou en lavement de résine échangeuse d’ions (Kayexalate ), d’insuline rapide et de glucose en intraveineuse, de salbutamol en aérosol (effet synergique avec l’insuline/glucose). La réalisation d’un électrocardiogramme est systématique en cas d’hyperkaliémie > 5,5 mmol/L et amène à administrer du gluconate de calcium à visée cardioprotectrice s’il existe des signes électriques. En cas d’hyperkaliémie menaçante, le patient doit bénéficier d’une surveillance scopée et d’une épuration extrarénale en urgence par hémodialyse ;
- surcharge hydrosodée : la recherche de signes cliniques de surcharge gauche (désaturation, dyspnée, polypnée, crépitants des bases) et droite (turgescence jugulaire, reflux hépato- jugulaire, œdème des lombes, du visage ou des membres inférieurs) permet de l’affirmer, ainsi que les signes biologiques d’hémodilution et l’élévation du brain natriuretic peptid protein (BNP). La gestion de la volémie se fait principalement par l’administration de diurétiques de l’anse, per os ou intraveineuse (effet plus rapide et jusqu’à deux fois plus efficace), dont il faut savoir que l’effet diminue avec la baisse de la fonction rénale (perte d’efficacité d’une même dose avec la baisse du DFG, et donc nécessité d’augmenter les doses). La restriction sodée (2 g/j si surcharge sévère) et hydrique (500 mL/j) fait partie intégrante du traitement en aigu. En cas d’œdème aigu pulmonaire réfractaire au traitement standard (oxygénothérapie, diurétique et vasodilatateur) ou chez un patient anurique, une épuration extrarénale par hémodialyse doit être débutée en urgence afin de réaliser de l’ultrafiltration ;
- acidose : l’acidose est en règle respectée (elle permet une épargne énergétique). La seule indication à une alcalinisation est la perte digestive ou urinaire de bicarbonates. En revanche, on considère l’acidose sévère (pH < 7 ou bicarbonates < 10 mmol/L) comme un signe de sévérité, prédisposant aux troubles du rythme et associée à une surmortalité. Il faut rechercher des causes spécifiques d’acidose sévère dans ces cas-là : métabolique (acidose lactique ou acidocétose) ou toxique (intoxication à l’éthylène glycol ou au méthanol). L’épuration extrarénale peut être indiquée en cas d’acidose sévère sur perte de bicarbonates avec contre-indication volémique à la perfusion intraveineuse de bicarbonate de sodium.
Mesures générales
- arrêt des néphrotoxiques ;
- adaptation des doses des médicaments éliminés par le rein ;
- lutte contre la dénutrition (apports caloriques entre 20 à 40 cal/kg/j et protidiques entre 0,2 à 0,3 g/kg/j d’azote) ;
- protection gastrique par IPP à dose préventive ;
- rééquilibration hydro-électrolytique ;
- et bien évidemment le traitement étiologique (drainage urinaire, remplissage ou réhydratation, antibiothérapie, immunosuppresseurs, échanges plasmatiques, chimiothérapie…).
L’épuration extra-rénale est indiquée en cas d’échec du traitement médical et/ou d’urgence néphrologique menaçant immédiatement le pronostic vital. C’est l’hémodialyse intermittente qui est indiquée en première intention en l’absence d’instabilité hémodynamique, après pose d’un abord veineux de gros calibre (cathéter d’hémodialyse fémoral ou jugulaire).
Le but est par mécanisme osmotique d’équilibrer le milieu intérieur du patient avec un bain pauvre en potassium et dépourvu de toxines urémiques et par mécanisme convectif d’ultrafiltrer de l’eau en cas de surcharge.
L’indication du recours à l’hémodialyse en aigu est posée par le néphrologue ou le réanimateur, et résulte d’une combinaison entre les critères biologiques (individuellement non suffisants sauf si menace du pronostic vital immédiat), la réponse au traitement médical, les perspectives d’évolution et le contexte clinique. Par exemple, une insuffisance rénale aiguë d’étiologie obstructive avec hyperkaliémie menaçante pourra être traitée médicalement si le drainage des urines est réalisé rapidement. À l’inverse, dans un contexte de nécrose tubulaire aiguë suspectée chez un sujet âgé, cardiopathe, en surcharge, on y a plus rapidement recours.
Le timing idéal de démarrage de l’hémodialyse en cas d’insuffisance rénale aiguë en dehors des situations d’urgence (œdème pulmonaire ou hyperkaliémie menaçante) est débattu et fait l’objet d’études en cours.
Surveillance
Le risque d’hémorragie digestive haute doit être rappelé (apparition de selles noires, avec déglobulisation biologique et réascension de l’urée plasmatique sans augmentation parallèle de la créatininémie).
Prévention de l’insuffisance rénale aiguë
Les mesures spécifiques ont déjà été détaillées plus haut. De façon plus globale, l’insuffisance rénale aiguë se prévient en optimisant la volémie pour toute situation dans laquelle le rein pourrait être soumis à une ischémie même relative, particulièrement chez l’insuffisant rénal chronique (l’insuffisance rénale chronique est le facteur de risque principal de développer une insuffisance rénale aiguë). L’optimisation volémique, la lutte contre l’hypoxie, le respect des seuils transfusionnels font partie des mesures à établir.
Insuffisance rénale aiguë - Anurie
Devant toute insuffisance rénale aiguë il faut écarter l’obstacle sur les voies excrétrices par une imagerie rénale.
Il faut ensuite écarter l’insuffisance rénale aiguë fonctionnelle principalement par l’anamnèse et l’examen clinique mais en s’aidant des critères biologiques (ionogramme urinaire par exemple).
Il faut ensuite identifier les deux urgences principales nécessitant une épuration extra-rénale en urgence : l’œdème pulmonaire réfractaire ou l’hyperkaliémie menaçante (avec signes ECG de gravité).
L’insuffisance rénale aiguë est associée à une surmortalité et une grande morbidité en particulier pour les patients de réanimation. Toute insuffisance rénale aiguë peut évoluer vers une insuffisance rénale chronique terminale.
Les mesures préventives sont importantes à connaître surtout en cas de facteur de risque associé (âge, diabète, myélome, insuffisance cardiaque ou hépatique…) ou d’insuffisance rénale chronique préexistante.
Dans cet article
- Définition de l’insuffisance rénale aiguë et de l’anurie
- Physiopathologie de l’insuffisance rénale aiguë
- Déterminer le caractère aigu ou chronique de l’insuffisance rénale
- Insuffisance rénale aiguë post-rénale (obstructive)
- Insuffisance rénale aiguë fonctionnelle
- Insuffisance rénale aiguë parenchymateuse
- Principes de traitement et surveillance

 Encadrés
Encadrés