Dans les formes les plus sévères d’acné, 4 à 6 mois de traitement suffisent habituellement pour obtenir une rémission et espérer une guérison. Si le médicament est tératogène, imposant une contraception efficace chez la femme, il ne semble pas induire un sur-risque suicidaire.
L’isotrétinoïne a été introduite en 1982 par le laboratoire Roche sous le nom de Roaccutane, qui n’existe plus désormais sous cette dénomination sur le marché. Il s’agit d’un médicament de la famille des rétinoïdes, molécule de première génération dérivée de la vitamine A. Sa principale indication est l’acné, en première ou deuxième intention selon le stade de sévérité, où il a constitué une révolution thérapeutique. Il est également utilisé dans d’autres dermatoses faciales.
Acné
Propriétés pharmacologiques, mécanisme d’action
L’isotrétinoïne est administrée par voie orale, absorbée par voie digestive. Dans le plasma, elle est liée à l’albumine à 99,9 %. L’absorption est variable, proportionnelle à la posologie. Après administration orale, le pic de concentration plasmatique s’observe entre 1 et 4 heures ; la prise au cours d’un repas augmente significativement sa biodisponibilité et réduit la variabilité interindividuelle. L’isotrétinoïne se métabolise en 4-oxo-isotrétinoïne (métabolite majoritaire), trétinoïne et 4-oxo-trétinoïne, puis est éliminée principalement par voie biliaire. La demi-vie d’élimination varie entre 13 et 22 heures (19 heures en moyenne) et celle de la 4-oxo-isotrétinoïne est de 29 heures en moyenne.
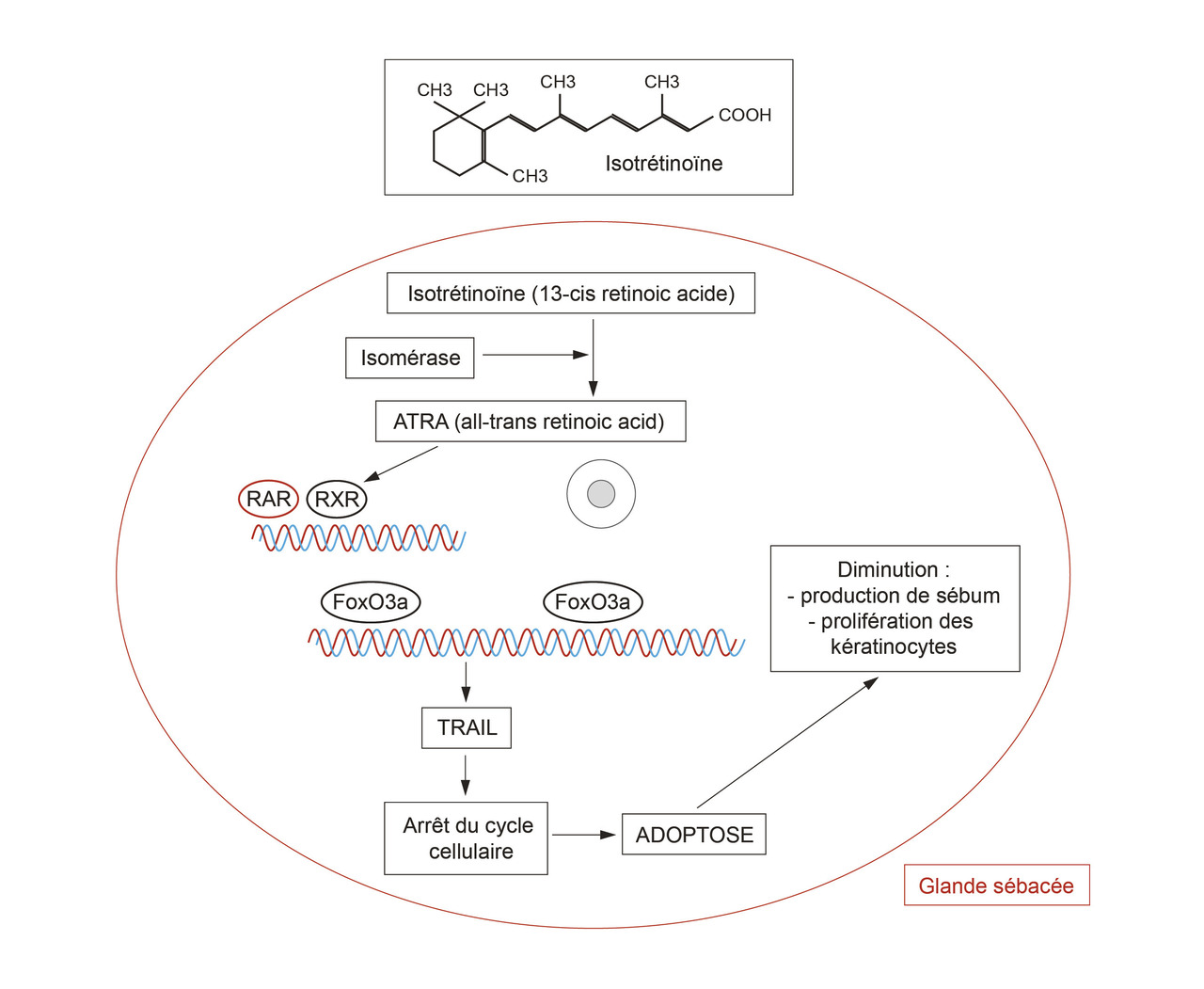
L’isotrétinoïne agit sur tous les mécanismes physiopathologiques impliqués dans l’acné, avec comme principal effet une sébosuppression (fig. 1 ). Il agit également sur le développement de Cutibacterium acnes et ses conséquences inflammatoires via des propriétés immunomodulatrices et anti-inflammatoires complexes (freination du chimiotactisme des polynucléaires neutrophiles, réduction des radicaux libres oxygénés, inhibition de la synthèse des prostaglandines et du leucotriène B4…).
L’isotrétinoïne agit sur tous les mécanismes physiopathologiques impliqués dans l’acné, avec comme principal effet une sébosuppression (
Indications
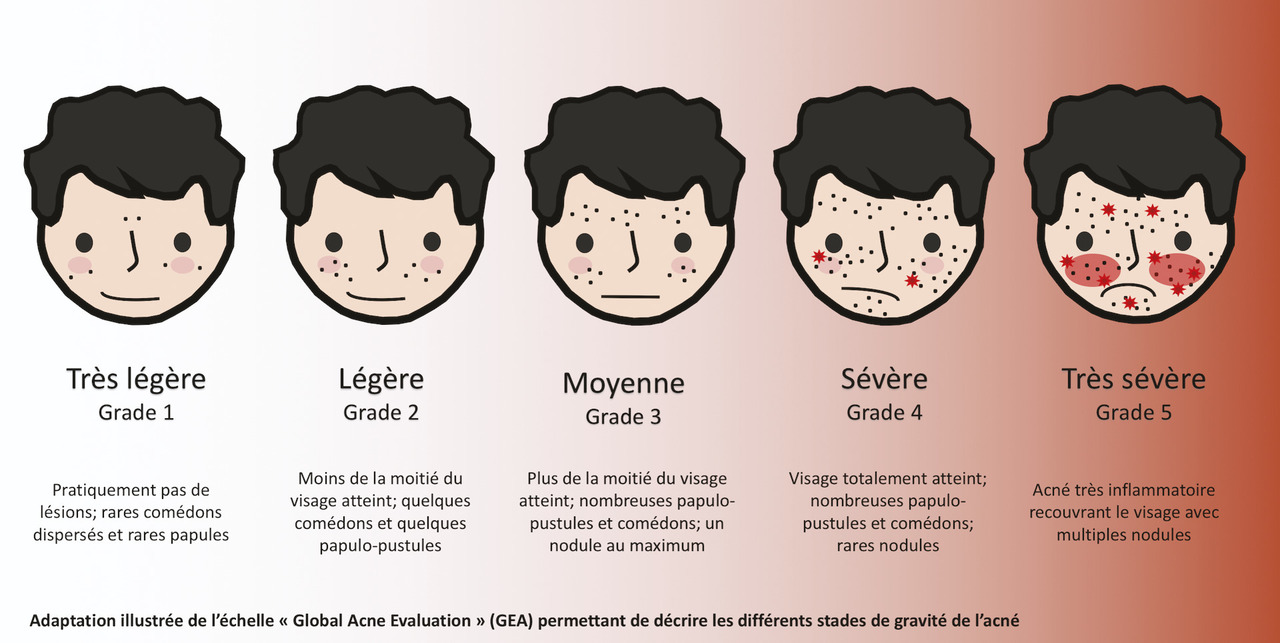
L’échelle « global acne evaluation » (GEA) est utile pour décrire les différents stades de gravité de l’acné et aider au choix thérapeutique :1
– très légère : pratiquement pas de lésion, rares comédons ouverts ou fermés dispersés et rares papules ;
– légère : moins de la moitié du visage atteinte, quelques comédons ouverts ou fermés, quelques papulopustules ;
– modérée : plus de la moitié de la surface du visage atteinte, nombreuses papulopustules, nombreux comédons ouverts ou fermés, un nodule peut être présent ;
– sévère : visage totalement atteint, couvert de nombreuses papulopustules, comédons ouverts ou fermés, rares nodules ;
– très sévère : acné très inflammatoire recouvrant le visage avec nodules.
Selon les dernières recommandations* de la Société française de dermatologie (SFD), l’isotrétinoïne est indiquée dans les acnés modérées, sévères et très sévères en première ou deuxième intention :
– dans les acnés modérées, en deuxième intention après échec d’un traitement par peroxyde de benzoyle (PBO) et rétinoïdes topiques ou cyclines associées à du PBO et des rétinoïdes topiques pendant 3 mois ;
– dans les acnés sévères, en deuxième intention après traitement par cyclines associé à du PBO et des rétinoïdes topiques pendant 3 mois. ll peut être initié (hors autorisation de mise sur le marché [AMM]) sans attendre 3 mois d’échec du traitement de première intention, en cas de risque cicatriciel important ou en cas de récidive rapide ;
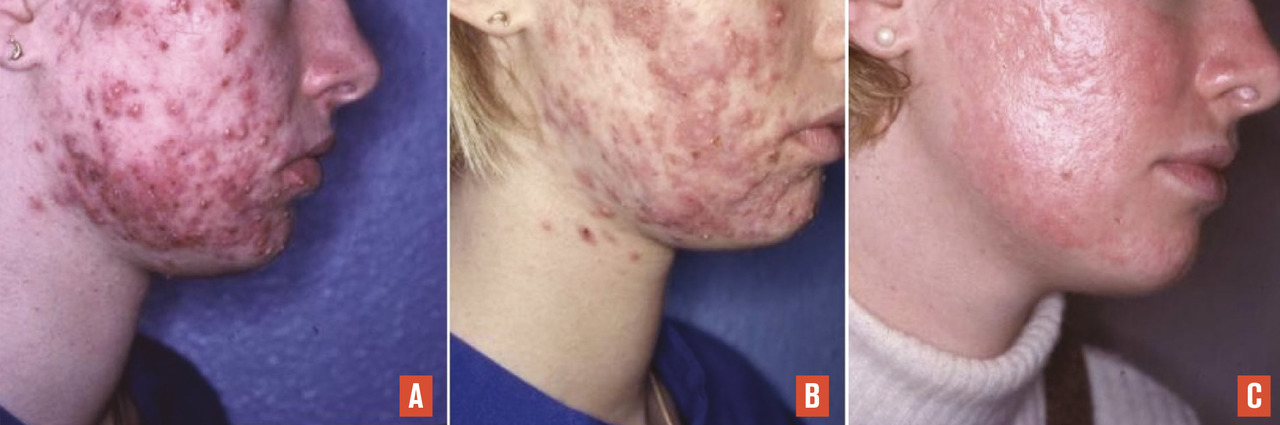
– dans les acnés très sévères (fig. 2 ), acné nodulaire, acné conglobata ou acné susceptible d’entraîner des cicatrices définitives, l’isotrétinoïne, seule molécule pouvant constituer un traitement curatif de l’acné, est recommandée en première intention (hors AMM). Le risque majeur de l’acné très sévère (v. supra) est d’entraîner des cicatrices définitives avec, notamment sur les peaux pigmentées, une évolution hypertrophique ou chéloïdienne. Le traitement par isotrétinoïne permet de limiter ce risque cicatriciel, d’où l’importance d’une prescription précoce dans certaines situations à risque.
À noter que ce traitement n’est pas indiqué dans l’acné prépubertaire et n’est pas recommandé avant l’âge de 12 ans.
– très légère : pratiquement pas de lésion, rares comédons ouverts ou fermés dispersés et rares papules ;
– légère : moins de la moitié du visage atteinte, quelques comédons ouverts ou fermés, quelques papulopustules ;
– modérée : plus de la moitié de la surface du visage atteinte, nombreuses papulopustules, nombreux comédons ouverts ou fermés, un nodule peut être présent ;
– sévère : visage totalement atteint, couvert de nombreuses papulopustules, comédons ouverts ou fermés, rares nodules ;
– très sévère : acné très inflammatoire recouvrant le visage avec nodules.
Selon les dernières recommandations* de la Société française de dermatologie (SFD), l’isotrétinoïne est indiquée dans les acnés modérées, sévères et très sévères en première ou deuxième intention :
– dans les acnés modérées, en deuxième intention après échec d’un traitement par peroxyde de benzoyle (PBO) et rétinoïdes topiques ou cyclines associées à du PBO et des rétinoïdes topiques pendant 3 mois ;
– dans les acnés sévères, en deuxième intention après traitement par cyclines associé à du PBO et des rétinoïdes topiques pendant 3 mois. ll peut être initié (hors autorisation de mise sur le marché [AMM]) sans attendre 3 mois d’échec du traitement de première intention, en cas de risque cicatriciel important ou en cas de récidive rapide ;
– dans les acnés très sévères (
À noter que ce traitement n’est pas indiqué dans l’acné prépubertaire et n’est pas recommandé avant l’âge de 12 ans.
Contre-indications
En raison de son caractère tératogène, l’isotrétinoïne est contre-indiquée chez les femmes en âge de procréer en l’absence de contraception efficace sauf si toutes les conditions du programme de prévention de grossesse en place depuis 1997 sont remplies.
Elle est contre-indiquée au cours de la grossesse et de l’allaitement.
L’ensemble des contre-indications est résumé dans letableau 1 .
Elle est contre-indiquée au cours de la grossesse et de l’allaitement.
L’ensemble des contre-indications est résumé dans le
Modalités de traitement
L’Agence nationale de sécurité du médicament (ANSM) a édité un rapport en 2015 stipulant que la prescription initiale d’isotrétinoïne orale était désormais réservée aux dermatologues. Le renouvellement peut ensuite être effectué par tout médecin. Les conditions à remplir avant l’initiation et le renouvellement du traitement sont indiquées dans le tableau 2 .
tableau 1 ).
Le dosage initial est habituellement de 0,5 mg/kg/j avec, selon la tolérance et l’efficacité, une possible augmentation progressive des doses (jusqu’à 1 mg/kg/j). Ce schéma est à moduler dans les acnés à risque de poussée inflammatoire réactionnelle (« flare-up »), qui doivent faire l’objet d’un suivi dermatologique spécifique.
Une cure de traitement d’une durée de 16 à 24 semaines suffit habituellement à atteindre la rémission et espérer obtenir une guérison complète de l’acné (envisageable en raison de l’effet sébosuppresseur de la molécule).
Cependant, en cas de rechute, une nouvelle cure d’isotrétinoïne est possible avec la même posologie quotidienne et la même dose thérapeutique cumulée. L’amélioration de l’acné peut se poursuivre jusqu’à 8 semaines après l’arrêt du traitement, expliquant que toute nouvelle cure ne doit être proposée qu’après la fin de ce délai.
Les facteurs de récidive sont les suivants : dose cumulative insuffisante, jeune âge, sévérité de l’acné, hyperséborrhée (qui peut entrer dans le cadre d’un hyperandrogénisme, à rechercher de principe chez la femme en cas de résistance au traitement).
Molécules disponibles et posologie
Différentes molécules sont disponibles (Le dosage initial est habituellement de 0,5 mg/kg/j avec, selon la tolérance et l’efficacité, une possible augmentation progressive des doses (jusqu’à 1 mg/kg/j). Ce schéma est à moduler dans les acnés à risque de poussée inflammatoire réactionnelle (« flare-up »), qui doivent faire l’objet d’un suivi dermatologique spécifique.
Durée du traitement
En France, on considère que les taux de rémission prolongée et de rechute après une cure d’isotrétinoïne dépendent plus de la dose cumulée totale reçue que de la durée du traitement ou de la posologie quotidienne. Ainsi, au-delà d’une dose cumulée totale de 120 à 150 mg/kg, aucun bénéfice supplémentaire notable n’est attendu.Une cure de traitement d’une durée de 16 à 24 semaines suffit habituellement à atteindre la rémission et espérer obtenir une guérison complète de l’acné (envisageable en raison de l’effet sébosuppresseur de la molécule).
Cependant, en cas de rechute, une nouvelle cure d’isotrétinoïne est possible avec la même posologie quotidienne et la même dose thérapeutique cumulée. L’amélioration de l’acné peut se poursuivre jusqu’à 8 semaines après l’arrêt du traitement, expliquant que toute nouvelle cure ne doit être proposée qu’après la fin de ce délai.
Les facteurs de récidive sont les suivants : dose cumulative insuffisante, jeune âge, sévérité de l’acné, hyperséborrhée (qui peut entrer dans le cadre d’un hyperandrogénisme, à rechercher de principe chez la femme en cas de résistance au traitement).
Effets indésirables
Les effets secondaires (tableau 3 ) avec l’isotrétinoïne sont assez fréquents, et en général mineurs. La plupart ne nécessite pas un arrêt du traitement mais un ajustement des mesures associées (v. infra). Une revue de la littérature en 2017 avait identifié que seulement 3,2 % des patients sous isotrétinoïne avaient eu des effets indésirables majeurs ayant conduit à un arrêt du traitement.2
– les pilules estroprogestatives en première intention et en l’absence de contre-indication, essentiellement les pilules de 2e et 3e génération, qui contiennent de plus faibles doses d’éthinylestradiol et des progestatifs moins androgéniques, moins inductrices d’acné ;
– les pilules microprogestatives prises à heure fixe, qui ne sont prescrites qu’en cas de contre-indication aux pilules estroprogestatives ;
– les implants hormonaux ;
– les patchs contraceptifs.
Le stérilet est autorisé associé à une contraception locale (préservatif, spermicide).
Une surveillance mensuelle des bêta-hCG plasmatiques est obligatoirement réalisée chez les femmes en âge de procréer pendant le traitement (datant de moins de 3 jours lors de la prescription initiale, puis avant chaque renouvellement mensuel de la prescription) et 5 semaines après la fin du traitement (tableau 2 ).
L’incidence des malformations fœtales est difficile à apprécier puisque la majorité des grossesses sous isotrétinoïne est interrompue. Les malformations possibles sont : des anomalies du système nerveux central (hydrocéphalie, malformations ou anomalies cérébelleuses, microcéphalie), des dysmorphies faciales, fentes palatines, des anomalies de l’oreille externe (absence d’oreille externe, conduit auditif externe petit ou absent), des anomalies oculaires (microphtalmie) ou cardiovasculaires (anomalies conotruncales telles que tétralogie de Fallot, transposition des gros vaisseaux, communications interventriculaires), des anomalies du thymus et des glandes parathyroïdes. Il existe également une augmentation du risque d’avortement spontané.
En cas de grossesse sous isotrétinoïne, le traitement doit absolument être interrompu, et il faut orienter la patiente vers un médecin spécialisé en tératologie pour évaluation, une interruption médicale de grossesse (IMG) pouvant être proposée en raison du risque de malformation. Ce risque persiste jusqu’à 1 mois après l’arrêt du traitement. Si, en raison de conviction personnelle, une femme était opposée à toute idée d’IMG, la prescription initiale d’isotrétinoïne ne pourrait être proposée.
Une étude de pharmacovigilance française en 20144 a repris sur 25 ans (entre 1987 et 2011) cinq études rapportant des grossesses sous isotrétinoïne pendant la période à risque. Sur les 553 grossesses avec issue connue, il y a eu 430 (78 %) IMG (dont 11 pour malformation fœtale in utero), 96 (17 %) grossesses menées à terme (dont 11 naissances avec malformation fœtale), une mort fœtale in utero et 26 (5 %) fausses couches spontanées.
Des programmes de prévention de la grossesse (PPG) ont été mis en place (iPeldge lancé en 2006 aux États-Unis, PPG initié en France en 1997, suivi d’un renforcement par l’Agence française de sécurité sanitaire et des produits de santé [Afssaps] en 2009 pour réduire l’exposition fœtale à l’isotrétinoïne). Ces programmes ont été efficaces, permettant une diminution du nombre de grossesses survenues sous traitement.5
Chez l’homme, les données disponibles suggèrent que le niveau d’exposition maternelle à partir du sperme des patients traités par isotrétinoïne n’est pas suffisamment élevé pour être associé à des effets tératogènes. Cependant, il doit être impérativement rappelé aux patients qu’ils ne doivent pas donner leur médicament à d’autres personnes, en particulier à des femmes.
Des suicides ainsi que des épisodes dépressifs sous traitement par isotrétinoïne ont été décrits chez des individus avec même « déchallenge » (arrêt du médicament avec disparition des symptômes) et « rechallenge » (réintroduction du médicament avec réapparition). Cependant, la majorité des études populationnelles ne montre pas de sur-risque d’être dépressif,6 et les études positives sont possiblement biaisées.7 Par ailleurs, le risque de suicide est plus élevé dans la population d’adolescents avec une acné importante par rapport à une population sans acné. Il existe donc un risque « idiosyncrasique » individuel non retrouvé en population dans cette tranche d’âge particulièrement « sensible » (et ce d’autant qu’il existe une acné qu’il faut évidemment traiter).
Une étude française récente faite à partir des bases de données de l’Assurance maladie ne montre pas de sur-risque et même un taux de suicide plus faible dans la population exposée à l’isotrétinoïne.8 Outre le fait que les patients aient eu potentiellement un bénéfice thérapeutique sous isotrétinoïne (et par voie de conséquence une amélioration psychologique), il est probable que désormais les adolescents à traiter sont mieux « sélectionnés », avec moins de risques psychiatriques au départ. C’est avec cette démarche qu’une étude utilisant un score de dépression de l’adolescent, l’échelle « adolescent depression rating scale » (ADRS), a été utilisée chez des patients acnéiques consultant en dermatologie avec une indication de traitement par isotrétinoïne. La faisabilité et la pertinence de l’utilisation de ce score ont pu être démontrées, faisant de l’ARDS un élément de dépistage à intégrer dans la prise en charge des patients acnéiques sévères, candidats potentiels à une prescription d’isotrétinoïne.
Ils comprennent majoritairement une chéilite, parfois fissuraire, une xérose cutanée, qui est quasi constante. La sécheresse des muqueuses (oreilles, nez, muqueuses buccale, génitale et conjonctivale) est fréquente (11,6 %) et doit être anticipée par des mesures préventives et d’accompagnement (émollients, lubrifiants, collyres, arrêt si nécessaire du port des verres de contact). Les traitements locaux antiacnéïques, qui peuvent être asséchants, doivent être arrêtés.
Une exacerbation de l’acné est parfois observée en début de traitement, elle s’améliore dans la majorité des cas tout en poursuivant le traitement, habituellement en 7 à 10 jours sans qu’il soit nécessaire d’ajuster les doses. Les formes graves (« flare-up ») nécessitent une prise en charge spécialisée (corticothérapie par voie générale notamment). Le meilleur traitement est préventif, en débutant l’isotrétinoïne chez les patients à risque (formes avec kystes et macrocomédons) par de faibles doses.
L’isotrétinoïne est un photosensibilisant, et l’exposition solaire importante aux rayons ultraviolets doit être évitée, nécessitant l’application répétée d’écran solaire à score de protection élevé (SPF 50).
Les effets indésirables ophtalmologiques à type de sécheresse oculaire, irritation ou conjonctivite sont observés chez 7,2 % des patients sous isotrétinoïne. Le recours à des lunettes de vue plutôt qu’à des lentilles de contact, l’utilisation de pommades ophtalmiques ou de larmes artificielles peut être nécessaire au cours du traitement.
Les plus fréquentes sont :
– une augmentation des enzymes hépatiques (alanine et aspartate aminotransférases [ALAT et ASAT]) très souvent dans les limites de la normale, et qui s’amende spontanément malgré la poursuite du traitement à la même dose ;
– une augmentation des taux de lipides sanguins, notamment des triglycérides, qui régresse après réduction des doses ou arrêt du traitement. Les mesures diététiques peuvent également être utiles. L’arrêt du traitement s’envisage lorsque l’augmentation ne peut être contrôlée et expose à un risque de pancréatite (supérieur à 800 mg/dL ou 9 mmol/L).
Un contrôle biologique, avec enzymes hépatiques et bilan lipidique, est recommandé avant et 1 mois après le début du traitement, puis une fois tous les 3 mois.
Tératogénicité
L’isotrétinoïne a des effets tératogènes démontrés,3,** expliquant pourquoi une contraception efficace doit absolument et réglementairement être mise en place 1 mois avant le début du traitement et jusqu’à 1 mois après la fin (v. supra). Les patientes doivent donc recevoir une information complète sur la prévention des grossesses et signer l’accord de soins et de contraception. Les préservatifs ne sont pas une technique contraceptive suffisante pour prévenir le risque de grossesse sous isotrétinoïne. Les contraceptions autorisées sont :– les pilules estroprogestatives en première intention et en l’absence de contre-indication, essentiellement les pilules de 2e et 3e génération, qui contiennent de plus faibles doses d’éthinylestradiol et des progestatifs moins androgéniques, moins inductrices d’acné ;
– les pilules microprogestatives prises à heure fixe, qui ne sont prescrites qu’en cas de contre-indication aux pilules estroprogestatives ;
– les implants hormonaux ;
– les patchs contraceptifs.
Le stérilet est autorisé associé à une contraception locale (préservatif, spermicide).
Une surveillance mensuelle des bêta-hCG plasmatiques est obligatoirement réalisée chez les femmes en âge de procréer pendant le traitement (datant de moins de 3 jours lors de la prescription initiale, puis avant chaque renouvellement mensuel de la prescription) et 5 semaines après la fin du traitement (
L’incidence des malformations fœtales est difficile à apprécier puisque la majorité des grossesses sous isotrétinoïne est interrompue. Les malformations possibles sont : des anomalies du système nerveux central (hydrocéphalie, malformations ou anomalies cérébelleuses, microcéphalie), des dysmorphies faciales, fentes palatines, des anomalies de l’oreille externe (absence d’oreille externe, conduit auditif externe petit ou absent), des anomalies oculaires (microphtalmie) ou cardiovasculaires (anomalies conotruncales telles que tétralogie de Fallot, transposition des gros vaisseaux, communications interventriculaires), des anomalies du thymus et des glandes parathyroïdes. Il existe également une augmentation du risque d’avortement spontané.
En cas de grossesse sous isotrétinoïne, le traitement doit absolument être interrompu, et il faut orienter la patiente vers un médecin spécialisé en tératologie pour évaluation, une interruption médicale de grossesse (IMG) pouvant être proposée en raison du risque de malformation. Ce risque persiste jusqu’à 1 mois après l’arrêt du traitement. Si, en raison de conviction personnelle, une femme était opposée à toute idée d’IMG, la prescription initiale d’isotrétinoïne ne pourrait être proposée.
Une étude de pharmacovigilance française en 20144 a repris sur 25 ans (entre 1987 et 2011) cinq études rapportant des grossesses sous isotrétinoïne pendant la période à risque. Sur les 553 grossesses avec issue connue, il y a eu 430 (78 %) IMG (dont 11 pour malformation fœtale in utero), 96 (17 %) grossesses menées à terme (dont 11 naissances avec malformation fœtale), une mort fœtale in utero et 26 (5 %) fausses couches spontanées.
Des programmes de prévention de la grossesse (PPG) ont été mis en place (iPeldge lancé en 2006 aux États-Unis, PPG initié en France en 1997, suivi d’un renforcement par l’Agence française de sécurité sanitaire et des produits de santé [Afssaps] en 2009 pour réduire l’exposition fœtale à l’isotrétinoïne). Ces programmes ont été efficaces, permettant une diminution du nombre de grossesses survenues sous traitement.5
Chez l’homme, les données disponibles suggèrent que le niveau d’exposition maternelle à partir du sperme des patients traités par isotrétinoïne n’est pas suffisamment élevé pour être associé à des effets tératogènes. Cependant, il doit être impérativement rappelé aux patients qu’ils ne doivent pas donner leur médicament à d’autres personnes, en particulier à des femmes.
Effets psychiatriques
Les données concernant les effets indésirables psychiatriques sous isotrétinoïne sont variables selon les études.Des suicides ainsi que des épisodes dépressifs sous traitement par isotrétinoïne ont été décrits chez des individus avec même « déchallenge » (arrêt du médicament avec disparition des symptômes) et « rechallenge » (réintroduction du médicament avec réapparition). Cependant, la majorité des études populationnelles ne montre pas de sur-risque d’être dépressif,6 et les études positives sont possiblement biaisées.7 Par ailleurs, le risque de suicide est plus élevé dans la population d’adolescents avec une acné importante par rapport à une population sans acné. Il existe donc un risque « idiosyncrasique » individuel non retrouvé en population dans cette tranche d’âge particulièrement « sensible » (et ce d’autant qu’il existe une acné qu’il faut évidemment traiter).
Une étude française récente faite à partir des bases de données de l’Assurance maladie ne montre pas de sur-risque et même un taux de suicide plus faible dans la population exposée à l’isotrétinoïne.8 Outre le fait que les patients aient eu potentiellement un bénéfice thérapeutique sous isotrétinoïne (et par voie de conséquence une amélioration psychologique), il est probable que désormais les adolescents à traiter sont mieux « sélectionnés », avec moins de risques psychiatriques au départ. C’est avec cette démarche qu’une étude utilisant un score de dépression de l’adolescent, l’échelle « adolescent depression rating scale » (ADRS), a été utilisée chez des patients acnéiques consultant en dermatologie avec une indication de traitement par isotrétinoïne. La faisabilité et la pertinence de l’utilisation de ce score ont pu être démontrées, faisant de l’ARDS un élément de dépistage à intégrer dans la prise en charge des patients acnéiques sévères, candidats potentiels à une prescription d’isotrétinoïne.
Effets indésirables cutanéomuqueux
Ces effets indésirables dermatologiques sont les plus fréquents (autour de 65 %).Ils comprennent majoritairement une chéilite, parfois fissuraire, une xérose cutanée, qui est quasi constante. La sécheresse des muqueuses (oreilles, nez, muqueuses buccale, génitale et conjonctivale) est fréquente (11,6 %) et doit être anticipée par des mesures préventives et d’accompagnement (émollients, lubrifiants, collyres, arrêt si nécessaire du port des verres de contact). Les traitements locaux antiacnéïques, qui peuvent être asséchants, doivent être arrêtés.
Une exacerbation de l’acné est parfois observée en début de traitement, elle s’améliore dans la majorité des cas tout en poursuivant le traitement, habituellement en 7 à 10 jours sans qu’il soit nécessaire d’ajuster les doses. Les formes graves (« flare-up ») nécessitent une prise en charge spécialisée (corticothérapie par voie générale notamment). Le meilleur traitement est préventif, en débutant l’isotrétinoïne chez les patients à risque (formes avec kystes et macrocomédons) par de faibles doses.
L’isotrétinoïne est un photosensibilisant, et l’exposition solaire importante aux rayons ultraviolets doit être évitée, nécessitant l’application répétée d’écran solaire à score de protection élevé (SPF 50).
Les effets indésirables ophtalmologiques à type de sécheresse oculaire, irritation ou conjonctivite sont observés chez 7,2 % des patients sous isotrétinoïne. Le recours à des lunettes de vue plutôt qu’à des lentilles de contact, l’utilisation de pommades ophtalmiques ou de larmes artificielles peut être nécessaire au cours du traitement.
Troubles musculosquelettiques
Ont été rapportées des myalgies, des arthralgies et une élévation du taux de créatine phosphokinase, notamment en cas d’activité physique intense. Une information des patients ayant une activité physique importante est nécessaire.Anomalies biologiques
Les anomalies biologiques sont rares (2 % des patients).Les plus fréquentes sont :
– une augmentation des enzymes hépatiques (alanine et aspartate aminotransférases [ALAT et ASAT]) très souvent dans les limites de la normale, et qui s’amende spontanément malgré la poursuite du traitement à la même dose ;
– une augmentation des taux de lipides sanguins, notamment des triglycérides, qui régresse après réduction des doses ou arrêt du traitement. Les mesures diététiques peuvent également être utiles. L’arrêt du traitement s’envisage lorsque l’augmentation ne peut être contrôlée et expose à un risque de pancréatite (supérieur à 800 mg/dL ou 9 mmol/L).
Un contrôle biologique, avec enzymes hépatiques et bilan lipidique, est recommandé avant et 1 mois après le début du traitement, puis une fois tous les 3 mois.
Effets indésirables gastro-intestinaux
Seulement 2 % des patients ont des troubles intestinaux à type de nausées, vomissements, diarrhée ou douleurs abdominales. Il n’a pas été démontré d’aggravation des maladies inflammatoires chroniques de l’intestin sous isotrétinoïne.Don du sang
Il existe une contre-indication au don du sang au cours du traitement et pendant 1 mois après la fin du traitement en raison du risque potentiel pour les fœtus des femmes enceintes transfusées.
Autres dermatoses faciales
Des essais contrôlés randomisés et l’expérience des dermatologues plaident pour l’utilisation de l’isotrétinoïne dans d’autres dermatoses faciales comme la rosacée, la dermite séborrhéique, la dermatose périorale ou les dermatoses mixtes. Ce traitement n’a pas l’AMM dans ces indications mais est cité dans les recommandations ou les articles de synthèse. La décision thérapeutique repose sur un avis d’expert dermatologique.
Rosacée
Il s’agit d’une dermatose faciale inflammatoire chronique. Le traitement initial recommandé des lésions inflammatoires papulopustuleuses d’intensité minime comporte surtout le métronidazole topique. Les formes modérées à sévères peuvent être traitées par les cyclines pendant 3 mois, traitement purement suspensif. Une étude multicentrique française en double insu, ayant inclus plus de 156 patients (en rechute ou résistants aux cyclines), a montré une efficacité de l’isotrétinoïne à faible dose (0,25 mg/kg/j) après 4 mois de traitement (57 % des patients avec une disparition d’au moins 90 % des lésions initiales).9 Cependant, il ne s’agit que d’un traitement suspensif, et il n’y a pas d’étude évaluant les modalités du traitement de maintenance.
Dermite séborrhéique
La dermite séborrhéique est une dermatose faciale chronique en lien avec une hyperséborrhée et la présence d’une levure lipophile du genre Malassezia. Le traitement repose sur des antifongiques locaux. Un essai randomisé comparatif entre un traitement local et un traitement par isotrétinoïne à faible dose (10 mg/j) pendant 6 mois a montré l’efficacité de ce dernier pour les dermatoses séborrhéiques modérées à sévères.10 Cependant, cet effet est suspensif, comme dans la rosacée.
Références
1. Le Cleach L, Lebrun-Vignes B, Bachelot A, et al. Guidelines for the management of acne: recommendations from a French multidisciplinary group. Br J Dermatol 2017;177:908-13.
2. Vallerand IA, Lewinson RT, Farris MS, et al. Efficacy and adverse events of oral isotretinoin for acne: a systematic review. Br J Dermatol 2018;178:76-85.
3. Bérard A, Azoulay L, Koren G, et al. Isotretinoin, pregnancies, abortions and birth defects: a population-based perspective. Br J Clin Pharmacol 2007;63:196-205.
4. Rouzès A, Jonville-Béra AP. Exposure to Isotretinoin during pregnancy in France : 25 years of follow up. Therapies 2014;69:53-63.
5. Tkachenko E, Singer S, Sharma P, et al. US Food and Drug Administration reports of pregnancy and pregnancy-related adverse events associated with isotretinoin. JAMA Dermatol 2019;155:11-75.
6. Huang YC, Cheng YC. Isotretinoin treatment for acne and risk of depression: A systematic review and meta-analysis. J Am Acad Dermatol 2017;76:1068-76.
7. Azoulay L, Blais L, Koren G, et al. Isotretinoin and the risk of depression in patients with acne vulgaris: a case-crossover study. J Clin Psychiatry 2008;69:526-32.
8. Droitcourt C, Nowak E, Rault C, et al. Risk of suicide attempt associated with isotretinoin: a nationwide cohort and nested case-time-control study. Int J Epidemiol 2019;48:1623-35.
9. Sbidian E, Vicaut É, Chidiack H, et al. A randomized-controlled trial of oral low-dose isotretinoin for difficult-to-treat papulopustular rosacea. J Invest Dermatol 2016;136:1124-9.
10. De Souza L, Kamamoto C, Sanudo A, Hassun KM, Bagatin E. Low-dose oral isotretinoin for moderate to severe seborrhea and seborrheic dermatitis: a randomized comparative trial. Int J Dermatol 2017;56:80-5.
2. Vallerand IA, Lewinson RT, Farris MS, et al. Efficacy and adverse events of oral isotretinoin for acne: a systematic review. Br J Dermatol 2018;178:76-85.
3. Bérard A, Azoulay L, Koren G, et al. Isotretinoin, pregnancies, abortions and birth defects: a population-based perspective. Br J Clin Pharmacol 2007;63:196-205.
4. Rouzès A, Jonville-Béra AP. Exposure to Isotretinoin during pregnancy in France : 25 years of follow up. Therapies 2014;69:53-63.
5. Tkachenko E, Singer S, Sharma P, et al. US Food and Drug Administration reports of pregnancy and pregnancy-related adverse events associated with isotretinoin. JAMA Dermatol 2019;155:11-75.
6. Huang YC, Cheng YC. Isotretinoin treatment for acne and risk of depression: A systematic review and meta-analysis. J Am Acad Dermatol 2017;76:1068-76.
7. Azoulay L, Blais L, Koren G, et al. Isotretinoin and the risk of depression in patients with acne vulgaris: a case-crossover study. J Clin Psychiatry 2008;69:526-32.
8. Droitcourt C, Nowak E, Rault C, et al. Risk of suicide attempt associated with isotretinoin: a nationwide cohort and nested case-time-control study. Int J Epidemiol 2019;48:1623-35.
9. Sbidian E, Vicaut É, Chidiack H, et al. A randomized-controlled trial of oral low-dose isotretinoin for difficult-to-treat papulopustular rosacea. J Invest Dermatol 2016;136:1124-9.
10. De Souza L, Kamamoto C, Sanudo A, Hassun KM, Bagatin E. Low-dose oral isotretinoin for moderate to severe seborrhea and seborrheic dermatitis: a randomized comparative trial. Int J Dermatol 2017;56:80-5.