C’est une maladie de l’oreille interne (labyrinthe), structure anatomique dédiée à l’audition et à l’équilibre. L’endolymphe, faible volume de liquide y circulant, a des caractéristiques – composition chimique, pression – permettant le bon fonctionnement des cellules sensorielles. La physiopathologie est discutée, mais des variations de la pression de l’endolymphe, définissant l’hydrops endolymphatique, sont probablement responsables. En cause : un défaut de sa résorption (dans le sac endolymphatique) et/ou un excès de sécrétion. La première théorie est renforcée par les études expérimentales. Chez l’animal, on voit une fibrose autour du sac, une hypoplasie ou une atrophie de celui-ci.2
Diagnostic : priorité à la clinique
Par exemple, il peut s’agir d’épisodes vertigineux répétés, sans manifestation auditive, ou d’acouphènes unilatéraux de tonalité grave sans troubles de l’équilibre.
Le diagnostic requiert les 4 types de manifestations :
– des crises vertigineuses rotatoires durant au minimum 20 minutes, parfois plusieurs heures ;
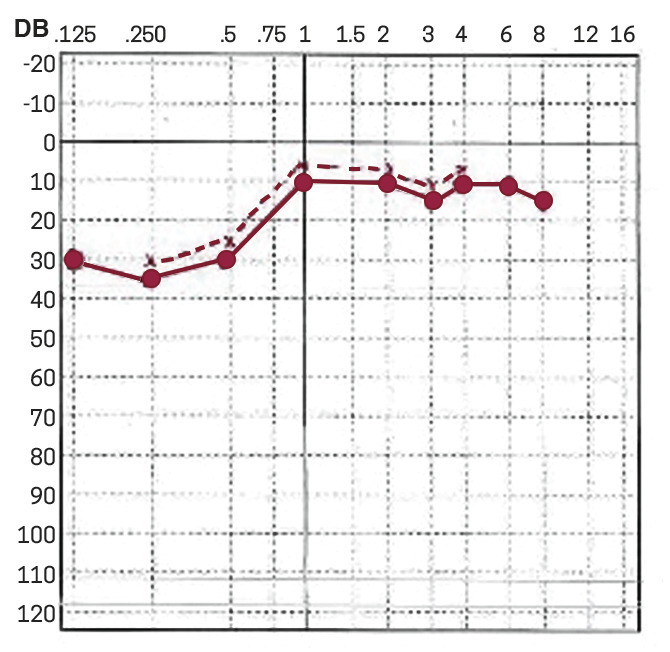
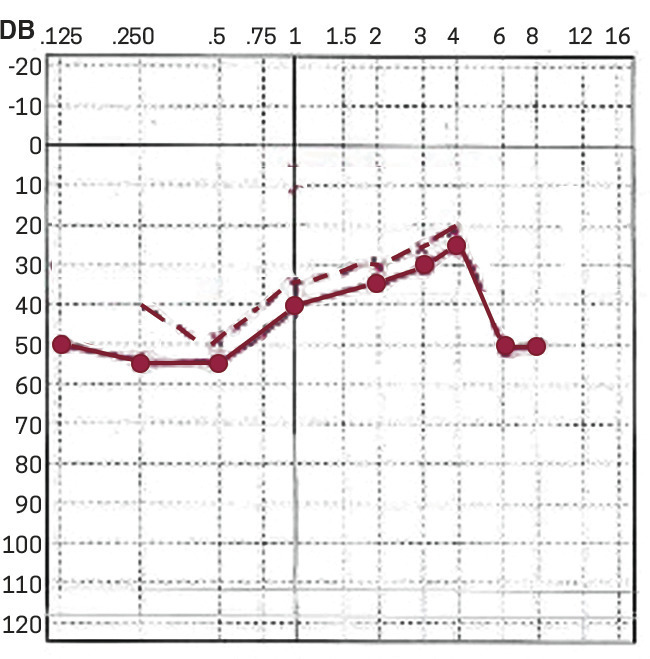
– une hypoacousie, touchant surtout les fréquences graves, à identifier en audiométrie. Cette baisse peut précéder de plusieurs mois ou années les vertiges ;
– des acouphènes de tonalité plutôt grave, et s’accompagnant d’une sensation de plénitude de l’oreille atteinte ;
– des symptômes fluctuants qui varient d’un jour à l’autre, voire au cours d’une même journée.
En raison de cette diversité, la classification fait la distinction entre possible, probable ou définie (
Habituellement recommandée, l’IRM vise à éliminer une lésion évolutive dont les symptômes seraient comparables (schwannome vestibulaire). En outre, des protocoles spécifiques semblent capables d’identifier des modifications morphologiques de l’oreille interne caractéristiques de l’hydrops endolymphatique. Les autres examens complémentaires apprécient l’impact sur les fonctions auditive et vestibulaire de l’oreille interne et évaluent par des mesures indirectes les variations pressionnelles des liquides du labyrinthe.
Examens de l’audition
Symptômes associés, plénitude d’oreille et acouphènes parfois importants, de tonalité grave, peuvent rendre difficile l’évaluation précise des seuils auditifs. D’où l’intérêt de la corrélation des données de l’audiométrie tonale, qui mesure les seuils pour les sons, avec celles de l’audiométrie vocale, qui évalue la compréhension des mots.
Répéter le bilan auditif permet d’apprécier le retentissement sur la communication, de surveiller l’audition du côté non atteint, et dans certains cas de décider (ou non) de certains traitements locaux.
Épreuves vestibulaires
La vidéonystagmographie (VNG) est réalisée en enregistrant les déplacements des yeux grâce à un système informatique, lors de différents tests de stimulation des capteurs de l’équilibre. La VNG explore principalement ceux localisés au niveau des canaux semi-circulaires. À cette occasion sont réalisées habituellement des épreuves rotatoires : le patient étant dans l’obscurité, l’examinateur fait tourner le fauteuil d’examen et enregistre la réponse au niveau oculaire. Normalement, lors de la rotation d’un côté, on observe un nystagmus : déplacement des globes oculaires dans le sens de la rotation du fauteuil. Au cours de la maladie, les réponses des 2 côtés peuvent être différentes.
Les épreuves caloriques consistent à réaliser une stimulation thermique en instillant de l’eau froide (30 °C) puis chaude (44 °C) durant 20 à 30 secondes, successivement dans chaque oreille, avec une pause de 5 minutes entre chaque test. En cas de perforation du tympan notamment, l’eau est remplacée par de l’air. Cela déclenche un nystagmus dont on comptabilise les secousses durant 30 secondes, pour chacun des 2 côtés, afin de mesurer et comparer la réflectivité vestibulaire.
Pour le test vibratoire osseux, la vibration au niveau de la mastoïde induit une stimulation brève (quelques secondes) à haute fréquence des capteurs de l’oreille interne. Son intérêt est de mettre en évidence une asymétrie entre les 2 côtés.
Le test d’Halmagyi (Head Impulse Test) a pour but de vérifier que les capteurs jouent bien leur rôle de stabilisation du regard, lors de mouvements très rapides que l’examinateur déclenche en mobilisant la tête du patient, ce dernier fixant un point. L’examinateur contrôle, soit directement en observant les yeux soit à l’aide d’un système vidéo, que le regard est bien stable en permanence. En effet, en cas de lésion de l’oreille interne, un mouvement très rapide des globes oculaires, appelé saccade, peut apparaître. Ce test peut être tout à fait normal en dehors des crises, mais il est très utile lors du suivi pour mesurer l’évolution de l’atteinte des 3 canaux semi-circulaires. Il est rapide à réaliser, comparé aux épreuves caloriques.
Identifier des modifications pressionnelles
Le plus ancien, l’électrocochléographie (EcoG), enregistre divers potentiels électriques générés par la cochlée et le premier relais nerveux des voies auditives lors d’une stimulation acoustique, l’électrode étant extratympanique (posée contre le tympan) ou transtympanique (à travers). Les temps d’examen relativement longs font que cette modalité est actuellement moins utilisée.
L’admittancemétrie multifréquentielle (AMF) développée en particulier à Bordeaux, repose sur l’analyse des mouvements du tympan. Vincent Darrouzet et Valérie Franco ont montré que la fréquence de résonance était plus basse chez des patients souffrant de Menière en dehors des crises que chez des témoins.
Tests de déphasage acoustique. Les otoémissions acoustiques (OEA) et les produits de distorsion des otoémissions acoustiques (PDA) ont fait l’objet de nombreux développements et utilisations : dépistage néonatal de la surdité en particulier, mais aussi évaluation de la fonction cochléaire lors de certaines surdités évolutives. Ils sont en effet les marqueurs de l’activité des cellules ciliées externes. Les perturbations pressionnelles dans le canal cochléaire accompagnant l’hydrops altèrent la mécanique de ces cellules. Dans la maladie de Menière, les OEA ont une sensibilité accrue aux faibles variations de pression intracrânienne.
Les travaux de Paul Avan et Thierry Mom, à Clermont-Ferrand, ont abouti à leur application en pratique courante. Un des moyens de faire varier ces pressions est une manœuvre posturale, par exemple le passage de debout à couché en décubitus dorsal. Les modifications pressionnelles se traduisent par une augmentation du déphasage.
Mesurer le retentissement fonctionnel est l’objet de ces examens. L’impact au quotidien est évalué par un autoquestionnaire (
Traitement
La bétahistine est le traitement de fond (24 mg matin et soir pendant 3 mois, renouvelable) le plus prescrit en France. Contre-indications : asthme et ulcère gastroduodénal. Les diurétiques (acétazolamide) sont à proscrire en cas de lithiases au niveau des voies urinaires. Les corticoïdes sont utilisés, là aussi en respectant leurs CI, par voie générale ou locale. Dans ce dernier cas, on peut injecter la dexaméthasone (3 fois en 3 à 10 jours) sous anesthésie locale, à travers le tympan. Cette solution est parfois proposée quand les symptômes restent importants et invalidants malgré les médicaments. Dans la majorité des cas, le traitement de fond réduit la fréquence et la sévérité des vertiges. Si crise aiguë : acétylleucine par voie orale ou injectable.
Si les symptômes ne sont toujours pas contrôlés (médicaments + rééducation vestibulaire), un traitement plus « radical » peut être envisagé. Il peut s’agir d’injections de gentamicine, là aussi par voie transtympanique, ou d’une intervention chirurgicale qui consiste à sectionner le nerf vestibulaire : neurotomie vestibulaire. D’autres solutions existent.
L’élément important est que le patient soit pris en charge par un praticien qui puisse d’une part évaluer l’impact des symptômes, et d’autre part envisager avec lui chacune des options, en l’informant des avantages et inconvénients.
Par ailleurs, l’appareillage audioprothétique est à discuter selon l’importance de la perte auditive et des éventuels acouphènes.
Les atteintes bilatérales sont rares. Si elles sont simultanées avec baisse auditive bilatérale rapidement évolutive et vertiges fréquents, on doit rechercher une pathologie auto-immune s’exprimant au niveau de l’oreille interne. Elle peut faire partie d’une maladie systémique (syndrome de Cogan…) ou être isolée.
Maladie de Menière : évaluer l’impact symptomatique par un autoquestionnaire
Stade 1
Ma maladie vertigineuse n’a aucun retentissement sur mes activités.
Stade 2
Quand j’ai un vertige, je dois arrêter mes activités pour un certain temps, mais le vertige s’arrête rapidement et je peux les reprendre.
Je continue à travailler, à conduire et m’implique dans la plupart de mes activités.
Je n’ai pas eu besoin d’aménager mes projets ni de faire certaines adaptations de mes activités à cause de mes vertiges.
Stade 3
Quand j’ai un vertige, je dois arrêter mes activités pour un certain temps, mais le vertige s’arrête rapidement et je peux les reprendre.
Je continue à travailler, à conduire et m’impliquer dans la plupart de mes activités.
J’ai dû aménager mes projets et faire certaines adaptations de mes activités à cause de mes vertiges.
Stade 4
Je suis capable de travailler, conduire, m’occuper de ma famille et m’impliquer dans la plupart de mes activités, mais cela me demande constamment des efforts importants et d’économiser mon énergie.
Stade 5
Je suis incapable de travailler, conduire, m’occuper de ma famille ou m’impliquer dans la plupart des activités que j’avais l’habitude de faire. Même les activités essentielles me sont difficiles à réaliser. Je suis handicapé(e).
Stade 6
J’ai arrêté de travailler depuis 1 an ou plus et/ou je touche une indemnisation à cause de mes problèmes de vertiges ou déséquilibre.
2. Ferrary E, Bouccara D. Maladie de Menière. EMC - Oto-rhino-laryngologie 2017;13:1-13 [Article 20-205-A-10].
3. Committee on Hearing and Equilibrium guidelines for the diagnosis and evaluation of therapy in Meniere’s disease. American Academy of Otolaryngology-Head and Neck Foundation, Inc. Otolaryngol Head Neck Surg 1995;113:181-5.
4. Derrebery MJ, KI Berliner. Characteristics, onset and progression in Meniere’s disease. In: Lim DJ. Proceedings of the 5 th International Symposium on Menière’s disease & inner ear homeostasis disorders. Los Angeles: House Ear Institute publications; 2005:128-30.
5. Huppert D, Strupp M, Brandt T. Long-term course of Menière’s disease revisited. Acta Otolaryngol 2010;130:644-51.

 Encadrés
Encadrés