La maladie de Willebrand est une affection hémorragique héréditaire résultant d’un déficit du facteur von Willebrand (vWF). Ce facteur, synthétisé par les cellules endothéliales et les mégacaryocytes, intervient dans l’hémostase primaire et permet l’adhésion des plaquettes au sous-endothélium ; il a également pour rôle de transporter le facteur VIII et de le protéger contre la dégradation.
On en distingue trois types, de gravité variable selon l’importance du déficit en facteur Willebrand :
- le type 1 correspond à un déficit en vWF quantitatif et partiel (60 à 80 % des cas) ;
- le 2 à un défaut qualitatif (fonction altérée, 20 à 35 %) ;
- le 3 à un déficit quasi-total (forme la plus sévère mais extrêmement rare, avec une prévalence de 1/1 000 000).
Sa transmission est habituellement autosomique dominante : elle touche ainsi les deux sexes.
La prise en charge et le suivi spécialisés sont réalisés par les médecins spécialistes de l’hémostase des Centres de ressources et de compétence des maladies hémorragiques constitutionnelles (CRC-MHC). Le médecin du CRC-MHC remet au patient une carte de soins et d’urgence, précisant le type de la maladie et les traitements appropriés, à présenter aux professionnels de santé amenés à le prendre en charge. Le médecin traitant intervient dans le diagnostic et le suivi au long cours de ces patients ; il doit connaître les précautions à prendre pour éviter les situations à risque de saignement.
Quand l’évoquer ?
La plupart des patients sont asymptomatiques, avec des déficits mineurs ne provoquant pas de problème hémorragique dans la vie courante. Dans les formes symptomatiques, le tableau est dominé par des saignements muqueux (épistaxis, gingivorragies), cutanés (ecchymoses, saignements prolongés de plaies mineures) et des ménométrorragies. En cas de maladie de type 3, en raison d’un taux de FVIII très bas (souvent 10 %), les signes hémorragiques sont proches de ceux des hémophiles sévères : hémarthroses et arthropathies chroniques, hématomes musculaires, parfois graves.
On peut aussi observer des hémorragies gastro-intestinales et des complications hémorragiques post-opératoires, gynéco-obstétricales ou au décours d’extractions dentaires.
Ces manifestations doivent faire évoquer le diagnostic et motiver un hémogramme et un bilan de l’hémostase. Une thrombopénie chronique inexpliquée doit également faire rechercher une maladie de Willebrand. Mais attention : des tests standards de l’hémostase normaux (TP, TCA, TCK) n’excluent pas le diagnostic. Au moindre doute, adresser le patient en consultation spécialisée. La confirmation du diagnostic repose sur des dosages spécifiques du complexe facteur Willebrand/facteur VIII (VWF/FVIII) ; leur interprétation, délicate et fonction du contexte clinique, est du ressort du spécialiste de l’hémostase.
Médicaments
Parfois, un traitement symptomatique antifibrinolytique per os (ou en bain de bouche) est prescrit par le spécialiste, pour arrêter les saignements de nez ou de bouche, ou pour réduire les ménorragies. Le médecin traitant peut renouveler ces traitements adjuvants (acide tranexamique : Exacyl ou Spotof), mais aussi les hémostatiques d’appoint (Coalgan, Algosteril, pommade cicatrisante HEC, pommade type Hemoclar ou contenant de l’arnica).
Attention : sauf cas très spécifiques, les agents antiplaquettaires comme l’aspirine sont contre-indiqués ; il faut aussi éviter les AINS car susceptibles d’aggraver la symptomatologie hémorragique, ainsi que certaines plantes telles que le Ginkgo biloba.
Vaccination : quelles précautions ?
Les enfants et les adultes atteints d’une maladie de Willebrand, quelle que soit la sévérité du déficit, doivent bénéficier de la couverture vaccinale complète selon les recos actuelles. Il était habituellement recommandé de réaliser cette vaccination par voie sous-cutanée en raison du risque d’hématome intramusculaire. Des données récentes de la littérature laissent penser que la voie IM reste acceptable en termes d’efficacité (meilleure tolérance locale, respect des RCP du vaccin) et de risque (hématome). Les vaccinations peuvent donc être réalisées soit par voie IM soit par voie SC (selon le choix du praticien et le vaccin), en privilégiant la région deltoïdienne ou la partie supéro-externe de la cuisse (selon l’âge), ce qui facilite une compression locale prolongée après injection (10 minutes) ; il est recommandé d’utiliser une aiguille de petit diamètre (25 G).
Adapter les activités
Pour les formes les plus sévères, le médecin traitant intervient dans la mise en place du Protocole d’accueil individualisé (PAI) établi par le médecin du CRC-MHC dans l’enfance.
De même, la pratique des sports de contact à risque traumatique et de certaines activités de parc d’attraction se discute en fonction du degré de sévérité de la maladie avec le médecin du CRCMHC.
Chez les femmes : ménorragies, anémie, désir de grossesse, IVG…
Les ménorragies sont fréquentes chez les femmes atteintes de maladie de Willebrand et retentissent sur la qualité de vie. Lorsque l’anomalie de l’hémostase est connue dès l’enfance, le risque de ménorragie est à anticiper, notamment dans les formes sévères. Néanmoins, les ménorragies peuvent être le point d’appel clinique initial.
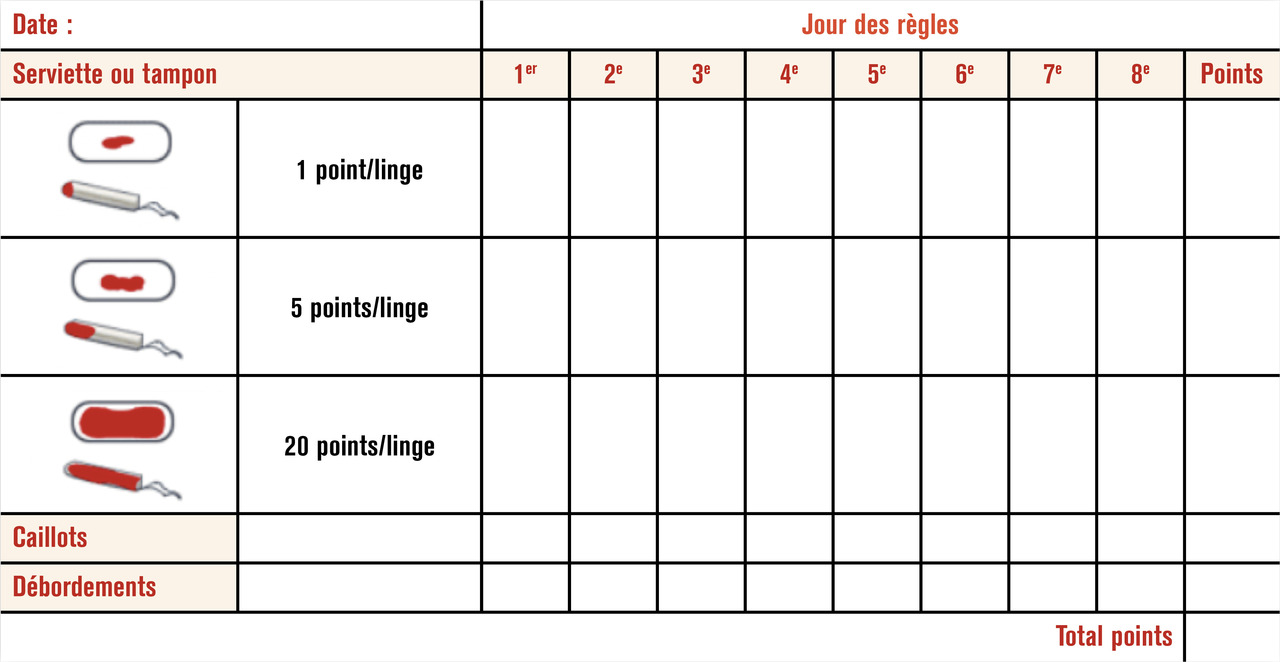
Il est important d’évaluer leur intensité par le score de Higham (fig. 1), qui permet de quantifier le nombre quotidien de changes, l’abondance de l’imprégnation du change et la durée des règles. La fiche de score est complétée au domicile par la jeune fille en temps réel sur 3 cycles consécutifs. Un score > à 100 définit la ménorragie (correspondant à un saignement > à 80 mL).
Un bilan martial doit être régulièrement pratiqué pour dépister précocement une anémie ferriprive afin de proposer le cas échéant un traitement per os de la carence martiale.
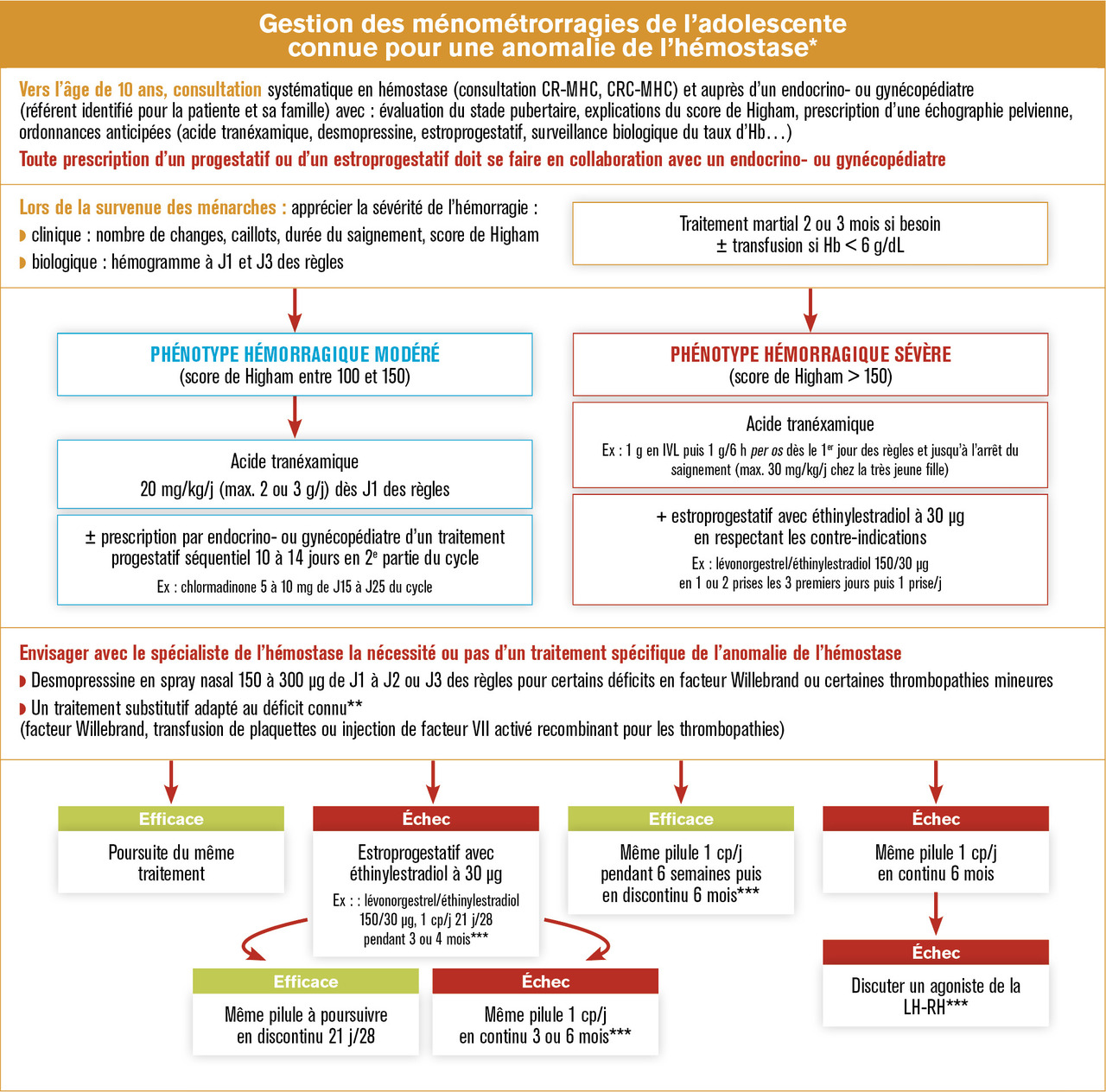
Le traitement des ménorragies varie en fonction des différentes étapes de la vie génitale des femmes et de la sévérité des symptômes. Dans un premier temps, il est non spécifique : contre-indication aux AINS, acide tranexamique. Un traitement hormonal peut ensuite être associé, en séquentiel ou en continu. Chez les patientes non répondantes, un traitement spécifique (substitutif vWF et/ou FVIII ou desmopressine) peut être nécessaire. La conduite à tenir thérapeutique est résumée dans la figure 2. Attention : les progestatifs à faible dose (pilule microprogestative) ne sont pas recommandés en première intention du fait du risque de spotting associé ; les DIU au cuivre simple sont fortement déconseillés car ils augmentent les ménorragies.
En prévision d’une grossesse ou d’une intervention chirurgicale, une prise en charge multidisciplinaire est indispensable. Les fausses couches sont une autre situation à risque : la prise en charge varie en fonction de l’abondance du syndrome hémorragique (classique, ou acide tranexamique, ou traitement substitutif ou desmopressine) ; il faut préférer l’aspiration à un traitement médicamenteux en raison du risque d’hémorragie à domicile dont la survenue n’est pas prévisible. Ces précautions peuvent être appliquées aussi en cas d’IVG.
Personnes âgées
La population des patients atteints de cette maladie vieillit, et de nombreuses comorbidités (maladies cardiovasculaires, arthrose, cancers…) viennent compliquer leur prise en charge. Le facteur Willebrand augmente physiologiquement avec l’âge, d’où une diminution de la fréquence et de la sévérité de la symptomatologie hémorragique.
En principe, la maladie hémorragique ne devrait pas être un facteur limitant le traitement adéquat de ces comorbidités. Mais il faut toujours réaliser les procédures invasives si et seulement si leur indication est formelle pour que cela ne soit pas une perte de chance pour le patient. Le risque hémorragique est à évaluer avant toute procédure invasive ou tout traitement pouvant majorer ce risque (anticoagulants, antiagrégants plaquettaires, certaines chimiothérapies). Pour en savoir plus : Bally C, Lasne D, Harroche A. Maladie de Willebrand : grande hétérogénéité clinique et biologique. Rev Prat Med Gen 2019;33(1018);258-9.
Itzhar-Baïkian N, Veyradier A, Dillinger JG, et al. Maladie de Willebrand du sujet âgé. Rev Prat 2018;68(10);1125-30.
Bally C, Lasne D, Harroche A. Maladie de Willebrand : grande hétérogénéité clinique et biologique. Rev Prat Med Gen 2019;33(1018);258-9.
Harroche A, Meunier S, Falaise C, et al. Ménométrorragies de l’adolescente et de la jeune femme ayant un trouble héréditaire de l’hémostase. Rev Prat 2019;69(4);417.