Une nouvelle trithérapie a récemment été autorisée pour le traitement de certains patients atteints de mucoviscidose. La HAS vient d’en élargir les indications en accès précoce. Qui est concerné ? Quels bénéfices ? Quelle place pour le MG dans la surveillance ? Le point sur cette grande avancée thérapeutique.
Les personnes atteintes d’une mucoviscidose et porteuses d’au moins une mutation F508del du gène CFTR (cystic fibrosis transmembrane regulator) peuvent bénéficier d’une nouvelle spécialité, Kaftrio 75 mg/50 mg/100 mg comprimé pelliculé, une trithérapie composée de :
– tézacaftor et élexacaftor, deux substances qui augmentent le nombre de protéines CFTR,
– et ivacaftor, qui améliore l’activité de la protéine CFTR défectueuse (substance déjà disponible dans la spécialité Kalydeco, et utilisée en association dans d’autres spécialités).
Pour rappel, la mucoviscidose, maladie génétique autosomique récessive, a une prévalence en Europe de 1/3 000 naissances. Affection chronique touchant de nombreux organes (poumons, pancréas, foie, intestins, peau, appareil urogénital...), elle est responsable d’une importante altération de la qualité de vie, malgré un support nutritionnel, l’apport d’extraits pancréatiques, une kinésithérapie respiratoire pluriquotidienne et des cures répétées d’antibiotiques. Le dépistage néonatal systématique, les traitements non spécifiques et une prise en charge multidisciplinaire dans les 47 centres de ressources et de compétences (CRCM) français ont permis de porter l’espérance de vie à la naissance au-delà de 35 ans, mais cette maladie est encore responsable d’une mortalité parfois précoce, et ce malgré la transplantation pulmonaire ou de multiples organes.
En août 2020, la trithérapie Kaftrio a obtenu une AMM en France pour les patients de 12 ans et plus atteints de mucoviscidose et porteurs d’au moins une mutation F508del du gène CFTR, ayant démontré une excellente efficacité notamment sur la réduction du chlore sudoral, l’amélioration de la fonction respiratoire, la diminution des exacerbations pulmonaires annuelles et la consommation d’antibiotiques.
Le 7 janvier 2022, une extension d’AMM a été accordée pour les patients âgés de 6 ans à 11 ans, et la HAS vient de l’autoriser en accès précoce dans cette classe d’âge, mais uniquement pour les patients qui sont hétérozygotes pour la mutation F508del du gène CFTR et porteurs d’une mutation de ce même gène à fonction minimale (une indication plus restreinte que dans l’AMM). Selon les chiffres de 2018 du registre français de la mucoviscidose (dont l’exhaustivité est estimée à 90 %) et en prenant en compte l’augmentation de la prévalence de cette maladie (3,09 % par an), 288 enfants seraient concernés par cette autorisation d’accès précoce.
Quelles indications ?
Ce médicament est indiqué comme traitement de fond de première intention, en association avec l’ivafactor, chez les patients :
– homozygotes pour la mutation F508del du gène CFTR (présente chez plus de 80 % des patients du registre français de la mucoviscidose, elle conduit à un défaut de conformation, de maturation et de transport intracellulaire de la protéine CFTR) ;
– ou hétérozygotes pour cette mutation et porteurs d’une mutation du gène CFTR à fonction minimale, c’est-à-dire entraînant l’absence de synthèse de la protéine ou la synthèse d’une protéine insuffisamment fonctionnelle, peu susceptible de répondre à d’autres modulateurs du canal CFTR (tézacaftor, ivacaftor ou une association des deux).
Le traitement est soumis à prescription initiale hospitalière semestrielle, établie par un médecin expérimenté dans le traitement de la mucoviscidose, mais son renouvellement n’est pas restreint. Il est remboursable à 65 %, au prix de 10 158,27 € (boîte de 56, pour 28 jours de traitement).
Si le génotype du patient n’est pas connu, un génotypage par une méthode fiable et validée devra être réalisé pour confirmer la présence d’au moins une mutation F508del.
Quelle posologie ?
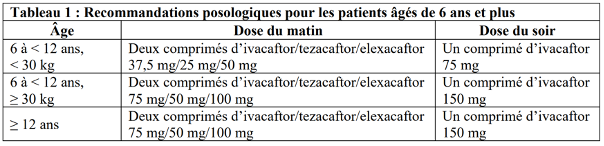
Ce médicament est utilisé en association avec l’ivacaftor (Kalydeco) selon le schéma suivant (tableau 1) :
– matin : 2 comprimés de Kaftrio avec un repas ou une collation riche en graisse (contenant par exemple beurre, huile, œufs, fromage, fruits à coque, lait entier ou viande) ; à l’inverse, éviter des aliments ou boissons contenant du pamplemousse (inhibiteur du CYP3A) ;
– soir (intervalle de 12 heures avec prise du matin) : 1 comprimé de Kalydeco.
Certaines situations imposent une adaptation de la dose ou une utilisation prudente :
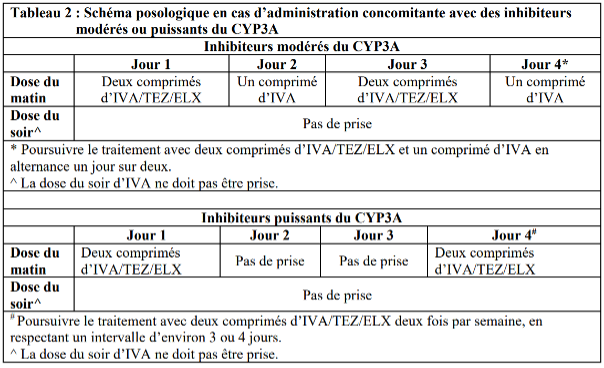
– posologie réduite en cas d’administration concomitante avec des inhibiteurs du CYP3A (modérés tels que fluconazole, érythromycine, vérapamil, ou puissants tels que kétoconazole, itraconazole, posaconazole, voriconazole, télithromycine et clarithromycine) (tableau 2) ;
– insuffisance hépatique : utilisation (avec éventuelle adaptation de posologie) à envisager selon son niveau de sévérité (tableau 3).
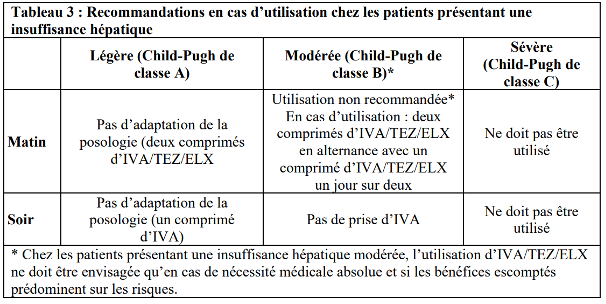
Source : Résumé des caractéristiques du produit. Kaftrio 75 mg/50 mg/100 mg, comprimé pelliculé.
Quelle surveillance ?
1. Foie
Les taux de transaminases (ALAT et ASAT) doivent être contrôlés :
– avant l’instauration du traitement,
– tous les 3 mois durant la première année de traitement,
– puis 1 fois par an.
La surveillance doit être plus fréquente chez les patients ayant des antécédents d’augmentation des transaminases.
2. Cristallin
Chez les patients pédiatriques, des examens ophtalmologiques avant et pendant le traitement sont recommandés afin de surveiller le risque d’opacité du cristallin.
En outre, cette spécialité fait l’objet d’une surveillance supplémentaire qui doit permettre l’identification rapide de nouvelles informations relatives à la sécurité : les professionnels de santé déclarent tout effet indésirable suspecté.
Globalement, quelle place pour le généraliste ?
Si la prise en charge et le suivi des malades sont assurés par les 47 CRCM français, le médecin traitant gère surtout les pathologies intercurrentes survenant en dehors des consultations au CRCM. Son rôle clé est le dépistage précoce des complications : exacerbations pulmonaires, hémoptysies, pneumothorax et décompensations diabétiques.
LMA, La Revue du Praticien
Pour en savoir plus :
HAS. Mucoviscidose : accès précoce accordé à l’association Kaftrio/Kalydeco. 29 mars 2022.
Paitraud D. Mucoviscidose : Kaftrio, première trithérapie à base d’ivacaftor, tezacaftor et elexacaftor. Vidal 22 juillet 2021.
Académie nationale de médecine. Mucoviscidose : la révolution thérapeutique des modificateurs du canal CFTR. 5 octobre 2021.
À lire aussi :
Corvol H. Mucoviscidose.Rev Prat Med Gen 2018;32(993);23-9.
Corvol H. Mucoviscidose : quel traitement de fond ?Rev Prat Med Gen 2020;34(1051);817-8.
Mortuaire G. Rhinosinusite chronique de l’adulte et mucoviscidose.Rev Prat 2019;69(3);279-80.
