Connaître l’urgence du diagnostic et de la prise en charge des mononeuropathies multiples.
Il est donc possible de s’appuyer sur ces recommandations pour guider la démarche diagnostique devant un patient suspect de NP.
Définitions et principaux cadres pathogéniques
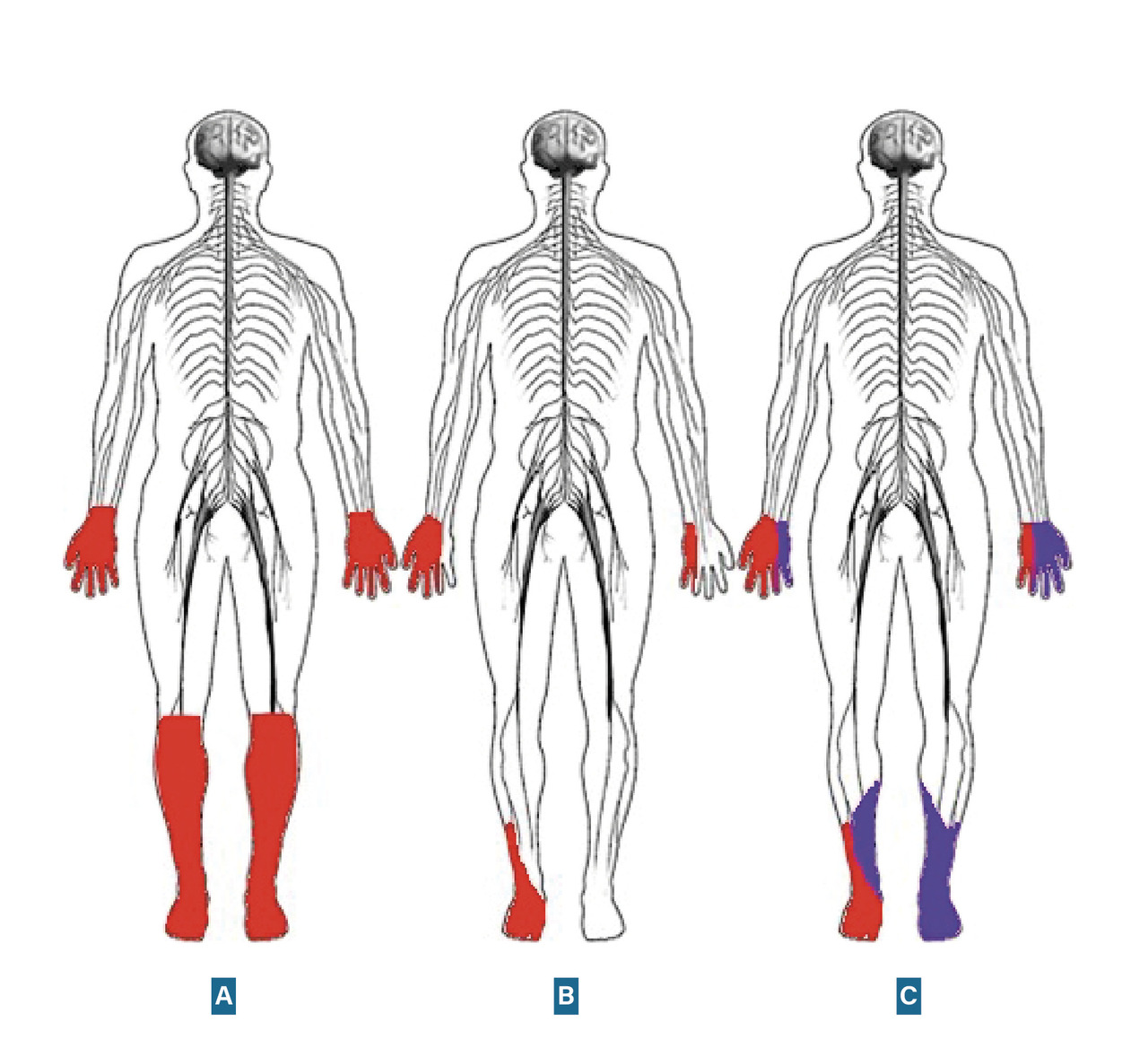
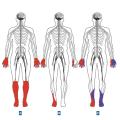
Selon la topographie
Selon la structure atteinte
En cas d’atteinte des grosses fibres myélinisées, les patients ont une aréflexie généralisée, des troubles de la statique avec signe de Romberg, parfois une main instable ataxique, des troubles sensitifs proprioceptifs et, assez fréquemment, un tremblement des extrémités.
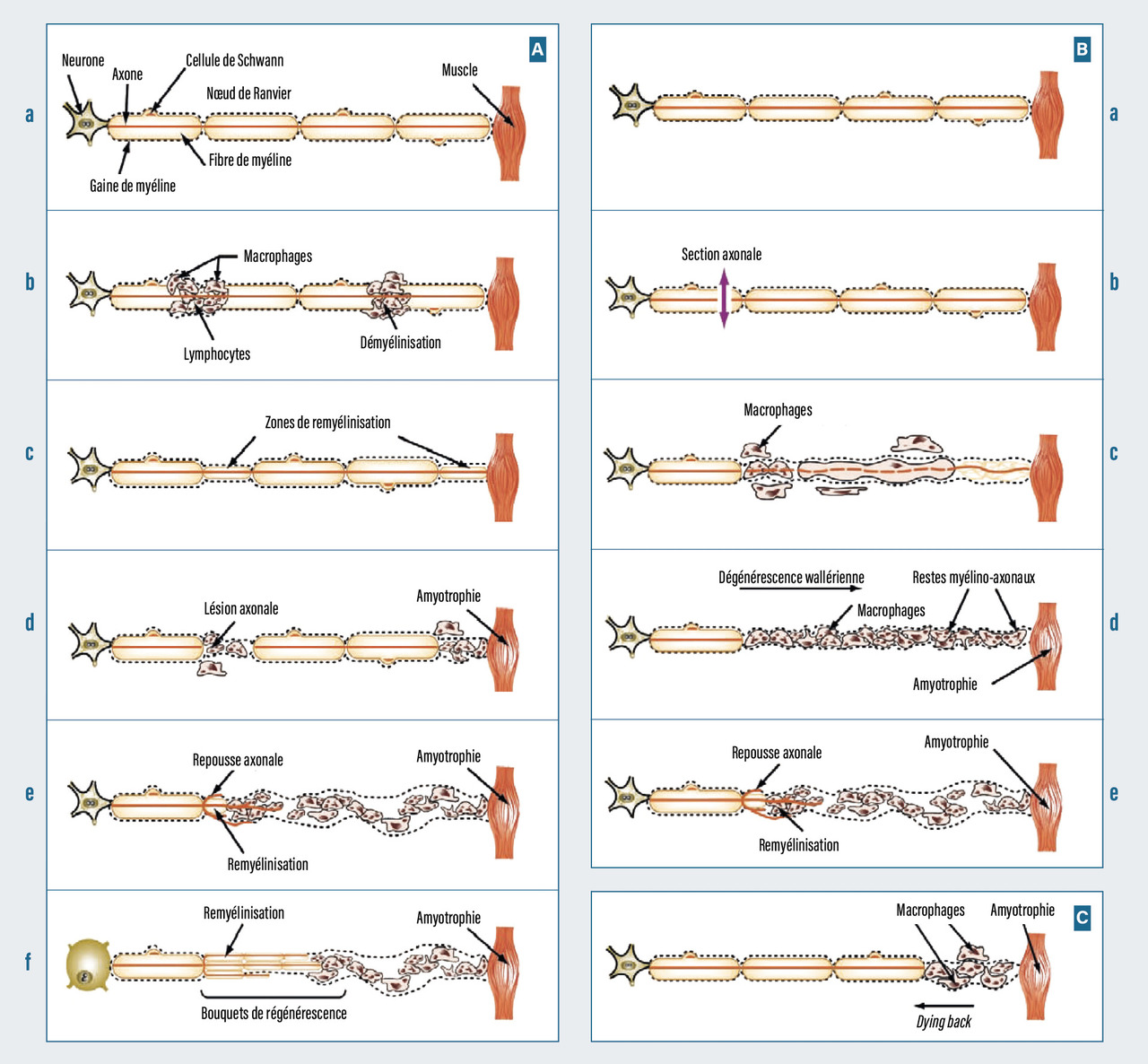
L’atteinte peut concerner directement les fibres nerveuses, comme dans les neuropathies toxiques. Dans d’autres cas, ce sont des lésions variées du tissu interstitiel au niveau des trois tuniques du nerf (endonèvre, épinèvre et périnèvre) qui occasionnent une atteinte secondaire des fibres nerveuses. Il peut s’agir d’anomalies concernant les vaisseaux (infiltrats cellulaires périvasculaires, vascularites), d’une prolifération exagérée du tissu interstitiel, de l’apparition de macrophages plus ou moins chargés de débris lipidiques, de cellules inflammatoires, de granulomes, de cellules anormales parfois malignes ou de dépôts divers (amylose, immunoglobulines).
Démarche diagnostique
Principes
La première consiste à évoquer puis confirmer le diagnostic de neuropathie périphérique : c’est le rôle de l’interrogatoire, puis de l’examen clinique et de l’examen électrophysiologique.
La deuxième étape consiste à tenter de classer la neuropathie dans un grand cadre topographique (polyneuropathie, mononeuropathie multiple, polyradiculonévrite, etc.) et pathogénique (axonopathie, myélinopathie...) : c’est le rôle de l’examen clinique puis de l’examen électrophysiologique. La troisième étape consiste à établir le diagnostic étiologique de la neuropathie. Cette étape est plus ou moins longue et difficile en fonction des cas. Elle s’appuie d’une part sur une analyse rigoureuse des données cliniques et électrophysiologiques, et d’autre part sur une bonne connaissance des grands cadres étiologiques relevant de spécialités aussi variées que l’endocrinologie, l’infectiologie, l’hématologie et la médecine interne. Les principales causes de mononeuropathie multiple et de neuropathie périphérique sont listées dans les
Approche clinique
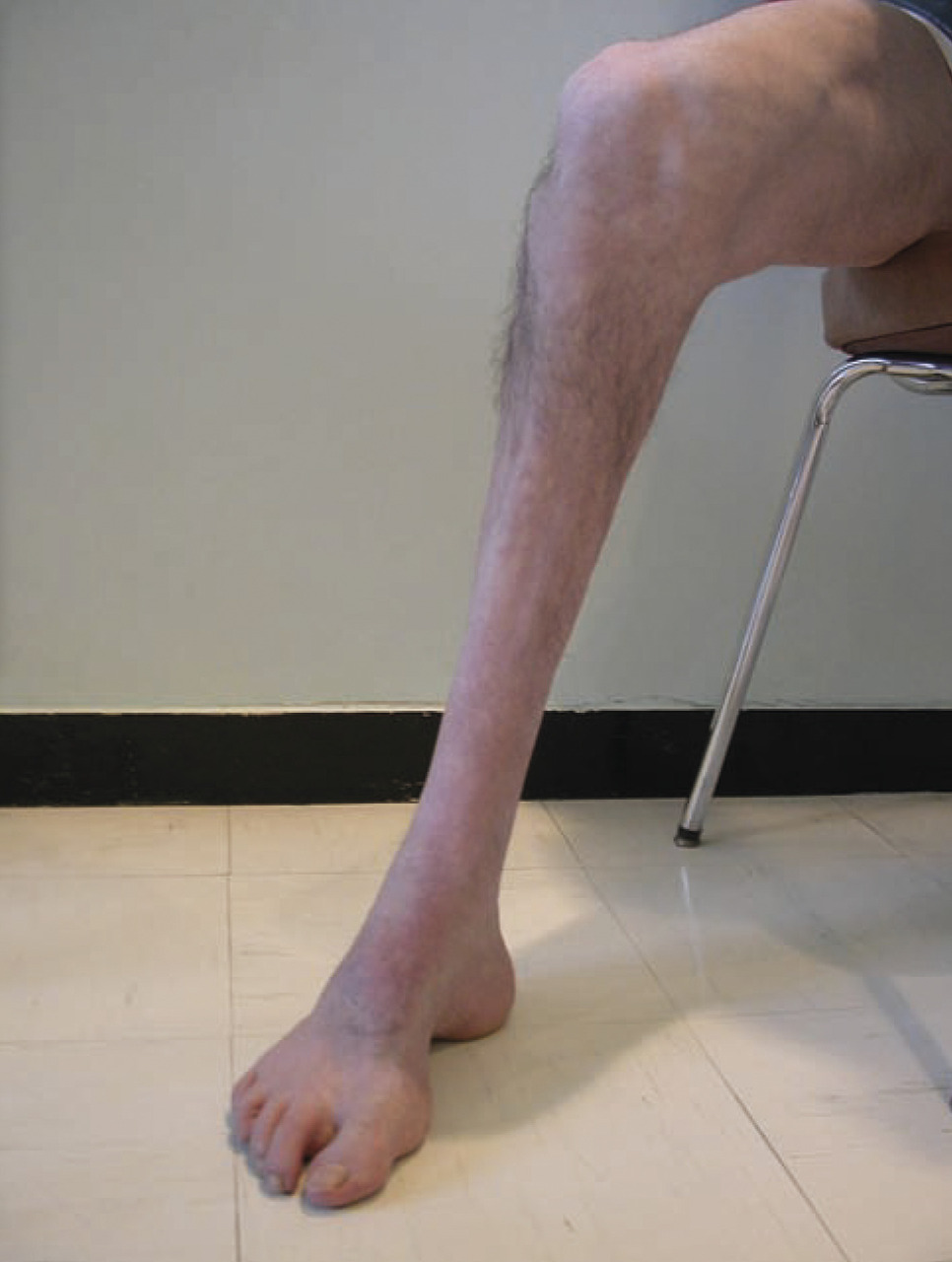
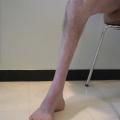
L’examen clinique recherche des arguments objectifs en faveur d’une neuropathie périphérique : troubles sensitifs objectifs, aréflexie tendineuse, déficits moteurs, amyotrophie. Il peut mettre en évidence des signes orientant vers une neuropathie héréditaire : pieds creux, amyotrophie péronière marquée, cyphoscoliose (
Au terme de cette première étape, l’interrogatoire du patient doit s’attacher à rechercher des causes communes de NP : consommation éthylique, diabète (son ancienneté, ses complications), prise de médicaments neurotoxiques, maladie systémique, hypothyroïdie, affection maligne, exposition à des toxiques environnementaux.
Examen électrophysiologique
Dans les autres cas, l’examen électroneuromyographique constitue un temps crucial dans le bilan d’une NP. Il est utile d’en connaître les grands principes et les limites, la limite principale étant que l’étude des vitesses de conduction nerveuse ne renseigne que sur le fonctionnement des fibres les plus rapides, c’est-à-dire les fibres myélinisées de gros calibre. Ainsi, les vitesses de conduction et les amplitudes motrices ou sensitives peuvent être normales en cas d’atteinte élective des petites fibres myélinisées et/ou des fibres amyéliniques.
L’étude des vitesses de conduction motrice s’effectue en stimulant électriquement les troncs nerveux en différents points de leur trajet, et en recueillant un potentiel moteur (potentiel global d’action musculaire) en surface, sur les muscles innervés par les nerfs stimulés. Différents paramètres sont enregistrés tels que la vitesse de conduction, l’amplitude des potentiels, les latences distales et proximales.
L’étude des vitesses sensitives s’effectue par stimulation des fibres sensitives d’un tronc nerveux en un point de son trajet, et enregistrement d’un potentiel sensitif en un autre point, sur le même tronc nerveux. Les paramètres enregistrés sont l’amplitude du potentiel et la vitesse de conduction sensitive.
L’examen, en plus de confirmer et topographier l’atteinte du système nerveux périphérique, permet d’en apprécier de façon non invasive le processus physiopathologique. Schématiquement, une neuropathie démyélinisante se traduit surtout par une réduction des vitesses de conduction, des latences distales allongées, éventuellement par des blocs de conduction ou des aspects de dispersion temporelle des potentiels. En revanche, une neuropathie axonale se traduit par des baisses d’amplitude des potentiels sensitifs et/ou moteurs sans altération significative des vitesses de conduction nerveuse. L’examen de détection à l’aiguille se déroule en introduisant dans les muscles à étudier une aiguille de petit calibre permettant d’enregistrer les activités musculaires spontanées (de repos) et lors d’efforts de contraction volontaire. Différentes activités musculaires anormales peuvent être enregistrées au repos, traduisant un dysfonctionnement plus ou moins marqué des axones moteurs. Les aspects observés sur les tracés d’effort renseignent, quant à eux, sur l’étendue de la perte en fibres nerveuses (la réduction des unités motrices enregistrables étant directement liée à la perte en fibres nerveuses motrices) ; c’est pourquoi cette partie de l’examen a une valeur pronostique.
Au terme du premier bilan que constituent l’examen clinique et l’exploration électrophysiologique, le clinicien doit, dans le meilleur des cas, être en mesure de porter un diagnostic électroclinique, précisant le mode d’installation et l’évolution des symptômes et signes, le type de fibres nerveuses atteintes, la distribution des lésions, le processus pathologique supposé et la sévérité de l’atteinte.
Examens de base
Pour la HAS, la pratique d'une électrophorèse des protéines sériques ou, plus volontiers, d’une immunofixation du sérum pour recherche d’un composant monoclonal n’est pas recommandée en première intention.
Bilan approfondi
Sérologies
VIH : elle est réalisée de façon systématique.Borrelia : elle est demandée en cas de contexte évocateur de méningoradiculonévrite après morsure de tique.
Hépatite B : la sérologie est surtout utile dans un contexte de mononeuropathie multiple si une périartérite noueuse est suspectée.
Hépatite C : la sérologie est nécessaire en cas de mononeuropathie multiple ou de neuropathie axonale sensitive, et surtout en cas de cryoglobulinémie.
Campylobacter jejuni : la sérologie est réalisée en cas de suspicion de syndrome de Guillain-Barré (
Examens immunologiques
Anticorps antinucléaires, anticorps anti-ADN, anticorps anti-SSA, anti-SSB, anticorps anticytoplasme des polynucléaires (ANCA), enzyme de conversion de l’angiotensine, cryoglobulinémie : ces recherches sont intéressantes pour identifier une maladie de système ou une vascularite associée à la neuropathie.Ponction lombaire
Elle présente trois intérêts principaux :- étayer un diagnostic de polyradiculonévrite aiguë ou chronique en montrant une hyperprotéinorachie isolée (dissociation albuminocytologique) ;
- rechercher une méningite lymphocytaire associée à la neuropathie (dans le cadre d’une méningoradiculonévrite) et la présence éventuelle de micro-organismes par sérologie ou PCR (borréliose) ;
- mettre en évidence des cellules anormales, notamment en cas de suspicion de lymphome malin avec infiltration radiculaire.
Biopsie nerveuse, neuromusculaire, cutanée
Elle est utile, notamment si elle permet de contribuer à identifier une neuropathie curable ou si elle peut préciser le mécanisme d’une neuropathie et influer sur la prise en charge ultérieure. La biopsie nerveuse a perdu de son intérêt pour le diagnostic de la plupart des neuropathies héréditaires, où elle est supplantée par la génétique moléculaire, et dans les polyradiculonévrites chroniques, où l’analyse électroclinique combinée à celle du liquide céphalorachidien suffit souvent pour poser le diagnostic.Parmi les principales indications actuelles de la biopsie nerveuse subsistent :
- la recherche de vascularite, généralement devant une mononeuropathie multiple ou une polyneuropathie axonale d’évolution rapide et sévère accompagnée d’un syndrome inflammatoire biologique (on prélève alors souvent un fragment de muscle en même temps que de nerf pour augmenter le rendement de l’examen). Il s’agit là d’une urgence diagnostique et thérapeutique ;
- la recherche d’amylose, devant un contexte évocateur : neuropathie axonale de cause indéterminée avec atteinte préférentielle des petites fibres et signes de dysautonomie. Dans ce cas de figure, la biopsie nerveuse n’est réalisée que si la recherche de mutation du gène de la transthyrétine est négative (amylose héréditaire) et si aucun dépôt amyloïde n’a été mis en évidence par des biopsies de tissus plus facilement accessibles (glandes salivaires accessoires, graisse abdominale, peau) ;
- confirmation d’une infiltration lymphomateuse, surtout en cas d’altération de l’état général et de neuropathie douloureuse ;
- confirmation d’une lèpre ou d’une sarcoïdose.
Autres
Selon le contexte, divers examens peuvent être réalisés, tels que : scanner thoraco-abdomino-pelvien, radiographies du squelette, biopsie ostéomédullaire à la recherche d’un cancer solide ou d’un lymphome malin, biopsie des glandes salivaires accessoires (pour confirmer un diagnostic de syndrome de Gougerot-Sjögren ou une amylose), recherche d’anticorps antineuronaux (en cas de suspicion de neuropathie paranéoplasique).Une étude en génétique moléculaire est également réalisée en fonction du contexte : histoire familiale, pieds creux, cyphoscoliose, amyotrophie péronière sévère chez un adulte jeune, etc.
Diagnostic différentiel des neuropathies
Distinguer cliniquement une neuropathie périphérique d’une sclérose latérale amyotrophique
L’examen clinique attentif montre souvent que certains troncs nerveux sont atteints et d’autres épargnés, ce qui n’est pas compatible avec la SLA dont l’atteinte concerne les motoneurones.
C’est surtout dans les formes débutantes que le diagnostic de SLA se discute, mais l’ENMG permet de redresser le diagnostic en montrant la présence de multiples blocs de conduction sur le trajet des nerfs moteurs, en dehors des zones d’étroitesse anatomique. En pratique, une atteinte bulbaire avec dysarthrie, une amyotrophie de la langue, des troubles cognitifs de type frontal, des troubles de déglutition, un syndrome pyramidal associé, des fasciculations très diffuses et une amyotrophie évoluant rapidement et de façon asymétrique sont autant d’éléments évocateurs de SLA.
Autres diagnostics différentiels à évoquer
Dans certaines atteintes sensitives symétriques, les signes objectifs peuvent manquer ou être très pauvres. Devant l’absence d’aréflexie, même si on ne constate pas de syndrome pyramidal, on évoque de principe une pathologie médullaire (compressive, inflammatoire). La recherche de symptômes sphinctériens, d’un signe de Lhermitte, d’un niveau sensitif prend alors toute sa valeur.
POINTS FORTS À RETENIR
Devant une neuropathie chronique avec atteinte des petites fibres associée à des troubles végétatifs, deux causes principales sont à évoquer : le diabète et l’amylose.
L’éthylisme chronique et le diabète sont les deux principales causes de neuropathie périphérique dans les pays industrialisés.
Environ 10 à 20 % de neuropathies sont de cause indéterminée (presque toujours des neuropathies axonales chroniques).
On évoque particulièrement une neuropathie héréditaire devant une histoire familiale, des pieds creux et l’absence de troubles sensitifs subjectifs. Une discordance entre des anomalies électrophysiologiques très marquées et des doléances minimes est également considérée comme très évocatrice.
La biopsie nerveuse est indiquée en particulier devant : – une mononeuropathie multiple, surtout avec des douleurs, une évolution rapide et un syndrome inflammatoire ; – une neuropathie axonale chronique d’évolution péjorative, après un bilan étiologique poussé.
L’électroneuromyogramme est un prolongement direct de l’examen clinique. Il a pour but de confirmer la neuropathie et d’apporter des renseignements sur sa topographie et sur le type d’atteinte (axonale ou démyélinisante). Il est indispensable en cas de neuropathie de cause indéterminée.
Message de l'auteur
Dans un dossier concernant une neuropathie périphérique, l’étudiant doit savoir décrire la démarche diagnostique, connaître les grandes entités nosologiques et savoir ce qu’on peut attendre de l’examen électroneuromyographique. Il s’agit également de savoir orienter le diagnostic étiologique en proposant les explorations appropriées à chaque situation clinique. De nombreuses pathologies sont donc concernées. Bien sûr, ces objectifs ne peuvent être atteints qu’après un interrogatoire et un examen clinique systématiques conduisant à une demande hiérarchisée d’examens complémentaires. Au cours du dossier, le patient pourrait avoir une aggravation de sa constipation ou la présence d’un signe d’alarme. Il faudrait alors argumenter la réalisation d’une coloscopie totale pour éliminer une étiologie cancéreuse. Il faut parfaitement connaître les signes d’alarme à rechercher à l’interrogatoire et à l’examen clinique. Le dossier peut alors rebondir sur l’annonce d’un diagnostic grave et la prise en charge étiologique de cette constipation organique.
Un autre dossier qui semblerait intéressant pourrait être la prise en charge d’une pathologie douloureuse (douleur rhumatologique par exemple), avec la prescription d’opioïdes qui peut engendrer une constipation. Cette pathologie étant un vrai problème de santé publique, elle est d’actualité et peut concerner tous les types de dossiers transversaux nécessitant des antalgiques au long cours.
2. Bouche P, Léger JM, Vallat JM. Neuropathies périphériques : polyneuropathies et mononeuropathies multiples. Volume 1 et 2. Paris: Doin, 2003.

 Encadrés
Encadrés