Uvéites. Des progrès thérapeutiques significatifs sont apparus avec les possibilités d’administration locale des médicaments et les applications aux uvéites des traitements par anti-TNF.
Sous le terme d’uvéites sont regroupées diverses formes d’inflammation intraoculaire, dont la prévalence est d’environ 1 cas pour 1 000 habitants et qui sont responsables d’à peu près 10 % des cécités légales. Les manifestations des uvéites sont particulièrement hétérogènes, isolées ou s’inscrivant dans le cadre de maladies générales. L’inflammation peut être aiguë ou chronique, uni- ou bilatérale, parfois d’origine infectieuse.
Uvéites antérieures aiguës de l’adulte
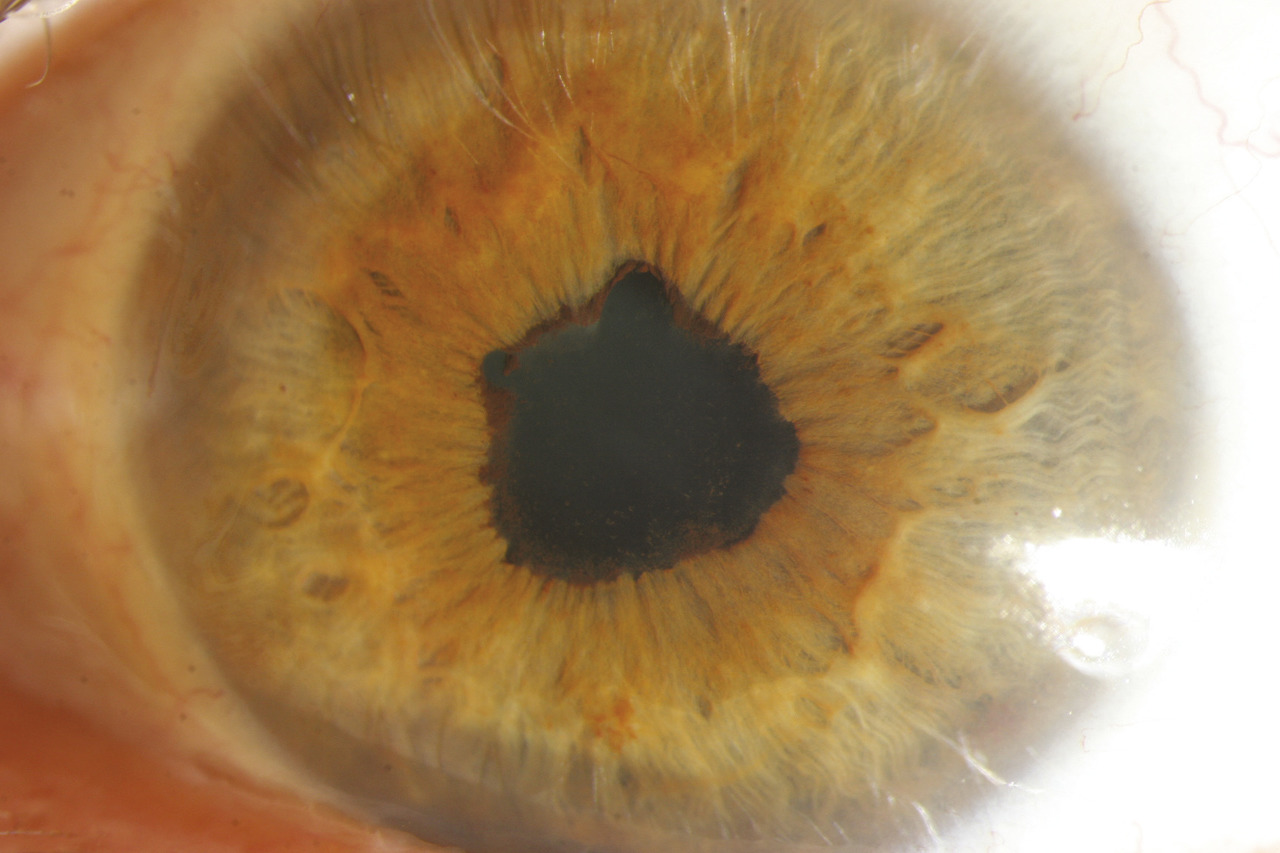
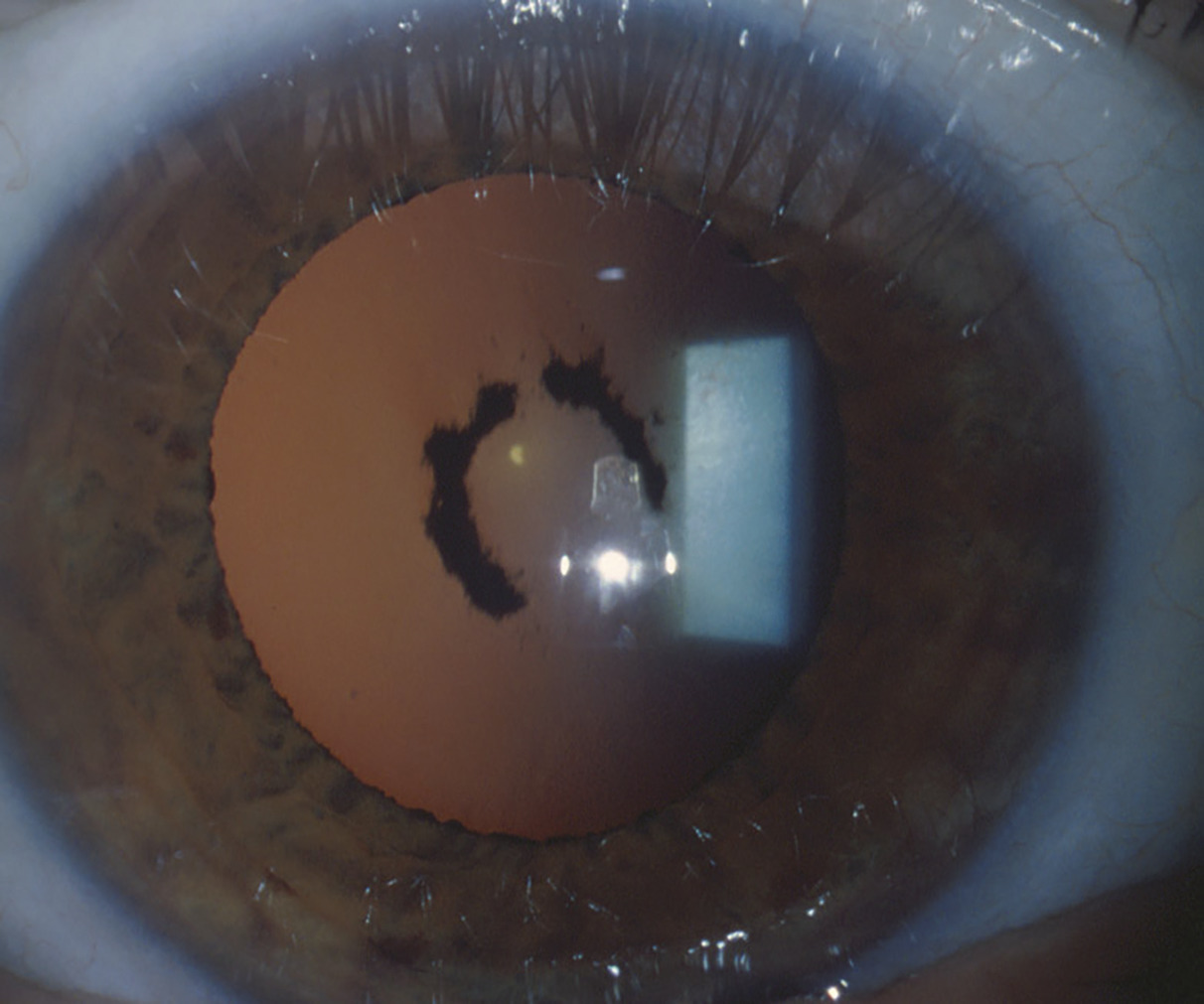
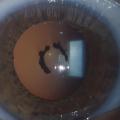
Les uvéites antérieures sont celles dont le traitement est habituellement le plus simple, car le site primitif de l’inflammation est accessible à un traitement par collyres. La corticothérapie topique est le socle du traitement de ces uvéites. Celle-ci est associée à une dilatation de la pupille par des collyres à l’atropine, ou à ses dérivés d’action plus brève, pour prévenir la formation de synéchies (adhérences d’origine inflammatoire) entre la face postérieure de l’iris et la face antérieure du cristallin (fig. 1). Dans le domaine des uvéites antérieures, les innovations thérapeutiques concernent essentiellement les uvéites associées aux spondylarthrites chez des sujets porteurs de l’allèle HLA-B27.
La première innovation est du domaine de l’éducation thérapeutique. Tout patient ayant une spondylarthrite doit être prévenu que la survenue d’une rougeur ou d’une douleur oculaire peut être le signe d’une poussée d’uvéite et doit justifier une consultation ophtalmologique en urgence. Chez un patient ayant déjà eu une poussée d’uvéite et qui en connaît donc déjà les signes, la remise d’une ordonnance prescrivant une automédication précoce par la dexaméthasone en collyre permet de limiter le degré de l’inflammation et par conséquent ses complications. Cette automédi- cation débutée précocement doit être suivie dans les 24 heures d’une consultation ophtalmologique en urgence, permettant de confirmer le diagnostic et d’adapter le traitement.
La deuxième innovation concerne la prévention. La qualité de vie des patients ayant des poussées répé- tées d’uvéite associées à des spondylarthrites peut être très dégradée. L’impact des uvéites sur la vie professionnelle de patients en pleine activité peut être considérable car ces derniers sont forcés de consulter régulièrement dans des centres d’urgence ophtalmologique. Parfois, un véritable syndrome d’épée de Damoclès s’installe chez eux, avec la crainte à tout moment d’une nouvelle poussée, dont la prise en charge peut être encore plus compliquée lorsque celle-ci survient lors de déplacements professionnels, en vacances ou pendant les week-ends. Pour ces patients ayant des uvéites récidivantes, le bénéfice d’un trai- tement préventif peut être très significatif. Aujourd’hui, plusieurs méta-analyses ont montré que la prescription d’anticorps monoclonaux anti-tumor necrosis growth factor (anti-TNF) permettait de réduire de plus de la moitié la fréquence des poussées et de réduire leur intensité.1 Il est cependant important de souligner que cet objectif thérapeutique n’a jamais été le critère principal d’étude de ces traitements, qui n’ont donc pas d’autorisation de mise sur le marché (AMM) pour l’indication spécifique de la prévention des poussées d’uvéite. La prescription doit donc être fondée sur une indication rhumatologique principale, avec l’objectif secondaire d’une réduction des poussées d’uvéite. Cet objectif secondaire est généralement pris en compte chez les patients ayant au minimum deux poussées d’uvéite par an, dont au moins une a été particulièrement difficile à juguler
La première innovation est du domaine de l’éducation thérapeutique. Tout patient ayant une spondylarthrite doit être prévenu que la survenue d’une rougeur ou d’une douleur oculaire peut être le signe d’une poussée d’uvéite et doit justifier une consultation ophtalmologique en urgence. Chez un patient ayant déjà eu une poussée d’uvéite et qui en connaît donc déjà les signes, la remise d’une ordonnance prescrivant une automédication précoce par la dexaméthasone en collyre permet de limiter le degré de l’inflammation et par conséquent ses complications. Cette automédi- cation débutée précocement doit être suivie dans les 24 heures d’une consultation ophtalmologique en urgence, permettant de confirmer le diagnostic et d’adapter le traitement.
La deuxième innovation concerne la prévention. La qualité de vie des patients ayant des poussées répé- tées d’uvéite associées à des spondylarthrites peut être très dégradée. L’impact des uvéites sur la vie professionnelle de patients en pleine activité peut être considérable car ces derniers sont forcés de consulter régulièrement dans des centres d’urgence ophtalmologique. Parfois, un véritable syndrome d’épée de Damoclès s’installe chez eux, avec la crainte à tout moment d’une nouvelle poussée, dont la prise en charge peut être encore plus compliquée lorsque celle-ci survient lors de déplacements professionnels, en vacances ou pendant les week-ends. Pour ces patients ayant des uvéites récidivantes, le bénéfice d’un trai- tement préventif peut être très significatif. Aujourd’hui, plusieurs méta-analyses ont montré que la prescription d’anticorps monoclonaux anti-tumor necrosis growth factor (anti-TNF) permettait de réduire de plus de la moitié la fréquence des poussées et de réduire leur intensité.1 Il est cependant important de souligner que cet objectif thérapeutique n’a jamais été le critère principal d’étude de ces traitements, qui n’ont donc pas d’autorisation de mise sur le marché (AMM) pour l’indication spécifique de la prévention des poussées d’uvéite. La prescription doit donc être fondée sur une indication rhumatologique principale, avec l’objectif secondaire d’une réduction des poussées d’uvéite. Cet objectif secondaire est généralement pris en compte chez les patients ayant au minimum deux poussées d’uvéite par an, dont au moins une a été particulièrement difficile à juguler
Uvéites associées aux arthrites idiopathiques juvéniles
Les uvéites constituent une complication redoutée des arthrites idiopathiques juvéniles. Chez les enfants atteints, des consultations ophtalmologiques systématiques régulières sont indispensables pour détecter une inflammation intraoculaire et pour instaurer à temps un traitement lorsque cela est nécessaire. Les uvéites compliquant les arthrites idiopathiques juvéniles sont antérieures et habituellement chroniques. Une des caractéristiques de ces uvéites de l’enfant est leur taux élevé de complications induites par l’inflammation chronique et/ou par le traitement des corticoïdes en collyre : cataracte, glaucome et kératopathie en bandelette. En outre, l’œil atteint ou celui le plus atteint en cas de manifestations bilatérales est à haut risque de développer une amblyopie. Dans ce contexte, une étude récente a montré de manière nette le bénéfice de l’adalimumab, ajouté au méthotrexate, pour le traitement des uvéites associées aux arthrites idiopathiques juvéniles.2
Uvéites non infectieuses non antérieures
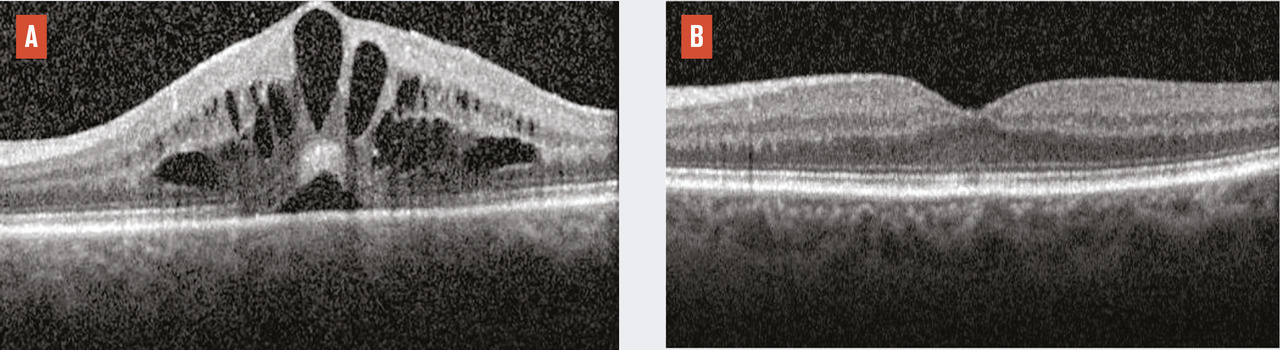
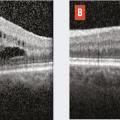
Plus rares que les uvéites antérieures, les non infectious non anterior uveitis (NINAU) sont aussi celles qui engagent le plus fréquemment le pronostic visuel. En effet, le site primitif de l’inflammation est intermédiaire (vitré) ou postérieur (rétine, choroïde), donc directement susceptible d’atteinte maculaire. Or l’œdème maculaire est la première cause de baisse d’acuité visuelle irréversible au cours des uvéites (fig. 2). Le traitement des uvéites non infectieuses non antérieures est plus délicat que celui des uvéites antérieures, car les collyres n’ont pas d’effet sur les manifestations inflammatoires du segment postérieur de l’œil. Seuls les traitements par voie générale ou les traitements locaux par injection permettant une diffusion au vitré, à la rétine ou à la choroïde sont donc susceptibles d’être efficaces.
Corticothérapie par injection intravitréenne ou sous-ténonienne
La voie d’injection intravitréenne de médicaments a été pour la première fois utilisée de manière généralisée pour le traitement des rétinites à cytomégalovirus, lorsque les thérapeutiques antirétrovirales n’étaient pas encore disponibles pour les patients atteints de sida. Cette voie d’injection s’est ensuite développée pour l’injection d’anti- vascular endothelial growth factor pour le traitement des formes néovascularisées de dégénérescence maculaire liée à l’âge. La thérapeutique des uvéites s’est également enrichie de ce mode d’administration avec la possibilité d’injecter une forme à libération prolongée de dexaméthasone. Ozurdex est un implant à biodégra- dation spontanée, destiné à une administration par injection intravitréenne et contenant 700 µg de dexaméthasone (fig. 3).3 Le béné- fice de l’injection d’Ozurdex sur l’inflammation du segment postérieur, en particulier sur l’œdème maculaire, peut être attendu pour une durée d’environ 3 mois et parfois plus. Les principales compli- cations de l’injection sont une hypertonie oculaire cortico-induite et l’apparition secondaire d’opacités cristalliniennes. D’autres produits injectables par voie intra- vitréenne, dont le tacrolimus, sont en cours d’évaluation pour le traitement des uvéites non infectieuses non antérieures.
La voie d’administration sous-ténonienne* peut être également utilisée pour l’injection de corticoïdes à effet prolongé (triamcinolone). Ces injections sous-ténoniennes de triamcinolone sont fréquemment utilisées dans des indications similaires à celles d’Ozurdex, mais en dehors d’une AMM dans cette indication.
La voie d’administration sous-ténonienne* peut être également utilisée pour l’injection de corticoïdes à effet prolongé (triamcinolone). Ces injections sous-ténoniennes de triamcinolone sont fréquemment utilisées dans des indications similaires à celles d’Ozurdex, mais en dehors d’une AMM dans cette indication.
Anticorps monoclonaux anti-TNF
L’hétérogénéité des uvéites postérieures et leur rareté limitent la quantité de données fondées sur des preuves pour guider leur traitement. Lorsque les uvéites sont associées à des manifestations systémiques, celles-ci dictent parfois les indications thérapeutiques. Cependant, dans de nombreux cas, y compris au cours des sarcoïdoses ou des maladies de Behçet, l’uvéite constitue l’élément déterminant des indications thérapeutiques. Dans le contexte d’inflammation intrao- culaire chronique, l’épargne corti- sonée est un objectif essentiel pour limiter les effets indésirables au long cours d’une corticothérapie par voie générale. Jusqu’à récemment, cette épargne cortisonée ne pouvait reposer que sur des immunosuppresseurs « conventionnels » : azathioprine, méthotrexate, mycophénolate ou autres. Leur utilisation pour le traitement au long cours des uvéites non infectieuses non antérieures était empirique, sans AMM reconnue pour cette indication.
Après de nombreuses études non randomisées suggérant l’effet favorable des anticorps monoclonaux anti-TNF pour le traitement des uvéites non infectieuses non antérieures, les études VISUAL ont apporté la preuve de l’efficacité de l’adalimumab dans cette indication. L’étude VISUAL I a montré le bénéfice d’un traitement par adalimumab pour obtenir une quiescence intraoculaire dans le contexte d’une uvéite active.4 L’étude VISUAL II a montré le bénéfice d’un traitement par adalimumab pour la prévention des rechutes chez des patients ayant des antécédents d’uvéites.5 Il reste aujourd’hui à définir des algorithmes décisionnels précis guidant les indications thérapeutiques au cours des uvéites non infectieuses non antérieures. Pour chaque entité, décider du moment optimal de l’introduction d’une biothérapie, ni trop tôt, de manière inutile, ni trop tard, lorsque des dégâts structuraux irréversibles ont limité la vision, constitue un des objectifs thérapeutiques à définir.
Après de nombreuses études non randomisées suggérant l’effet favorable des anticorps monoclonaux anti-TNF pour le traitement des uvéites non infectieuses non antérieures, les études VISUAL ont apporté la preuve de l’efficacité de l’adalimumab dans cette indication. L’étude VISUAL I a montré le bénéfice d’un traitement par adalimumab pour obtenir une quiescence intraoculaire dans le contexte d’une uvéite active.4 L’étude VISUAL II a montré le bénéfice d’un traitement par adalimumab pour la prévention des rechutes chez des patients ayant des antécédents d’uvéites.5 Il reste aujourd’hui à définir des algorithmes décisionnels précis guidant les indications thérapeutiques au cours des uvéites non infectieuses non antérieures. Pour chaque entité, décider du moment optimal de l’introduction d’une biothérapie, ni trop tôt, de manière inutile, ni trop tard, lorsque des dégâts structuraux irréversibles ont limité la vision, constitue un des objectifs thérapeutiques à définir.
QUELLE DURÉE DE TRAITEMENT ?
Après de nombreuses années d’empirisme thérapeutique, des données fondées sur les preuves sont aujour- d’hui disponibles pour guider le traitement des uvéites. Ces traitements peuvent être locaux ou par voie générale, ou combiner ces modes d’administration.6 Cependant, des questions restent en suspens, en particulier concernant la durée des traitements : lorsqu’une uvéite est en rémission sous traitement, quand celui-ci peut-il être interrompu ? Des études randomisées supplémentaires sont nécessaires pour répondre à ces interrogations. Cependant, après des années de retard par rapport à d’autres disciplines, le domaine des uvéites est en train de moderniser ses approches thérapeutiques.
Références
1. Rudwaleit M, Rødevand E, Holck P, Vanhoof J, Kron M, Kary S, Kupper H. Adalimumab effectively reduces the rate of anterior uveitis flares in patients with active ankylosing spondylitis: results of a prospective open-label study. Ann Rheum Dis 2009;68:696-701.
2. Ramanan AV, Dick AD, Beresford MW. Adalimumab for uveitis in juvenile idiopathic arthritis. N Engl J Med 2017;377:789-90.
3. Lowder C, Belfort R Jr, Lightman S, et al.; Ozurdex HURON study group. Dexamethasone intravitreal implant for noninfectious intermediate or posterior uveitis. Arch Ophthalmol 2011;129:545-53.
4. Jaffe GJ, Dick AD, Brézin AP, et al. Adalimumab in patients with active noninfectious uveitis. N Engl J Med 2016;375:932-43.
5. Nguyen QD, Merrill PT, Jaffe GJ, et al. Adalimumab for prevention of uveitic flare in patients with inactive non-infectious uveitis controlled by corticosteroids (VISUAL II): a multicentre, double-masked, randomised, placebo-controlled phase 3 trial. Lancet 2016;388:1183-92.
6. Dick AD, Rosenbaum JT, Al-Dhibi HA, et al.; Fundamentals of Care for Uveitis International consensus group. Guidance on noncorticosteroid systemic immunomodulatory therapy in noninfectious uveitis: fundamentals of care for uveitis (FOCUS) initiative. Ophthalmology 2018 Jan 6. [Epub ahead of print].
2. Ramanan AV, Dick AD, Beresford MW. Adalimumab for uveitis in juvenile idiopathic arthritis. N Engl J Med 2017;377:789-90.
3. Lowder C, Belfort R Jr, Lightman S, et al.; Ozurdex HURON study group. Dexamethasone intravitreal implant for noninfectious intermediate or posterior uveitis. Arch Ophthalmol 2011;129:545-53.
4. Jaffe GJ, Dick AD, Brézin AP, et al. Adalimumab in patients with active noninfectious uveitis. N Engl J Med 2016;375:932-43.
5. Nguyen QD, Merrill PT, Jaffe GJ, et al. Adalimumab for prevention of uveitic flare in patients with inactive non-infectious uveitis controlled by corticosteroids (VISUAL II): a multicentre, double-masked, randomised, placebo-controlled phase 3 trial. Lancet 2016;388:1183-92.
6. Dick AD, Rosenbaum JT, Al-Dhibi HA, et al.; Fundamentals of Care for Uveitis International consensus group. Guidance on noncorticosteroid systemic immunomodulatory therapy in noninfectious uveitis: fundamentals of care for uveitis (FOCUS) initiative. Ophthalmology 2018 Jan 6. [Epub ahead of print].