Diagnostiquer une intoxication par les psychotropes, les antalgiques opioïdes, le paracétamol, les médicaments cardiotropes, le monoxyde de carbone, l’alcool.
Diagnostiquer une intoxication aiguë par le cannabis, la cocaïne, les amphétamines, les nouvelles drogues de synthèse.
Connaître l’épidémiologie des intoxications chez l’enfant.
Identifier les situations d’urgence et planifier leur prise en charge préhospitalière et hospitalière.
Intoxication par le paracétamol
Le paracétamol (acétaminophène) fait partie des médicaments les plus prescrits ou pris en automédication, pour soulager des douleurs ou à visée antipyrétique. En décembre 2019, l’Agence nationale de sécurité du médicament et des produits de santé (ANSM) a rappelé les règles de bon usage des « médicaments contenant du paracétamol ». Même si ces médicaments restent accessibles sans ordonnance, ils devront être placés derrière le comptoir du pharmacien et ne plus être disponibles en vente libre, c’est-à-dire en rayon.
Règles d’utilisation (prévention des intoxications)
Les principales règles d’utilisation qui ont été rappelées sont les suivantes :
- prendre la dose la plus faible, le moins longtemps possible ;
- respecter la dose maximale par prise, la dose maximale quotidienne, l’intervalle minimal entre les prises et la durée maximale de traitement recommandée (3 jours en cas de fièvre, 5 jours en cas de douleur, en l’absence d’ordonnance) ;
- vérifier l’absence de paracétamol dans les autres médicaments (utilisés pour douleurs, fièvre, allergies, symptômes du rhume ou état grippal) ;
- alerter les populations particulières (poids inférieur à 50 kg, insuffisance hépatique légère à modérée, insuffisance rénale sévère, alcoolisme chronique…).
Apprécier les circonstances qui modifient la pharmacocinétique du paracétamol
Plusieurs circonstances peuvent modifier la pharmacocinétique du paracétamol et l’interprétation du seuil toxique de paracétamolémie, comme le trouble d’usage de l’alcool, la malnutrition, les prises répétées de paracétamol, des traitements inducteurs enzymatiques et des ralentisseurs de la vidange gastrique ou des formes à libération prolongée.
Évolution de l’intoxication
L’intoxication par le paracétamol est asymptomatique au début et peut passer inaperçue. La dose toxique est supérieure à 125 mg/kg chez l’adulte (soit 5 à 15 g pour un adulte en une prise unique). Cependant, quand les signes cliniques sont visibles, il est le plus souvent trop tard pour que le traitement de l’intoxication soit efficace. Les symptômes tardifs associent des troubles digestifs peu spécifiques à des troubles neurologiques de type asthénie, somnolence, sensation de faiblesse qui, malheureusement, annoncent l’encéphalopathie hépatique.
Le foie est l’organe cible de ces intoxications. Le paracétamol provoque une cytolyse hépatique vers le troisième et le quatrième jour qui suivent le surdosage. Sur le plan physiopathologique, il est transformé en métabolites réactifs qui s’accumulent. Le principal métabolite toxique, le N-acétyl-p-benzoquinone imine (NAPQI), est rapidement conjugué au glutathion, puis excrété. Lors d’une intoxication massive, le stock de glutathion est rapidement déplété. Lorsque son taux est inférieur à 30 % de son niveau basal, le NAPQI, hautement réactif, se fixe au niveau des protéines de surface hépatocytaires et mitochondriales, induisant un stress oxydatif et une altération de l’homéostasie calcique intracellulaire, responsable d’une nécrose centrolobulaire. La nécrose hépatique prédomine donc en zone centrolobulaire. Une nécrose tubulaire aiguë est également possible.
Dans les formes les plus sévères, le tableau d’hépatite fulminante se développe en trois à six jours, associant ictère, troubles de l’hémostase, coagulation intravasculaire disséminée (CIVD), hypoglycémie, insuffisance rénale, encéphalopathie et hypertension intracrânienne. À ce stade, la mortalité atteint 50 %.
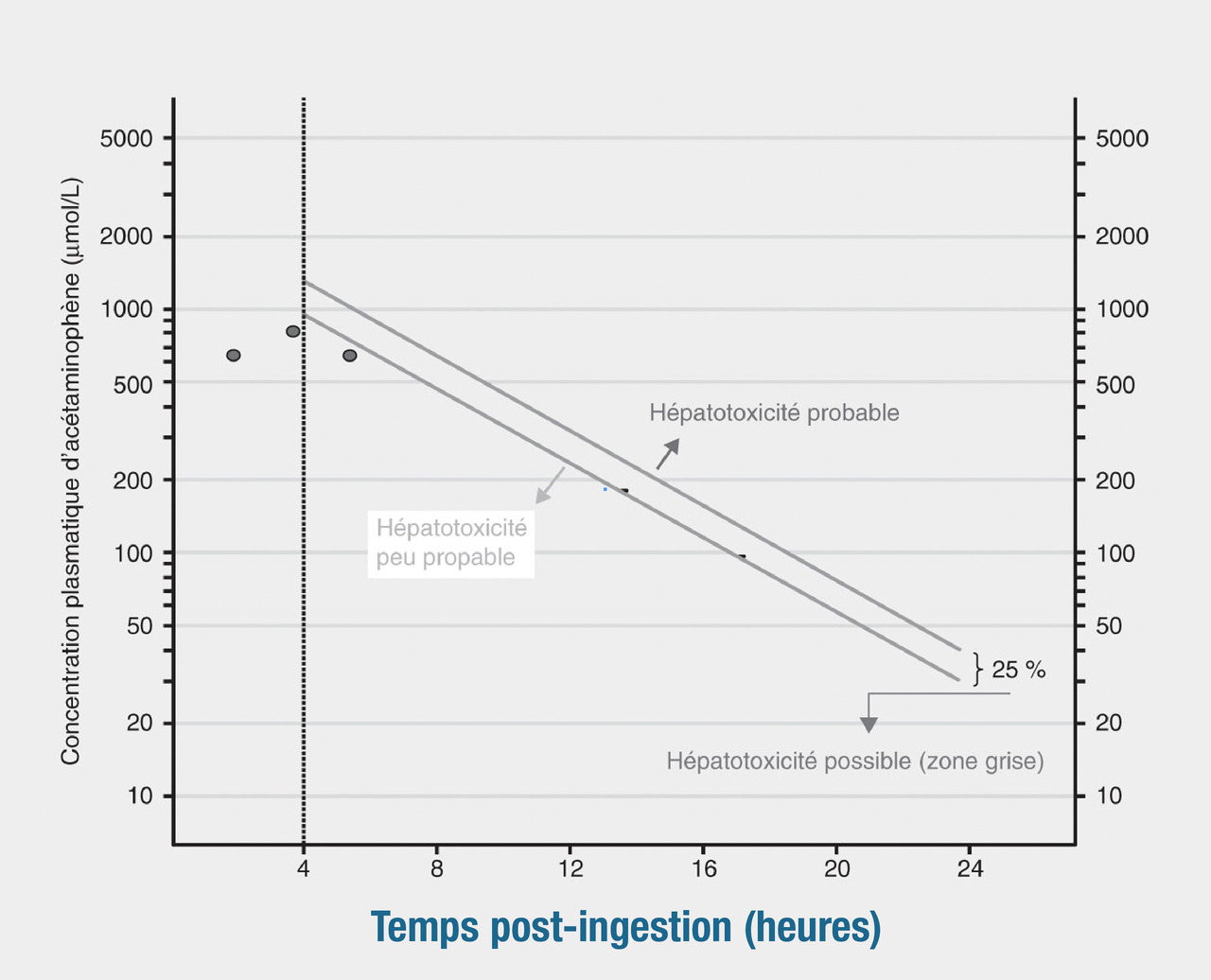
Le diagnostic repose sur le dosage de la paracétamolémie, mesurée 4 à 16 heures après l’exposition. Cette fourchette indique le traitement par la N-acétylcystéine mais est aussi un bon marqueur de la gravité du tableau clinique. Le nomogramme de Prescott modifié par Rumack et Matthew décrit le risque d’hépatite en fonction de la paracétamolémie et du délai écoulé par rapport à l’ingestion (
La paracétamolémie ne doit pas être dosée avant la quatrième heure qui suit l’intoxication.
Traitement (encadré)
L’antidote de l’intoxication au paracétamol est la N-acétylcystéine (NAC) qui régénère le stock de glutathion intracellulaire, a une action antioxydante et réduit la réaction inflammatoire intrahépatique, améliore la fonction hépatique, stabilise l’hémodynamique et réduit l’œdème cérébral (action non spécifique pour une présentation plus tardive). La N-acétylcystéine est d’autant plus efficace qu’elle est administrée dans les 8 à 10 heures après l’ingestion.
Le protocole de référence en France consiste à administrer la N-acétylcystéine à la posologie de 150 mg/kg en 1 heure (dose de charge) puis de 50 mg/kg en 4 heures, enfin de 100 mg/kg sur 16 heures par voie veineuse. C’est le « protocole en 21 heures ».
Les indications de la N-acétylcystéine sont détaillées dans l’
La dose de charge de N-acétylcystéine doit être injectée lentement (en une heure dans le protocole français), pour éviter les réactions anaphylactoïdes. Les symptômes en sont généralement bénins, sous la forme de troubles digestifs (nausées et vomissements), fréquents, d’une urticaire, d’un flush, voire de bronchospasme et de douleur thoracique. Le retentissement tensionnel et l’état de choc sont possibles mais rares. Il est important de noter que le risque de réaction anaphylactoïde est majoré par l’administration rapide de la dose de charge de N-acétylcystéine ou chez les patients dont la paracétamolémie est faible.
L’arrêt du traitement par N-acétylcystéine requiert la validation de tous les critères suivants :
- paracétamolémie indétectable ;
- baisse significative des transaminases ;
- amélioration significative de tous les indices de fonction d’organes (temps de prothrombine et international normalized ratio [INR] mais aussi créatininémie, phosphorémie, pH artériel et lactatémie).
Un risque de tableau sévère dans les intoxications accidentelles
Le paracétamol étant délivré sans ordonnance, le risque de consommation au-delà des doses toxiques pour traiter des douleurs rebelles ne doit pas être sous-estimé. Le risque de développer une insuffisance hépatique est tout aussi important que lors d’une ingestion unique.
Ces observations soulignent l’importance de réaliser un traitement antidotique par la N-acétylcystéine sans attendre le résultat de la paracétamolémie, et sans utiliser le nomogramme, dans les situations où l’ingestion est supérieure à :
- 10 g (ou 200 mg/kg) dans les 24 heures précédentes ;
- 6 g (ou 150 mg/kg) par 24 heures au cours des 48 heures précédentes ;
- 4 g (ou 100 mg/kg) par 24 heures pendant plus de 24 heures en présence de nausées, de vomissements ou de douleurs abdominales.
Intoxication par les opioïdes
Les intoxications par les opioïdes résultent :
- soit des complications d’un trouble de l’usage des opiacés ;
- soit d’un accident thérapeutique ;
- soit d’un surdosage médicamenteux non suicidaire ;
- soit d’un surdosage à but suicidaire.
Ces antalgiques deviennent la classe médicamenteuse la plus impliquée dans les intoxications intentionnelles. L’éducation du patient sur les intoxications devrait intervenir dès la prescription médicamenteuse. En effet, il est observé en France, depuis 2004, une augmentation très importante des prescriptions d’opioïdes forts (+104 %). Le phénomène est marqué pour l’oxycodone, dont les prescriptions représentaient 39 % des prescriptions d’opioïdes forts en 2017 contre 3 % en 2004.
Toxidrome opioïde
Le toxidrome opioïde comporte un tableau clinique assez caractéristique de coma calme. Les symptômes s’installent plus ou moins rapidement en fonction de la nature et de la puissance de l’opioïde absorbé, de la voie de consommation et de la tolérance du patient intoxiqué, surtout s’il est consommateur de substances opioïdes.
Le mécanisme d’action des opioïdes repose sur l’effet agoniste pur sur les récepteurs cérébraux µ, δ, et κ. Il en résulte un effet antalgique, sédatif et euphorisant.
Le tableau clinique complet associe une dépression respiratoire avec une bradypnée, une perte du contrôle volontaire de la respiration, jusqu’à l’apnée, ainsi qu’une bradycardie.
Les principales substances sont l’héroïne, qui est le chef de file, mais aussi tous les médicaments opiacés agonistes des récepteurs µ et les médicaments de substitution aux opiacés, la méthadone et la buprénorphine haut dosage.
Symptômes du toxidrome opioïde (v. item 337, partie 1, tableau 1, Rev Prat 2021;71(8):896)
Le myosis serré (pupilles en « tête d’épingle ») est l’un des symptômes du surdosage en opioïde les plus connus.
La dépression respiratoire est un signe clinique sensible, facilement évaluable par la mesure de la fréquence respiratoire en cycles par minute. Les signes de gravité comprennent une fréquence respiratoire entre 8 et 10 cycles par minute. La cyanose, lorsqu’elle est présente, doit alerter sur la gravité de la situation. Des bruits inspiratoires ou des ronflements sont des signes d’alerte.
La dépression du système nerveux central évolue avec la dose absorbée et la rapidité d’installation des troubles est fonction de la puissance de l’opioïde et de sa voie d’administration. On peut observer d’une simple sédation jusqu’au coma. La mesure du score de Glasgow, même si elle est imparfaite, permet d’avoir une idée de la profondeur de la détresse neurologique.
Le retentissement cardiovasculaire associe une bradycardie sinusale et une hypotension artérielle.
Autres symptômes : des nausées et des vomissements causés par un iléus digestif sont également décrits. De plus, le nombre de symptômes et leur intensité peuvent varier si les opioïdes sont absorbés avec d’autres substances.
Focus sur le tramadol
Le tramadol a vu ses prescriptions flamber depuis le retrait du dextropropoxyphène en Europe, à partir de 2009. Ce médicament est aussi de plus en plus mésusé, du fait de falsifications d’ordonnances ou d’un mésusage de rue par des patients addicts. Le tramadol est un agoniste faible des récepteurs µ mais a aussi des propriétés d’inhibiteur de la recapture de la sérotonine et de la noradrénaline. Dans les intoxications, des convulsions dose-dépendantes sont présentes dans 15 à 20 % des cas ; plus rarement, le tramadol peut être la cause d’un syndrome sérotoninergique.
Intoxication par la buprénorphine
Ces intoxications sont plus souvent accidentelles chez les enfants, puis la proportion d’intoxications volontaires augmente avec l’âge. Les propriétés pharmacologiques de la buprénorphine, agoniste partiel des récepteurs μ des opioïdes et antagoniste des récepteurs κ des opioïdes, expliquent l’inefficacité de la naloxone, d’une part en raison de sa courte demi-vie (de 30 à 80 min) comparée à celle de la buprénorphine (de 2 à 4 h), d’autre part au regard de son métabolite actif, la norbuprénorphine dont le profil pharmacologique est différent de celui de la buprénorphine. La norbuprénorphine est un puissant agoniste des récepteurs μ, δ, et κ, avec une haute affinité.
Le traitement repose sur l’antagonisation par la naloxone
La naloxone reste l’antidote de choix dans cette indication. Son pic d’action est compris entre 30 secondes et 6 minutes, selon la voie d’administration. La naloxone administrée par voie intraveineuse agit en 1 à 2 minutes, par voie intramusculaire en 6 minutes, par voie sous-cutanée en 5 minutes et par voie intranasale en 4 minutes.
La naloxone intraveineuse reste la voie d’administration de choix pour la titration de l’antidote. Des doses initiales de 0,04 mg toutes les 2 minutes doivent être administrées, jusqu’à l’obtention d’une fréquence respiratoire de 12 à 15 cycles par minute. Après le bolus, une perfusion de naloxone à la seringue électrique est souvent indiquée pour éviter le rebond de toxicité de l’opioïde, dont la durée d’action est généralement plus longue que celle de la naloxone injectée en bolus intraveineux.
D’autres formes de naloxone ont été commercialisées et sont délivrées aux patients souffrant d’un trouble de l’usage des opioïdes afin que, de façon autonome, ils puissent antagoniser une surdose dans le cadre de la réduction des risques et des dommages.
La naloxone intranasale : avec cette formulation, le délai d’antagonisation des symptômes de l’intoxication est plus long qu’avec la voie intraveineuse. Le pic plasmatique est atteint en 20 à 30 minutes, ce qui est très proche de celui de la voie intramusculaire. Le témoin de l’overdose administre le contenu d’un pulvérisateur dans chaque narine, soit 1,8 mg. Cette pulvérisation peut être renouvelée en attendant les secours.
La naloxone par voie intramusculaire est habituellement utilisée par les équipes de soins, surtout quand l’accès veineux est difficile. En France, une nouvelle présentation de naloxone intramusculaire est proposée sous la forme de seringues préremplies de 5 mL, dosées à 0,4 mg/mL, soit 2 mg au total. Le kit comporte en plus 2 aiguilles permettant de renouveler l’injection.
POINTS FORTS À RETENIR
L’intoxication par le paracétamol est asymptomatique au début et peut passer inaperçue. Quand les signes cliniques sont visibles, il est le plus souvent trop tard pour que le traitement de l’intoxication soit efficace.
L’antidote de l’intoxication au paracétamol est la N-acétylcystéine.
La N-acétylcystéine est d’autant plus efficace qu’elle est administrée dans les 8 à 10 heures après l’ingestion de paracétamol.
Le toxidrome opioïde est un tableau clinique assez caractéristique de coma calme.
L’héroïne, les médicaments opiacés agonistes des récepteurs µ et les médicaments de substitution aux opiacés, la méthadone et la buprénorphine sont les principales substances impliquées dans les intoxications par les opiacés.
La naloxone est l’antidote de choix des intoxications par les opioïdes.
Principales intoxications aiguës
La toxicologie clinique est une spécialité transversale qui, par sa nature, peut être questionnée dans les dossiers de toutes les spécialités et dans tous les items de l’ECN.
Il est possible de rencontrer une question isolée sur un toxique particulier ou d’insérer un toxique dans un tableau clinique d’agitation ou de coma. Il faut penser à cette cause dans ce type de dossier.
La prise en charge de l’intoxication, qualifiée de « systématisée », objet du focus, doit être maîtrisée par l’étudiant. Elle lui permet de n’oublier aucune phase : appel des secours, évaluation initiale, mesures initiales de secours, évaluation des moyens mis en jeu, accueil dans l’établissement de santé, examens complémentaires, administration ou non d’antidotes, mesures spécifiques avant la sortie du patient (avis psychiatrique, évaluation de la situation sociale, mesures de protection infantile…).
Enfin, les nouvelles drogues psychostimulantes et les opiacés font l’objet d’une surveillance récente et actuellement renforcée, en termes de risques de surdosage et de mésusage. Ces molécules, causes d’intoxications qui peuvent engager le pronostic vital, doivent être connues, et des questions de toxicologie peuvent s’insérer dans un dossier plus général de psychiatrie ou d’addictologie.
Indications de la N-acétylcystéine
Ingestion unique d’une surdose de paracétamol avec consultation précoce (dans les 24 heures), quand l’heure d’ingestion est connue et après interprétation de la paracétamolémie sur le nomogramme et si le point se situe en zone de toxicité possible ou probable (au-delà de la ligne qui commence à 150 mg/L à la 4e heure).
Ingestion unique d’une surdose de paracétamol avec consultation tardive (au-delà des 24 heures), heure d’ingestion connue et en présence d’une élévation des transaminases (et ce quelle que soit la paracétamolémie).
Ingestion suspectée d’une surdose de paracétamol sans heure d’ingestion connue quand la paracétamolémie n’est pas nulle.
Hépatite cytolytique avec ou sans insuffisance hépatique aiguë dans un contexte d’exposition possible au paracétamol, même si la paracétamolémie est nulle.
Exposition au paracétamol d’un sujet fortement vulnérable : traiter largement sans prendre en compte les lignes du nomogramme.
Ingestion répétée ou chronique de paracétamol en dose élevée.
Prise en charge des intoxications médicamenteuses et par drogues récréatives 2020. Recommandations formalisées d’experts communes Société de réanimation de langue française-Société française de médecine d’urgence (SRLF-SFMU). Révision du consensus 2005 sur les intoxications aiguës.
Haute Autorité de santé. ECN. Mode d’emploi. https://www.has-sante.fr/jcms/p_3076609/fr/ecn
Intoxications graves par médicaments et substances illicites en réanimation. Conférence d’experts de la Société de réanimation de langue française, 2006.

 Encadrés
Encadrés