Prise en charge immédiate pré-hospitalière et à l’arrivée à l’hôpital. évaluation des complications chez : un brûlé, un polytraumatisé, un traumatisé abdominal, un traumatisé des membres, un traumatisé du rachis, un traumatisé thoracique, un traumatisé oculaire, un patient ayant une plaie des parties molles.
Nous détaillerons les étapes de la prise en charge préhospitalière et hospitalière, puis nous aborderons les spécificités propres à chaque type de traumatisme.
Prise en charge préhospitalière
- l’évaluation de la gravité et le bilan lésionnel ;
- le conditionnement du patient et la mise en œuvre de gestes de « sauvetage » thérapeutique en cas de détresse vitale ;
- la pré-alerte et l’orientation vers une structure adaptée (trauma center) à la gravité et aux lésions présentées par le patient ;
- la maîtrise du timing de prise en charge en visant une prise en charge préhospitalière la plus rapide possible.
Évaluation de la gravité et bilan lésionnel
Détresse neurologique
Un traumatisme crânien grave est défini par un score de Glasgow inférieur ou égal à 8. Dans ce cadre, il est indispensable de rechercher des anomalies pupillaires telles qu’une anisocorie ou une mydriase bilatérale aréactive pouvant évoquer une hypertension intracrânienne (HIC) et un engagement cérébral.Détresse respiratoire
Une atteinte thoracique directe (fracture de côte, épanchement intrapleural) ou indirecte (inhalation) peut induire une hypoxie et/ou une hypercapnie et se traduire par une détresse respiratoire (polypnée, respiration superficielle, balancement thoraco-abdominal) avec diminution de la SpO2.Détresse hémodynamique
Il est important de souligner que, malgré une détresse hémodynamique, la pression artérielle peut être maintenue dans des valeurs normales par activation du système nerveux sympathique responsable d’une tachycardie compensatrice. Par ailleurs, la fréquence cardiaque peut également être augmentée du fait de la douleur ou de l’anxiété induite par le traumatisme. Ainsi pour s’affranchir de ces pièges lors de l’interprétation des paramètres macrocirculatoires, il convient d’utiliser le « shock index » qui correspond au rapport de la pression artérielle systolique (PAS) sur la fréquence cardiaque. Un rapport supérieur à 0,8, autrement dit une tachycardie associée à une PAS « anormalement normale » doit être considéré comme un élément de gravité et faire suspecter un processus hémorragique.La défaillance circulatoire est la plus fréquente. Ses causes sont :
- principalement l’hémorragie ; elle peut être extériorisée au niveau des membres, du massif facial (épistaxis) ou du scalp ; il peut aussi s’agir d’une hémorragie interne localisée dans le thorax, l’abdomen ou l’espace rétropéritonéal et pelvien à la suite notamment d’un fracas du bassin ;
- un pneumothorax compressif ;
- une lésion médullaire ;
- une contusion myocardique ou une tamponnade.
Thérapeutique
Principes de la réanimation hémodynamique
La réanimation d’un arrêt cardiaque post-traumatique doit impérativement comprendre la réalisation précoce d’une exsufflation bilatérale par thoracostomie dans l’hypothèse d’un pneumothorax compressif. À cette exsufflation s’ajoutent le massage cardiaque, la ventilation artificielle, l’utilisation d’adrénaline et le remplissage vasculaire.Les objectifs tensionnels doivent être contrôlés sous peine d’aggraver une hémorragie interne. Il est recommandé de maintenir une PAS entre 80 et 90 mmHg avant le contrôle de l’hémorragie. En cas de traumatisme crânien grave, l’objectif est une PAS > 120 mmHg (pression artérielle moyenne [PAM] comprise entre 80 et 90 mmHg). Dans le contexte de traumatisme crânien, il faut supposer qu’il existe une hypertension intracrânienne ; il devient impératif dès lors de maintenir la pression de perfusion cérébrale en augmentant la PAM. Le maintien de la pression artérielle repose sur l’administration d’un remplissage vasculaire par cristalloïde (sérum salé isotonique, Ringer Lactate). Ce remplissage doit cependant être contrôlé sous peine d’aggraver l’hypothermie ainsi que la coagulopathie par dilution. Les solutés hypotoniques tels que le Ringer Lactate sont contre-indiqués en cas de traumatisme crânien grave. L’administration de noradrénaline, qui est le vasopresseur à utiliser, doit être précoce (dès 1 000 mL de remplissage vasculaire) afin d’atteindre rapidement les objectifs de pression artérielle tout en limitant le remplissage vasculaire. Les abords veineux centraux ne sont pas indiqués en préhospitalier, et la noradrénaline doit être perfusée sur une voie périphérique ou à défaut sur un cathéter intra-osseux.
Contrôle des voies aériennes
L’anesthésie générale, l’intubation orotrachéale et la ventilation mécanique peuvent aggraver une détresse hémodynamique et exposent à un risque d’inhalation du contenu gastrique. Leurs bénéfices à la phase préhospitalière doivent être mis en balance avec leurs risques. Leurs indications sont la détresse respiratoire et l’hypoxémie persistante sous oxygénothérapie, le traumatisme crânien grave, une analgésie incontrôlable. L’abord des voies aériennes peut être compliqué en cas de lésions maxillofaciales, et le recours à un abord trachéal peut être nécessaire.Contrôle de l’hémorragie
Il n’existe pas de moyen de contrôler une hémorragie interne à ce stade de la prise en charge, ce qui justifie le transport rapide vers une structure médicale adaptée. En cas de fracas du bassin, la mise en place d’une ceinture de contention pelvienne permet de limiter le déplacement des structures osseuses du bassin ainsi que le volume de diffusion de l’hématome rétropéritonéal. Elle permet donc de partiellement contrôler l’hémorragie à ce niveau. Sa mise en place est donc systématique devant toute suspicion de traumatisme pelvien grave (douleur pelvienne spontanée, mobilité osseuse anormale) mais également pour tout patient inconscient ou en état de choc. En cas d’hémorragie au niveau d’un membre, si la compression directe s’avère insuffisante, un garrot doit être mis en place rapidement. Les épistaxis doivent être tamponnés, et les plaies du scalp suturées précocement. La coagulopathie chez le polytraumatisé apparaît précocement. Elle est en outre caractérisée par une suractivation inappropriée des mécanismes de dégradation physiologiques du caillot appelée fibrinolyse. L’administration d’acide tranexamique qui est un agent antifibrinolytique doit être systématique.Autres points fondamentaux
Les autres points fondamentaux de la prise en charge préhospitalière sont :- le traitement de la douleur ;
- la prévention de l’hypothermie ;
- l’immobilisation des fractures ;
- en cas de traumatisme crânien grave : le contrôle des facteurs d’agression cérébrale secondaire d’origine systémique (ACSOS) et en cas de signe d’hypertension intracrânienne (HIC) ou d’engagement, l’administration d’une osmothérapie (mannitol ou sérum salé hypertonique) afin de diminuer l’œdème cérébral ;
- la prévention de lésions médullaires secondaires ; en effet, tout polytraumatisé doit être considéré comme un patient vertébrolesé, et l’immobilisation du rachis ainsi que le respect de l’axe tête-cou-tronc lors des mobilisations doivent être systématiques afin de prévenir la survenue de déplacements secondaires.
Prise en charge hospitalière
Principe du « damage control »
Bilan biologique
- les examens prétransfusionnels, à réaliser impérativement avant toute transfusion ;
- un hémogramme et un bilan de coagulation comprenant la mesure du fibrinogène ;
- une gazométrie artérielle, à la recherche d’une acidose et d’une hyperlactatémie marqueurs de gravité et pronostiques majeurs ;
- des dosages enzymatiques tels que CPK, troponine, ASAT-ALAT, lipase ;
- un ionogramme ;
- une évaluation de la sérologie antitétanique ;
- un dosage de la β-hCG chez la femme en âge de procréer.
Bilan radiologique
Ce bilan d’urgence comprend :
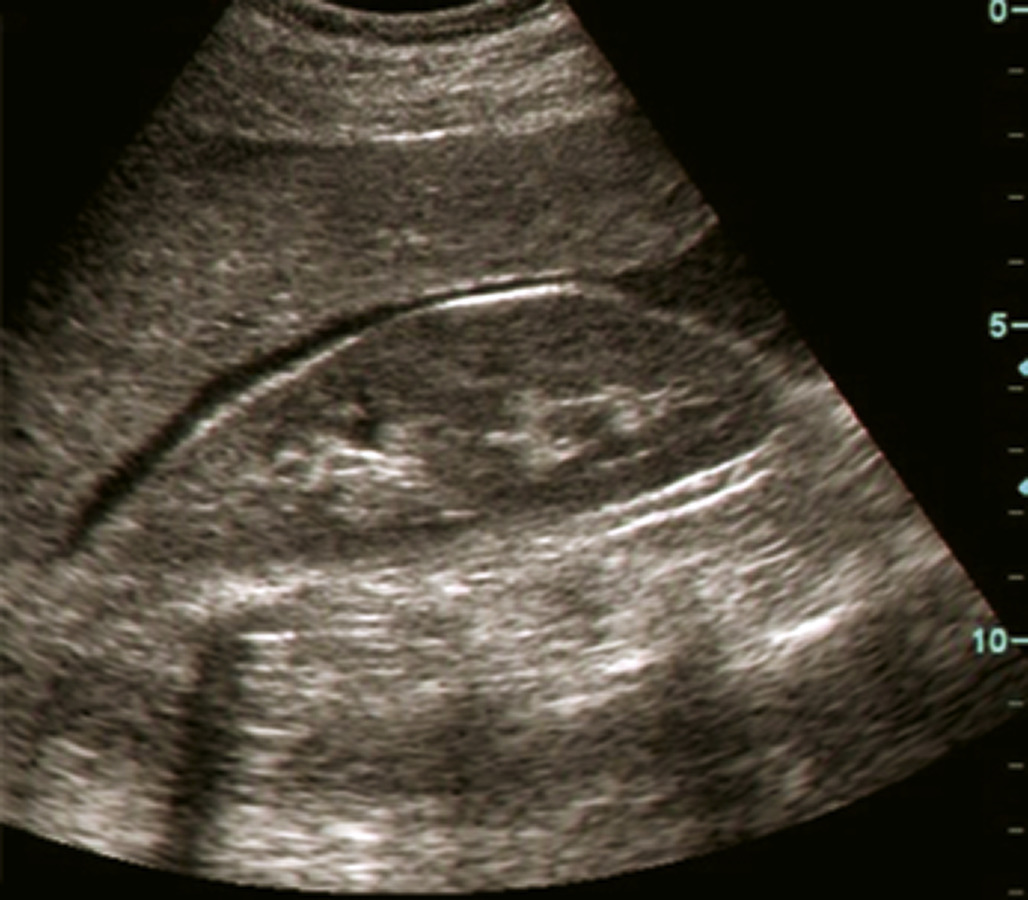
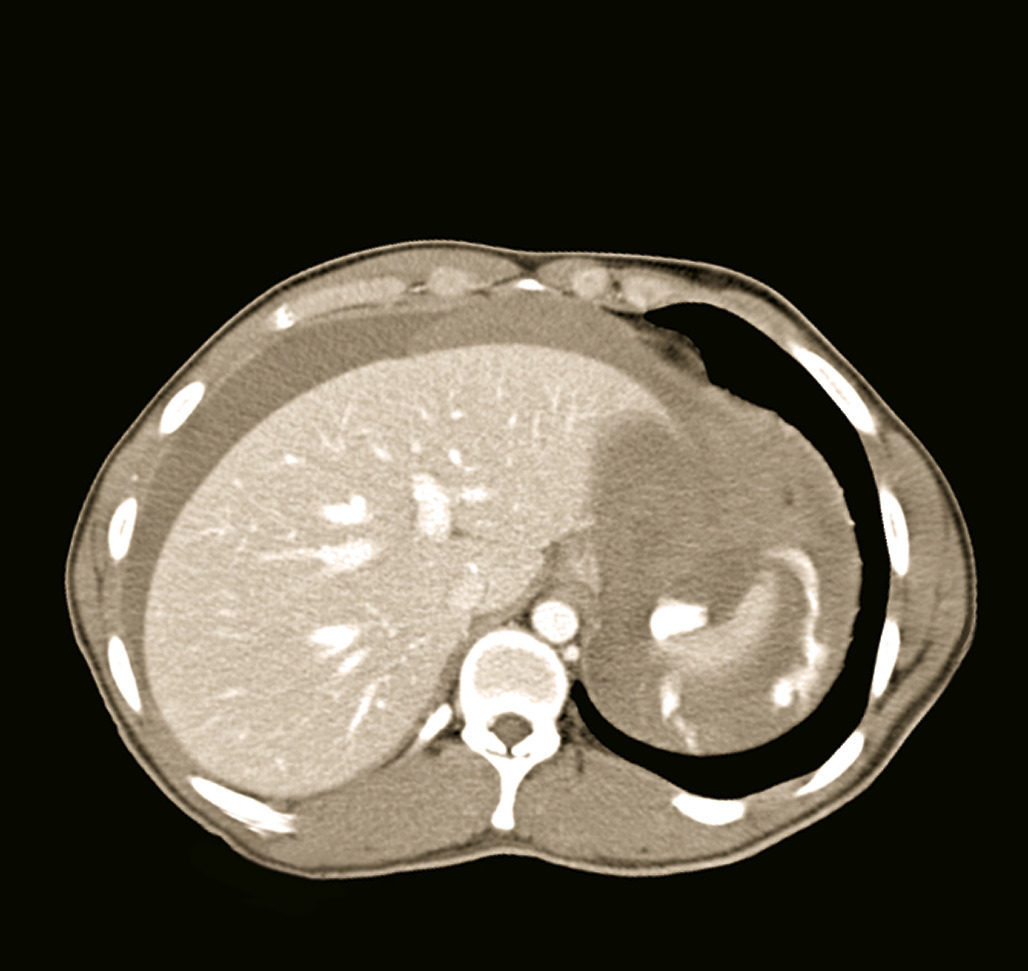
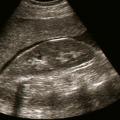
- une FAST échographie, à la recherche d’un épanchement intrapéritonéal ou intrapleural ; il peut alors montrer un hémothorax, un hémopéritoine, un pneumothorax, une tamponnade ou une dysfonction cardiaque ;
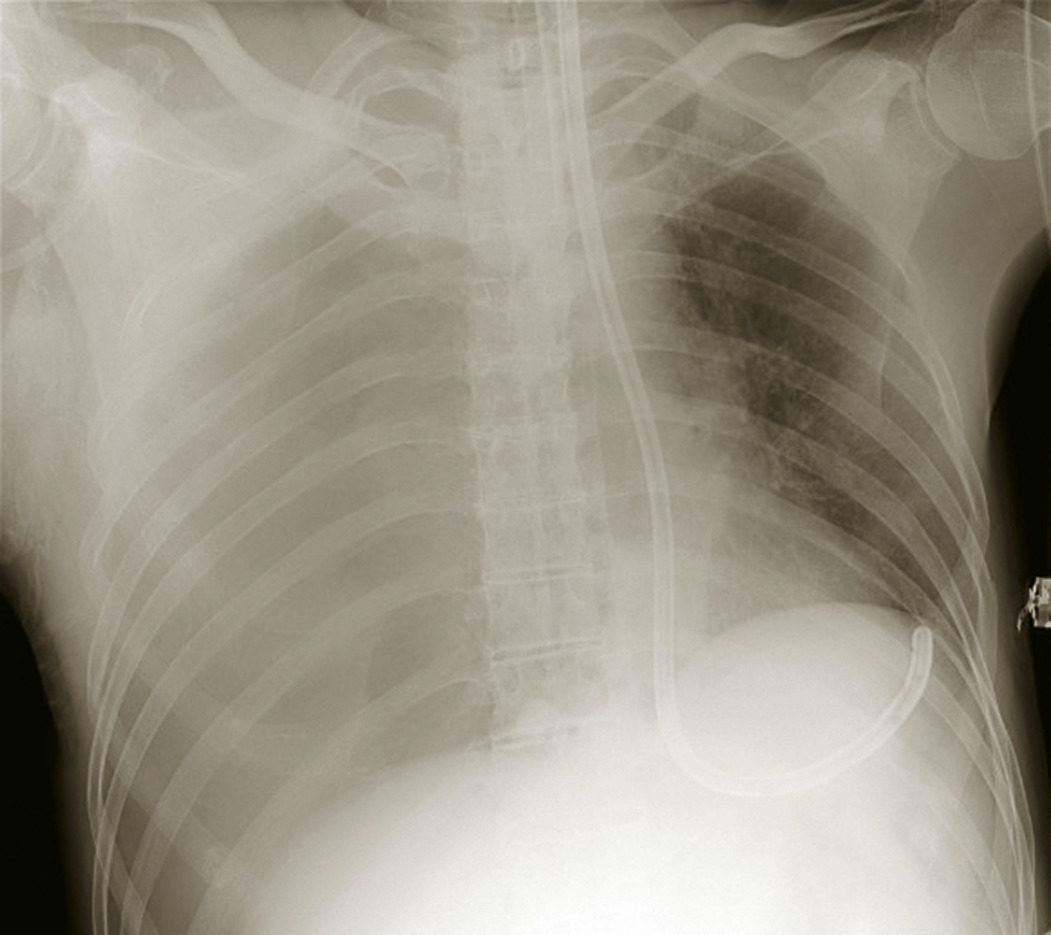
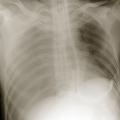
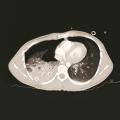
- une radiographie thoracique de face (fig. 2) pour confirmer un pneumothorax compressif ;
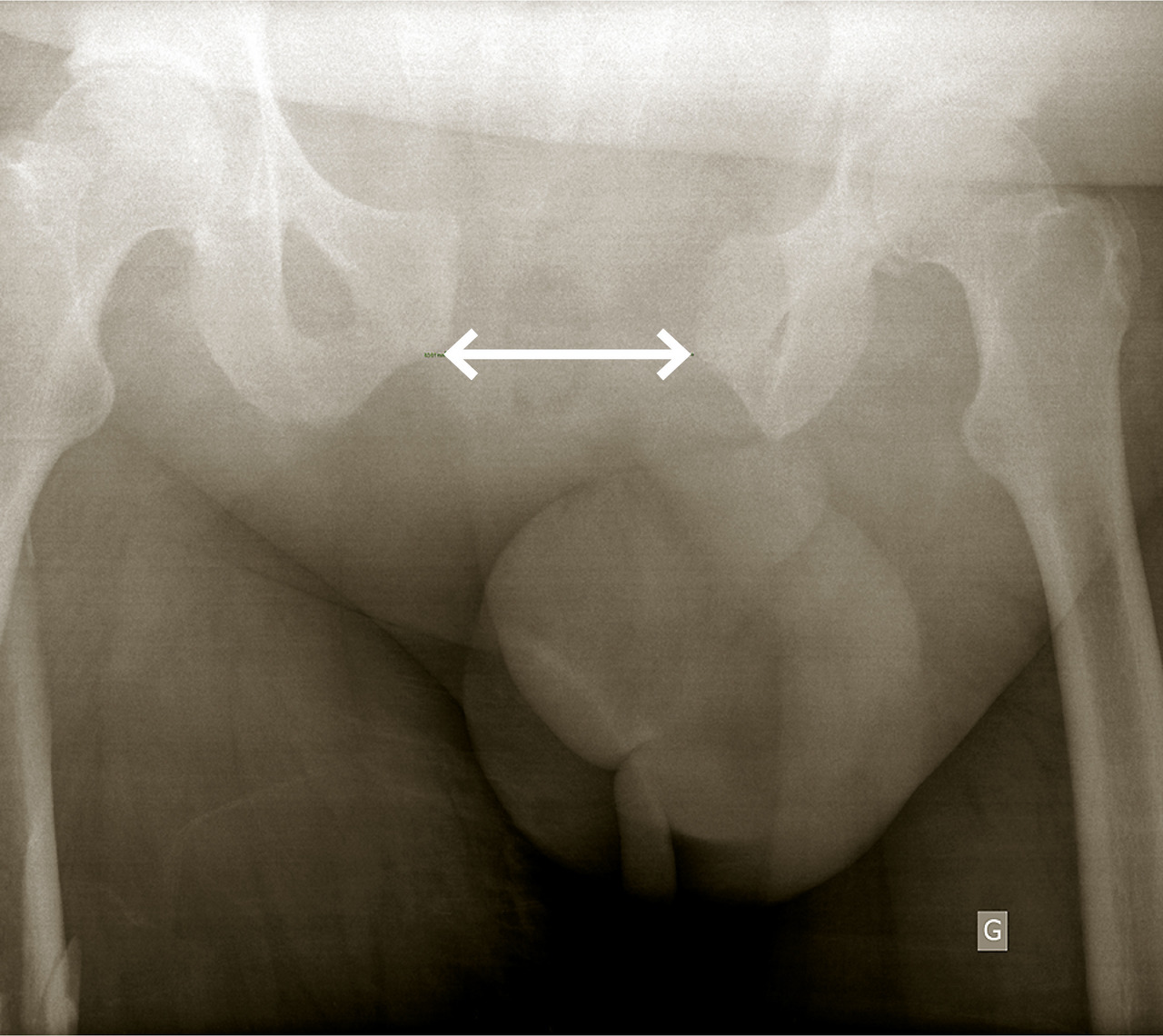
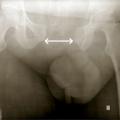
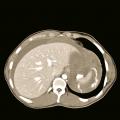
- une radiographie du bassin de face (fig. 3), à la recherche d’un fracas de l’anneau pelvien ; en l’absence d’autre cause évidente de défaillance circulatoire, elle oriente vers une hémorragie pelvienne et rétropéritonéale.
Principes de la réanimation intrahospitalière
Contrôle de l’hémorragie
C'est la priorité. Il peut être réalisé de façon chirurgicale ou par embolisation artérielle en radiologie interventionnelle. Ces deux types de techniques sont complémentaires et peuvent être associées. Pour les patients en état de choc, les protocoles de soins incluent généralement la mise en place d’un abord veineux central fémoral de gros calibre, qui va permettre d’administrer des catécholamines de façon plus sûre et de perfuser rapidement un grand volume de fluide ainsi que la mise en place d’un cathéter artériel fémoral afin de monitorer en continu la pression artérielle et de réaliser des bilans sanguins itératifs.Stratégie transfusionnelle chez le patient en état de choc hémorragique.
Il faut transfuser précocement des concentrés de globules rouges (CGR) pour un objectif d’hémoglobine compris entre 7 et 9 g/dL. Il faut également tenir compte de la cinétique de l’hémorragie. La coagulopathie est fréquente, précoce et grève le pronostic du patient polytraumatisé. Elle justifie un traitement dès les premières minutes de la prise en charge, et ce dernier ne peut donc pas être guidé par les résultats du bilan de coagulation. Il est donc recommandé d’administrer des unités de plasma frais congelé (PFC) en association avec la transfusion de CGR selon un ration PFC/CGR compris entre 1/1 et 1/2. Il faut également maintenir un taux de fibrinogène > 1,5 g/L en administrant précocement des concentrés de fibrinogène. La transfusion de concentrés plaquettaires doit être précoce, avec un objectif de 50 G/L ou 100 G/L (traumatisme crânien grave associé ou à hémorragie active). La correction d’une hypocalcémie, d’une acidose métabolique et la lutte contre l’hypothermie sont des mesures primordiales pour permettre l’hémostase biologique. De l’acide tranexamique doit être injecté dans les 3 premières heures suivant le traumatisme, et il est recommandé d’entretenir cette administration.Spécificités propres à chaque type de traumatisme
Traumatisme thoracique
Fractures costales
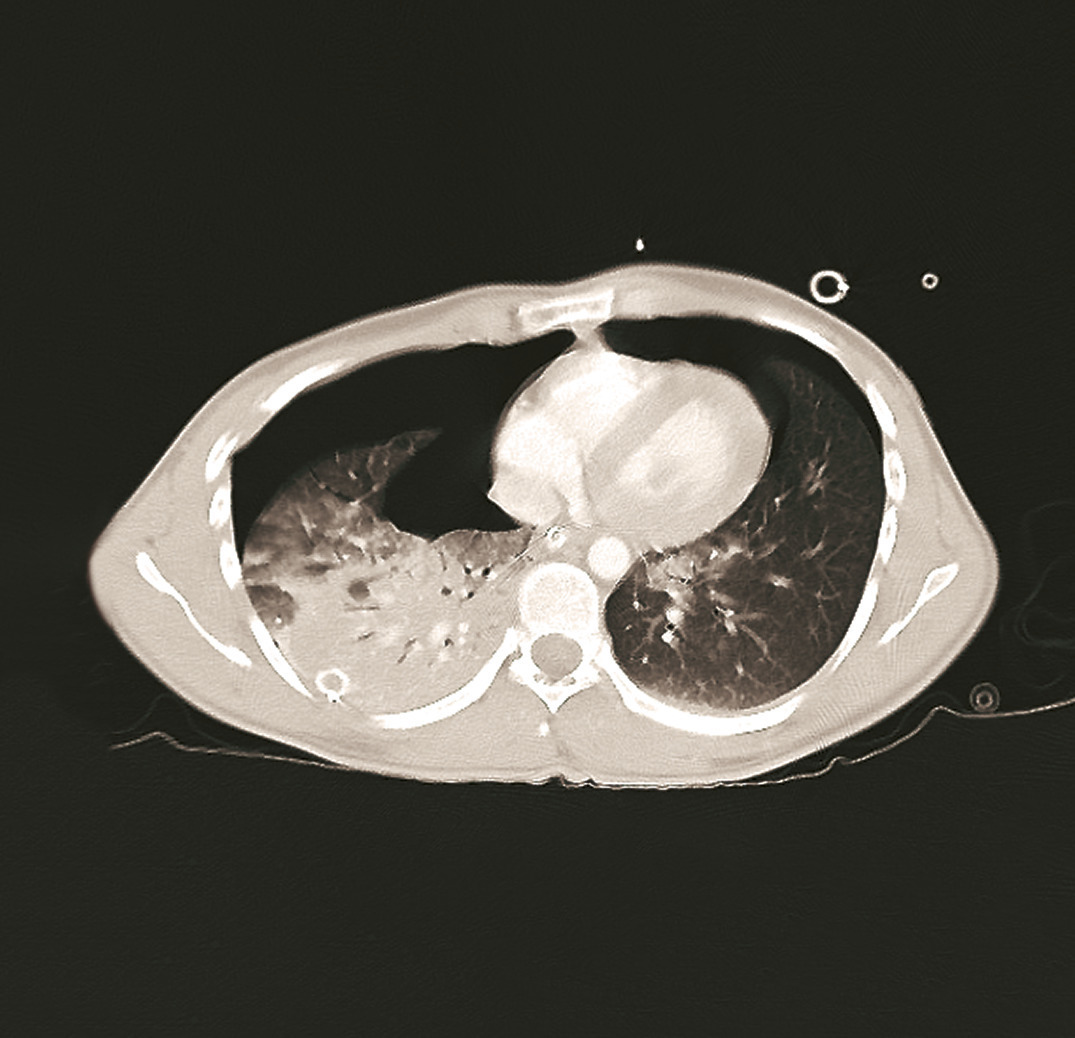
Elles nécessitent une ostéosynthèse chirurgicale en urgence seulement en cas de volet costal mobile associé à une détresse respiratoire, défini par la présence d’au moins 2 fractures par côte sur au moins 3 étages contigus. Le volet costal peut être responsable d’un mouvement inversé (« paradoxal ») de cette portion de la paroi durant le cycle ventilatoire avec réduction paradoxale du volume thoracique à l’inspiration conduisant à un épuisement respiratoire.Pneumothorax (fig. 4)
Il est secondaire à une plaie pariétale, du parenchyme pulmonaire ou de l’arbre trachéobronchique. Il justifie un drainage s’il est complet ou mal toléré. Il peut être compressif si l’air qui entre dans la cavité pleurale y reste trappé, aboutissant à une compression des structures médiastinales et de l’hémithorax controlatéral. Il doit alors être drainé en urgence ou exsufflé par voie médio-claviculaire au 2e espace intercostal ou sur la ligne axillaire antérieure au 4e espace intercostal.Hémothorax
Un hémothorax peut se former aux dépens d’un saignement pariétal, pulmonaire ou médiastinal. Son drainage est obligatoire. L’intérêt est double :- le drain permet de surveiller l’abondance du saignement ; il est recommandé de proposer une hémostase chirurgicale en cas d’hémothorax d’emblée supérieur à 1 500 mL ou une hémorragie d’un débit supérieur à 200 mL/h pendant 3 heures ;
- l’évolution à distance peut se faire vers une surinfection ou la formation d’adhérences pleurales, responsables d’un syndrome restrictif.
Lésions cardiaques
Elles comprennent la contusion myocardique pouvant être responsable d’un trouble du rythme ou d’un choc cardiogénique, la dissection ou rupture coronarienne et les lésions valvulaires. Les atteintes vasculaires sont dominées par la dissection de l’isthme aortique. En dehors de la rupture complète associée à un état de choc, le traitement conservateur consistant à exclure la lésion avec une prothèse posée par voie endovasculaire est recommandé. La complication à craindre dans les suites d’un traumatisme thoracique est la survenue d’une pneumopathie ou d’un syndrome de détresse respiratoire aiguë (SDRA), et ce en dépit d’un tableau clinique initial rassurant. L’inhibition de la toux et de la mécanique ventilatoire par la douleur favorise l’encombrement bronchique, la formation d’atélectasies, puis la surinfection. Ce risque est majoré chez les patients de plus de 65 ans, la présence de comorbidités cardiorespiratoires sous-jacentes (BPCO, tabagisme, insuffisance respiratoire, coronaropathie, insuffisance cardiaque) ou une contusion pulmonaire post-traumatique associée. Sa prévention et son traitement reposent sur une analgésie multimodale suffisante, avec notamment un recours à des techniques locorégionales comme le bloc paravertébral ou la péridurale. Elle doit permettre le drainage bronchique, la kinésithérapie respiratoire intensive et la mobilisation précoce. En cas d’hypoxémie, le recours à la ventilation non invasive est recommandé (VNI).Traumatisme médullaire
La tomodensitométrie permet l’analyse du cadre osseux mais n’explore pas les lésions de l’appareil disco-ligamentaire et des structures nerveuses. Tout patient ayant un déficit neurologique et dont la tomodensitométrie est normale doit bénéficier d’une imagerie par résonance magnétique panrachidienne en urgence afin de rechercher une hernie discale compressive, un hématome péri- ou intradural ou une contusion médullaire.
Une lésion médullaire peut mettre en jeu le pronostic vital immédiat car :
- les atteintes cervicales peuvent compromettre totalement l’autonomie respiratoire du patient par paralysie des nerfs phréniques, en cas de niveau supérieur à C5 ; au-dessous de ce niveau, l’atteinte des muscles respiratoires accessoires (sterno-cléido- mastoïdiens, intercostaux, abdominaux) peut favoriser l’encombrement bronchique et l’hypoventilation alvéolaire, et précipiter une décompensation respiratoire et une pneumopathie ;
- l’atteinte du système nerveux sympathique pour les niveaux supérieurs à T6 est responsable d’une hypotension secondaire à une perte du tonus vasculaire artériel et veineux ; la sévérité de cette dysautonomie dépend de la hauteur du niveau lésionnel ; à l’extrême, elle peut être responsable d’une bradycardie profonde, voire d’un arrêt cardiaque, notamment lors des mobilisations.
À l’instar du traumatisme crânien, la prévention des facteurs d’agression nerveuse d’origine secondaire est primordiale en cas de lésion médullaire. La pression artérielle moyenne doit être maintenue supérieure à 80 mmHg afin de préserver la pression de perfusion médullaire, et ce dès la phase préhospitalière. Le monitorage invasif continu de la pression artérielle et le recours à un traitement vasopresseur en réanimation sont donc nécessaires. Le contrôle de la pO2, de la pCO2, de la natrémie, de l’hyperthermie et de la glycémie est également indispensable. Aucun traitement médulloprotecteur n’a actuellement démontré de bénéfice dans ce contexte, notamment la corticothérapie, pouvant favoriser des complications infectieuses et dont l’usage n’est pas recommandé.
Enfin, la prévention, le diagnostic précoce et le traitement des complications de décubitus, respiratoires et urinaires (lithiases, infections) doivent être mis en œuvre.
Traumatisme abdominal
Traumatisme pelvien
Traumatisme des membres et plaie des parties molles
La fixation définitive et les réparations anatomiques et esthétiques définitives, notamment au moyen de greffes de tissus et de lambeaux de recouvrement, seront réalisées à distance. Une antibioprophylaxie de courte durée et une prévention du tétanos en cas de statut vaccinal incomplet sont la règle.
Prise en charge du patient brûlé
La brûlure est caractérisée par :
- sa profondeur : le 1er degré correspond à un érythème douloureux ; le 2e degré correspond à une atteinte du derme caractérisée par des décollements épidermiques appelés phlyctènes, la brûlure est hyperalgique, humide et inflammatoire ; le 3e degré correspond à une atteinte cutanée sur toute sa profondeur ; la peau est dévascularisée (pas de saignements, pas de décoloration à la vitropression), sèche, cartonnée, insensible et indolore ; les phanères (poils, ongles) n’adhèrent plus ;
- son étendue calculée selon la règle des 9 de Wallace : la paume de la main du patient représente environ 1 % de sa surface corporelle (tableau 2) ;
- sa localisation : une brûlure de la face expose à un risque d’œdème des voies aériennes et à une asphyxie. L’inhalation de fumées d’incendie peut provoquer des lésions pulmonaires pouvant évoluer vers un syndrome de détresse respiratoire aiguë (SDRA) ou provoquer une intoxication par des gaz asphyxiants (monoxyde de carbone et cyanure). Des lésions étendues et circonférentielles provoquent des rétractions et une perte de l’élasticité cutanée pouvant aboutir à un syndrome des loges, un syndrome restrictif thoracique ou un syndrome du compartiment abdominal. Elles imposent des escarrotomies et des aponévrotomies de décharge précoces.
- les lésions de 3e degré ;
- les lésions de 2e degré étendues à plus de 10 % de surface corporelle ;
- l’atteinte d’une zone à risque vitale ou fonctionnelle : les mains, les pieds, la face, le cou si circulaire, le périnée ;
- les lésions circulaires profondes ;
- les brûlures électriques ;
- les brûlures chimiques ;
- les brûlures chez l’enfant et l’adulte de plus de 70 ans.
- le retrait des vêtements sauf en cas d’adhérence aux lésions et la couverture par des pansements des zones brûlées ;
- la gestion de la douleur, ce qui peut justifier une anesthésie générale ;
- le contrôle rapide des voies aériennes en cas de troubles de la conscience ou d’œdème des voies aériennes ;
- un remplissage vasculaire précoce et abondant ;
- la prévention de l’hypothermie ;
- le traitement d’une intoxication aux fumées d’incendie associée (hydroxocobalamine et oxygénothérapie).
Traumatismes oculaires
L’interrogatoire s’attache à définir l’heure et le mécanisme du traumatisme : écrasement, lacération par un objet contondant ou projection d’un corps étranger. L’examen physique recherche des signes de plaies du globe : hypotonie, issue choroïdienne noirâtre, altération du reflet cornéen et corectopie. Les signes cliniques devant faire suspecter un hématome intraorbitaire compressif sont des douleurs intenses, une baisse de l’acuité visuelle par compression du nerf optique, une exophtalmie, une ophtalmoplégie, une mydriase. Avant tout examen ophtalmologique, il est recommandé d’éviter toute compression sur le globe oculaire, ainsi que les efforts à glotte fermée et de mettre en place une coque de protection. Dans les autres circonstances, un examen ophtalmologique est recommandé dans les 24 heures.
L’examen ophtalmologique commence par une mesure de l’acuité visuelle et de la pression intraoculaire. L’examen de la conjonctive recherche l’existence d’un ulcère conjonctival, d’une plaie conjonctivale ou d’une hémorragie sous-conjonctivale. En présence d’une hémorragie sous-conjonctivale diffuse associée à une hypotonie, une exploration est demandée sous anesthésie, à la recherche d’une plaie sclérale sous-jacente. L’examen de la cornée recherche un ulcère après instillation de fluorescéine, ou une plaie cornéenne. On distingue les plaies lamellaires (lacérations) non perforantes et les plaies transfixiantes caractérisées par une fuite d’humeur aqueuse bien visualisée après instillation de fluorescéine (signe de Seidel). L’examen cornéen recherche également la présence d’un corps étranger superficiel ou intracornéen profond. L’examen de la chambre antérieure recherche principalement la présence de sang (hyphéma), qui peut être associée à une hypertonie intra-oculaire par obstruction trabéculaire. L’examen de l’iris s’attache à mesurer le diamètre et à évaluer la forme de la pupille avant dilation pharmacologique. L’existence d’une mydriase post-traumatique peut avoir différentes causes : rupture traumatique du sphincter de l’iris, sidération irienne post-traumatique ou lésion neurologique (périphérique dans le cadre d’un hématome intraorbitaire compressif ou centrale). Ainsi, dans un contexte de traumatisme oculaire aigu, la valeur de l’examen pupillaire dans l’évaluation neurologique doit être prudente. L’examen de l’angle iridocornéen (gonioscopie) cherche des signes de récession angulaire (approfondissement de l’angle iridocornéen par clivage au sein du muscle ciliaire) qui peut s’associer à une hypertonie retardée (de plusieurs mois à des années), de cyclodialyse (désinsertion des corps ciliaires) qui peut s’associer à une hypotonie, ou d’iridodialyse (désinsertion de la base de l’iris). L’examen du cristallin recherche des signes de luxation cristallinienne antérieure ou postérieure. La survenue d’une cataracte post-traumatique aiguë est observée en cas de plaie pénétrante associée à une plaie cristallinienne. Tout traumatisme oculaire contusif peut s’associer à un risque de cataracte traumatique à distance. Enfin, l’examen du fond d’œil après dilation pupillaire recherche une hémorragie intravitréenne, un hématome sous-rétinien ou choroïdien, une contusion rétinienne périphérique ou centrale (œdème de Berlin), des déchirures rétiniennes ou un décollement de rétine. L’existence d’un œdème papillaire unilatéral oriente vers une contusion du nerf optique ou sa compression dans le cadre d’un hématome compressif. Si le fond d’œil est rendu impossible par un trouble des milieux et en l’absence de plaie transfixiante, une échographie en mode B permet d’effectuer un bilan lésionnel.
En cas de plaie du globe oculaire, une prise en charge chirurgicale est indiquée en urgence associée à une antibioprophylaxie dans le but de prévenir la survenue d’une endophtalmie.
En cas d’hématome intraorbitaire compressif, une prise en charge chirurgicale urgente (dans les 6 heures) est également requise en cas de signes de compression du nerf optique (baisse de l’acuité visuelle, œdème papillaire) afin de limiter le risque de séquelles fonctionnelles. La prise en charge consiste en une décompression orbitaire médicale (mannitol, acétazolamide et solumédrol intraveineux) et chirurgicale (canthotomie et cantholyse et/ou effondrement de la paroi orbitaire). Le traitement d’un ulcère conjonctival ou cornéen repose sur la prescription d’un collyre antiseptique afin de prévenir une surinfection, de larmes artificielles, voire de pommades ophtalmiques à visée antalgique et cicatrisante (vitamine B12 ou vitamine A). En cas d’hyphéma, le traitement a pour objectif de prévenir la survenue de complications (hypertonie intraoculaire, saignement secondaire, synéchies iridocristalliniennes) ; un traitement local associant un collyre corticoïde topique (dexaméthasone), un collyre cycloplégique (atropine), voire un collyre hypotonisant en cas d’hypertonie aiguë est prescrit.
Les autres situations (luxation du cristallin, hémorragie intravitréenne, sous-rétinienne ou choroïdienne, décollement de rétine) requièrent un avis chirurgical différé.•
POINTS FORTS À RETENIR
La prise en charge du patient polytraumatisé débute sur les lieux de l’accident et doit traiter les détresses vitales immédiates, assurer l’analgésie et prévenir le déplacement secondaire des fractures, en particulier du rachis, par une immobilisation de l’axe tête-cou-tronc mais également des différents foyers de fracture.
Plusieurs lésions sont souvent associées, justifiant une prise en charge pluridisciplinaire. Les patients les plus graves doivent être orientés vers des centres de référence ou « trauma centers ».
Chez le patient instable, il faut appliquer initialement une stratégie de type « damage control » visant à ne traiter que les lésions mettant en jeu le pronostic vital.
L’hémorragie est la principale cause de mortalité. Sa gestion repose, à la phase préhospitalière, sur la limitation des saignements, le respect des objectifs de pression artérielle, l’administration intraveineuse d’acide tranexamique et l’orientation rapide sur un centre de référence. À l’arrivée à l’hôpital, les techniques d’hémostase chirurgicales et radiologiques sont mises en œuvre.
Le bilan lésionnel exhaustif repose sur la tomodensitométrie corps entier avec injection de produit de contraste. L’instabilité hémodynamique peut initialement compromettre sa réalisation et faire réaliser une échographie de type FAST, des radiographies du thorax et du bassin pour guider la prise en charge.
L’anesthésie générale, l’intubation orotrachéale et la ventilation mécanique sont justifiées en cas de traumatisme crânien grave, de détresse respiratoire grave ou pour assurer l’analgésie.
La réanimation hémodynamique repose sur le remplissage vasculaire et l’emploi précoce de noradrénaline. Les objectifs tensionnels doivent être respectés en attendant que l’hémostase chirurgicale soit faite. En l’absence d’un traumatisme crânien grave, la pression artérielle systolique doit être de 80 à 90 mmHg. En présence d’un traumatisme crânien grave, elle doit être supérieure à 120 mmHg.
Les tests de coagulation standard sont soumis à des délais de réalisation incompatibles avec la gestion de la coagulopathie précoce et rapidement évolutive qui accompagne l’hémorragie. La transfusion doit donc être précoce et associer CGR, PFC, plaquettes et concentrés de fibrinogène.
Message de l'auteur
Les traumatismes sévères représentent la première cause de décès du sujet jeune. Parmi les causes de décès, le traumatisme crânien et le choc hémorragique sont les deux causes les plus fréquentes et le choc hémorragique représente la première cause de décès évitable. En France, les traumatismes font le plus souvent suite à un traumatisme fermé (accident de voiture, chute…) par opposition au traumatisme pénétrant (arme blanche ou à feu).
La prise en charge préhospitalière en France a comme particularité d’être médicalisée et de reposer sur le système des SAMU-SMUR. La première étape lors de la prise en charge d’un polytraumatisé consiste à évaluer la gravité et dépister les détresses vitales qui nécessitent un traitement urgent. Les patients qui présentent les traumatismes les plus graves doivent être orientés préférentiellement dans les centres experts qui permettent la prise en charge de toutes les lésions post- traumatiques et qui ont l’habitude de recevoir des traumatisés sévères. Plusieurs travaux montrent dans la littérature qu’orienter un patient dans un centre expert permet d’améliorer le pronostic des patients les plus graves.
à l’admission dans les centres experts, dans un service spécialisé dit de « déchocage », les patients traumatisés sont pris en charge par des anesthésistes-réanimateurs qui supervisent des équipes multidisciplinaires. Le diagnostic des lésions associe un examen clinique et le scanner corps entier. Quand les patients ont une instabilité hémodynamique qui empêche leur transfert au scanner, il faut réaliser une échographie de type FAST, une radiographie du bassin et du thorax de face. Les détresses vitales sont prises en charge au déchocage, et les anomalies biologiques, en particulier les troubles de l’hémostase dépistés précocement et traités rapidement. Le traitement des troubles de l’hémostase repose sur l’association de produits sanguins labile et de concentrés de facteurs de coagulation. Une fois l’imagerie réalisée, des avis spécialisés sont demandés et les traitement spécifiques entrepris. Pour les patients en état de choc hémorragique, la stratégie proposées est désormais celle de Damage Control Resuscitation ou l’objectif est d’abréger toutes les étapes de la prise en charge pour obtenir une hémostase la plus rapide possible.Une fois cette phase initiale passée, le parcours du traumatisé sévère n’est pas terminé puisque ces patients nécessiteront souvent de nombreuses reprises chirurgicales puis de la rééducation fonctionnelle. Ne pas oublier que certains patients nécessiteront également une prise en charge psychiatrique en raison de syndrome de stress post-traumatique.

 Encadrés
Encadrés