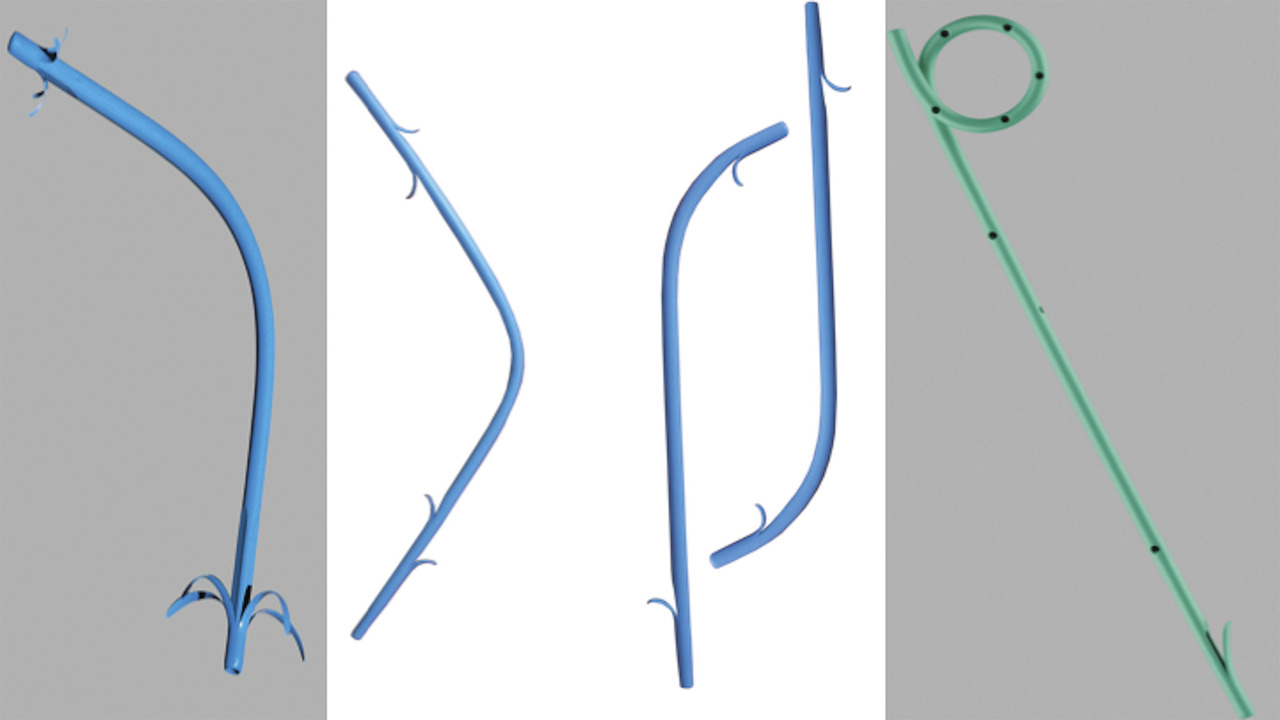Les prothèses digestives sont des tubes en plastique (polyéthylène ou téflon) ou constitués d’un maillage métallique (Nitinol) visant à restaurer la lumière digestive obstruée. De nombreux modèles existent, avec divers types de couverture (fig. 1 ) pour limiter le risque de migration, principale complication.
En général, les prothèses métalliques non couvertes (PMNC) sont adaptées à la pathologie tumorale car elles deviennent inamovibles par bourgeonnement intraprothétique. Dans les sténoses bénignes, on préfère celles couvertes (PMC), qui peuvent être extraites ultérieurement.
Leur indication initiale était la prise en charge palliative des cancers digestifs occlusifs :
– de l’œsophage (principalement), où on privilégie les prothèses partiellement couvertes (PMPC) ;1
– du pancréas ou de l’estomac en cas d’obstruction pyloro-duodénale par envahissement tumoral (PMNC) ;
– du côlon, en palliatif ou en solution temporaire avant chirurgie ; en raison des perforations et migrations, elles sont de moins en moins utilisées.
Autre indication, la pathologie biliopancréatique, incluant :
– les obstructions biliaires tumorales, par cholangiocarcinome, adénocarcinome de la tête du pancréas ou de la papille : le drainage biliaire par prothèse est le traitement en cas d’ictère. Dans cette situation, les PMNC sont la règle ;2
– les sténoses bénignes, notamment biliaires indéterminées ou postopératoires, ou celles du canal de Wirsung sur pancréatite chronique calcifiante, bénéficiant de prothèses extractibles (plastiques multiples [fig. 2 ] ou PMC).
Leur pose respecte généralement une procédure standard : repérage de la zone sténosée ; opacification sous radioscopie pour confirmer et caractériser l’obstruction ; mise en place d’un fil guide ; avancée du cathéter porteur sur le guide puis déploiement de la prothèse.
Aujourd’hui, l’endoscopie thérapeutique a une place croissante dans la gestion des perforations, fistules ou collections, où elle s’est révélée plus efficace et moins morbide que la chirurgie, élargissant les indications des prothèses.
En général, les prothèses métalliques non couvertes (PMNC) sont adaptées à la pathologie tumorale car elles deviennent inamovibles par bourgeonnement intraprothétique. Dans les sténoses bénignes, on préfère celles couvertes (PMC), qui peuvent être extraites ultérieurement.
Leur indication initiale était la prise en charge palliative des cancers digestifs occlusifs :
– de l’œsophage (principalement), où on privilégie les prothèses partiellement couvertes (PMPC) ;1
– du pancréas ou de l’estomac en cas d’obstruction pyloro-duodénale par envahissement tumoral (PMNC) ;
– du côlon, en palliatif ou en solution temporaire avant chirurgie ; en raison des perforations et migrations, elles sont de moins en moins utilisées.
Autre indication, la pathologie biliopancréatique, incluant :
– les obstructions biliaires tumorales, par cholangiocarcinome, adénocarcinome de la tête du pancréas ou de la papille : le drainage biliaire par prothèse est le traitement en cas d’ictère. Dans cette situation, les PMNC sont la règle ;2
– les sténoses bénignes, notamment biliaires indéterminées ou postopératoires, ou celles du canal de Wirsung sur pancréatite chronique calcifiante, bénéficiant de prothèses extractibles (plastiques multiples [
Leur pose respecte généralement une procédure standard : repérage de la zone sténosée ; opacification sous radioscopie pour confirmer et caractériser l’obstruction ; mise en place d’un fil guide ; avancée du cathéter porteur sur le guide puis déploiement de la prothèse.
Aujourd’hui, l’endoscopie thérapeutique a une place croissante dans la gestion des perforations, fistules ou collections, où elle s’est révélée plus efficace et moins morbide que la chirurgie, élargissant les indications des prothèses.
Fistules œsogastriques postopératoires
L’endoscopie est la méthode de choix dans la prise en charge des complications de la chirurgie œsogastrique, qu’elle soit carcinologique ou bariatrique (sleeve gastrectomy, bypass). L’une des principales est la fistule anastomotique (5 à 15 %), dont la reprise chirurgicale (suture) est souvent inefficace et très morbide. L’endoscopie a amélioré le pronostic.
Après sleeve gastrectomy, la fistule se développe au bord supérieur de la ligne d’agrafes. Les premières approches endoscopiques consistaient à placer une prothèse métallique pour la couvrir, mais les migrations étaient fréquentes et le taux de succès < 70 %. Puis le drainage interne – pose de prothèse plastique (PP) de petit calibre, dite queue de cochon, à travers l’orifice de la fistule entre la collection et l’œsophage, pour nettoyer celle-ci et guider la cicatrisation (fig. 3 ) – est devenu la référence3 (taux de succès 85-90 %).
La fistule après chirurgie œsophagienne carcinologique requiert une PMC pour dériver les sécrétions et les aliments, avec un risque de migration limité. Ainsi, des prothèses adaptées (fig. 4 ) sont placées pendant 6 à 8 semaines, induisant une réépithélialisation qui referme l’orifice fistuleux. L’efficacité est de 70 %, souvent après plusieurs changements de prothèse et en moyenne 3 à 6 mois de traitement.
Après sleeve gastrectomy, la fistule se développe au bord supérieur de la ligne d’agrafes. Les premières approches endoscopiques consistaient à placer une prothèse métallique pour la couvrir, mais les migrations étaient fréquentes et le taux de succès < 70 %. Puis le drainage interne – pose de prothèse plastique (PP) de petit calibre, dite queue de cochon, à travers l’orifice de la fistule entre la collection et l’œsophage, pour nettoyer celle-ci et guider la cicatrisation (
La fistule après chirurgie œsophagienne carcinologique requiert une PMC pour dériver les sécrétions et les aliments, avec un risque de migration limité. Ainsi, des prothèses adaptées (
Drainage biliopancréatique sous écho-endoscopie
La cholangiopancréatographie rétrograde endoscopique (CPRE) est la technique de choix pour désobstruer les voies biliaires et pancréatiques. En cas d’échec (5 %), les options étaient le drainage percutané radiologique, assez morbide, ou la chirurgie (anastomose biliodigestive).
L’écho-endoscopie (EE) permet d’analyser les structures par voie transgastrique et transduodénale, grâce à une sonde d’échographie placée à l’extrémité de l’endoscope. En outre, dans le canal opérateur, on passe des instruments, notamment des prothèses dites « TTS » (Trough The Scope), réalisant des anastomoses hépatico-gastriques (AHG), cholédoco-duodénales (ACD) et plus récemment wirsungo-gastriques (AWG). La pose suit le même procédé, mais une ponction à l’aiguille du canal à drainer est pratiquée pour y glisser le guide.
Les indications préférentielles pour les AHG et les ACD sont les tumeurs du pancréas ou des voies biliaires obstructives avec ictère,2 où on privilégie les PMPC. Les AWG sont réalisées dans la pancréatite chronique hyperalgique par obstruction canalaire, le plus souvent par prothèse plastique. Le succès technique est respectivement de 90-95 %, 98 % et 70 %, avec une réussite clinique de 80 (AWG) à 98 %, une morbidité de 4 à 15 % (essentiellement hémorragie et migration, gérées médicalement) et une mortalité faible.4
L’écho-endoscopie (EE) permet d’analyser les structures par voie transgastrique et transduodénale, grâce à une sonde d’échographie placée à l’extrémité de l’endoscope. En outre, dans le canal opérateur, on passe des instruments, notamment des prothèses dites « TTS » (Trough The Scope), réalisant des anastomoses hépatico-gastriques (AHG), cholédoco-duodénales (ACD) et plus récemment wirsungo-gastriques (AWG). La pose suit le même procédé, mais une ponction à l’aiguille du canal à drainer est pratiquée pour y glisser le guide.
Les indications préférentielles pour les AHG et les ACD sont les tumeurs du pancréas ou des voies biliaires obstructives avec ictère,2 où on privilégie les PMPC. Les AWG sont réalisées dans la pancréatite chronique hyperalgique par obstruction canalaire, le plus souvent par prothèse plastique. Le succès technique est respectivement de 90-95 %, 98 % et 70 %, avec une réussite clinique de 80 (AWG) à 98 %, une morbidité de 4 à 15 % (essentiellement hémorragie et migration, gérées médicalement) et une mortalité faible.4
Drainage et nécrosectomie
Grâce à l’écho-endoscopie, les prothèses permettent de drainer des collections péridigestives infectées ou symptomatiques. La paroi digestive est alors volontairement traversée. Les 2 indications sont les collections périgastriques (postopératoires ou secondaires à une pancréatite nécrosante : pseudokyste ou surinfection de nécrose organisée) ou pelviennes, après chirurgie ou liées à une pathologie inflammatoire.
Le principe du drainage est le même : ponction échoguidée à l’aiguille, afin d’enrouler un guide dans la collection, puis élargissement du passage par un cystotome et enfin pose soit de plusieurs PP, soit d’une PMC.
– localisations pelviennes : efficacité proche de 100 %, sans complications, ce qui est incomparablement supérieur au drainage chirurgical, difficile à réaliser dans cette zone.
– localisations pancréatiques : drainage transgastrique très efficace (résolution des pseudokystes quasi constante).
La nécrosectomie pancréatique par voie transgastrique réduit la mortalité de la pancréatite aiguë nécrosante, qui est passée de 80 % – lorsque les drainages étaient chirurgicaux – à moins de 20 %, avec une morbidité faible et une efficacité de plus de 90 % sur le sepsis.5 Depuis 3 ans, de nouvelles prothèses métalliques spéciales, soit en forme de diabolo (Nagi) soit « d’apposition tissulaire » (Axios ou Spaxus) facilitent l’accès au péritoine et améliorent encore la technique, en réduisant le nombre de séances (fig. 5 ).
Le principe du drainage est le même : ponction échoguidée à l’aiguille, afin d’enrouler un guide dans la collection, puis élargissement du passage par un cystotome et enfin pose soit de plusieurs PP, soit d’une PMC.
– localisations pelviennes : efficacité proche de 100 %, sans complications, ce qui est incomparablement supérieur au drainage chirurgical, difficile à réaliser dans cette zone.
– localisations pancréatiques : drainage transgastrique très efficace (résolution des pseudokystes quasi constante).
La nécrosectomie pancréatique par voie transgastrique réduit la mortalité de la pancréatite aiguë nécrosante, qui est passée de 80 % – lorsque les drainages étaient chirurgicaux – à moins de 20 %, avec une morbidité faible et une efficacité de plus de 90 % sur le sepsis.5 Depuis 3 ans, de nouvelles prothèses métalliques spéciales, soit en forme de diabolo (Nagi) soit « d’apposition tissulaire » (Axios ou Spaxus) facilitent l’accès au péritoine et améliorent encore la technique, en réduisant le nombre de séances (
Nouvelles indications ?
Très récemment, les prothèses ont été utilisées pour des anastomoses gastro-intestinales endoscopiques. Le principe : faire communiquer la lumière gastrique avec celle du duodénum distal ou du jéjunum proximal, par un abord sous EE exclusif, notamment grâce au design d’Axios. Indications : obstructions antro-pyloro- duodénales tumorales ou bénignes, en échec du stenting duodénal classique. C’est donc une alternative à la gastro- entéro-anastomose chirurgicale.
Depuis la 1re intervention dans notre centre, plusieurs cas ont été publiés, avec des résultats très prometteurs et une faible morbidité. Cette évolution est liée aux progrès des endoscopes mais également des prothèses, évaluées actuellement dans le bypass.
Depuis la 1re intervention dans notre centre, plusieurs cas ont été publiés, avec des résultats très prometteurs et une faible morbidité. Cette évolution est liée aux progrès des endoscopes mais également des prothèses, évaluées actuellement dans le bypass.
Références
1. Spaander MC, et al. Esophageal stenting for benign and malignant disease: European Society of Gastrointestinal Endoscopy Clinical Guideline. Endoscopy 2016;48:939-48.
2. Dumonceau JM, et al. Endoscopic biliary stenting: indications, choice of stents, and results: ESGE Clinical Guideline. Updated Oct 2017. Endoscopy 2018;50: 910-30.
3. Gonzalez JM, et al. Internal endoscopic drainage as first line or second line treatment in case of postsleeve gastrectomy fistulas. Endosc Int Open 2018;6: E745-50.
4. Baars JE, et al. EUS-guided biliary drainage: A comprehensive review of the literature. Endosc Ultrasound 2018;7:4-9.
5. Arvanitakis M, et al. Endoscopic management of acute necrotizing pancreatitis:ESGE evidence-based multi- disciplinary guidelines. Endoscopy 2018;50:524-46.
2. Dumonceau JM, et al. Endoscopic biliary stenting: indications, choice of stents, and results: ESGE Clinical Guideline. Updated Oct 2017. Endoscopy 2018;50: 910-30.
3. Gonzalez JM, et al. Internal endoscopic drainage as first line or second line treatment in case of postsleeve gastrectomy fistulas. Endosc Int Open 2018;6: E745-50.
4. Baars JE, et al. EUS-guided biliary drainage: A comprehensive review of the literature. Endosc Ultrasound 2018;7:4-9.
5. Arvanitakis M, et al. Endoscopic management of acute necrotizing pancreatitis:ESGE evidence-based multi- disciplinary guidelines. Endoscopy 2018;50:524-46.