De nombreux autres agents infectieux, des maladies systémiques – en particulier la sarcoïdose et les connectivites auxquelles on rattache les myocardites à cellules géantes –, des médicaments ou des toxines peuvent être incriminés. Parmi les causes toxiques citons l’alcool, les catécholamines, la cocaïne, les anthracyclines, certains antirétroviraux.
Les myocardites peuvent être pauci- symptomatiques (douleurs thoraciques légères et/ou palpitations et modifications ECG transitoires), mais le tableau peut dans certains cas être dramatique avec choc cardiogénique ou troubles du rythme ventriculaire sévères imposant une hospitalisation.
La physiopathologie est complexe mais peut expliquer la diversité des scénarios cliniques rencontrés. Ainsi, on décrit une phase initiale d’agression myocardique (virale ou liée à un autre mécanisme).
Lui succède (ou non) un phénomène d’auto-immunité dans le contexte d’une éventuelle prédisposition génétique.
La progression vers une cardiomyopathie dilatée semble concerner principalement les patients gardant une inflammation chronique à la biopsie endomyocardique, ceux n’ayant pas éliminé l’agent infectieux ou encore ceux qui ont développé des auto-anticorps cardiaques pathogènes dirigés contre des protéines du myocarde.
Ainsi, dans certains cas, l’évolution se fait à bas bruit et la maladie est découverte au stade de cardiomyopathie dilatée d’allure primitive.1
Démarche diagnostique
La myocardite est souvent un diagnostic différentiel du syndrome coronaire aigu à coronaires angiographiquement normales.
Selon le dernier avis d’experts de la Société européenne de cardiologie,2 cette maladie inflammatoire du myocarde doit répondre aux critères de « Dallas » : nécessité d’une preuve d’infiltration inflammatoire myocardique (leucocytes ≥ 14/mm2 incluant jusqu’à 4 monocytes/mm2 avec lymphocytes T CD3 positifs ≥ 7 cellules/mm2) avec dégénérescence myocytaire et nécrose des cellules, d’origine non ischémique. La biopsie offre également la possibilité de rechercher le génome viral au sein du myocarde, sa présence contre-indiquant les immunosuppresseurs en phase aiguë.
En urgence et en cas d’instabilité hémodynamique, la biopsie endomyocardique est l’approche à privilégier, l’accès à l’IRM étant le plus souvent difficile (
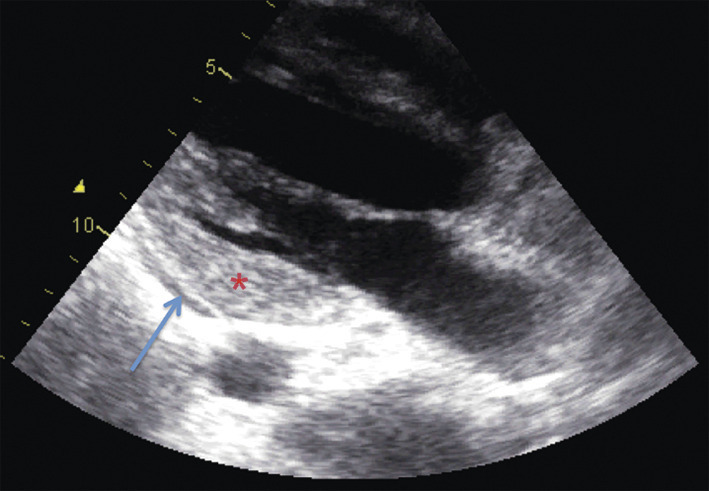
Le plus souvent, l’échocardiographie, indispensable à la prise en charge, est le premier examen réalisé (
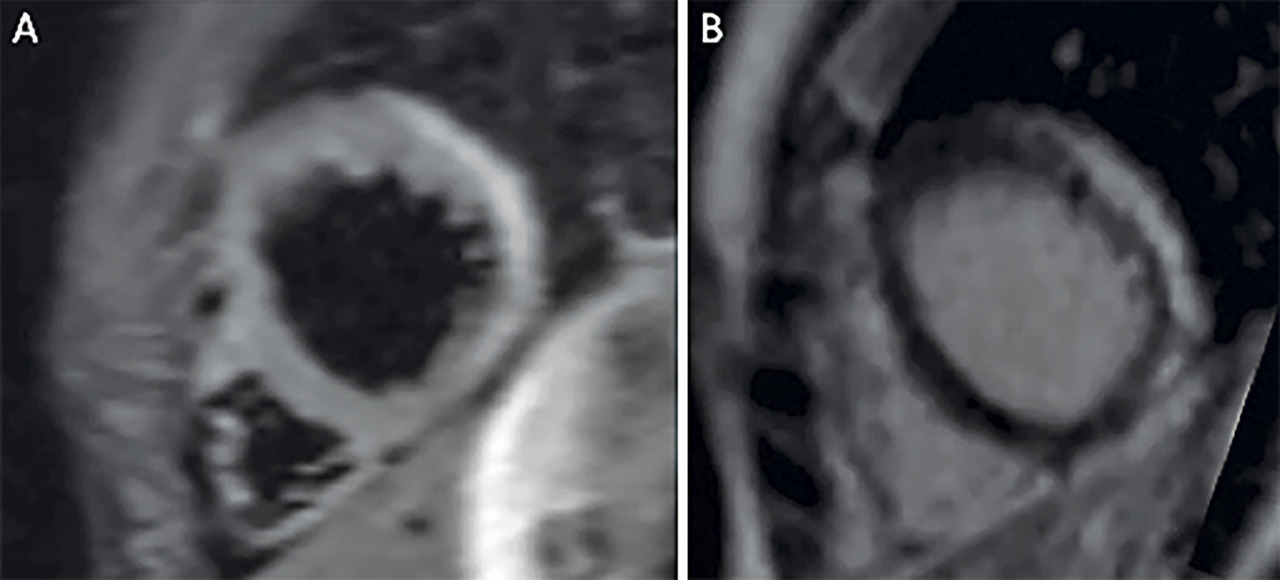
Si l’état clinique est stabilisé, l’IRM cardiaque est devenue incontournable pour le diagnostic étiologique à la phase aiguë : elle objective l’œdème myocardique, permet de suivre sa régression et l’apparition d’une fibrose séquellaire.
L’IRM ne remplace cependant pas la biopsie endomyocardique et ne doit pas la retarder lorsqu’elle est nécessaire.
En cas de suspicion de sarcoïdose cardiaque, une inflammation au sein du myocarde n’est réellement objectivée en imagerie qu’avec un TEP-scan ou un TEP-IRM et guide la thérapeutique.
L’électrocardiogramme peut prendre des aspects très variés.
Les modifications sont peu sensibles et peu spécifiques mais il faut s’alarmer d’un allongement du PR, d’un élargissement du QRS ou de troubles du rythme ventriculaires.
Les sérologies virales, peu utiles, ne sont pas recommandées compte tenu de la prévalence élevée d’immunisation dans la population générale indemne d’infection myocardique évolutive.
Selon les experts européens, elles peuvent aider si on suspecte une hépatite C, une rickettsiose, une maladie de Lyme en zone endémique et l’infection par le VIH.2
Formes cliniques
L’une des formes les plus fréquentes est le pseudo-infarctus, sans lésion coronaire, installé en quelques heures ou jours, traduisant le plus souvent une myocardite lymphocytaire ou, plus rarement, nécrosante à éosinophiles ou à cellules géantes.
Autre tableau courant : une insuffisance cardiaque apparue en moins de 2 semaines avec une instabilité hémodynamique et un ventricule gauche de diamètre normal ou peu dilaté. En cause le plus souvent : une myocardite lymphocytaire ou, plus rarement, nécrosante à éosinophiles ou à cellules géantes.
La survenue en quelques semaines d’une défaillance cardiaque avec dilatation ventriculaire gauche, troubles du rythme ventriculaire, bloc auriculo- ventriculaire de haut degré, résistance au traitement médical conventionnel fait redouter une myocardite à cellules géantes dont le pronostic est grave en l’absence de traitement.
Une sarcoïdose cardiaque est suspectée en cas d’antécédent de forme pulmonaire de la maladie, de troubles du rythme ventriculaire et de la conduction atrio-ventriculaire et d’une histoire clinique évoluant depuis plusieurs semaines ou mois avec des troubles de la cinétique ventriculaire gauche non systématisés à un territoire coronaire en échocardiographie. L’inflammation persistante doit être recherchée au TEP- scan.
Une insuffisance cardiaque avec dilatation ventriculaire gauche isolée sans arythmie ventriculaire significative, ni trouble de la conduction auriculoventriculaire, installée en quelques semaines à mois peut évoquer une myocardite lymphocytaire chronique, vue souvent au stade cicatriciel ou de cardiomyopathie inflammatoire chronique.
Une hyperéosinophilie doit faire évoquer une myocardite à éosinophiles ou d’hypersensibilité. Elles ont en général un pronostic plus réservé en l’absence de prise en charge immédiate.
Prise en charge thérapeutique
Les cardioprotecteurs (β-bloquants, bloqueurs du système rénine-angiotensine-aldostérone dont les IEC) doivent être instaurés sans retard en cas de dysfonction systolique ventriculaire gauche et/ou de troubles du rythme.
La question la plus difficile est celle du traitement immunosuppresseur (corticoïdes, azathioprine, ciclosporine A) qui dépend des résultats de la biopsie endomyocardique et de l’absence d’infection cardiaque active, à l’exception de la sarcoïdose dont diagnostic et traitement peuvent être guidés uniquement par les imageries non invasives (IRM et TEP-scan).
La reprise de l’activité physique et sportive après une myocardite aiguë est une question fréquente chez ces patients souvent jeunes. L’exercice est contre-indiqué pendant au moins 3 mois après l’épisode aigu, 6 mois en cas de signes de gravité initiaux (dysfonction VG et troubles du rythme).
Une fibrose myocardique séquellaire après guérison, visible sur l’IRM de contrôle qui est systématique avant la reprise du sport, peut favoriser des troubles du rythme (risque de mort subite).
Selon le récent consensus européen, on autorise la reprise du sport en compétition en l’absence de dysfonction résiduelle du ventricule gauche et de troubles du rythme lors d’une épreuve d’effort maximale et d’un Holter rythmique sur 24 heures incluant un effort physique, idéalement sans traitement.4 Ces sportifs doivent ensuite être revus annuellement.
1. Critères diagnostiques d’une myocardite suspectée cliniquement*
Cliniques
• Douleur thoracique aiguë, péricardique ou pseudo-ischémique
• Début (quelques jours jusqu’à 3 mois) ou aggravation d’une dyspnée au repos ou à l’effort et/ou fatigue ± signe d’IC gauche et/ou droite
• Subaiguë/chronique (> 3 mois) ou aggravation d’une dyspnée au repos ou à l’effort et/ou fatigue ± signe d’IC gauche et/ou droite
• Palpitations et/ou symptômes d’arythmie et/ou syncope inexpliqués et/ou mort cardiaque subite récupérée
• Choc cardiogénique inexpliqué
Paracliniques
• ECG/Holter/stress test
Anomalies récentes à l’ECG 12 dérivations et/ou Holter et/ou test d’effort (l’un ou l’autre des éléments suivants) : BAV de degré I à III, ou bloc de branche, modifications du ST/onde T (sus-/ sous-décalage du ST, inversion de l’onde T), arrêt sinusal, tachycardie ou fibrillation ventriculaire et asystolie, fibrillation auriculaire, diminution de l’amplitude de l’onde R, trouble de la conduction intraventriculaire (QRS élargi), ondes Q anormales, microvoltage, extrasystolie fréquente, tachycardie supraventriculaire.
• Marqueurs de myolyse
Troponine T/troponine I élevée
• Anomalies fonctionnelles et structurelles en imagerie (écho/angio/IRM)
Anomalie récente, sans autre explication, de la structure et de la fonction ventriculaire gauche et/ou ventriculaire droite (y compris découverte fortuite chez des sujets apparemment asymptomatiques) : altération de la fonction systolique ou diastolique régionale ou globale ± dilatation ventriculaire ± augmentation de l’épaisseur de la paroi ± épanchement péricardique ± thrombus endocavitaire
• Caractérisation tissulaire en IRM
Œdème et/ou rehaussement tardif
La myocardite est soupçonnée si ≥ 1 critère clinique et ≥ 1 critère paraclinique, en l’absence de : maladie coronaire (sténose ≥ 50 % à l’angiographie) ; MCV préexistante connue ou causes extracardiaques qui pourraient expliquer le syndrome (maladie valvulaire, cardiopathie congénitale, hyperthyroïdie…).
La suspicion est plus élevée lorsque le nombre de critères augmente.
Si le patient est asymptomatique, il faut ≥ 2 critères.
2. Myocardite : quels marqueurs biologiques ?
Un examen sensible mais non spécifique en faveur du diagnostic est le dosage de la troponine, mais il peut être également normal en cas de myocardite ou de cardiomyopathie inflammatoire.
Les peptides natriurétiques ne témoignent que de l’augmentation des pressions intracardiaques ou du remodelage ventriculaire, ils ne sont donc pas spécifiques.
La CRP est souvent élevée mais ne confirme pas le diagnostic. Les auto-anticorps et anticorps anti-cœur ne sont pas dosés en routine.
2. Caforio AL, Pankuweit S, Arbustini E, et al. Current state of knowledge on aetiology, diagnosis, management, and therapy of myocarditis: a position statement of the European Society of Cardiology Working Group on Myocardial and Pericardial Diseases. Eur Heart J 2013;34:2636-48.
3. Trochu JN, Piriou N, Toquet C, et al. Myocardites. Rev Med Interne 2012;33:567-74.
4. Pelliccia A, Solberg EE, Papadakis M, et al. Recommendations for participation in competitive and leisure time sport in athletes with cardiomyopathies, myocarditis, and pericarditis: position statement of the Sport Cardiology Section of the European Association of Preventive Cardiology (EAPC). Eur Heart J 2019;40:19-33.

 Encadrés
Encadrés