La même initiative publique qui guide les programmes de dépistage des cancers se doit d’en assurer par la suite l’organisation et l’assurance qualité-sécurité mais également de tenir compte des innovations afin de mettre à disposition un programme sans cesse optimisé. De fait, on recherche en permanence un équilibre entre, d’une part, la facilitation de l’intégration de ces innovations dans un programme et, d’autre part, l’exigence de satisfaction des prérequis en termes de qualité et de sécurité de la procédure de dépistage.
Bien que des évolutions à très long terme soient d’ores et déjà envisageables, notamment en termes de personnalisation des procédures, cet article se bornera à évoquer les évolutions en cours ou à moyen terme du dispositif. Les enjeux ne sont pas comparables pour les différents programmes : il s’agit pour le dépistage des cancers du sein d’une rénovation du programme et de l’intégration d’innovations technologiques, pour le dépistage du cancer colorectal de répondre à l’enjeu d’un programme efficace mais pour lequel la participation est insuffisante, et pour le dépistage du cancer du col de l’utérus de la généralisation d’un programme se fondant sur une pratique de dépistage déjà répandue.
Bien que des évolutions à très long terme soient d’ores et déjà envisageables, notamment en termes de personnalisation des procédures, cet article se bornera à évoquer les évolutions en cours ou à moyen terme du dispositif. Les enjeux ne sont pas comparables pour les différents programmes : il s’agit pour le dépistage des cancers du sein d’une rénovation du programme et de l’intégration d’innovations technologiques, pour le dépistage du cancer colorectal de répondre à l’enjeu d’un programme efficace mais pour lequel la participation est insuffisante, et pour le dépistage du cancer du col de l’utérus de la généralisation d’un programme se fondant sur une pratique de dépistage déjà répandue.
Cancer du sein : un programme de dépistage en pleine rénovation
Le programme de dépistage des cancers du sein a été déployé en 20041 et repose sur l’invitation systématique, tous les deux ans, de l’ensemble des femmes de 50 à 74 ans, sans facteur de risque autre que leur âge, à bénéficier d’un examen clinique des seins ainsi que d’une mammographie par un radiologue agréé. Il a connu bon nombre d’évolutions, parmi lesquelles l’intégration de la mammographie numérique.
Si certaines des évolutions à venir sont également d’ordre technologique et concernent en particulier la tomosynthèse (mammographie « 3D ») et la dématérialisation des clichés, d’autres sont menées dans le cadre d’un plan de rénovation ambitieux de ce programme adopté par les pouvoirs publics à la suite des conclusions d’une concertation nationale citoyenne et scientifique menée en 2016.2, 3 L’enjeu à relever est de « proposer à toutes les femmes, quels que soient leur âge et leur niveau de risque, un suivi personnalisé, mieux coordonné et impliquant davantage le médecin traitant ». Ce plan a été structuré par tranche d’âge avec :
Le ministère de la Santé a également saisi mi-2018 la Haute Autorité de santé (HAS) et l’INCa pour définir le cadre de la consultation de prévention à 25 ans. L’objectif principal est de pouvoir proposer, suffisamment tôt et avec une fréquence adaptée, une approche de dépistage ou de suivi pour les femmes ayant des antécédents familiaux et un sur-risque de cancer du sein. Ce temps dédié doit permettre de réaliser une analyse des antécédents personnels et familiaux, d’exposer les modalités et le calendrier de dépistage ou de surveillance adaptés, pour le cancer du sein mais aussi pour le cancer du col de l’utérus, et d’informer sur les facteurs de risque susceptibles de favoriser la survenue de cancers. Ce contact spécifique pourra être renouvelé à l’âge de 50 ans pour une femme à niveau de risque standard, lors de l’entrée dans le programme ; une femme aura ainsi le choix de faire réaliser la mammographie sur la base de son invitation ou de se rendre chez son médecin pour obtenir plus d’informations avant de prendre sa décision.
L’accessibilité au dépistage sera renforcée, avec la possibilité d’inclusion dans le dépistage par des outils spécifiques (serveurs d’éligibilité, bons de prise en charge…). La limitation des freins liés à des difficultés d’accès géographiques est aussi traitée par l’expérimentation et l’évaluation d’une offre de mammographie au sein de structures mobiles (« mammobiles »).
Le renforcement de la qualité impose notamment une plus grande attention à la douleur lors de la réalisation de la mammographie et un rendu des résultats dès la réalisation de la mammographie initiale. La recherche développe trois axes prioritaires : limiter le surtraitement, mieux évaluer l’impact du dépistage et réduire les inégalités d’accès ou de recours (recherche interventionnelle).
Si certaines des évolutions à venir sont également d’ordre technologique et concernent en particulier la tomosynthèse (mammographie « 3D ») et la dématérialisation des clichés, d’autres sont menées dans le cadre d’un plan de rénovation ambitieux de ce programme adopté par les pouvoirs publics à la suite des conclusions d’une concertation nationale citoyenne et scientifique menée en 2016.2, 3 L’enjeu à relever est de « proposer à toutes les femmes, quels que soient leur âge et leur niveau de risque, un suivi personnalisé, mieux coordonné et impliquant davantage le médecin traitant ». Ce plan a été structuré par tranche d’âge avec :
- 10 mesures pour les femmes de 50 à 74 ans, cible initiale du dépistage organisé, afin d’offrir aux femmes et aux professionnels une information et une formation optimisées et de faciliter l’accès au dépistage tout en en renforçant la qualité ;
- la mise en place pour les femmes de 25 ans d’une consultation dédiée à la prévention et au dépistage et prise en charge à 100 % par l’assurance maladie ;
- enfin pour les femmes de plus de 74 ans une possibilité de suivi personnalisé (en l’état, le dépistage organisé cesse de leur être proposé à cet âge).
Le ministère de la Santé a également saisi mi-2018 la Haute Autorité de santé (HAS) et l’INCa pour définir le cadre de la consultation de prévention à 25 ans. L’objectif principal est de pouvoir proposer, suffisamment tôt et avec une fréquence adaptée, une approche de dépistage ou de suivi pour les femmes ayant des antécédents familiaux et un sur-risque de cancer du sein. Ce temps dédié doit permettre de réaliser une analyse des antécédents personnels et familiaux, d’exposer les modalités et le calendrier de dépistage ou de surveillance adaptés, pour le cancer du sein mais aussi pour le cancer du col de l’utérus, et d’informer sur les facteurs de risque susceptibles de favoriser la survenue de cancers. Ce contact spécifique pourra être renouvelé à l’âge de 50 ans pour une femme à niveau de risque standard, lors de l’entrée dans le programme ; une femme aura ainsi le choix de faire réaliser la mammographie sur la base de son invitation ou de se rendre chez son médecin pour obtenir plus d’informations avant de prendre sa décision.
L’accessibilité au dépistage sera renforcée, avec la possibilité d’inclusion dans le dépistage par des outils spécifiques (serveurs d’éligibilité, bons de prise en charge…). La limitation des freins liés à des difficultés d’accès géographiques est aussi traitée par l’expérimentation et l’évaluation d’une offre de mammographie au sein de structures mobiles (« mammobiles »).
Le renforcement de la qualité impose notamment une plus grande attention à la douleur lors de la réalisation de la mammographie et un rendu des résultats dès la réalisation de la mammographie initiale. La recherche développe trois axes prioritaires : limiter le surtraitement, mieux évaluer l’impact du dépistage et réduire les inégalités d’accès ou de recours (recherche interventionnelle).
Prendre en compte les innovations technologiques
Au-delà des actions du plan de rénovation, les principales évolutions technologiques en cours concernent la dématérialisation et la tomosynthèse. L’INCa a lancé une dynamique d’expérimentation afin de préciser la stratégie nationale de dématérialisation des mammographies de dépistage. Deux appels à projets ont été lancés en 2016 et 2017, qui ont retenu 4 projets : en Alsace, en Île-de-France, en Normandie et à La Réunion. Ces projets, dont les premiers résultats sont attendus en 2019, visent à évaluer la mise à disposition dématérialisée et sécurisée des clichés et éléments connexes (autres éléments d’imagerie, fiche d’interprétation, bilans de diagnostic immédiat et différé, compte-rendu, etc.) :
– en 2nde lecture organisée dans le cadre du programme de dépistage ;
– en 1re lecture dans les centres d’imagerie médicale ;
– pour les femmes concernées et leur médecin traitant, généraliste ou gynécologue.
Par ailleurs, plusieurs études ont mis en avant l’intérêt d’une nouvelle technologie dans la détection du cancer du sein : la tomosynthèse.6 Il s’agit d’une technique d’imagerie permettant une exploration du sein en trois dimensions. Cet examen, actuellement utilisé en 2e intention pour préciser une anomalie, n’est pas autorisé dans le cadre du programme de dépistage.
Plusieurs études suggèrent que l’utilisation de la tomosynthèse pourrait, en situation de dépistage, conduire à une augmentation de l’ordre de 40 % de la détection des cancers, notamment invasifs, et à une diminution de l’ordre de 15 % du taux de rappel après mammographie. Ce qui permettrait d’envisager une amélioration à la fois de la sensibilité et de la spécificité, et une limitation du risque de surdiagnostic. Cependant, les preuves d’une meilleure performance sont concentrées sur un constructeur (or la tomosynthèse diffère techniquement d’un constructeur à un autre). Parallèlement est soulevée la question d’une augmentation du risque théorique de cancers radio-induits liés à l’augmentation de la dose de rayon X délivrée. De fait, cette technologie, utilisable dans le cadre du diagnostic, diffuse donc légitimement (environ 10 % du parc d’appareils), et une pratique de tomosynthèse s’est développée dans le cadre de démarches individuelles de dépistage.
L’INCa a, en mars 2013 et juin 2014, réalisé un état des lieux et pointé les prérequis nécessaires à l’intégration de cette technologie dans le programme de dépistage organisé.6 Depuis, la HAS a engagé une évaluation de l’acte et de l’opportunité d’intégrer cette technologie dans le programme de dépistage organisé. Des travaux complémentaires ont par ailleurs déjà été engagés par l’INCa pour préciser la description du parc d’appareils et des pratiques de dépistage par tomosynthèse. La définition d’un protocole de contrôle qualité est en cours par l’Agence nationale de sécurité du médicament et des produits de santé (ANSM). Enfin, le développement d’un programme de formation des radiologues devrait être défini en 2019, avec l’appui de la Société française de radiologie.
– en 2nde lecture organisée dans le cadre du programme de dépistage ;
– en 1re lecture dans les centres d’imagerie médicale ;
– pour les femmes concernées et leur médecin traitant, généraliste ou gynécologue.
Par ailleurs, plusieurs études ont mis en avant l’intérêt d’une nouvelle technologie dans la détection du cancer du sein : la tomosynthèse.6 Il s’agit d’une technique d’imagerie permettant une exploration du sein en trois dimensions. Cet examen, actuellement utilisé en 2e intention pour préciser une anomalie, n’est pas autorisé dans le cadre du programme de dépistage.
Plusieurs études suggèrent que l’utilisation de la tomosynthèse pourrait, en situation de dépistage, conduire à une augmentation de l’ordre de 40 % de la détection des cancers, notamment invasifs, et à une diminution de l’ordre de 15 % du taux de rappel après mammographie. Ce qui permettrait d’envisager une amélioration à la fois de la sensibilité et de la spécificité, et une limitation du risque de surdiagnostic. Cependant, les preuves d’une meilleure performance sont concentrées sur un constructeur (or la tomosynthèse diffère techniquement d’un constructeur à un autre). Parallèlement est soulevée la question d’une augmentation du risque théorique de cancers radio-induits liés à l’augmentation de la dose de rayon X délivrée. De fait, cette technologie, utilisable dans le cadre du diagnostic, diffuse donc légitimement (environ 10 % du parc d’appareils), et une pratique de tomosynthèse s’est développée dans le cadre de démarches individuelles de dépistage.
L’INCa a, en mars 2013 et juin 2014, réalisé un état des lieux et pointé les prérequis nécessaires à l’intégration de cette technologie dans le programme de dépistage organisé.6 Depuis, la HAS a engagé une évaluation de l’acte et de l’opportunité d’intégrer cette technologie dans le programme de dépistage organisé. Des travaux complémentaires ont par ailleurs déjà été engagés par l’INCa pour préciser la description du parc d’appareils et des pratiques de dépistage par tomosynthèse. La définition d’un protocole de contrôle qualité est en cours par l’Agence nationale de sécurité du médicament et des produits de santé (ANSM). Enfin, le développement d’un programme de formation des radiologues devrait être défini en 2019, avec l’appui de la Société française de radiologie.
Cancer du col de l’utérus : un programme de dépistage en cours de généralisation
Le cancer du col de l’utérus est le 12e cancer le plus fréquent chez la femme en France. Malgré l’existence d’une pratique de dépistage par frottis largement portée par les gynécologues et qui a pu démontrer son efficacité,7 il reste responsable de 1 100 décès par an. C’est d’ailleurs en France l’un des seuls cancers pour lesquels le pronostic se dégrade.8
Le Plan cancer 2014-2019 prévoyait la généralisation d’un programme de dépistage organisé du cancer du col de l’utérus à l’ensemble du territoire ;9 son déploiement a débuté en 2018. L’objectif affiché est de réduire l’incidence et le nombre de décès par cancer du col de l’utérus de 30 % à 10 ans, en atteignant un taux de couverture de 80 % et en rendant le dépistage plus facilement accessible aux populations vulnérables ou éloignées du système de santé. Outre cette réduction, il s’agit également de se donner l’opportunité d’intervenir le plus précocement possible, le cas échéant avant même un engagement vers un processus cancérogène, de sorte à minimiser le risque obstétrical lié aux conisations (accouchements prématurés, fausses couches).
Sa conception et la structuration du dispositif ont été définies par arrêté en mai 201810 à partir des enseignements des expérimentations menées sur 13 départements,11 après une caractérisation « épidémiologique » des femmes ne participant pas au dépistage et à la suite d’une analyse stratégique sous un angle médico-économique.12 Le dépistage reposera dans un 1er temps sur un examen cytologique à partir d’un prélèvement cervico-utérin réalisé en milieu liquide pour toutes les femmes asymptomatiques de 25 à 65 ans, tous les 3 ans.
L’invitation par les professionnels de santé assurant le suivi gynécologique des femmes reste le mode d’entrée principal dans le dépistage. Il sera complété dans le cadre du programme organisé par l’envoi d’invitations et de relances en direction des femmes n’ayant pas réalisé de dépistage dans les 3 dernières années.
En outre, ce programme prévoit :
– la prise en charge intégrale par l’Assurance maladie, sans avance de frais, du test de dépistage et de son analyse ;
– le recueil par la structure de coordination des dépistages des informations sur le diagnostic, le traitement et le devenir des femmes dont le test de dépistage est positif (qu’elles aient participé spontanément ou aient été invitées par courrier) ;
– un retour d’information vers les professionnels de santé et des actions d’amélioration des pratiques professionnelles (respect de l’intervalle entre deux tests, suivi des femmes ayant un résultat anormal, etc.) ;
– la mise en place d’actions spécifiques en direction de populations vulnérables et/ou très éloignées du système de santé (accompagnement au dépistage, médiation sanitaire, utilisation de l’autoprélèvement, unités mobiles, etc.) ;
– la diversification de l’offre de prélèvement en s’appuyant en particulier sur les médecins généralistes et les sages-femmes.
Compte-tenu des résultats de l’étude médico-économique réalisée par l’INCa en préalable au déploiement, la HAS évalue parallèlement la place, dans ce programme de dépistage, des tests de recherche de papillomavirus en première intention. Le programme en cours de déploiement prévoit d’ores et déjà l’utilisation d’un prélèvement en phase liquide, ce qui permettra, si ce type de test était retenu, d’opérer une transition, sans changement majeur pour la population concernée (hormis l’information naturellement).
Le Plan cancer 2014-2019 prévoyait la généralisation d’un programme de dépistage organisé du cancer du col de l’utérus à l’ensemble du territoire ;9 son déploiement a débuté en 2018. L’objectif affiché est de réduire l’incidence et le nombre de décès par cancer du col de l’utérus de 30 % à 10 ans, en atteignant un taux de couverture de 80 % et en rendant le dépistage plus facilement accessible aux populations vulnérables ou éloignées du système de santé. Outre cette réduction, il s’agit également de se donner l’opportunité d’intervenir le plus précocement possible, le cas échéant avant même un engagement vers un processus cancérogène, de sorte à minimiser le risque obstétrical lié aux conisations (accouchements prématurés, fausses couches).
Sa conception et la structuration du dispositif ont été définies par arrêté en mai 201810 à partir des enseignements des expérimentations menées sur 13 départements,11 après une caractérisation « épidémiologique » des femmes ne participant pas au dépistage et à la suite d’une analyse stratégique sous un angle médico-économique.12 Le dépistage reposera dans un 1er temps sur un examen cytologique à partir d’un prélèvement cervico-utérin réalisé en milieu liquide pour toutes les femmes asymptomatiques de 25 à 65 ans, tous les 3 ans.
L’invitation par les professionnels de santé assurant le suivi gynécologique des femmes reste le mode d’entrée principal dans le dépistage. Il sera complété dans le cadre du programme organisé par l’envoi d’invitations et de relances en direction des femmes n’ayant pas réalisé de dépistage dans les 3 dernières années.
En outre, ce programme prévoit :
– la prise en charge intégrale par l’Assurance maladie, sans avance de frais, du test de dépistage et de son analyse ;
– le recueil par la structure de coordination des dépistages des informations sur le diagnostic, le traitement et le devenir des femmes dont le test de dépistage est positif (qu’elles aient participé spontanément ou aient été invitées par courrier) ;
– un retour d’information vers les professionnels de santé et des actions d’amélioration des pratiques professionnelles (respect de l’intervalle entre deux tests, suivi des femmes ayant un résultat anormal, etc.) ;
– la mise en place d’actions spécifiques en direction de populations vulnérables et/ou très éloignées du système de santé (accompagnement au dépistage, médiation sanitaire, utilisation de l’autoprélèvement, unités mobiles, etc.) ;
– la diversification de l’offre de prélèvement en s’appuyant en particulier sur les médecins généralistes et les sages-femmes.
Compte-tenu des résultats de l’étude médico-économique réalisée par l’INCa en préalable au déploiement, la HAS évalue parallèlement la place, dans ce programme de dépistage, des tests de recherche de papillomavirus en première intention. Le programme en cours de déploiement prévoit d’ores et déjà l’utilisation d’un prélèvement en phase liquide, ce qui permettra, si ce type de test était retenu, d’opérer une transition, sans changement majeur pour la population concernée (hormis l’information naturellement).
Cancer colorectal : programme de dépistage efficace mais faible participation
La France dispose d’un programme de dépistage organisé du cancer colorectal efficace mais dont l’impact reste encore trop faible compte tenu du niveau de participation.
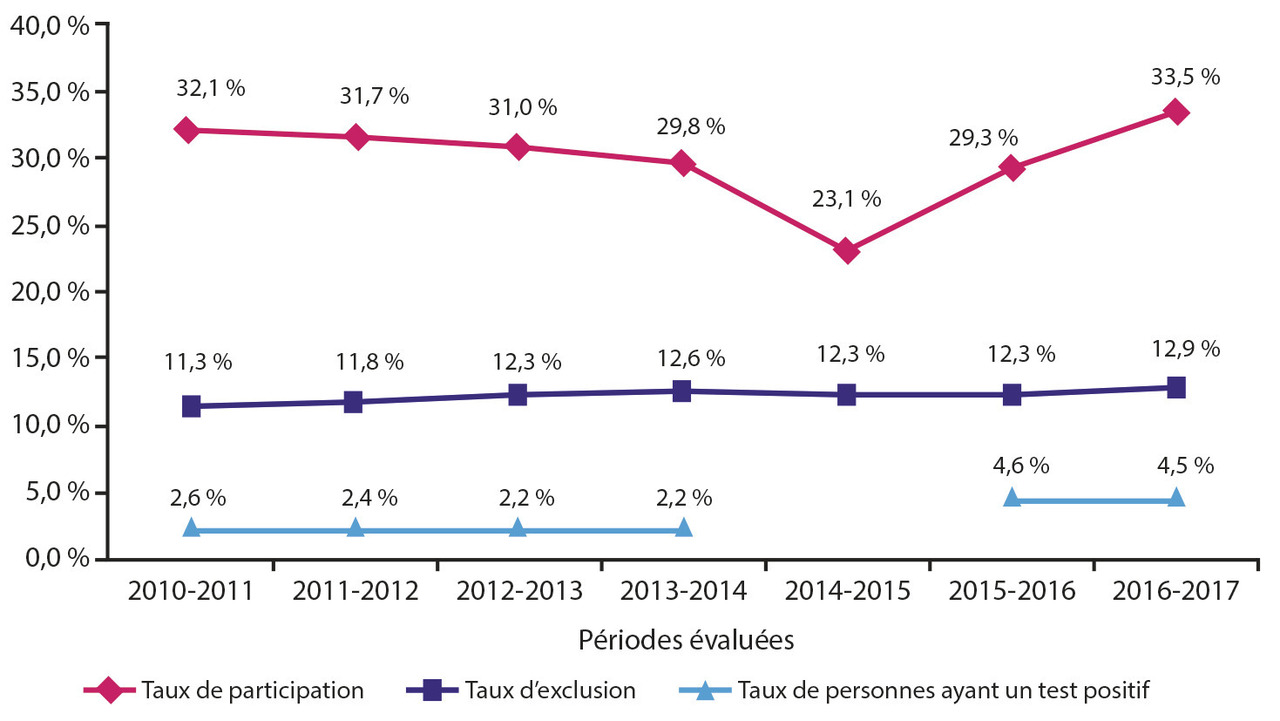
Le programme actuel, utilisant un test immunologique, est en place en France depuis avril 2015 et fait suite à un 1er programme utilisant un test au gaïac de recherche de sang occulte dans les selles, moins performant. La participation reste, comme avec le précédent test, en deçà de l’objectif défini au niveau européen (45 %) : 33,5 % de la population cible (Santé publique France, 2018) [v . figure ]. Même si le programme s’est redynamisé et si la participation est à la hausse dans les évaluations intermédiaires, le bénéfice du passage au test immunologique provient principalement, à ce jour, de la meilleure performance du test en termes de détection de cancers invasifs (2,9 ‰ vs 1,2 ‰) et d’adénomes avancés (12,1 ‰ vs 3,3 ‰).
La faiblesse de la participation réduit l’impact attendu en termes de santé publique. Elle pose la question d’éventuelles pertes de chance et remet en question la stratégie de remise des tests aux personnes concernées via le seul médecin traitant. Plusieurs voies d’amélioration de l’accès et du recours au test sont envisageables. Elles peuvent notamment porter sur :
La remise du test par le médecin traitant permet d’évaluer le niveau de risque de la personne, de lui apporter les informations nécessaires sur le dépistage et ses conséquences de manière ajustée à ses connaissances et ses représentations et de « prépositionner » le médecin dans son accompagnement si le test devait s’avérer positif. On sait cependant (données du Système national d’information inter-régimes de l’Assurance maladie) que seuls de l'ordre de 50 % des personnes de la tranche d’âge consultent leur médecin généraliste dans l’année.
L’organisation du programme de dépistage qui est fixée par arrêté ministériel a fait l’objet en mars 2018 d’une révision17 et prévoit de nouvelles modalités d’accès au kit de dépistage notamment via un envoi par courrier directement au domicile des personnes (pour celles qui n’auraient pas consulté leur médecin et auraient déjà réalisé antérieurement ce dépistage), via une remise en centres d’examens de santé (en l’absence de médecin traitant) ou via les gynécologues et gastroentérologues. Par ailleurs, des expérimentations sont menées par le Collège de médecine générale et le Collège national des généralistes enseignants en vue d’expérimenter et de consolider la formation et l’implication des médecins généralistes.
En complément de ce qui est déjà porté dans la révision du cahier des charges du programme et de ce qui a été expérimenté ou est en cours d’expérimentation, trois options, encore à évaluer, paraissent envisageables :
Le programme actuel, utilisant un test immunologique, est en place en France depuis avril 2015 et fait suite à un 1er programme utilisant un test au gaïac de recherche de sang occulte dans les selles, moins performant. La participation reste, comme avec le précédent test, en deçà de l’objectif défini au niveau européen (45 %) : 33,5 % de la population cible (Santé publique France, 2018) [
La faiblesse de la participation réduit l’impact attendu en termes de santé publique. Elle pose la question d’éventuelles pertes de chance et remet en question la stratégie de remise des tests aux personnes concernées via le seul médecin traitant. Plusieurs voies d’amélioration de l’accès et du recours au test sont envisageables. Elles peuvent notamment porter sur :
- la perception des personnes cibles vis-à-vis du test de dépistage et du cancer colorectal ;
- l’accès au dépistage (question du reste à charge lié à la consultation) ou aux suites, facilitation de l'accès par exemple pour un travailleur social;13, 14
- la facilitation ou l’incitation des professionnels à la remise du test, par exemple par la transmission aux médecins généralistes par les structures de gestion de la liste des patients éligibles au dépistage de sa patientèle n’ayant pas réalisé de test ;15, 16
- la diversification des modalités d’accès au test, directes ou indirectes.
La remise du test par le médecin traitant permet d’évaluer le niveau de risque de la personne, de lui apporter les informations nécessaires sur le dépistage et ses conséquences de manière ajustée à ses connaissances et ses représentations et de « prépositionner » le médecin dans son accompagnement si le test devait s’avérer positif. On sait cependant (données du Système national d’information inter-régimes de l’Assurance maladie) que seuls de l'ordre de 50 % des personnes de la tranche d’âge consultent leur médecin généraliste dans l’année.
L’organisation du programme de dépistage qui est fixée par arrêté ministériel a fait l’objet en mars 2018 d’une révision17 et prévoit de nouvelles modalités d’accès au kit de dépistage notamment via un envoi par courrier directement au domicile des personnes (pour celles qui n’auraient pas consulté leur médecin et auraient déjà réalisé antérieurement ce dépistage), via une remise en centres d’examens de santé (en l’absence de médecin traitant) ou via les gynécologues et gastroentérologues. Par ailleurs, des expérimentations sont menées par le Collège de médecine générale et le Collège national des généralistes enseignants en vue d’expérimenter et de consolider la formation et l’implication des médecins généralistes.
En complément de ce qui est déjà porté dans la révision du cahier des charges du programme et de ce qui a été expérimenté ou est en cours d’expérimentation, trois options, encore à évaluer, paraissent envisageables :
- effectuer un envoi direct du test au domicile des personnes concernées, lors de l’invitation. Cette modalité pourrait être déclinée avec ou sans ciblage préalable des personnes en fonction de leur niveau de risque (les Pays-Bas ont retenu par exemple avec succès un envoi sans ciblage) et pourrait permettre de préfigurer une approche d’invitation stratifiée selon le niveau de risque. On perçoit bien, néanmoins, la nécessité de tester l’apport d’un envoi direct sans phase médicale préalable ;
- ouvrir l’accès au test via le pharmacien. Les modalités précises (délivrance sur prescription du médecin, sur lettre d’invitation ou à l’aide d’un serveur d’éligibilité) sont à définir et à expérimenter. Dans le cas d’un positionnement du pharmacien en alternative vraie au médecin, les deux questions essentielles seront celles de l’orientation adaptée des personnes selon le niveau de risque et celle d’un non-désengagement significatif des médecins ;
- ouvrir l’accès à la commande du test via une interface internet. Cette modalité paraît envisageable, associée à une vérification de l’éligibilité, ce qui pourrait apporter un niveau de sécurité comparable à celui de l’envoi de test avec la seconde relance.
Références
1. Arrêté du 29 septembre 2006 relatif aux programmes de dépistage des cancers. www.legifrance.gouv.fr ou https://bit.ly/2BfRXaW
2. Concertation citoyenne et scientifique. Ensemble améliorons le dépistage du cancer du sein. http://www.concertation-depistage.fr/
3. Plan d’action pour la rénovation du dépistage organisé du cancer du sein. http://solidarites-sante.gouv.fr ou https://bit.ly/2SIz5sk
4. Livret d’information sur le dépistage organisé du cancer du sein « S’informer et décider » www.e-cancer.fr ou https://bit.ly/2UGoGze
5. https://cancersdusein.e-cancer.fr/
6. Indication de la tomosynthèse dans une stratégie de détection précoce des cancers du sein. Collection appui à la décision, Boulogne-Billancourt : INCa, 2015.
7. Haute Autorité de santé. État des lieux et recommandations pour le dépistage du cancer du col de l’utérus en France : argumentaire. Recommandations en santé publique, HAS 2010. www.has-sante.fr ou https://bit.ly/2rBsNit
8. Cowppli-Bony A, Uhry Z, Remontet L, et al. Survie des personnes atteintes de cancer en France métropolitaine, 1989-2013. Partie 1 – Tumeurs solides. Saint-Maurice : InVS ; Boulogne-Billancourt : INCa, 2016. www.e-cancer.fr ou https://bit.ly/2GdEQN7
9. Plan cancer 2014-2019. Guérir et prévenir les cancers : donnons les mêmes chances à tous, partout en France. Paris : ministère des Affaires sociales et de la Santé, ministère de l’Enseignement supérieur et de la Recherche ; 2014. 150 p. www.e-cancer.fr ou https://bit.ly/2GgbFcn
10. Arrêté du 4 mai 2018 relatif à l’organisation du dépistage organisé du cancer du col de l’utérus. www.legifrance.gouv.fr ou https://bit.ly/2UHzdtL
11. Barré S, Massetti M, Leleu H, et al. Caractérisation des femmes ne réalisant pas de dépistage du cancer du col de l’utérus par frottis cervico-utérin en France. Bull Epidemiol Hebd 2017;(2-3):39-47. http://invs.santepubliquefrance.fr ou https://bit.ly/2zZwqU2
12. Généralisation du dépistage du cancer du col de l’utérus / étude médico- économique / Phase 2. Boulogne-Billancourt : INCa, 2016. www.e-cancer.fr ou https://bit.ly/2EtQD8l
13. Guillaume E, Dejardin O, Bouvier V, et al. Patient navigation to reduce social inequalities in colorectal cancer screening participation: a cluster randomized controlled trial. Prev Med 2017;103:76-83.
14. De Mil R, Guillaume E, Guittet L, et al. Cost-effectiveness analysis of a navigation program for colorectal cancer screening to reduce social health inequalities: a French cluster randomized controlled trial. Value in Health 2018;21:685-691.
15. Sicsic j, Krucien N, Franc C. What are GPs’ preferences for financial and non-financial incentives incancer screening? Evidence for breast, cervical, and colorectal cancers. Soc Sci Med 2016;167:1-127.
16. Rat C, Pogu C, Le Donné D, et al. Effect of physician notification regarding nonadherence to colorectal cancer screening on patient participation in fecal immunochemical test cancer screening. A randomized clinical trial. JAMA 2017;318:816-24.
17. Arrêté du 19 mars 2018 modifiant l’arrêté du 29 septembre 2006 relatif aux programmes de dépistage organisé des cancers et portant modification du cahier des charges du dépistage organisé du cancer colorectal. www.legifrance.gouv.fr ou https://bit.ly/2RVB2Sg
2. Concertation citoyenne et scientifique. Ensemble améliorons le dépistage du cancer du sein. http://www.concertation-depistage.fr/
3. Plan d’action pour la rénovation du dépistage organisé du cancer du sein. http://solidarites-sante.gouv.fr ou https://bit.ly/2SIz5sk
4. Livret d’information sur le dépistage organisé du cancer du sein « S’informer et décider » www.e-cancer.fr ou https://bit.ly/2UGoGze
5. https://cancersdusein.e-cancer.fr/
6. Indication de la tomosynthèse dans une stratégie de détection précoce des cancers du sein. Collection appui à la décision, Boulogne-Billancourt : INCa, 2015.
7. Haute Autorité de santé. État des lieux et recommandations pour le dépistage du cancer du col de l’utérus en France : argumentaire. Recommandations en santé publique, HAS 2010. www.has-sante.fr ou https://bit.ly/2rBsNit
8. Cowppli-Bony A, Uhry Z, Remontet L, et al. Survie des personnes atteintes de cancer en France métropolitaine, 1989-2013. Partie 1 – Tumeurs solides. Saint-Maurice : InVS ; Boulogne-Billancourt : INCa, 2016. www.e-cancer.fr ou https://bit.ly/2GdEQN7
9. Plan cancer 2014-2019. Guérir et prévenir les cancers : donnons les mêmes chances à tous, partout en France. Paris : ministère des Affaires sociales et de la Santé, ministère de l’Enseignement supérieur et de la Recherche ; 2014. 150 p. www.e-cancer.fr ou https://bit.ly/2GgbFcn
10. Arrêté du 4 mai 2018 relatif à l’organisation du dépistage organisé du cancer du col de l’utérus. www.legifrance.gouv.fr ou https://bit.ly/2UHzdtL
11. Barré S, Massetti M, Leleu H, et al. Caractérisation des femmes ne réalisant pas de dépistage du cancer du col de l’utérus par frottis cervico-utérin en France. Bull Epidemiol Hebd 2017;(2-3):39-47. http://invs.santepubliquefrance.fr ou https://bit.ly/2zZwqU2
12. Généralisation du dépistage du cancer du col de l’utérus / étude médico- économique / Phase 2. Boulogne-Billancourt : INCa, 2016. www.e-cancer.fr ou https://bit.ly/2EtQD8l
13. Guillaume E, Dejardin O, Bouvier V, et al. Patient navigation to reduce social inequalities in colorectal cancer screening participation: a cluster randomized controlled trial. Prev Med 2017;103:76-83.
14. De Mil R, Guillaume E, Guittet L, et al. Cost-effectiveness analysis of a navigation program for colorectal cancer screening to reduce social health inequalities: a French cluster randomized controlled trial. Value in Health 2018;21:685-691.
15. Sicsic j, Krucien N, Franc C. What are GPs’ preferences for financial and non-financial incentives incancer screening? Evidence for breast, cervical, and colorectal cancers. Soc Sci Med 2016;167:1-127.
16. Rat C, Pogu C, Le Donné D, et al. Effect of physician notification regarding nonadherence to colorectal cancer screening on patient participation in fecal immunochemical test cancer screening. A randomized clinical trial. JAMA 2017;318:816-24.
17. Arrêté du 19 mars 2018 modifiant l’arrêté du 29 septembre 2006 relatif aux programmes de dépistage organisé des cancers et portant modification du cahier des charges du dépistage organisé du cancer colorectal. www.legifrance.gouv.fr ou https://bit.ly/2RVB2Sg