Au cours de la bronchopneumopathie chronique obstructive, les corticostéroïdes ne sont pas utilisés en première intention. La corticothérapie inhalée est indiquée en cas d’exacerbations fréquentes, pour en diminuer la fréquence, en association à un bronchodilatateur inhalé de type bêta-2-agoniste de longue durée d’action, voire dans le cadre d’une triple thérapie inhalée en association avec un anticholinergique de longue durée d’action. La corticothérapie orale est réservée au traitement des exacerbations, en cures courtes et de façon non systématique, car son niveau de preuve dans cette indication est très faible. Il n’existe aucune indication de corticothérapie orale au long cours dans la BPCO.
Les corticostéroïdes, qu’ils soient administrés sous forme inhalée ou par voie orale, ne sont pas utilisés en première intention dans la bronchopneumopathie chronique obstructive (BPCO). Ils ont des indications spécifiques.
Corticothérapie inhalée en cas d’exacerbations fréquentes
Les corticostéroïdes inhalés (CSI) ne constituent pas le traitement de première intention de la BPCO à l’état stable. Ils sont à considérer uniquement en cas d’exacerbations fréquentes (au moins deux par an ou au moins une exacerbation sévère nécessitant une hospitalisation) sous traitement par au moins un bronchodilatateur inhalé de type bêta-2-agoniste de longue durée d’action (LABA) ou anticholinergique de longue durée d’action (LAMA) pris de façon optimale. Quand ils sont utilisés, les CSI doivent l’être en association avec un LABA, potentiellement associé à un LAMA dans le cadre d’une trithérapie inhalée. Il n’y a pas de place pour un traitement de la BPCO stable par CSI seul.
Diminution des exacerbations en association aux LABA, voire aux LAMA
De façon globale, les études randomisées démontrent un bénéfice de l’association LABA-CSI par rapport au LABA seul en matière de diminution des exacerbations. Concernant la comparaison de l’association LABA-LAMA à l’association LABA-CSI, les résultats des études doivent être interprétés avec prudence, car la plupart des patients étaient sous CSI à l’inclusion, avec donc potentiellement un effet sevrage en CSI pouvant favoriser le bras LABA-CSI. En cas de persistance d’exacerbations fréquentes sous bithérapie associant deux bronchodilatateurs (LABA-LAMA) ou de persistance de dyspnée significative sous une association de LABA-CSI, une triple thérapie associant CSI, LABA et LAMA peut être proposée, avec actuellement la possibilité de dispositifs uniques de trithérapie inhalée, pouvant améliorer l’observance et la persistance du traitement.1
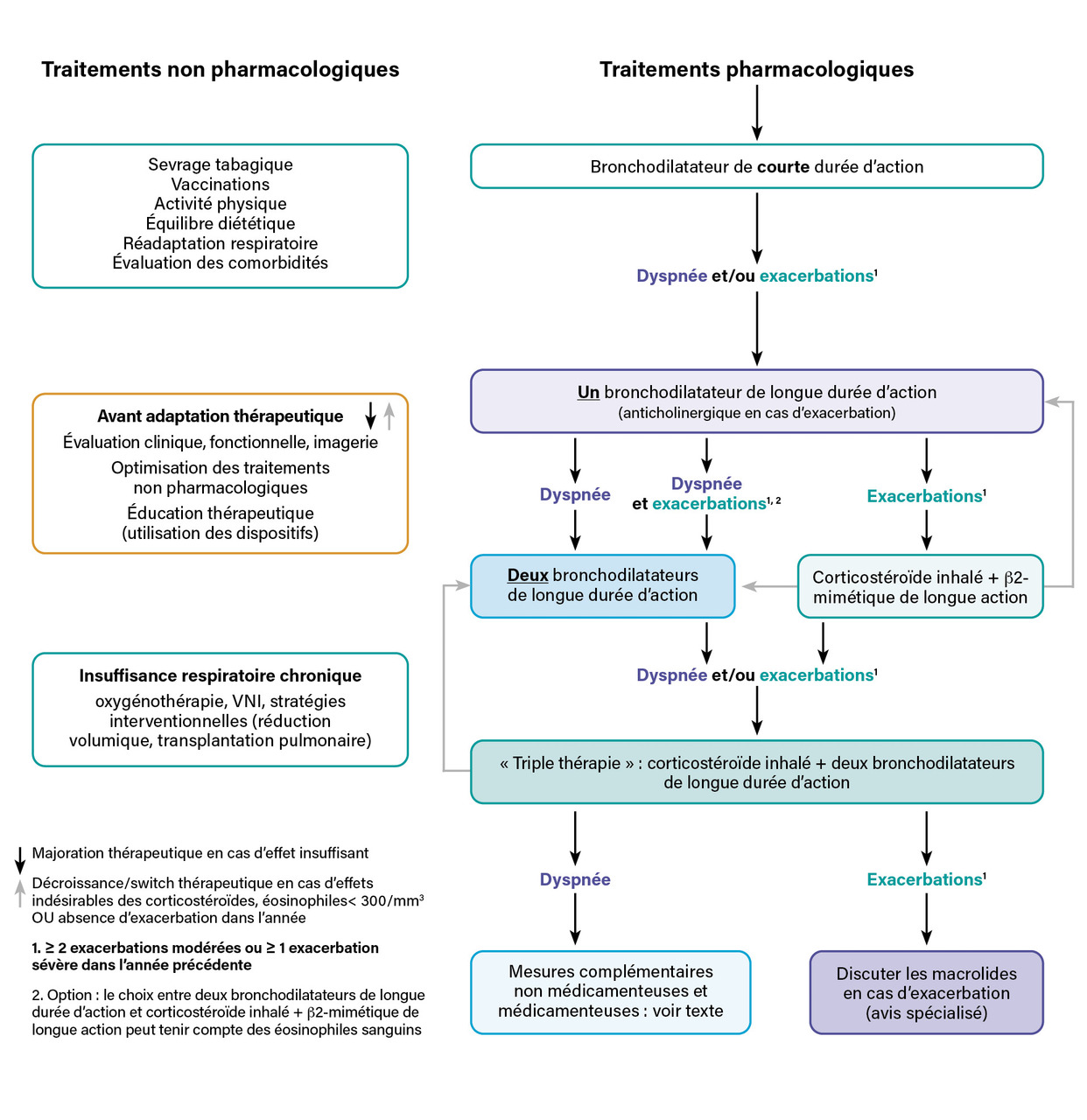
De nombreuses études ont été publiées ces dernières années évaluant la trithérapie inhalée LABALAMA-CSI en comparaison avec une bithérapie LABA-LAMA ou LABA-CSI démontrant une diminution du risque d’exacerbation, une amélioration de la fonction respiratoire, de la qualité de vie et de la dyspnée, mais avec une amplitude d’effet modeste. Comme pour les études comparant les bithérapies entre elles, la plupart des patients inclus dans ces études avaient un traitement par CSI à l’entrée, avec un effet potentiel de sevrage en CSI. Il faut être très prudent sur l’interprétation des données d’analyses post hoc montrant un bénéfice de la triple thérapie sur la mortalité.2 Il est important de souligner l’importance des mesures non pharmacologiques qui doivent être associées dans la prise en charge globale de la BPCO à l’état stable, incluant le sevrage tabagique, la vaccination (grippe, pneumocoque, Covid et VRS), l’activité physique, la réadaptation respiratoire et la prise en charge nutritionnelle (figure ). L’éducation thérapeutique intégrant l’évaluation de l’efficacité de la prise des traitements inhalés est un élément clé. Enfin, le dépistage et le traitement des comorbidités, notamment cardiovasculaires et métaboliques, très fréquentes au cours de la BPCO, sont des éléments majeurs de la prise en charge globale.
De nombreuses études ont été publiées ces dernières années évaluant la trithérapie inhalée LABALAMA-CSI en comparaison avec une bithérapie LABA-LAMA ou LABA-CSI démontrant une diminution du risque d’exacerbation, une amélioration de la fonction respiratoire, de la qualité de vie et de la dyspnée, mais avec une amplitude d’effet modeste. Comme pour les études comparant les bithérapies entre elles, la plupart des patients inclus dans ces études avaient un traitement par CSI à l’entrée, avec un effet potentiel de sevrage en CSI. Il faut être très prudent sur l’interprétation des données d’analyses post hoc montrant un bénéfice de la triple thérapie sur la mortalité.2 Il est important de souligner l’importance des mesures non pharmacologiques qui doivent être associées dans la prise en charge globale de la BPCO à l’état stable, incluant le sevrage tabagique, la vaccination (grippe, pneumocoque, Covid et VRS), l’activité physique, la réadaptation respiratoire et la prise en charge nutritionnelle (
Le taux d’éosinophiles sanguins peut-il être un facteur prédictif ?
Avant d’instaurer un traitement par CSI, une analyse des symptômes persistants doit être réalisée de façon rigoureuse pour déterminer les mécanismes impliqués dans les exacerbations fréquentes, la dyspnée et/ou la bronchite chronique. Parmi les éléments importants à évaluer, il faut rechercher des bronchectasies associées, réaliser une évaluation microbiologique (notamment à la recherche de Pseudomonas aeruginosa, mycobactéries et Aspergillus), rechercher d’éventuelles comorbidités cardiovasculaires, métaboliques et un carcinome bronchique.
Des données récentes suggèrent que le taux d’éosinophiles sanguins pourrait être un facteur prédictif de réponse aux CSI en matière de réduction des exacerbations. Il faut être très prudent sur ces données ; en effet, le taux d’éosinophiles sanguins est variable dans le temps, les valeurs seuils proposées par certaines sociétés savantes de 300/mm3, voire 100/mm3, sont dans les limites de la normale, et la plupart des données disponibles sont issues d’analyses secondaires ou post hoc, avec un faible niveau de preuve.2
Le taux d’éosinophiles sanguins est un élément secondaire et non déterminant pour le choix de débuter un CSI.
Un taux d’éosinophiles sanguins inférieur à 300/mm3 dans un contexte d’absence d’exacerbation dans l’année précédente peut cependant permettre d’envisager un sevrage en CSI, avec une désescalade vers un traitement par bronchodilatateur(s) inhalé(s) uniquement.3
Des données récentes suggèrent que le taux d’éosinophiles sanguins pourrait être un facteur prédictif de réponse aux CSI en matière de réduction des exacerbations. Il faut être très prudent sur ces données ; en effet, le taux d’éosinophiles sanguins est variable dans le temps, les valeurs seuils proposées par certaines sociétés savantes de 300/mm3, voire 100/mm3, sont dans les limites de la normale, et la plupart des données disponibles sont issues d’analyses secondaires ou post hoc, avec un faible niveau de preuve.2
Le taux d’éosinophiles sanguins est un élément secondaire et non déterminant pour le choix de débuter un CSI.
Un taux d’éosinophiles sanguins inférieur à 300/mm3 dans un contexte d’absence d’exacerbation dans l’année précédente peut cependant permettre d’envisager un sevrage en CSI, avec une désescalade vers un traitement par bronchodilatateur(s) inhalé(s) uniquement.3
Prévenir les effets indésirables
Les CSI sont susceptibles d’entraîner des effets indésirables, qu’il convient de connaître, rechercher et si possible prévenir.
Les plus fréquents sont loco-régionaux, incluant des mycoses buccales et une dysphonie. Un rinçage de la bouche doit être réalisé systématiquement après chaque utilisation des CSI.
L’utilisation des CSI est associée, dans la plupart des études randomisées, à un risque accru de pneumonie.
Les autres effets indésirables identifiés dans les études de cohorte et cas contrôles et dans les revues systématiques identifient également un risque accru de tuberculose, d’infection par une mycobactérie atypique, de diabète, de fracture osseuse et d’ostéoporose.
Compte tenu de l’efficacité modeste des CSI au cours de la BPCO à l’état stable et des effets indésirables potentiels, la balance bénéfice-risque des CSI au long cours doit donc être rigoureusement évaluée.
Les plus fréquents sont loco-régionaux, incluant des mycoses buccales et une dysphonie. Un rinçage de la bouche doit être réalisé systématiquement après chaque utilisation des CSI.
L’utilisation des CSI est associée, dans la plupart des études randomisées, à un risque accru de pneumonie.
Les autres effets indésirables identifiés dans les études de cohorte et cas contrôles et dans les revues systématiques identifient également un risque accru de tuberculose, d’infection par une mycobactérie atypique, de diabète, de fracture osseuse et d’ostéoporose.
Compte tenu de l’efficacité modeste des CSI au cours de la BPCO à l’état stable et des effets indésirables potentiels, la balance bénéfice-risque des CSI au long cours doit donc être rigoureusement évaluée.
Place des corticostéroïdes inhalés selon la SPLF et GOLD
La Société de pneumologie de langue française (SPLF) a réactualisé en 2021 ses propositions de prise en charge pharmacologique de la BPCO à l’état stable.3 Les CSI ne doivent jamais être utilisés seuls et sont clairement positionnés en deuxième ou troisième intention, avec une stratégie de traitement par palier reposant sur l’évaluation clinique de la réponse au traitement, fondée essentiellement sur les exacerbations et la dyspnée (figure ). Les propositions de la SPLF n’ont pas retenu le taux d’éosinophiles sanguins comme élément à considérer pour débuter un CSI, mais suggèrent d’utiliser ce critère en seconde intention dans le cadre de la discussion de l’arrêt des CSI chez un patient bien contrôlé en matière d’exacerbations.
Les recommandations internationales GOLD (Global Initiative for Chronic Obstructive Lung Disease) 20242 proposent de privilégier l’utilisation des CSI dans le cadre d’une triple thérapie inhalée (LAMA-LABA -CSI) en cas d’exacerbations fréquentes (au moins deux dans l’année précédente ou au moins une nécessitant une hospitalisation) et un taux sanguin d’éosinophiles d’au moins 300/mm3 ou en cas de persistance d’exacerbations fréquentes sous bithérapie LABA-LAMA et un taux d’éosinophiles d’au moins 100/mm2. En revanche, des antécédents de pneumonie, un taux d’éosinophiles inférieur à 100/mm3 et des antécédents d’infection à mycobactéries plaident contre l’utilisation des CSI.
Les recommandations internationales GOLD (Global Initiative for Chronic Obstructive Lung Disease) 20242 proposent de privilégier l’utilisation des CSI dans le cadre d’une triple thérapie inhalée (LAMA-LABA -CSI) en cas d’exacerbations fréquentes (au moins deux dans l’année précédente ou au moins une nécessitant une hospitalisation) et un taux sanguin d’éosinophiles d’au moins 300/mm3 ou en cas de persistance d’exacerbations fréquentes sous bithérapie LABA-LAMA et un taux d’éosinophiles d’au moins 100/mm2. En revanche, des antécédents de pneumonie, un taux d’éosinophiles inférieur à 100/mm3 et des antécédents d’infection à mycobactéries plaident contre l’utilisation des CSI.
Corticothérapie orale non indiquée au long cours
La seule indication de la corticothérapie systémique dans la BPCO concerne le traitement des exacerbations de BPCO. Il n’y a aucune indication de corticothérapie systémique au long cours dans la BPCO.
Dans les exacerbations sévères nécessitant une hospitalisation, les bénéfices démontrés de la corticothérapie systémique sont l’amélioration du volume expiratoire maximal à la première seconde (VEMS) et de la pression partielle d’oxygène artériel (PaO2) dans les jours suivant l’administration, une durée d’hospitalisation plus courte et une diminution du taux de rechute dans le mois suivant l’administration. Le niveau de preuve est cependant assez faible. Une étude randomisée multicentrique française évaluant l’efficacité de la corticothérapie orale en cas d’exacerbation de BPCO nécessitant une hospitalisation est en cours ; l’objectif est notamment d’estimer l’intérêt du dosage de l’éosinophilie sanguine comme facteur prédictif de réponse au traitement.4
Il n’a pas été démontré d’effet de la corticothérapie systémique sur la mortalité.
Le principal effet indésirable identifié dans les études est une hyperglycémie.
Les recommandations de la SPLF précisent que l’utilisation de la corticothérapie systémique n’est pas systématique mais constitue une option en cas d’absence de réponse au traitement optimal.3,4 Quand elle est proposée, la corticothérapie systémique doit être réalisée en cure courte (cinq jours), en privilégiant la voie orale, à une posologie de 0,5 mg/kg/j avec une dose maximale de 40 mg/j d’équivalent prednisone.5,6
Pour les exacerbations de sévérité modérée ne justifiant pas une hospitalisation, peu d’études sont disponibles. Par analogie, la SPLF recommande une utilisation identique, en proposant la corticothérapie systémique en seconde intention en cas de non-amélioration sous traitement optimal, également en cure courte (cinq jours) en privilégiant la voie orale, à une posologie de 0,5 mg/kg/j avec une dose maximale de 40 mg/j d’équivalent prednisone.5,6 Une étude française récente n’a pas montré de bénéfice de la corticothérapie orale en cas d’exacerbation modérée.7
Enfin, il faut souligner le risque de la répétition de cures courtes de corticothérapie systémique, pouvant conduire à des effets indésirables identiques à ceux d’une corticothérapie orale au long cours.
Dans les exacerbations sévères nécessitant une hospitalisation, les bénéfices démontrés de la corticothérapie systémique sont l’amélioration du volume expiratoire maximal à la première seconde (VEMS) et de la pression partielle d’oxygène artériel (PaO2) dans les jours suivant l’administration, une durée d’hospitalisation plus courte et une diminution du taux de rechute dans le mois suivant l’administration. Le niveau de preuve est cependant assez faible. Une étude randomisée multicentrique française évaluant l’efficacité de la corticothérapie orale en cas d’exacerbation de BPCO nécessitant une hospitalisation est en cours ; l’objectif est notamment d’estimer l’intérêt du dosage de l’éosinophilie sanguine comme facteur prédictif de réponse au traitement.4
Il n’a pas été démontré d’effet de la corticothérapie systémique sur la mortalité.
Le principal effet indésirable identifié dans les études est une hyperglycémie.
Les recommandations de la SPLF précisent que l’utilisation de la corticothérapie systémique n’est pas systématique mais constitue une option en cas d’absence de réponse au traitement optimal.3,4 Quand elle est proposée, la corticothérapie systémique doit être réalisée en cure courte (cinq jours), en privilégiant la voie orale, à une posologie de 0,5 mg/kg/j avec une dose maximale de 40 mg/j d’équivalent prednisone.5,6
Pour les exacerbations de sévérité modérée ne justifiant pas une hospitalisation, peu d’études sont disponibles. Par analogie, la SPLF recommande une utilisation identique, en proposant la corticothérapie systémique en seconde intention en cas de non-amélioration sous traitement optimal, également en cure courte (cinq jours) en privilégiant la voie orale, à une posologie de 0,5 mg/kg/j avec une dose maximale de 40 mg/j d’équivalent prednisone.5,6 Une étude française récente n’a pas montré de bénéfice de la corticothérapie orale en cas d’exacerbation modérée.7
Enfin, il faut souligner le risque de la répétition de cures courtes de corticothérapie systémique, pouvant conduire à des effets indésirables identiques à ceux d’une corticothérapie orale au long cours.
Références
1. Deslee G, Fabry-Vendrand C, Poccardi N, Thabut G, Eteve Pitsaer C, Coriat A, et al. Use and persistence of single and multiple inhaler triple therapy prescribed for patients with COPD in France: A retrospective study on THIN database (OPTI study). BMJ Open Respir Res 2023;10(1):e001585.
2. Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease. 2024 Report. https://goldcopd.org/
3. Zysman M, Ribeiro Baptista B, Soumagne T, Marques da Silva V, Martin C, de Menonville CT, et al. Optimisation du traitement médicamenteux des patients atteints de BPCO en état stable. Position de la Société de pneumologie de langue française. Actualisation 2021. Rev Mal Respir 2021;38(5):539-61.
4. Suehs CM, Zysman M, Chenivesse C, Burgel PR, Couturaud F, Deslee G, et al. Prioritising outcomes for evaluating eosinophil-guided corticosteroid therapy among patients with acute COPD exacerbations requiring hospitalisation: A Delphi consensus study. BMJ Open 2020;10(7):e035811.
5. Jouneau S, Dres M, Guerder A, Bele N, Bellocq A, Bernady A, et al. Prise en charge des exacerbations aiguës de la bronchopneumopathie chronique obstructive. Recommandations de la Société de pneumologie de langue française sur les exacerbations de la BPCO. Rev Mal Respir 2017;34(4):282-322.
6. Mal H. Place des corticoïdes systémiques dans les exacerbations de BPCO. Rev Mal Respir 2017;34(4):403-7.
7. Thebault JL, Roche N, Abdoul H, Lorenzo A, Similowski T, Ghasarossian C. Efficacy and safety of oral corticosteroids to treat outpatients with acute exacerbations of COPD in primary care: A multicentre pragmatic randomised controlled study. ERJ Open Res 2023;9(5):00057-2023.
2. Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease. 2024 Report. https://goldcopd.org/
3. Zysman M, Ribeiro Baptista B, Soumagne T, Marques da Silva V, Martin C, de Menonville CT, et al. Optimisation du traitement médicamenteux des patients atteints de BPCO en état stable. Position de la Société de pneumologie de langue française. Actualisation 2021. Rev Mal Respir 2021;38(5):539-61.
4. Suehs CM, Zysman M, Chenivesse C, Burgel PR, Couturaud F, Deslee G, et al. Prioritising outcomes for evaluating eosinophil-guided corticosteroid therapy among patients with acute COPD exacerbations requiring hospitalisation: A Delphi consensus study. BMJ Open 2020;10(7):e035811.
5. Jouneau S, Dres M, Guerder A, Bele N, Bellocq A, Bernady A, et al. Prise en charge des exacerbations aiguës de la bronchopneumopathie chronique obstructive. Recommandations de la Société de pneumologie de langue française sur les exacerbations de la BPCO. Rev Mal Respir 2017;34(4):282-322.
6. Mal H. Place des corticoïdes systémiques dans les exacerbations de BPCO. Rev Mal Respir 2017;34(4):403-7.
7. Thebault JL, Roche N, Abdoul H, Lorenzo A, Similowski T, Ghasarossian C. Efficacy and safety of oral corticosteroids to treat outpatients with acute exacerbations of COPD in primary care: A multicentre pragmatic randomised controlled study. ERJ Open Res 2023;9(5):00057-2023.