Les réactions transfusionnelles sont les événements indésirables liés aux transfusions sanguines se produisant chez les receveurs. Elles peuvent passer inaperçues ou à l’extrême être fatales. Elles peuvent survenir pendant ou dans les heures qui suivent la transfusion (réactions immédiates aiguës) ou au décours de celle-ci après plusieurs jours ou semaines (réactions retardées). Leur déclaration est obligatoire, et l’évalution de ces effets indésirables chez les receveurs est prise en charge par le dispositif d’hémovigilance qui est réglementairement définie en France par la loi n° 93-5 du 4 janvier 1993.1 Cela permet de définir un niveau de gravité (de 1 [non sévère] à 4 [décès]) et 5 niveaux d’imputabilité (de 0 [exclusion] à 3 [certitude] avec un niveau non évaluable).
Les réactions transfusionnelles peuvent être de mécanismes immunologiques ou non immunologiques et leur diagnostic est parfois difficile car il n’existe pas de symptomatologie spécifique (fig. 1). Les signes cliniques les plus fréquents sont la fièvre, les frissons, une urticaire et un prurit. Certains disparaissent spontanément ou avec un traitement symptomatique. Toutefois, d’autres, comme une hypotension, voire un état de choc, une hémoglo- binurie ou une détresse respiratoire, témoignent d’une réaction sévère. Qu’elles soient immédiates ou retardées, en fonction de leur mécanisme, on distingue les réactions transfusionnelles de type immunologique, infectieux ou de surcharge.
Les réactions transfusionnelles peuvent être de mécanismes immunologiques ou non immunologiques et leur diagnostic est parfois difficile car il n’existe pas de symptomatologie spécifique (fig. 1). Les signes cliniques les plus fréquents sont la fièvre, les frissons, une urticaire et un prurit. Certains disparaissent spontanément ou avec un traitement symptomatique. Toutefois, d’autres, comme une hypotension, voire un état de choc, une hémoglo- binurie ou une détresse respiratoire, témoignent d’une réaction sévère. Qu’elles soient immédiates ou retardées, en fonction de leur mécanisme, on distingue les réactions transfusionnelles de type immunologique, infectieux ou de surcharge.
Épidémiologie
Certaines réactions sont très fréquentes (réactions allergiques minimes, réaction fébrile non hémolytique) alors que d’autres sont plus rares (anaphylaxie, choc hémolytique ou septique). L’incidence des événements indésirables chez le receveur est évaluée pour 2016 à 216,2 pour 100 000 produits sanguins labiles transfusés.2 Les trois premiers diagnostics ayant un niveau d’imputabilité de 1 à 3 déclarés sont l’allo-immunisation (85/100 000), les réactions fébriles non hémolytiques (56/100 000) et l’allergie (33/100 000).
La mortalité est le plus souvent le fait d’œdèmes aigus du poumon de surcharge, de syndromes respiratoires aigus post-transfusionnels (transfusion-related acute lung injury [TRALI]), de chocs infectieux ou d’un décès à plus long terme lié à la transmission de pathologies infectieuses. En 2016,2 les décès ont été liés à 2 œdèmes pulmonaires de surcharge, 2 allergies, et 1 infection bactérienne transmise par transfusion. Toutefois, les mesures de prévention mises en œuvre depuis de nombreuses années tendent à réduire de plus en plus leur survenue et notamment les formes sévères.
La mortalité est le plus souvent le fait d’œdèmes aigus du poumon de surcharge, de syndromes respiratoires aigus post-transfusionnels (transfusion-related acute lung injury [TRALI]), de chocs infectieux ou d’un décès à plus long terme lié à la transmission de pathologies infectieuses. En 2016,2 les décès ont été liés à 2 œdèmes pulmonaires de surcharge, 2 allergies, et 1 infection bactérienne transmise par transfusion. Toutefois, les mesures de prévention mises en œuvre depuis de nombreuses années tendent à réduire de plus en plus leur survenue et notamment les formes sévères.
Réactions transfusionnelles immédiates
Causes immunologiques
Hémolyse aiguë
Elle peut être le fait d’un conflit antigènes-anticorps aboutissant à la destruction intravasculaire et/ou intratissulaire du globule rouge transfusé. Il faut cependant signaler qu’il existe aussi des destructions non immunologiques des hématies transfusées par mécanismes mécaniques, osmotiques ou thermiques. Les anticorps impliqués peuvent être ceux du système ABO (les plus graves) ou d’autres systèmes Rh, Kell, Duffy, Kidd, MNS, etc. Les manisfestations cliniques peuvent être plus ou moins bruyantes, allant d’une simple fièvre à un choc hémolytique avec douleur lombaire, hémoglobinurie et coagulation intravasculaire dissséminée. Le diagnostic repose sur la mise en évidence de stigmates d’hémolyse (haptoglobine, lacticodéshydrogénase, bilirubine…), d’une sensibilisation des hématies in vivo par le test direct à l’antiglobuline (test de Coombs direct) et sur l’identification de l’anticorps coupable par examen direct à l’antiglobuline. La prévention repose sur des règles strictes d’identitovigilance, de respect de la compatibilité des groupes sanguins et sur la performance de la détection des anticorps par la recherche d’agglutinines irrégulières avant la transfusion.Réaction fébrile non hémolytique
Elle est le plus souvent liée à l’injection de cytokines présentes dans les produits, notamment les plaquettes qui relarguent ces médiateurs dans le milieu durant leur conservation. Elle peut être aussi le fait d’un conflit antigène-anticorps dans le système HLA générant la synthèse de cytokines. Il s’agit d’un diagnostic d’exclusion qui doit être retenu après avoir éliminé toutes les autres causes de fièvre.Allergie aux protéines humaines
Les réactions sont plus ou moins intenses, pouvant aller du simple prurit au choc anaphylactique. Une des causes est le fait du déficit en immunoglobulines (Ig) de type A chez le receveur qui synthétise un anti-IgA, pouvant aboutir à une réaction sévère. La prévention des accidents allergiques sévères impose un recours à des produits (globules rouges et plaquettes) déplasmatisés.Transfusion-related acute lung injury (TRALI)
Il s’agit d’un œdème pulmonaire lésionnel lié le plus souvent à l’injection d’anticorps anti-leucocytaires (HLA ou HNA) présents dans le plasma des donneurs qui peuvent activer les leucocytes qui altèrent la paroi alvéolocapillaire. À côté de ce mécanisme immunologique, des conditions prédisposantes chez le patient sont possibles comme une infection, une chirurgie récente (transplantation) ou une inflammation importante. Il survient durant ou dans les 6 heures qui suivent une transfusion et se manifeste par une dyspnée, une hypoxémie, une hypotension et parfois une fièvre. Une partie de la prévention des TRALI immunologiques repose sur la détection des anticorps HLA de classes I et II chez les femmes non nullipares dont les dons sont destinés à préparer des plasmas thérapeutiques et des plaquettes.Causes infectieuses
Une contamination bactérienne peut causer un choc septique lié à l’injection directe des bactéries ou des endotoxines relarguées dans le produit, notamment dans les concentrés de plaquettes qui sont conservés à température ambiante, ce qui en facilite la pousse. La prévention repose sur des règles strictes de sélection des donneurs (incluant l’information post-don), de décontamination cutanée au moment du don et par la mise en place d’un procédé d’atténuation des pathogènes pour les plaquettes. Bien que plus rare du fait d’une conservation entre 2 et 6 °C, le risque persiste pour certains germes (Yersinia, Pseudomonas, Serratia, Acinetobacter) avec les concentrés de globules rouges.
Accidents de surcharge
Transfusion-associated circulatory overload (TACO)
Il survient quand le volume transfusé cause une hypervolémie responsable d’une surchage qui aboutit à un œdème de surcharge. Il peut survenir au cours ou au décours de la transfusion et se manifeste par une dyspnée et une hypoxie souvent chez le sujet âgé, l’enfant ou l’insuffisant cardiaque (matérialisation par les signes radiologiques, électriques et biologiques). La prévention repose dans les situations à risque, sur une adaptation de la quantité transfusée (en dehors de l’urgence, il est recommandé de ne prescrire qu’un seul concentré de globules rouges à la fois) et le réglage d’un débit adapté. Ce risque impose une surveillance particulièrement rapprochée qui doit se poursuivre lors du retour au domicile en cas de transfusion en hôpital de jour.Risque lié à une transfusion massive
L’apport de nombreuses unités de sang dans un temps très court (plus de 10 concentrés de globules rouges en moins de 24 heures ou le remplacement de la moitié de la masse sanguine en moins de 3 heures)3 peut être responsable d’hypothermie en cas de non-réchauffement des unités, de surchage en citrate avec risque d’hypocalcémie, voire d’hyperkaliémie chez les nouveau-nés ou les sujets en insuffisance rénale notamment.Réactions transfusionnelles retardées
Causes immunologiques
Hémolyse retardée
Les hémolyses peuvent être retardées et survenir même 2 à 3 semaines après l’épisode transfusionnel chez un patient initialement allo-immunisé et dont l’anticorps, du fait d’un taux très faible, n’a pas été détecté à la recherche d’agglutinines irrégulières. Cela est le plus souvent le fait d’une réactivation d’un anticorps lié à une immunisation préalable. Une attention particulière doit être apportée chez le drépanocytaire où ces hémolyses sont particulièrement sévères et où dans un tiers des cas l’anticorps ne peut être mis en évidence.Allo-immunisation
Elle est caractérisée par l’apparition d’un anticorps lié à l’exposition d’un antigène érythrocytaire. Cette possibilité explique l’obligation de réaliser une recherche des anticorps antiérythocytaires 1 à 3 mois après chaque épisode transfusionnel.4Purpura post-transfusionnel
Il survient 7 à 10 jours après une transfusion, le plus souvent chez une femme. Il s’agit dans la majorité des cas d’anticorps présents chez le receveur qui sont dirigés contre des antigènes plaquettaires (système HPA) présents chez le donneur. La transfusion de plaquettes supplémentaires aggrave le tableau, et le traitement repose sur l’administration d’immunoglobulines.Réaction du greffon contre l’hôte
Elle est liée à la greffe de lymphocytes T viables présents dans tous les produits sanguins malgré la déleucocytation systématique. Ces lymphocytes normalement éliminés par le système immunitaire du receveur peuvent persister, se greffer, se multiplier et agresser les tissus (foie, peau, etc.) chez un patient profondément immunodéprimé (chimiothérapie ou greffe de moelle) ou immuno-immature comme le fœtus, par exemple. Cet événement est très rare mais souvent fatal. La prévention repose sur l’irradiation des produits sanguins cellulaires. Il convient de noter que les méthodes d’atténuation des pathogènes mises en œuvre pour les plaquettes évitent de recourir à l’irradiation.Causes infectieuses
Les contaminations infectieuses sont caractérisées par l’apparition, chez le receveur, d’une pathologie transmise par le sang comme une hépatite B, C ou A, une infection par le virus de l’immunodéficience humaine (VIH), un paludisme, une infection par le virus du West Nile ou autre. Le processus de sélection des donneurs ainsi que les tests de dépistage mis en œuvre permettent de réduire considérablement le risque résiduel (hépatite B : 1 cas pour 2 millions d’unités transfusées ; hépatite C : 1 cas pour 8 millions d’unités ; VIH : 1 cas pour 3 millions d’unités).
Accidents de surcharge
Une unité de globules rouges contient de 200 à 250 mg de fer. Une surcharge est donc possible, notamment chez certains patients transfusés au long cours comme ceux atteints d’hémoglobinopathies (thalassémie, drépano- cytose) ou de syndromes myélodysplasiques. Elle peut aboutir à terme à de véritables hémochromatoses post-transfusionnelles. Classiquement, la survenue de symptômes (cardiaques, hépatiques, endocriniens) est possible après la transfusion d’une centaine de culots globulaires. La prévention repose sur le suivi de la quantité transfusée, de la ferritine et par le recours à des chélateurs du fer.
Sécuriser l’acte transfusionnel
Outre la sécurité des produits mis à disposition telle que définie dans les bonnes pratiques transfusionnelles,5 le respect des étapes de l’acte transfusionnel et la surveillance de la transfusion sont des éléments importants de la sécurité et de la prévention des réactions trans- fusionnelles. On distingue 4 étapes principales.
Respecter les recommandations de la HAS
L’indication et la prescription du produit sanguin repose sur les diverses recommandations de la Haute Autorité de santé (HAS).3, 6, 7 Il est rappelé que l’on ne transfuse pas de concentré de globules rouges sur un seul chiffre d’hémoglobine mais sur l’appréciation de l’impact clinique d’une anémie et sur le terrain et la pathologie du patient. De même, en dehors de la transfusion en situation d’urgence hémorragique, il est recommandé de transfuser un seul concentré avec une nouvelle évaluation conditionnant une nouvelle prescription éventuelle. Par ailleurs, comme pour toute thérapeutique, un consentement éclairé du patient est obligatoire. Tout refus doit être consigné afin de démontrer que les explications relatives au rapport bénéfices-risques de la transfusion ainsi que les possibilités d’alternatives ont été clairement évoquées. Des particularités à certaines confessions et aux mineurs doivent être prises en compte.
Prescription des analyses obligatoires
La prescription des analyses obligatoires avant toute transfusion avérée doit être réalisée conformément aux impératifs réglementaires,8 à savoir deux déterminations de groupage ABO-RH1 (ABO-D), de phénotype RH-KEL1 (Rh-Kell) et du dépistage et de l’identification d’anticorps anti-érythrocytaires (recherche d’agglutinines irrégulières).
Sélectionner le produit adéquat
La sélection du produit adéquat prend en compte plusieurs éléments :
– les résultats des analyses de groupages sanguins et de recherche d’anticorps qui permettront de respecter les règles de compatibilité transfusionnelle. Pour la transfusion de globules rouges, le groupe O est le donneur universel et, pour la transfusion de plasma, il s’agit du donneur AB. Il convient par ailleurs de ne pas apporter les antigènes correspondant aux anticorps détectés à la recherche d’agglutinines irrégulières dont le délai de validité est 3 jours maximum (qui peut être étendu à 21 jours en absence de situation à risque d’allo-immunisation [transfusion, accouchement…] dans les 6 mois précédents).8 Dans certains cas (femmes avant la ménopause et patients atteints d’hémoglobinopathies), la survenue d’une allo-immunisation dirigée contre les antigènes des systèmes RH et KEL doit être prévenue par un recours à des culots globulaires phénotypés RH-KEL1. De même, en situation d’urgence vitale immédiate, nécessitant la mise à disposition de produit sans délai, des concentrés de globules rouges O D négatif (RH:-1) sont délivrés à une femme avant la ménopause et O D positif (RH:1) à tous les autres patients. Dans tous les cas, on utilise du plasma AB ;
– en cas d’antécédents allergiques sévères, on prescrit des produits (globules rouges ou plaquettes) déplasmatisés, et en cas d’immunodépression profonde ou de transfusion intrafamiliale (groupes sanguins rares), on recourt à des concentrés de globules rouges irradiés afin de prévenir la réaction du greffon contre l’hôte.
– les résultats des analyses de groupages sanguins et de recherche d’anticorps qui permettront de respecter les règles de compatibilité transfusionnelle. Pour la transfusion de globules rouges, le groupe O est le donneur universel et, pour la transfusion de plasma, il s’agit du donneur AB. Il convient par ailleurs de ne pas apporter les antigènes correspondant aux anticorps détectés à la recherche d’agglutinines irrégulières dont le délai de validité est 3 jours maximum (qui peut être étendu à 21 jours en absence de situation à risque d’allo-immunisation [transfusion, accouchement…] dans les 6 mois précédents).8 Dans certains cas (femmes avant la ménopause et patients atteints d’hémoglobinopathies), la survenue d’une allo-immunisation dirigée contre les antigènes des systèmes RH et KEL doit être prévenue par un recours à des culots globulaires phénotypés RH-KEL1. De même, en situation d’urgence vitale immédiate, nécessitant la mise à disposition de produit sans délai, des concentrés de globules rouges O D négatif (RH:-1) sont délivrés à une femme avant la ménopause et O D positif (RH:1) à tous les autres patients. Dans tous les cas, on utilise du plasma AB ;
– en cas d’antécédents allergiques sévères, on prescrit des produits (globules rouges ou plaquettes) déplasmatisés, et en cas d’immunodépression profonde ou de transfusion intrafamiliale (groupes sanguins rares), on recourt à des concentrés de globules rouges irradiés afin de prévenir la réaction du greffon contre l’hôte.
Surveiller la transfusion
La pose et la surveillance de la transfusion imposent :9
– un contrôle ultime au lit du patient, qui comprend :
l un contrôle documentaire fondé sur les concordances d’identité entre les résultats des analyses de groupage et du patient interrogé en direct ainsi que sur les concordances de compatibilité entre les résultats des analyses et les poches à transfuser ;
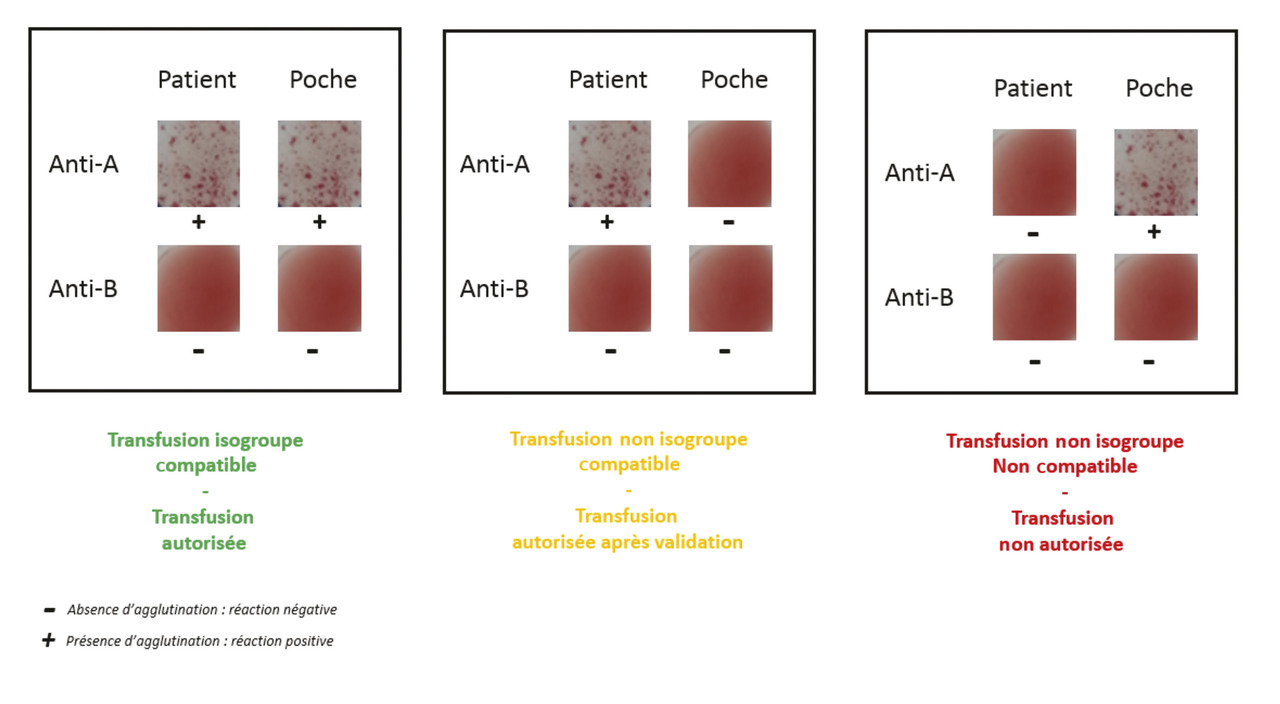
l un contrôle de compatibilité ABO entre le sang du patient et celui de la poche de globules rouges réalisé sur un dispositif dénommé carte de contrôle ultime représentant le dernier verrou de vérification de la compatibilité ABO (fig. 2) ;
l la mesure des paramètres de surveillance immédia- tement avant la transfusion (température, pression artérielle, pouls, respiration et état général du patient), puis toutes les 15 minutes ;
– un début de perfusion à un débit adapté à l’état du patient sous surveillance rapprochée. Des changements minimes sont considérés comme « normaux »10 comme une variation de ± 0,5 °C de température, ± 5 respirations par minute, ± 10 batt/min ou ± 20 mmHg de pression artérielle. Tout changement au-delà de ces paramètres ne signe pas pour autant un accident transfusionnel mais doit le suspecter et imposer une vigilance accrue dans le suivi. Les réactions anormales incluent urticaire, prurit, température supérieure de 1 °C par rapport à la température prétransfusionnelle, frissons, hypotension, dyspnée.
– un contrôle ultime au lit du patient, qui comprend :
l un contrôle documentaire fondé sur les concordances d’identité entre les résultats des analyses de groupage et du patient interrogé en direct ainsi que sur les concordances de compatibilité entre les résultats des analyses et les poches à transfuser ;
l un contrôle de compatibilité ABO entre le sang du patient et celui de la poche de globules rouges réalisé sur un dispositif dénommé carte de contrôle ultime représentant le dernier verrou de vérification de la compatibilité ABO (fig. 2) ;
l la mesure des paramètres de surveillance immédia- tement avant la transfusion (température, pression artérielle, pouls, respiration et état général du patient), puis toutes les 15 minutes ;
– un début de perfusion à un débit adapté à l’état du patient sous surveillance rapprochée. Des changements minimes sont considérés comme « normaux »10 comme une variation de ± 0,5 °C de température, ± 5 respirations par minute, ± 10 batt/min ou ± 20 mmHg de pression artérielle. Tout changement au-delà de ces paramètres ne signe pas pour autant un accident transfusionnel mais doit le suspecter et imposer une vigilance accrue dans le suivi. Les réactions anormales incluent urticaire, prurit, température supérieure de 1 °C par rapport à la température prétransfusionnelle, frissons, hypotension, dyspnée.
Diagnostic et prise en charge d’une réaction transfusionnelle aiguë
Le diagnostic d’une réaction transfusionnelle aiguë débute par la symptomatologie détectée au lit du malade. Il n’y a pas de symptomatologie spécifique (fig. 1). La survenue en contexte transfusionnel et des explorations complémentaires permettent de confirmer le diagnostic ainsi que la gravité et le niveau d’imputabilité de la transfusion.
Urticaire et prurit. Ils peuvent être le fait d’incidents allergiques mineurs ou les prémisses d’un accident plus grave de type anaphylaxie. La transfusion doit être suspendue et le patient surveillé de près afin de noter l’évolution de la symptomatologie. En cas de stabilisation, la transfusion peut être reprise avec un antihistamique et une surveillance directe continue.
Fièvre et frissons. Ils sont le plus souvent associés à une réaction fébrile non hémolytique. Toutefois, ils peuvent être les premiers signes d’une réaction plus sérieuse comme un incident immuno-hémolytique, une contamination bactérienne ou un TRALI (v. supra). Si la température augmente de plus de 1 °C, la transfusion doit être suspendue. Une réaction hémolytique ou infectieuse doit être suspectée si la température est plus haute et si des signes plus sévères font leur apparition. En cas de stabilisation à +1 °C sans autres signes, la transfusion peut être reprise avec un antipyrétique et une surveillance directe continue.
Dyspnée et détresse respiratoire. Une détresse respiratoire est le témoin d’une sévérité de la réaction transfusionnelle et peut être le fait d’une anaphylaxie, d’un TRALI ou d’un TACO (v. supra).
Hypotension ou état de choc. Devant une hypo- tension ou un état de choc, on évoque une anaphylaxie, un choc hémolytique, un choc septique ou un TRALI.
Hypothermie. Elle peut être notée notamment en situation de transfusion massive avec absence réchauf- fement des produits.
Urticaire et prurit. Ils peuvent être le fait d’incidents allergiques mineurs ou les prémisses d’un accident plus grave de type anaphylaxie. La transfusion doit être suspendue et le patient surveillé de près afin de noter l’évolution de la symptomatologie. En cas de stabilisation, la transfusion peut être reprise avec un antihistamique et une surveillance directe continue.
Fièvre et frissons. Ils sont le plus souvent associés à une réaction fébrile non hémolytique. Toutefois, ils peuvent être les premiers signes d’une réaction plus sérieuse comme un incident immuno-hémolytique, une contamination bactérienne ou un TRALI (v. supra). Si la température augmente de plus de 1 °C, la transfusion doit être suspendue. Une réaction hémolytique ou infectieuse doit être suspectée si la température est plus haute et si des signes plus sévères font leur apparition. En cas de stabilisation à +1 °C sans autres signes, la transfusion peut être reprise avec un antipyrétique et une surveillance directe continue.
Dyspnée et détresse respiratoire. Une détresse respiratoire est le témoin d’une sévérité de la réaction transfusionnelle et peut être le fait d’une anaphylaxie, d’un TRALI ou d’un TACO (v. supra).
Hypotension ou état de choc. Devant une hypo- tension ou un état de choc, on évoque une anaphylaxie, un choc hémolytique, un choc septique ou un TRALI.
Hypothermie. Elle peut être notée notamment en situation de transfusion massive avec absence réchauf- fement des produits.
ARRÊTER, ENQUÊTER ET DÉCLARER
En ce qui concerne la prise en charge, il faut rappeler qu’en cas de suspiscion d’une réaction transfusionnelle la transfusion doit être immédiatement arrêtée, la voie maintenue avec la mise en place d’un soluté salin à 0,9 %. Une enquête immédiate doit être menée afin de vérifier l’identité du patient et les caractéristiques et l’état des produits transfusés. Les signes vitaux doivent être notés toutes les 15 minutes. Un échantillon et les poches transfusées doivent être expédiés au laboratoire d’immuno-hématologie pour exploration d’une incompatibilité et au laboratoire de bactériologie référent11 en cas de suspiscion d’une contamination bactérienne. Un signalement doit être faite au plus tôt au correspondant d’hémovigilance de l’établissement de santé ou à celui de l’Établissement français du sang.
Références
1. Loi n° 93-5 du 4 janvier 1993.
2. Agence nationale du médicament et des produits de santé. Rapport d’hémovigilance 2016.
3. Haute Autorité de santé, Agence nationale du médicament et des produits de santé. Transfusion de globules rouges homologues : produits, indications, alternatives. Méthode Recommandations pour la pratique clinique HAS-ANSM, nov. 2014.
4. Décision rai post transfusionnelles 2006.
5. Décision du 10 juillet 2018 définissant les principes de bonnes pratiques prévues à l’article L.1222.12 du code de la santé publique.
6. Haute Autorité de santé, Agence nationale du médicament et des produits de santé. Transfusion de plaquettes : produits, indications. Méthode Recommandations pour la pratique clinique HAS-ANSM, oct 2015.
7. Haute Autorité de santé, Agence nationale du médicament et des produits de santé. Transfusion de plasma thérapeutique : produits, indications. Actualisation. Recommandations HAS-ANSM, actualisation 2012.
8. Arrêté du 15 mai 2018 fixant les conditions de réalisation des examens de biologie médicale d’immuno-hématologie érythrocytaire.
9. Circulaire DGS/DHOS/AFSSAPS n° 03/582 du 15 janvier 2003 relative à la réalisation de l’acte transfusionnel. Bulletin officiel n° 2004.
10. Suddock JT, Crookston KP. Transfusion, reactions. Source StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing, 2018.
11. Agence française de sécurité sanitaire des produits de santé ; groupe de travail « Validation des infections bactériennes transmises par transfusion ». Infections bactériennes transmises par transfusion. Fiche technique, Affssaps 2008. www.ansm.sante.fr ou https://bit.ly/2F6CeAi
2. Agence nationale du médicament et des produits de santé. Rapport d’hémovigilance 2016.
3. Haute Autorité de santé, Agence nationale du médicament et des produits de santé. Transfusion de globules rouges homologues : produits, indications, alternatives. Méthode Recommandations pour la pratique clinique HAS-ANSM, nov. 2014.
4. Décision rai post transfusionnelles 2006.
5. Décision du 10 juillet 2018 définissant les principes de bonnes pratiques prévues à l’article L.1222.12 du code de la santé publique.
6. Haute Autorité de santé, Agence nationale du médicament et des produits de santé. Transfusion de plaquettes : produits, indications. Méthode Recommandations pour la pratique clinique HAS-ANSM, oct 2015.
7. Haute Autorité de santé, Agence nationale du médicament et des produits de santé. Transfusion de plasma thérapeutique : produits, indications. Actualisation. Recommandations HAS-ANSM, actualisation 2012.
8. Arrêté du 15 mai 2018 fixant les conditions de réalisation des examens de biologie médicale d’immuno-hématologie érythrocytaire.
9. Circulaire DGS/DHOS/AFSSAPS n° 03/582 du 15 janvier 2003 relative à la réalisation de l’acte transfusionnel. Bulletin officiel n° 2004.
10. Suddock JT, Crookston KP. Transfusion, reactions. Source StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing, 2018.
11. Agence française de sécurité sanitaire des produits de santé ; groupe de travail « Validation des infections bactériennes transmises par transfusion ». Infections bactériennes transmises par transfusion. Fiche technique, Affssaps 2008. www.ansm.sante.fr ou https://bit.ly/2F6CeAi