La reconstruction mammaire permet d’améliorer la qualité de vie des patientes grâce à une restauration du schéma corporel et de la confiance en soi. Selon l’INCa, elle fait partie intégrante du traitement du cancer du sein et doit être proposée après une mastectomie de première intention ou de rattrapage.
De nos jours, la reconstruction mammaire fait partie intégrante de la prise en charge des patientes devant subir une mastectomie.1 En effet, bien que l’étalon-or du traitement des cancers du sein soit le traitement conservateur (chirurgie conservatrice et radiothérapie) avec des indications de plus en plus poussées, notamment depuis l’avènement des techniques d’oncoplastie, environ 30 % des patientes nécessitent un traitement radical. Elle doit être proposée à la patiente après une mastectomie de première intention ou de rattrapage ; dans tous les cas, elle est un choix de la patiente, en accord avec l’équipe médicale.2 Elle permet d’améliorer la qualité de vie de ces femmes grâce à une restauration du schéma corporel et de la confiance en soi.3 Il faut cependant respecter les contre-indications à la reconstruction mammaire immédiate comme les cancers inflammatoires et rester prudent chez les patientes ayant un risque de complication (tabagisme, diabète, obésité…) afin de ne pas retarder un éventuel traitement adjuvant.
Il existe de nombreuses techniques de reconstruction mammaire qui peuvent satisfaire toutes les situations cliniques : les reconstructions prothétiques utilisent des implants remplis de gel de silicone, les reconstructions autologues reconstruisent le volume mammaire avec les tissus de la patiente par le biais de lambeaux musculocutanés ou cutanéograisseux. Pendant de nombreuses années, la reconstruction mammaire a été principalement assurée par prothèse ou lambeau musculo-cutané pédiculé (conservation du pédicule vasculaire), notamment par lambeau de grand dorsal et TRAM (transverse rectus abdominis musculocutaneous flap) utilisant le muscle grand droit de l’abdomen.
L’évolution des techniques de reconstruction a été marquée par la démocratisation de la microchirurgie permettant la réalisation de « lambeaux libres » avec micro-anastomoses vasculaires du pédicule,4 l’apport des matrices synthétiques en reconstruction immédiate pour soutenir la prothèse et le lipomodelage qui parfait le résultat esthétique des reconstructions. La récente polémique sur le risque de survenue d’un lymphome anaplasique à grandes cellules a modifié les indications techniques.
Il existe de nombreuses techniques de reconstruction mammaire qui peuvent satisfaire toutes les situations cliniques : les reconstructions prothétiques utilisent des implants remplis de gel de silicone, les reconstructions autologues reconstruisent le volume mammaire avec les tissus de la patiente par le biais de lambeaux musculocutanés ou cutanéograisseux. Pendant de nombreuses années, la reconstruction mammaire a été principalement assurée par prothèse ou lambeau musculo-cutané pédiculé (conservation du pédicule vasculaire), notamment par lambeau de grand dorsal et TRAM (transverse rectus abdominis musculocutaneous flap) utilisant le muscle grand droit de l’abdomen.
L’évolution des techniques de reconstruction a été marquée par la démocratisation de la microchirurgie permettant la réalisation de « lambeaux libres » avec micro-anastomoses vasculaires du pédicule,4 l’apport des matrices synthétiques en reconstruction immédiate pour soutenir la prothèse et le lipomodelage qui parfait le résultat esthétique des reconstructions. La récente polémique sur le risque de survenue d’un lymphome anaplasique à grandes cellules a modifié les indications techniques.
Lambeaux perforants et lambeaux libres
Les lambeaux perforants sont l’aboutissement des connaissances de la physiologie de la vascularisation cutanée et de ses conséquences sur le prélèvement des lambeaux. Ces lambeaux cutanéograisseux sont vascularisés par un ou plusieurs vaisseaux qui perforent un plan profond (muscle, fascia). Le vaisseau perforant assure à lui seul la vascularisation de tout un territoire cutanéograisseux appelé angiosome. Il est donc possible de prélever ce territoire avec son pédicule perforant et de le positionner à distance du site donneur pour couvrir une perte de substance ou réaliser une reconstruction mammaire. Leur principal avantage est de dispenser d’une prise musculaire pouvant être source de douleur et de séquelles fonctionnelles au niveau du site donneur. Ils peuvent être pédiculés ou libres.
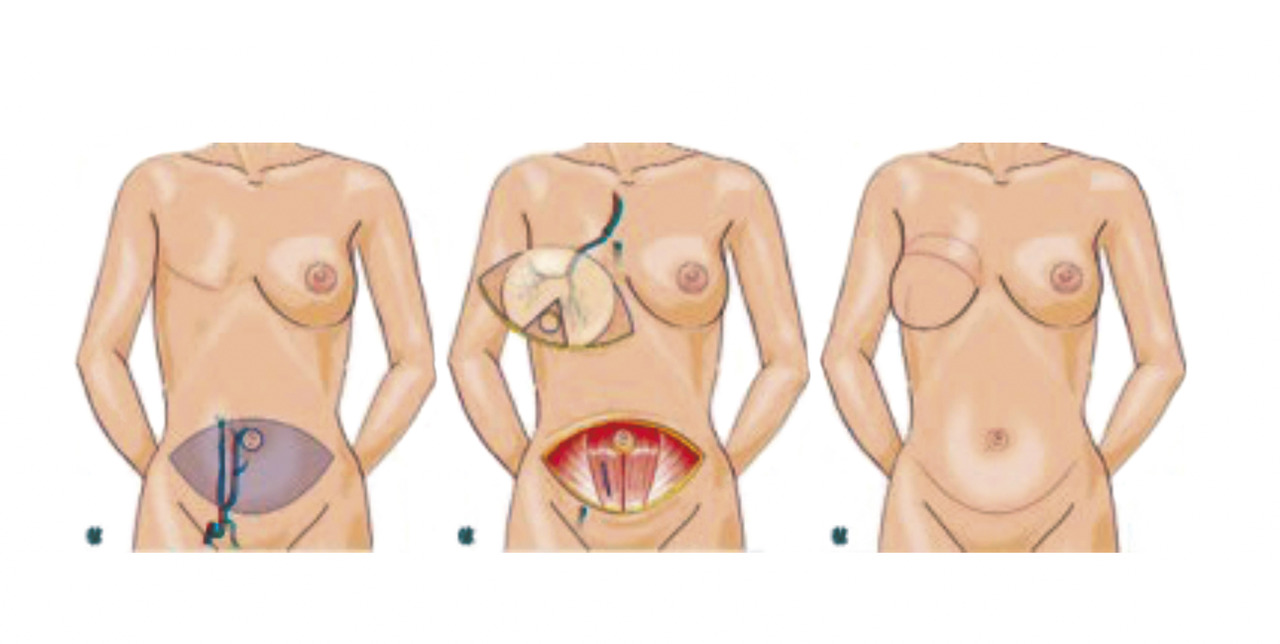
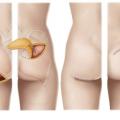
Le lambeau perforant libre le plus utilisé en reconstruction mammaire est le DIEP (deep inferior epigastric perforator flap) [fig. 1]. Il a été décrit pour la première fois en 19895 et utilisé en reconstruction mammaire en 1994,6 il découle d’un raffinement de la technique du TRAM pour diminuer les séquelles pariétales (pas de prise du muscle grand droit). Il utilise l’excédent cutanéograisseux abdominal qui est vascularisé par un pédicule perforant issu du pédicule épigastrique inférieur.
Le DIEP s’est rapidement imposé comme un lambeau de référence en reconstruction mammaire car c’est un lambeau fiable permettant de reconstruire en une seule fois un gros volume avec un aspect naturel (forme, ptose, souplesse).
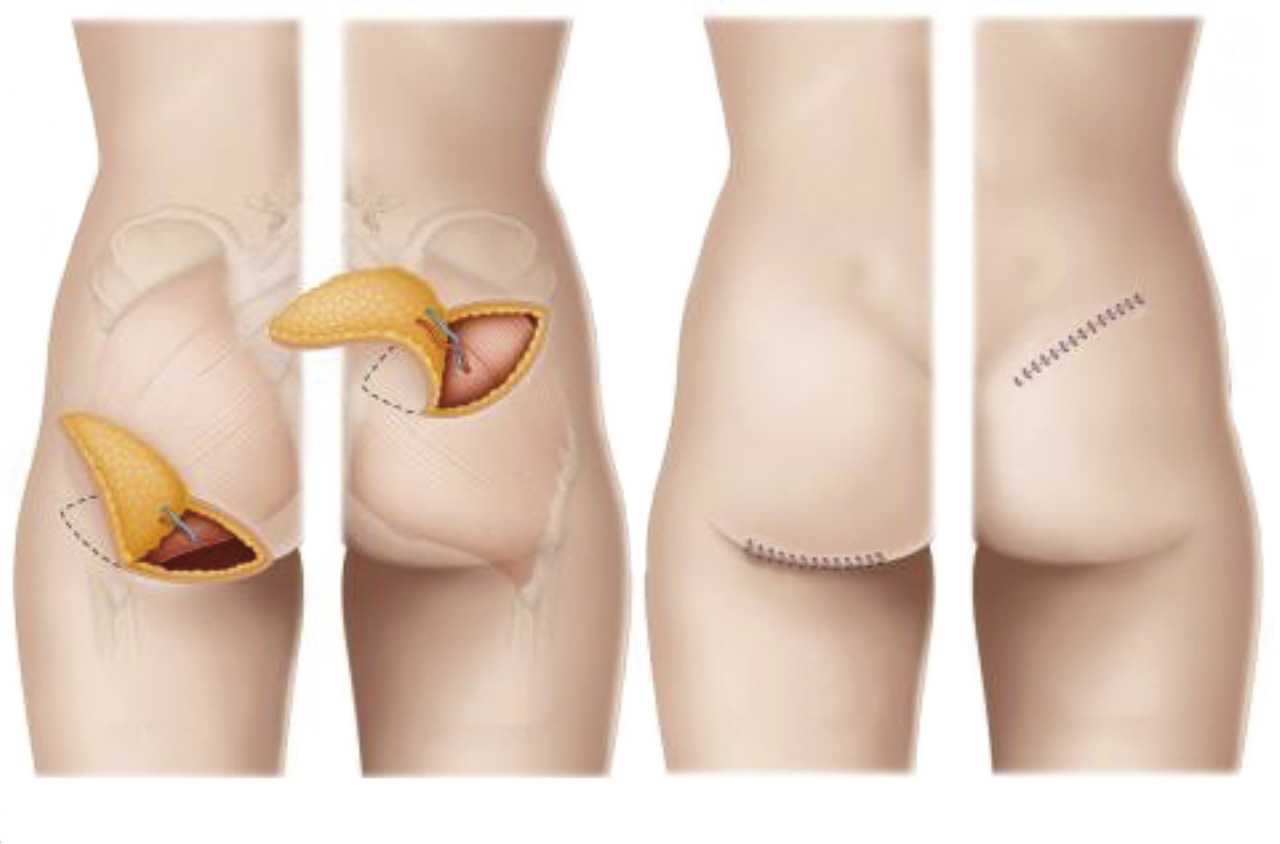
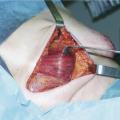
Devant le succès du DIEP, d’autres lambeaux perforants ont été décrits, notamment les lambeaux fessiers (fig. 2) et de la face interne de la cuisse (gracilis), qui permettent ainsi de s’adapter à la morphologie de chaque patiente.
Ces lambeaux sont cependant techniquement plus difficiles à réaliser du fait de la nécessité d’anastomoses microchirurgicales, avec un risque d’échec en lien comportant une thrombose des anastomoses. Ils doivent être réalisés par des chirurgiens entraînés et spécialisés, avec une sélection soigneuse des patientes.
Le lambeau perforant libre le plus utilisé en reconstruction mammaire est le DIEP (deep inferior epigastric perforator flap) [fig. 1]. Il a été décrit pour la première fois en 19895 et utilisé en reconstruction mammaire en 1994,6 il découle d’un raffinement de la technique du TRAM pour diminuer les séquelles pariétales (pas de prise du muscle grand droit). Il utilise l’excédent cutanéograisseux abdominal qui est vascularisé par un pédicule perforant issu du pédicule épigastrique inférieur.
Le DIEP s’est rapidement imposé comme un lambeau de référence en reconstruction mammaire car c’est un lambeau fiable permettant de reconstruire en une seule fois un gros volume avec un aspect naturel (forme, ptose, souplesse).
Devant le succès du DIEP, d’autres lambeaux perforants ont été décrits, notamment les lambeaux fessiers (fig. 2) et de la face interne de la cuisse (gracilis), qui permettent ainsi de s’adapter à la morphologie de chaque patiente.
Ces lambeaux sont cependant techniquement plus difficiles à réaliser du fait de la nécessité d’anastomoses microchirurgicales, avec un risque d’échec en lien comportant une thrombose des anastomoses. Ils doivent être réalisés par des chirurgiens entraînés et spécialisés, avec une sélection soigneuse des patientes.
Reconstructions mammaires immédiates par implant
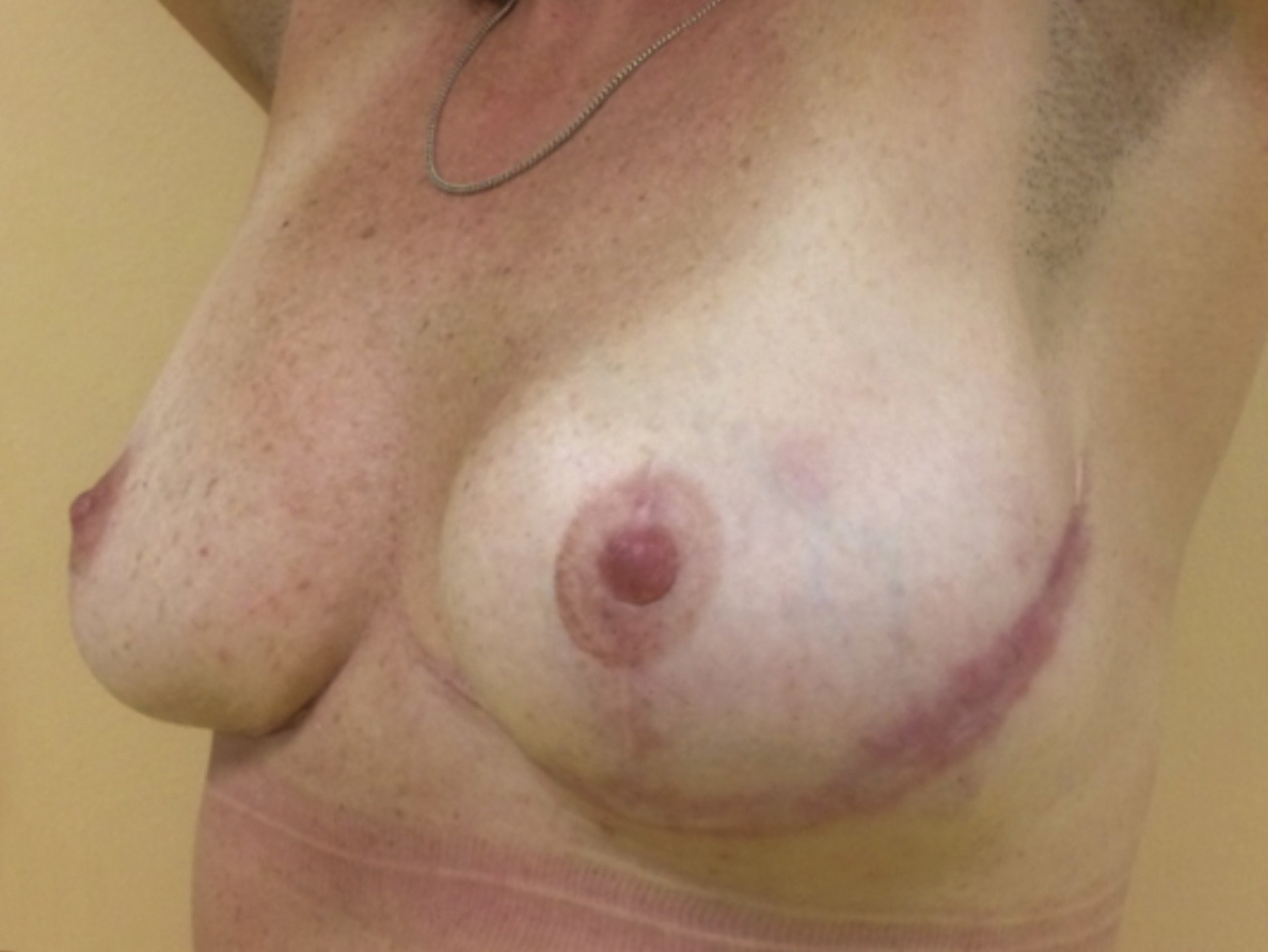
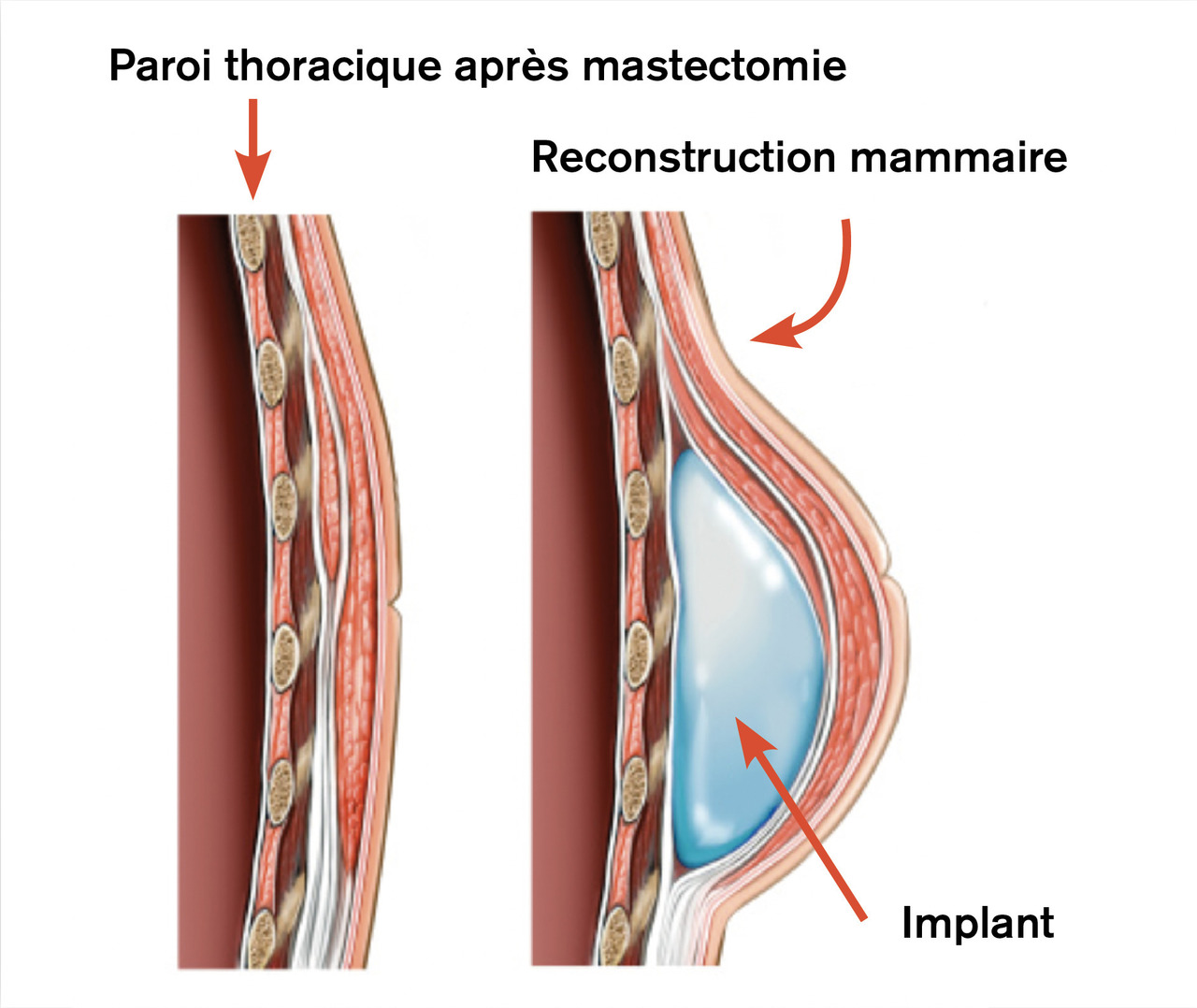
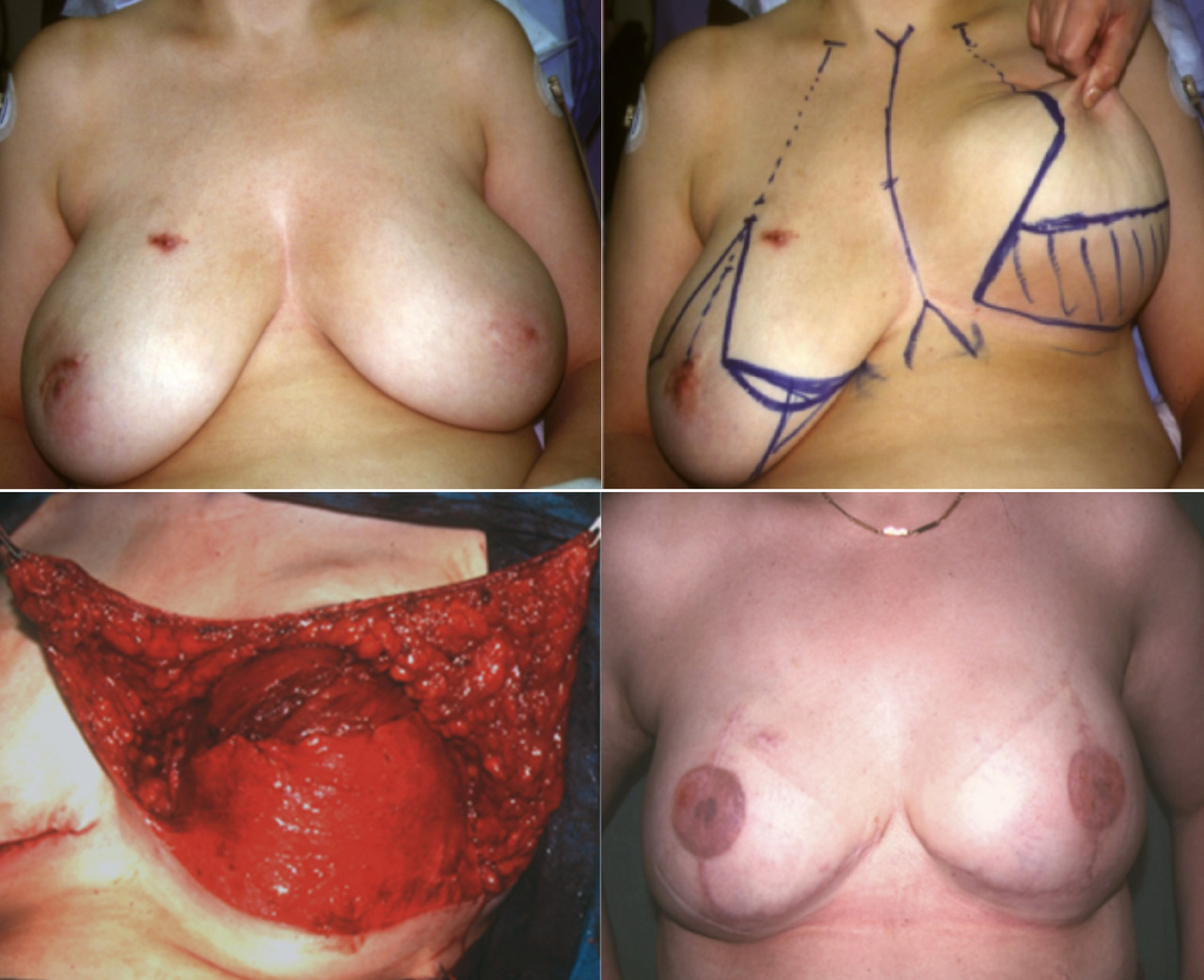
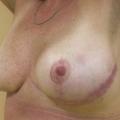
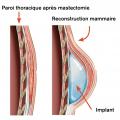
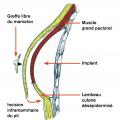
La mastectomie avec reconstruction immédiate (fig. 3) permet de préserver l’étui cutané du sein et de le reconstruire immédiatement tout en préservant sa forme ainsi que le sillon sous-mammaire. Pour les mastectomies prophylactiques motivées par des mutations génétiques, il est possible de conserver l’aréole et le mamelon, améliorant encore le rendu esthétique.
La pose de l’implant nécessite de créer une loge qui est de réalisation plus ou moins facile en fonction de la qualité des tissus, du volume du sein et de la trophicité du muscle pectoral.
Le dogme était d’obtenir une couverture musculaire complète de l’implant. Cela nécessitait parfois de mettre en place une prothèse d’expansion en arrière du muscle pectoral et du fascia sous-pectoral. La partie inféro-externe du volume reconstruit par la prothèse pouvant ne pas être recouverte par du tissu souple alors qu’elle correspond à la projection maximale du sein reconstruit. L’expansion progressive permettait de créer une loge prothétique, la prothèse d’expansion était ensuite remplacée par l’implant définitif.
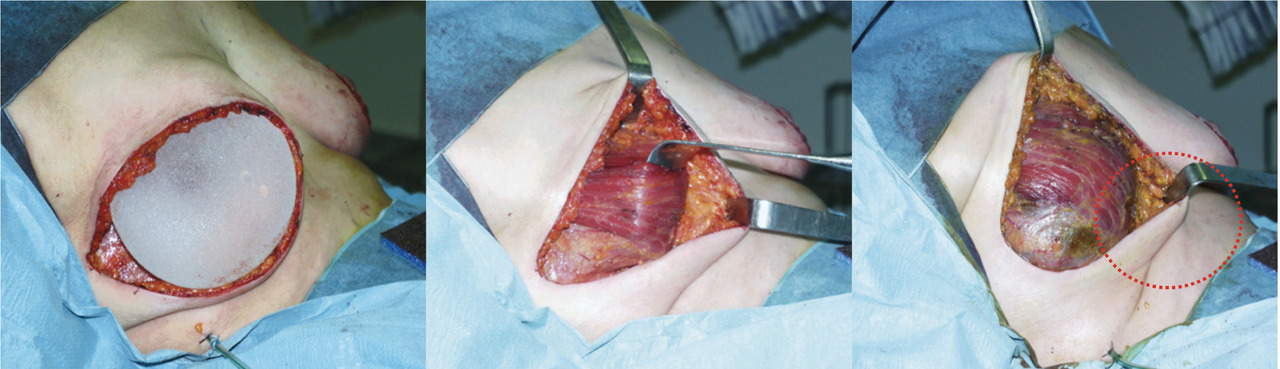
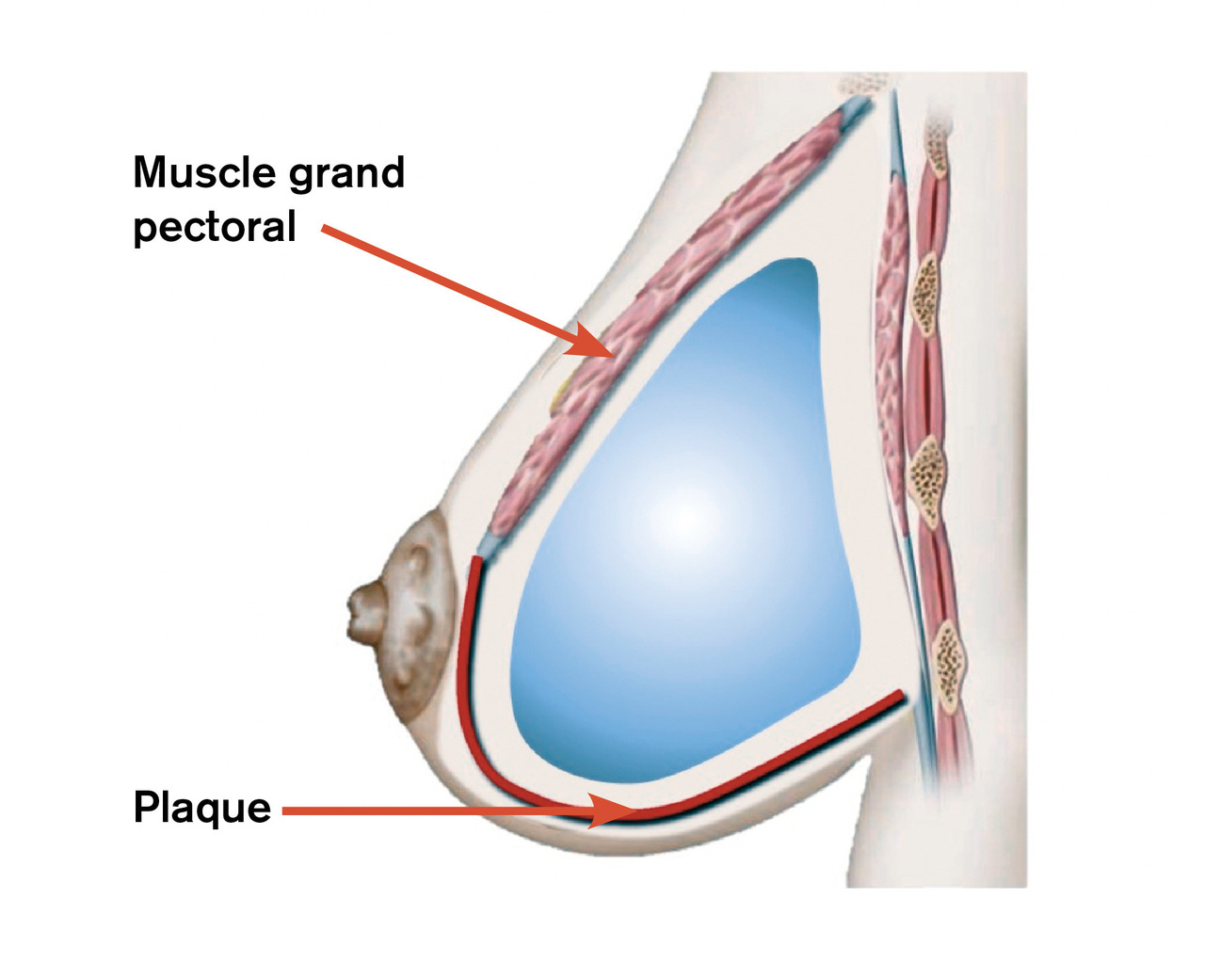
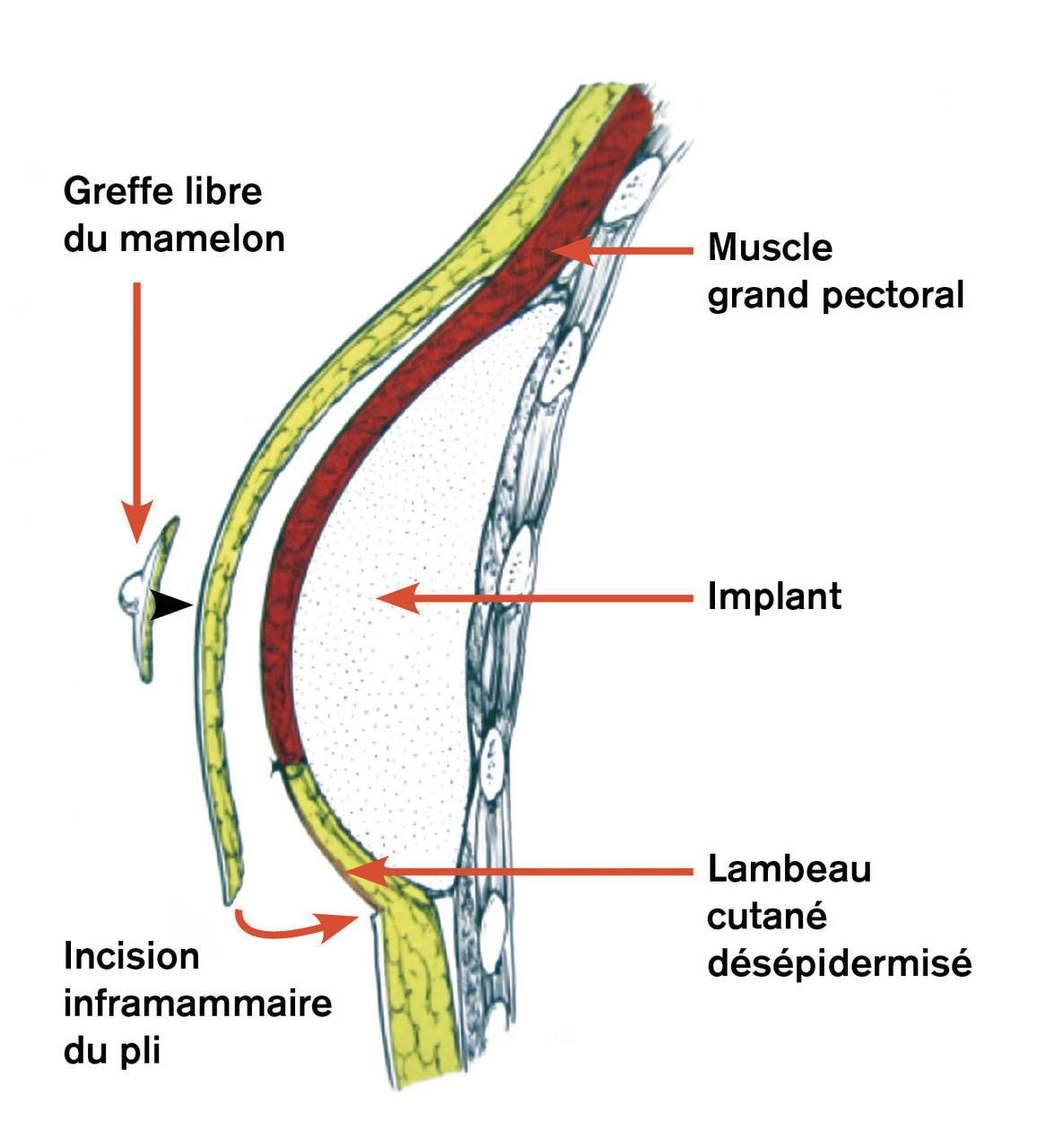
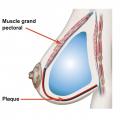
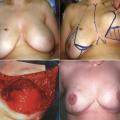
La confection immédiate d’une loge prothétique souple a bénéficié de l’apport soit de tissu autologue de la patiente (lambeau cutané désépidermisé inférieur) soit de matrices qui permettent l’expansion de ce quadrant inféro-externe en créant un hamac protecteur sur les quadrants inférieurs du sein reconstruit (fig. 4-7 ).
Ces plaques ou matrices peuvent être biologiques (derme de porc ou bovin) ou synthétiques (résorbables ou non). Elles sont assez onéreuses, avec des prix allant de 300 € à plus de 1 200 € pour les matrices biologiques, ne sont pas remboursées par la Sécurité sociale et restent donc à la charge de la patiente ou de l’établissement de soin qui les propose.
La pose de l’implant nécessite de créer une loge qui est de réalisation plus ou moins facile en fonction de la qualité des tissus, du volume du sein et de la trophicité du muscle pectoral.
Le dogme était d’obtenir une couverture musculaire complète de l’implant. Cela nécessitait parfois de mettre en place une prothèse d’expansion en arrière du muscle pectoral et du fascia sous-pectoral. La partie inféro-externe du volume reconstruit par la prothèse pouvant ne pas être recouverte par du tissu souple alors qu’elle correspond à la projection maximale du sein reconstruit. L’expansion progressive permettait de créer une loge prothétique, la prothèse d’expansion était ensuite remplacée par l’implant définitif.
La confection immédiate d’une loge prothétique souple a bénéficié de l’apport soit de tissu autologue de la patiente (lambeau cutané désépidermisé inférieur) soit de matrices qui permettent l’expansion de ce quadrant inféro-externe en créant un hamac protecteur sur les quadrants inférieurs du sein reconstruit (
Ces plaques ou matrices peuvent être biologiques (derme de porc ou bovin) ou synthétiques (résorbables ou non). Elles sont assez onéreuses, avec des prix allant de 300 € à plus de 1 200 € pour les matrices biologiques, ne sont pas remboursées par la Sécurité sociale et restent donc à la charge de la patiente ou de l’établissement de soin qui les propose.
Lymphomes anaplasiques à grandes cellules associés aux implants mammaires
Récemment, la polémique sur les lymphomes anaplasiques à grandes cellules associés aux implants mammaires7 a quelque peu impacté l’offre en reconstruction mammaire avec implant.
Le lymphome anaplasique à grandes cellules est une forme rare de lymphome non hodgkinien. Le risque de survenue de ce lymphome reste rare, actuellement 59 cas ont été répertoriés en France depuis 2011 et environ 600 cas au niveau mondial. Cette survenue semble liée à la texturation des implants mammaires. En effet, aucun cas de lymphomes anaplasiques à grandes cellules n’a été décrit avec des implants lisses.
Par mesure de précaution, l’Agence nationale de sécurité du médicament (ANSM) a pris la décision de retirer du marché les implants mammaires macrotexturés et en polyuréthane afin de réduire l’exposition des femmes au risque de lymphome anaplasique à grandes cellules. En revanche, elle ne recommande pas l’explantation préventive de ces implants, mais une surveillance clinique régulière, les examens d’imagerie mammaire ne sont nécessaires qu’en cas de signes cliniques avérés (hors surveillance annuelle des patientes ayant eu un cancer du sein).
Le signe clinique de loin le plus fréquent est la survenue d’une augmentation rapide du volume du sein sous la forme d’un sérome périprothétique important. Plus rarement, il peut s’agir de douleurs, d’une rougeur ou de l’apparition d’un syndrome tumoral au niveau du sein, mais dans ce cas le diagnostic de cancer du sein doit être évoqué en priorité. Dans la majorité des cas, les lésions sont purement intracapsulaires et sont traitées par capsulectomie totale et ablation de la prothèse. En cas de lésion à distance, la patiente doit être prise en charge au sein d’une unité spécialisée dans le traitement des lymphomes. Tout diagnostic de lymphome anaplasique à grandes cellules associé à un implant mammaire doit faire l’objet d’une déclaration de matériovigilance à l’ANSM.
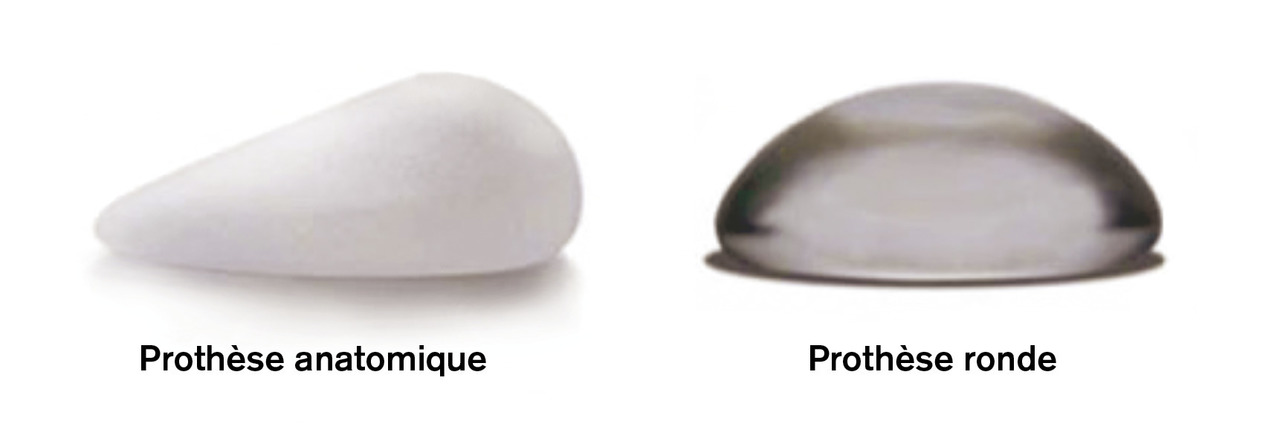
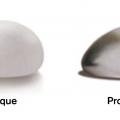
L’interdiction de mise sur le marché des implants macrotexturés a un impact non négligeable en reconstruction mammaire. En effet, dans la très grande majorité des cas, des implants dit « anatomiques » sont utilisés (fig. 8). Ils ont une forme de sein permettant une reconstruction mammaire avec une forme plus proche du sein natif. Malheureusement, il n’existe pas d’implant mammaire anatomique ayant une enveloppe lisse et il n’y a actuellement pas sur le marché en France d’implant anatomique microtexturé. Les reconstructions doivent donc être réalisées avec les implants « ronds » car ce sont actuellement les seuls disponibles sur le marché avec des enveloppes lisses ou microtexturées. Le désavantage principal de ces implants est qu’il est plus difficile d’obtenir un résultat esthétique similaire au sein natif, augmentant la nécessité d’interventions chirurgicales dites de « retouches » comme par exemple des lipomodelages ou des gestes de symétrisation du sein controlatéral.
Le lymphome anaplasique à grandes cellules est une forme rare de lymphome non hodgkinien. Le risque de survenue de ce lymphome reste rare, actuellement 59 cas ont été répertoriés en France depuis 2011 et environ 600 cas au niveau mondial. Cette survenue semble liée à la texturation des implants mammaires. En effet, aucun cas de lymphomes anaplasiques à grandes cellules n’a été décrit avec des implants lisses.
Par mesure de précaution, l’Agence nationale de sécurité du médicament (ANSM) a pris la décision de retirer du marché les implants mammaires macrotexturés et en polyuréthane afin de réduire l’exposition des femmes au risque de lymphome anaplasique à grandes cellules. En revanche, elle ne recommande pas l’explantation préventive de ces implants, mais une surveillance clinique régulière, les examens d’imagerie mammaire ne sont nécessaires qu’en cas de signes cliniques avérés (hors surveillance annuelle des patientes ayant eu un cancer du sein).
Le signe clinique de loin le plus fréquent est la survenue d’une augmentation rapide du volume du sein sous la forme d’un sérome périprothétique important. Plus rarement, il peut s’agir de douleurs, d’une rougeur ou de l’apparition d’un syndrome tumoral au niveau du sein, mais dans ce cas le diagnostic de cancer du sein doit être évoqué en priorité. Dans la majorité des cas, les lésions sont purement intracapsulaires et sont traitées par capsulectomie totale et ablation de la prothèse. En cas de lésion à distance, la patiente doit être prise en charge au sein d’une unité spécialisée dans le traitement des lymphomes. Tout diagnostic de lymphome anaplasique à grandes cellules associé à un implant mammaire doit faire l’objet d’une déclaration de matériovigilance à l’ANSM.
L’interdiction de mise sur le marché des implants macrotexturés a un impact non négligeable en reconstruction mammaire. En effet, dans la très grande majorité des cas, des implants dit « anatomiques » sont utilisés (fig. 8). Ils ont une forme de sein permettant une reconstruction mammaire avec une forme plus proche du sein natif. Malheureusement, il n’existe pas d’implant mammaire anatomique ayant une enveloppe lisse et il n’y a actuellement pas sur le marché en France d’implant anatomique microtexturé. Les reconstructions doivent donc être réalisées avec les implants « ronds » car ce sont actuellement les seuls disponibles sur le marché avec des enveloppes lisses ou microtexturées. Le désavantage principal de ces implants est qu’il est plus difficile d’obtenir un résultat esthétique similaire au sein natif, augmentant la nécessité d’interventions chirurgicales dites de « retouches » comme par exemple des lipomodelages ou des gestes de symétrisation du sein controlatéral.
Apport du lipomodelage en reconstruction mammaire
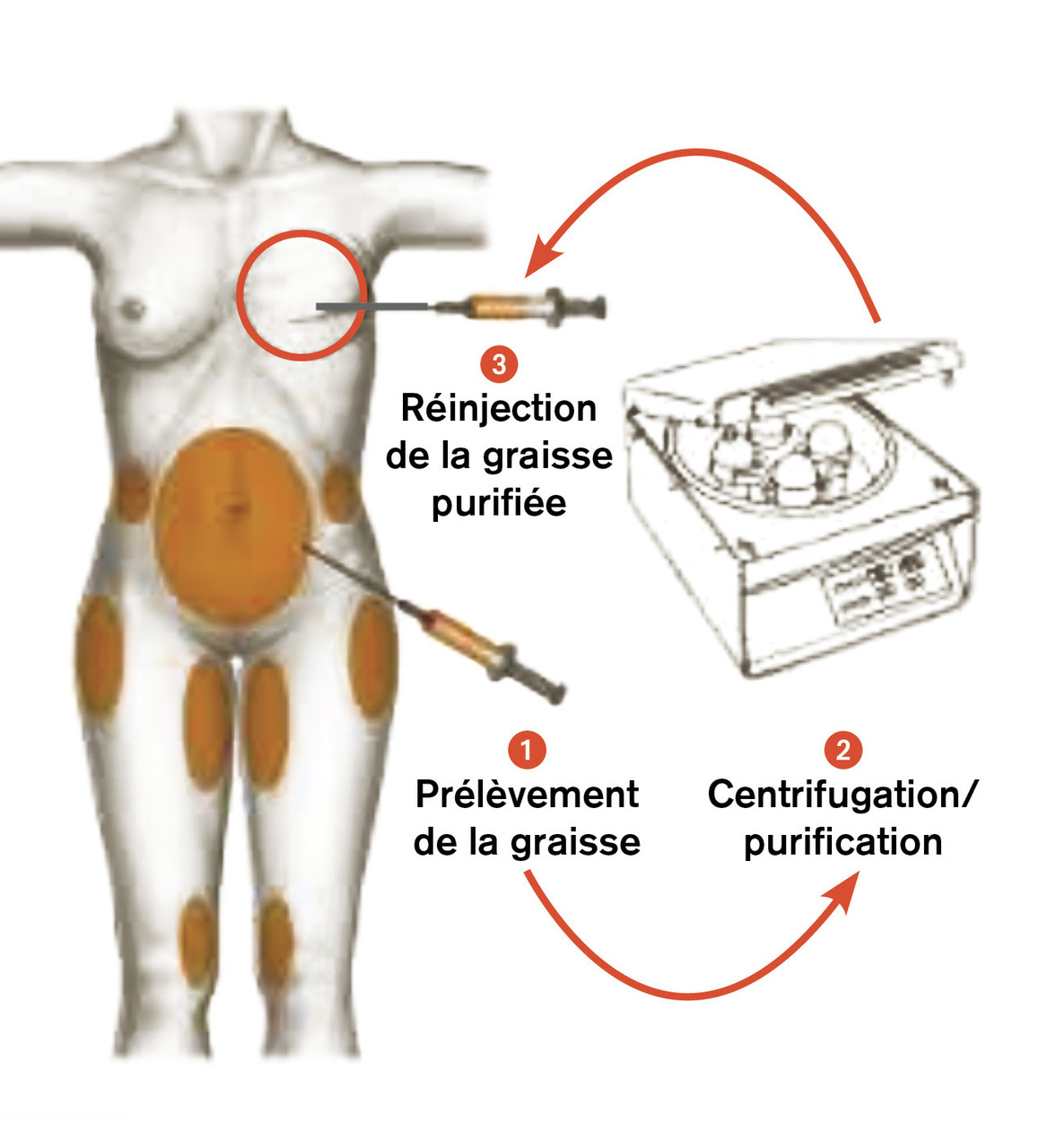
Le lipomodelage, outil majeur en reconstruction mammaire, consiste en un transfert de tissu adipeux d’un site donneur (le plus souvent cuisses, hanches et ventre) au sein reconstruit (fig. 9). Cette technique est en fait une greffe de cellules graisseuses dont la prise est estimée à 60 à 70 % selon les patientes. De ce fait, le résultat obtenu est définitif puisque les cellules adipeuses ainsi greffées vivront aussi longtemps que les tissus receveurs. En revanche, leur évolution se fera en fonction de l’adiposité de la patiente (si la patiente maigrit, le volume apporté diminue).
Son intérêt est double : il améliore la trophicité cutanée et sert de produit de comblement pour corriger de petits défauts sur la reconstruction à type d’irrégularités ou de manque de volume.
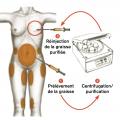
C’est une intervention chirurgicale réalisée au bloc opératoire, sous anesthésie générale, et plusieurs séances peuvent être nécessaires. Le prélèvement de tissu graisseux est effectué de façon atraumatique par de petites incisions à l’aide d’une canule d’aspiration. Il peut être réalisé de façon manuelle ou à l’aide d’appareils qui aspirent et recueillent la graisse. Cette dernière est ensuite purifiée soit par centrifugation, soit par lavage et décantation, avant d’être transférée à l’aide de microcanules par de toutes petites incisions.
Le lipomodelage a des utilisations multiples en reconstruction mammaire :
– en préparation de la paroi thoracique en vue d’une reconstruction mammaire par prothèse, notamment lorsque la patiente a eu une radiothérapie après la mastectomie ; cela permet d’améliorer la trophicité cutanée et lever d’éventuelles adhérences ;
– il permet de reconstituer le volume mammaire des reconstructions par lambeau, notamment pour les reconstructions par lambeau de grand dorsal ; dans ce cas, 3 à 5 séances peuvent être nécessaires ;
– pour parfaire le résultat esthétique des reconstructions mammaires par implant, pour corriger des irrégularités comme par exemple des contours de la prothèse trop visible, un manque de volume ou de projection ou une asymétrie au niveau du décolleté ;
– dans certains cas, la reconstruction mammaire peut être effectuée par lipomodelage exclusif mais nécessite en général 4 ou 5 séances.
Le lipomodelage peut également être utilisé pour corriger des séquelles esthétiques après un traitement conservateur du cancer du sein (chirurgie conservatrice et radiothérapie), mais il faut respecter un délai minimum de 2 ans après la fin des traitements et disposer d’un bilan d’imagerie récent (< 6 mois).
Actuellement, on peut considérer qu’un lipomodelage n’entraîne pas de difficulté diagnostique particulière pour un radiologue expérimenté en imagerie du sein. En revanche, le lipomodelage ne doit pas être réalisé en cas de maladie évolutive ou si les images radiologiques sont trop difficiles à interpréter afin de ne pas compromettre le suivi des patientes.
En conclusion, les reconstructions mammaires sont possibles pour la grande majorité des patientes. La multiplicité des techniques permet de personnaliser pour chaque femme une chirurgie adaptée à sa pathologie et à sa morphologie. L’information exhaustive des avantages et des inconvénients doit permettre à la patiente de participer au choix technique, l’indication finale lui revenant. La surveillance des prothèses est couplée à la surveillance oncologique et peut se résumer à l’examen clinique, avec prescription d’une imagerie par résonance magnétique à la moindre anomalie.
Son intérêt est double : il améliore la trophicité cutanée et sert de produit de comblement pour corriger de petits défauts sur la reconstruction à type d’irrégularités ou de manque de volume.
C’est une intervention chirurgicale réalisée au bloc opératoire, sous anesthésie générale, et plusieurs séances peuvent être nécessaires. Le prélèvement de tissu graisseux est effectué de façon atraumatique par de petites incisions à l’aide d’une canule d’aspiration. Il peut être réalisé de façon manuelle ou à l’aide d’appareils qui aspirent et recueillent la graisse. Cette dernière est ensuite purifiée soit par centrifugation, soit par lavage et décantation, avant d’être transférée à l’aide de microcanules par de toutes petites incisions.
Le lipomodelage a des utilisations multiples en reconstruction mammaire :
– en préparation de la paroi thoracique en vue d’une reconstruction mammaire par prothèse, notamment lorsque la patiente a eu une radiothérapie après la mastectomie ; cela permet d’améliorer la trophicité cutanée et lever d’éventuelles adhérences ;
– il permet de reconstituer le volume mammaire des reconstructions par lambeau, notamment pour les reconstructions par lambeau de grand dorsal ; dans ce cas, 3 à 5 séances peuvent être nécessaires ;
– pour parfaire le résultat esthétique des reconstructions mammaires par implant, pour corriger des irrégularités comme par exemple des contours de la prothèse trop visible, un manque de volume ou de projection ou une asymétrie au niveau du décolleté ;
– dans certains cas, la reconstruction mammaire peut être effectuée par lipomodelage exclusif mais nécessite en général 4 ou 5 séances.
Le lipomodelage peut également être utilisé pour corriger des séquelles esthétiques après un traitement conservateur du cancer du sein (chirurgie conservatrice et radiothérapie), mais il faut respecter un délai minimum de 2 ans après la fin des traitements et disposer d’un bilan d’imagerie récent (< 6 mois).
Actuellement, on peut considérer qu’un lipomodelage n’entraîne pas de difficulté diagnostique particulière pour un radiologue expérimenté en imagerie du sein. En revanche, le lipomodelage ne doit pas être réalisé en cas de maladie évolutive ou si les images radiologiques sont trop difficiles à interpréter afin de ne pas compromettre le suivi des patientes.
En conclusion, les reconstructions mammaires sont possibles pour la grande majorité des patientes. La multiplicité des techniques permet de personnaliser pour chaque femme une chirurgie adaptée à sa pathologie et à sa morphologie. L’information exhaustive des avantages et des inconvénients doit permettre à la patiente de participer au choix technique, l’indication finale lui revenant. La surveillance des prothèses est couplée à la surveillance oncologique et peut se résumer à l’examen clinique, avec prescription d’une imagerie par résonance magnétique à la moindre anomalie.
Références
1. Rouanet P. Place actuelle de la reconstruction mammaire en oncologie. Gynecol Obstet Fertil 2002;30:985-93.
2. Clough KB, Acosta-Marin V, Nos C, et al. Rates of neoadjuvant chemotherapy and oncoplastic surgery for breast cancer surgery: a french national survey. Ann Surg Oncol 2015;22:3104-11.
3. Al-Ghazal SK, Fallowfield L, Blamey RW. Comparison of psychological aspects and patient satisfaction following breast conserving surgery, simple mastectomy and breast reconstruction. Eur J Cancer 2000;36:1938-43.
4. Binder JP, Servant JM, Revol M. Lambeaux perforants. EMC - Techniques chirurgicales - Chirurgie plastique, reconstructrice et esthétique 2012;7:1-12.
5. Koshima I, Soeda S. Inferior epigastric artery skin flaps without rectus abdominis muscle. Br J Plastic Surg 1989;42:645-8.
6. Allen RJ, Treece P. Deep inferior epigastric perforator flap for breast reconstruction. Ann Plastic Surg 1994;32:32-8.
7. Société française de sénologie et pathologie mammaire. Éléments complémentaires pour la pratique clinique concernant les lymphomes anaplasiques à grandes cellules survenant sur prothèse mammaire. http://bit.ly/30BXwfc
2. Clough KB, Acosta-Marin V, Nos C, et al. Rates of neoadjuvant chemotherapy and oncoplastic surgery for breast cancer surgery: a french national survey. Ann Surg Oncol 2015;22:3104-11.
3. Al-Ghazal SK, Fallowfield L, Blamey RW. Comparison of psychological aspects and patient satisfaction following breast conserving surgery, simple mastectomy and breast reconstruction. Eur J Cancer 2000;36:1938-43.
4. Binder JP, Servant JM, Revol M. Lambeaux perforants. EMC - Techniques chirurgicales - Chirurgie plastique, reconstructrice et esthétique 2012;7:1-12.
5. Koshima I, Soeda S. Inferior epigastric artery skin flaps without rectus abdominis muscle. Br J Plastic Surg 1989;42:645-8.
6. Allen RJ, Treece P. Deep inferior epigastric perforator flap for breast reconstruction. Ann Plastic Surg 1994;32:32-8.
7. Société française de sénologie et pathologie mammaire. Éléments complémentaires pour la pratique clinique concernant les lymphomes anaplasiques à grandes cellules survenant sur prothèse mammaire. http://bit.ly/30BXwfc