Argumenter l'attitude thérapeutique et planifier le suivi du patient.
Définition
Physiopathologie
La physiopathologie du reflux gastro-œsophagien est multifactorielle, alliant des anomalies de la barrière anti-reflux, des anomalies de la clairance et de la sensibilité œsophagienne. Les relaxations transitoires (spontanées) du sphincter inférieur de l’œsophage (RTSIO), phénomène physiologique permettant de diminuer la pression intragastrique, représentent le principal mécanisme de reflux. Une hypotonie permanente du sphincter inférieur de l’œsophage peut également être à l’origine de reflux.
Pour une même exposition acide (temps de contact entre l’acide et la muqueuse œsophagienne), les symptômes ne sont pas identiques selon les individus. Certains patients ressentent de manière importante et douloureuse une exposition acide minime ou normale, ce qui témoigne d’une hypersensibilité œsophagienne. Le rôle physiopathologique de la hernie hiatale dans le reflux gastro-œsophagien est important, même s’il a longtemps été surestimé. La hernie hiatale affecte directement ou accentue les autres mécanismes physiopathologiques du reflux gastro-œsophagien, expliquant qu’elle soit plus fréquemment associée avec des symptômes sévères et/ou des lésions muqueuses. Elle n’est cependant ni nécessaire ni suffisante au diagnostic de reflux gastro-œsophagien .
Bien que le traitement soit fondé sur la diminution de la sécrétion acide, il n’est pas observé une hyperacidité gastrique chez les patients souffrant de reflux gastro-œsophagien.
Épidémiologie
Histoire naturelle et complications
œsophagite peptique et sténose peptique
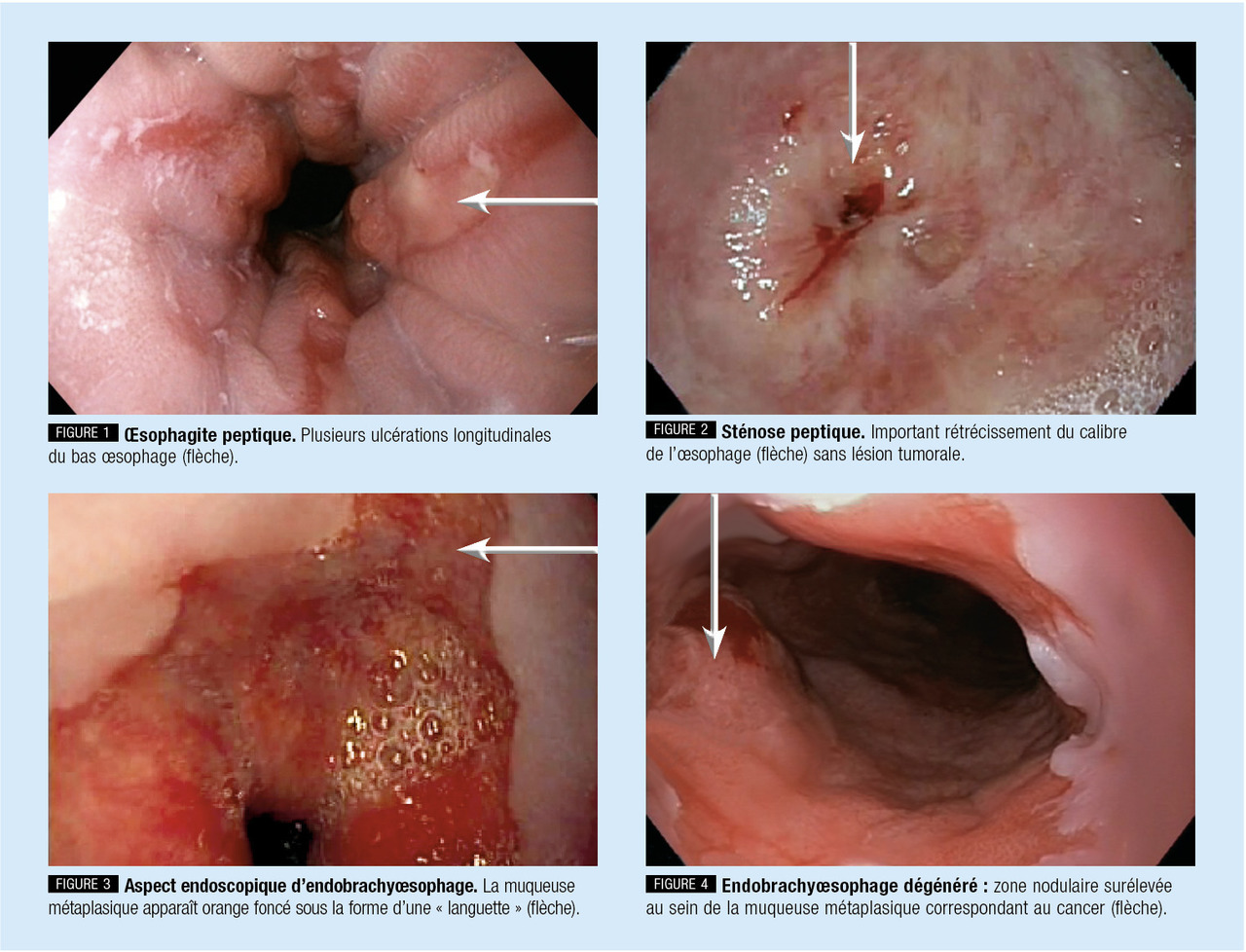
La réparation anormalement fibreuse des lésions inflammatoires d’œsophagite peut créer une sténose œsophagienne peptique
Endobrachyœsophage et adénocarcinome œsophagien
Elle peut évoluer vers la dysplasie, de bas grade puis de haut grade, faisant le lit de l’adénocarcinome œsophagien (AE)
Le développement de l’endobrachyœsophage nécessite une exposition prolongée à l’acide, l’âge moyen de découverte se situe donc aux alentours de 50 ans. C’est une affection asymptomatique, son diagnostic est endoscopique et impose une confirmation histologique (présence de métaplasie intestinale). Il peut être découvert au cours d’un bilan de reflux gastro-œsophagien ou de manière fortuite chez un patient n’ayant aucun symptôme de reflux gastro-œsophagien, dans la moitié des cas.
Le reflux gastro-œsophagien, par l’endobrachyœsophage, est le facteur de risque principal de l’adénocarcinome œsophagien. Un adénocarcinome œsophagien doit être suspecté devant une dysphagie, une altération de l’état général, surtout chez un patient connu pour un reflux gastro-œsophagien ancien. En endoscopie, on trouvera une lésion ulcérée et/ou bourgeonnante, volontiers sténosante, saignant au contact.
Diagnostic
Signes typiques de relux gastro-œsophagien
Ce sont le pyrosis, les régurgitations et le syndrome postural. Le pyrosis est défini comme une brûlure rétrosternale ascendante, il a une spécificité de 90 % pour le diagnostic de reflux gastro-œsophagien. Les régurgitations correspondent à la sensation d’une remontée de liquide acide ou non dans la bouche ou l’hypopharynx, sans effort de vomissement préalable. Le fait que les symptômes soient accentués à la flexion antérieure du tronc est appelé syndrome postural.Signes atypiques de reflux gastro-œsophagien
Le reflux gastro-œsophagien peut se manifester par une toux chronique, un asthme difficile à contrôler, des érosions dentaires ou des symptômes ORL comme un enrouement, une laryngite chronique. Les symptômes ORL pourraient résulter de lésions directes de la muqueuse laryngée et pharyngée par des épisodes de reflux atteignant au moins le tiers supérieur de l’œsophage. Cependant, l’imputabilité du reflux gastro-œsophagien dans ces symptômes pulmonaires ou ORL reste discutée, et une association fortuite doit être évoquée, surtout en l’absence de symptômes typiques. La preuve d’un reflux gastro-œsophagien devra être établie grâce à la fibroscopie œsogastroduodénale ou la pH-métrie, la concordance symptômes-reflux en pH-métrie étant un argument fort pour juger de la responsabilité du reflux gastro-œsophagien.
De la même façon, l’asthme et le reflux gastro-œsophagien sont fréquemment associés, sans qu’un lien de causalité puisse être affirmé, même si des boucles réflexes vagales ou des micro- inhalations ont été incriminées. À l’heure actuelle, il n’est pas recommandé de traiter les patients asthmatiques par inhibiteurs de la pompe à protons en l’absence d’argument formel, notamment pH-métrique en faveur d’un reflux gastro-œsophagien.
Examens complémentaires
Devant des signes typiques et en l’absence de signes d’alarme, le diagnostic de reflux gastro-œsophagien est clinique et ne nécessite aucun examen complémentaire.Fibroscopie œsogastroduodénale
Elle permet de rechercher un diagnostic différentiel ou des complications.Les indications de la fibroscopie œsogastroduodénale sont les suivantes : symptômes atypiques isolés ; signes d’alarme : perte de poids, anémie, dysphagie, hémorragie digestive ; facteurs de risque d’endobrachyœsophage et d’adénocarcinome de l’œsophage : âge de début des symptômes > 50 ans ; résistance au traitement initial ou rechute précoce à l’arrêt du traitement.
En cas de reflux gastro-œsophagien non compliqué, la fibroscopie œsogastroduodénale est normale. Il n’y a pas de corrélation entre l’intensité des symptômes et les signes endoscopiques.
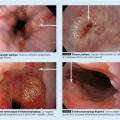
En présence d’une œsophagite ou d’une sténose peptique, le diagnostic positif de reflux gastro-œsophagien est affirmé, et la sévérité des lésions doit être classée selon la classification de Los Angeles
Un endobrachyœsophage peut être circonférentiel et/ou en languette, sous la forme d’une ligne Z irrégulière ou décalée vers le haut par rapport à la limite des plis gastriques et à la pince diaphragmatique, avec une muqueuse de type intestinale plane ou nodulaire. Les lésions sont décrites selon la classification de Prague, et les zones suspectes de métaplasie voire de dysplasie doivent être biopsiées.
pH-métrie œsophagienne et pH-impédancemétrie
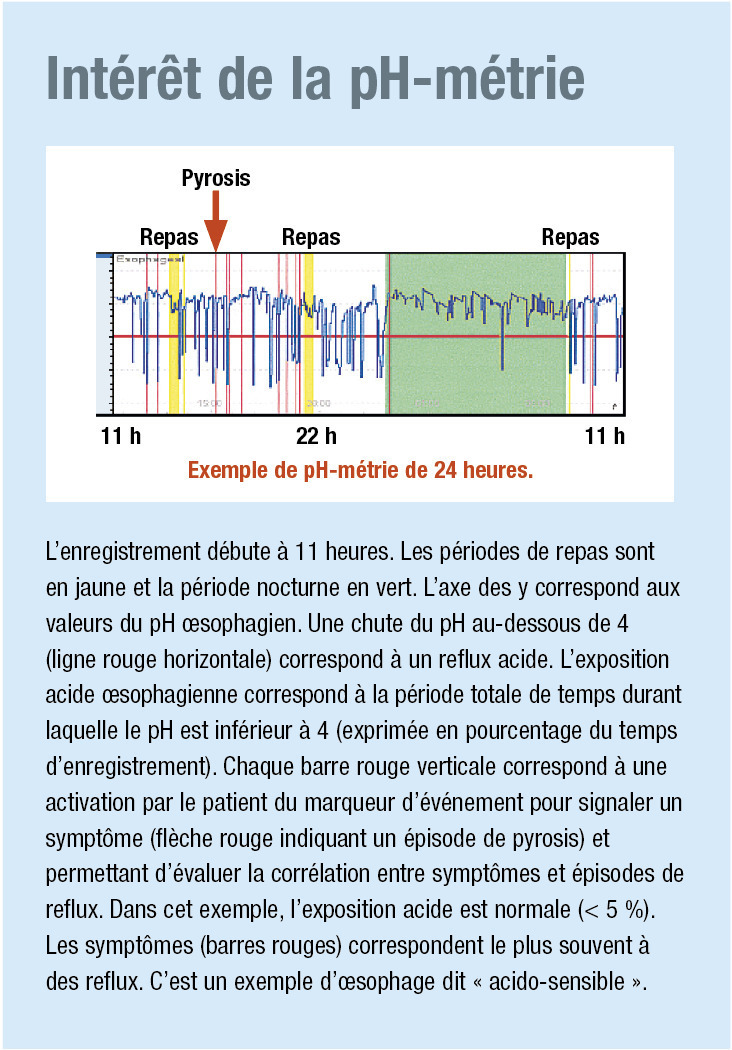
La pH-métrie établit le diagnostic positif du reflux gastro-œsophagien en détectant les épisodes de reflux, elle n’est donc pas nécessaire si les symptômes sont typiques ou s’il existe une œsophagite à la fibroscopie œso-gastro-duodénale. Elle est réalisée si les symptômes sont atypiques et la fibroscopie normale, si les symptômes résistent à un traitement bien conduit, ou en préopératoire si la fibroscopie était normale. Elle peut être filaire, réalisée grâce à une sonde placée dans la narine descendant jusqu’au bas œsophage, ou sans fil, avec une électrode unique placée dans le bas œsophage après repérage endoscopique. On mesure sur 24 heures, voire 48 heures pour la pH-métrie sans fil, les variations de pH dans le bas œsophage, transmises à un boîtier placé à la ceinture du patient et analysées informatiquement. Simultanément, le patient signale ses symptômes au niveau du boîtier, pour permettre d’analyser la concordance entre les symptômes ressentis et les épisodes de reflux. La pH-métrie sans fil est mieux tolérée, les enregistrements peuvent donc être plus longs, et le rendement diagnostique s’en trouve amélioré. Le diagnostic de reflux gastro-œsophagien est posé si l’œsophage est exposé à un pH < 4 plus de 5 % du temps ou si une association symptôme-reflux est mise en évidence.
La pH-impédancemétrie indique, en plus du pH, la nature liquide ou gazeuse du contenu de l’œsophage, ajoutant la détection de reflux non acides ou peu acides à celle des reflux acides. Le dispositif est le même que pour une pH-métrie filaire. Chez 1 patient sur 10 restant symptomatiques sous inhibiteur de la pompe à protons, elle permet de mettre en évidence un reflux acide persistant, et chez 1 patient sur 3, de relier les symptômes à des reflux non ou peu acides.
Manométrie œsophagienne et transit œso-gastro-duodénal
La manométrie œsophagienne explore la motricité de l’œsophage et mesure la pression du sphincter inférieur de l’œsophage. Au cours de la démarche diagnostique, elle sera uniquement utile en cas de dysphagie pour éliminer un trouble moteur de l’œsophage. En revanche, elle est indispensable en préopératoire, car les troubles moteurs œsophagiens sévères sont une contre- indication à la chirurgie anti-reflux.Le transit œso-gastro-duodénal peut éventuellement être utile en préopératoire pour rechercher une volumineuse hernie hiatale.
Diagnostic différentiel
Les troubles moteurs œsophagiens peuvent se manifester par des douleurs thoraciques et des régurgitations, rarement par un pyrosis. La dysphagie est très souvent présente. En cas de doute, une manométrie œsophagienne doit être réalisée.L’œsophagite à éosinophiles est une pathologie allergique, touchant surtout les hommes jeunes avec un terrain atopique. La dysphagie est souvent au premier plan, mais le pyrosis et les régurgitations peuvent exister. L’œsophage est normal en endoscopie (ou présente de subtiles anomalies), et le diagnostic est histologique.
Le carcinome épidermoïde de l’œsophage est le plus souvent diagnostiqué chez des patients de plus de 50 ans, ayant pour facteurs de risque une intoxication alcoolique et tabagique chronique, et pour symptômes une dysphagie et une altération de l’état général.
Le tableau clinique permet généralement d’éliminer les autres diagnostics différentiels digestifs (ulcère ou néoplasie gastrique, dyspepsie fonctionnelle, pathologie lithiasique biliaire) ou extradigestifs (insuffisance coronarienne). En cas de douleurs thoraciques isolées, l’urgence est d’éliminer une origine coronarienne.
Moyens thérapeutiques
Règles hygiéno-diététiques
Traitements médicamenteux
Traitements topiques : alginates, antiacides
Les alginates et les antiacides sont des traitements symptomatiques agissant comme des interfaces entre le contenu acide et la muqueuse œsophagienne. Les alginates (Gaviscon) forment une couche visqueuse au-dessus du contenu gastrique, ils sont potentiellement intéressants en postprandial pour cibler la « poche acide » non neutralisée par les aliments, localisée en région sous-cardiale. Les antiacides (Maalox, Rennie, etc.) combinent généralement du trisilicate de magnésium, de l’hydroxyde d’aluminium et du carbonate de calcium, et permettent de neutraliser temporairement l’acidité gastrique. Ils n’ont peu ou pas d’effets secondaires. Ils ne permettent pas la cicatrisation de la muqueuse.Anti-H2
Les anti-H2 (cimétidine, ranitidine, etc.) diminuent la sécrétion acide gastrique par leur effet antagoniste sur le récepteur H2 à l’histamine des cellules pariétales gastriques. Leur efficacité est moindre par rapport à celle des inhibiteurs de la pompe à protons à la fois sur le soulagement des symptômes et la cicatrisation œsophagienne. De plus, leur utilisation est limitée par un épuisement progressif de leur effet, ne permettant pas de les utiliser sur le long terme en prévention de la récidive. Ils gardent actuellement surtout une place chez l’enfant ou en alternative aux inhibiteurs de la pompe à protons.Inhibiteurs de la pompe à protons
Ils bloquent durablement la sécrétion d’ions H+ par la cellule pariétale gastrique, en se fixant par une liaison covalente irréversible à la pompe à protons H-K-ATPase. Ils doivent être pris 30 minutes avant un repas pour obtenir une concentration plasmatique maximale au début du repas où les pompes à protons se retrouvent sous forme activée à la surface des cellules pariétales. Il n’a pas été montré de différence significative entre les différentes molécules (oméprazole, ésoméprazole, lansoprazole, pantoprazole, rabéprazole).Les effets secondaires immédiats, céphalées ou diarrhée, sont peu fréquents. À long terme, ils exposent à un sur-risque de gastro- entérite infectieuse et de colite à Clostridium difficile, la sécrétion acide gastrique jouant un rôle antibactérien, et de fractures du col du fémur, probablement par malabsorption du calcium.
Ils sont le traitement de base du reflux gastro-œsophagien, notamment les formes modérées à sévères, et de ses complications. Ils permettent d’obtenir la cicatrisation des lésions œsophagiennes dans plus de 80 % des cas. La prescription d’inhibiteurs de la pompe à protons en traitement empirique chez l’adulte ne peut se faire qu’en cas de symptômes typiques de reflux gastro-œsophagien, au moins hebdomadaires, chez un patient de moins de 50 ans.
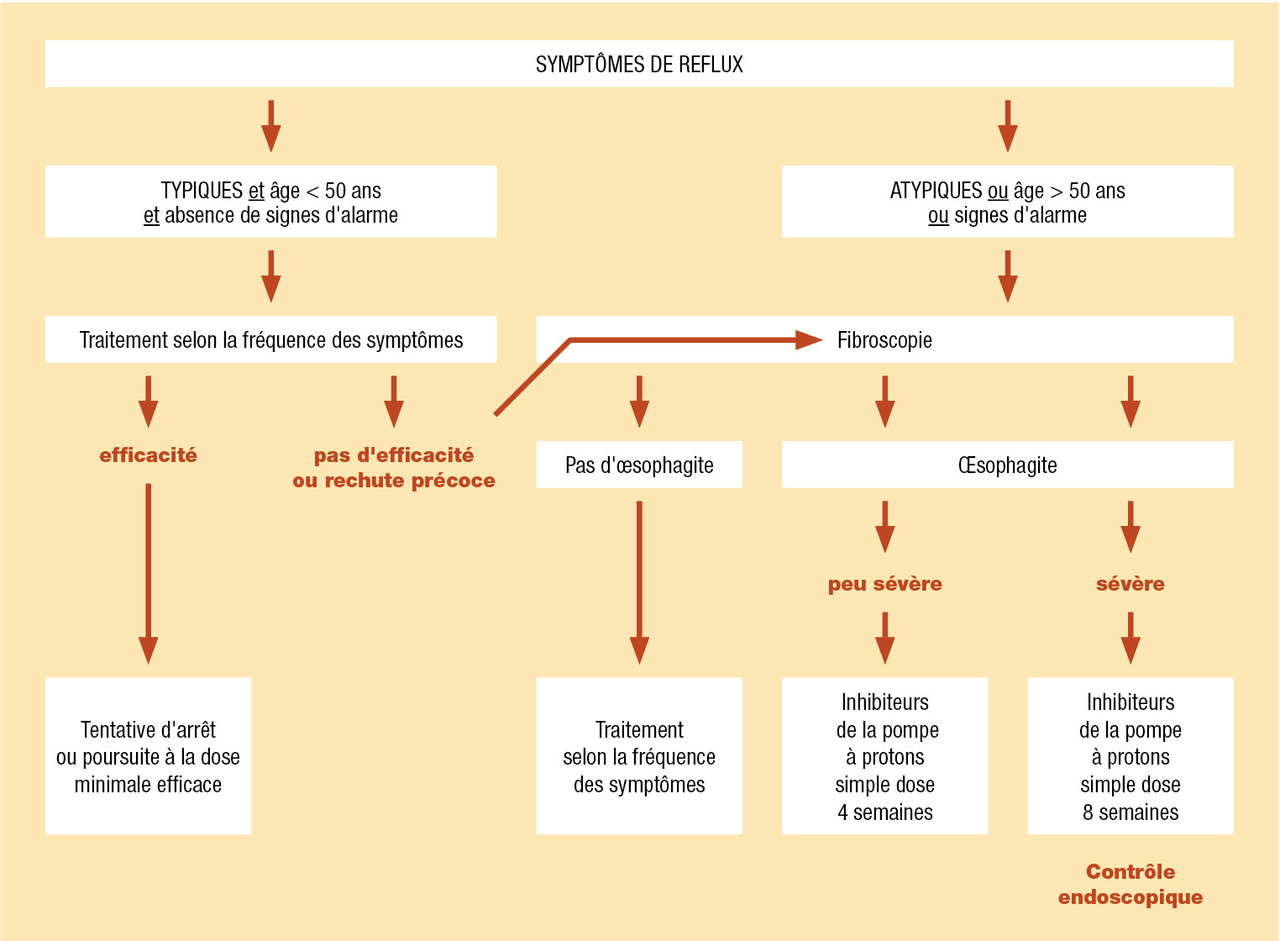
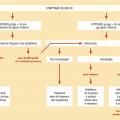
Stratégie thérapeutique (fig. 6)
Il n’a pas été prouvé que les traitements médicaux ou chirurgicaux diminuent le risque de survenue d’un endobrachyœsophage ou d’un adénocarcinome de l’œsophage.
Traitement d’un reflux gastro-œsophagien sans œsophagite peptique
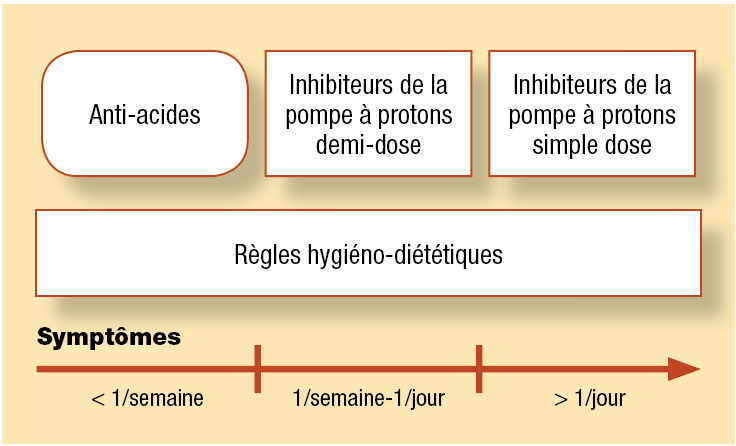
En cas de reflux gastro-œsophagien non compliqué, le traitement dépend de la fréquence des symptômes.Si les symptômes sont occasionnels (< 1 fois par semaine) et peu invalidants, les règles hygiéno-diététiques et un traitement topique à la demande peuvent suffire. Les inhibiteurs de la pompe à protons ne sont pas recommandés, puisque leur effet n’est pas immédiat.
Si les symptômes sont fréquents (> 1 fois par semaine), mais typiques, et qu’il n’y a pas de signes d’alarme, il est recommandé d’introduire un traitement par inhibiteurs de la pompe à protons à demi-dose associé aux règles hygiéno-diététiques. Au bout de 15 jours, si les symptômes ne sont pas contrôlés, les inhibiteurs de la pompe à protons peuvent être donnés à simple dose. Si les symptômes sont pluriquotidiens et altèrent la qualité de vie du patient, ils peuvent être débutés d’emblée à simple dose. En cas d’efficacité, ils sont poursuivis 4 semaines.
Au bout de 4 semaines, le traitement par inhibiteurs de la pompe à protons peut être poursuivi à demi-dose puis arrêté si le patient est asymptomatique. Si les symptômes réapparaissent à distance, ce qui est le cas pour 2 patients sur 3, on peut poursuivre le traitement par inhibiteurs de la pompe à protons par cures courtes séquentielles, en cas de symptômes, ou en continu à la dose minimale efficace observée par le patient. En cas de poussées symptomatiques occasionnelles, les antiacides peuvent être utiles.
Traitement de symptômes ORL ou pulmonaires
L’efficacité des inhibiteurs de la pompe à protons n’a pas été prouvée sur les symptômes ORL ou pulmonaires. À l’heure actuelle, il n’est pas recommandé de traiter par inhibiteurs de la pompe à protons les patients asthmatiques en l’absence de preuve formelle de reflux gastro-œsophagien (œsophagite ou pH-métrie positive).Traitement d’un reflux gastro-œsophagien avec œsophagite peptique
En cas d’œsophagite grade A ou B de la classification de Los Angeles, un traitement par inhibiteurs de la pompe à protons simple dose peut être prescrit pour 4 à 8 semaines. Comme dans le reflux gastro-œsophagien non compliqué, la poursuite des inhibiteurs de la pompe à protons est décidée en fonction des symptômes.En cas d’œsophagite sévère, grade C ou D, il faut traiter par inhibiteurs de la pompe à protons simple dose pendant 8 semaines, puis vérifier la cicatrisation par une fibroscopie œso-gastro-duodénale. En cas de non-cicatrisation et de bonne observance, des inhibiteurs de la pompe à protons double dose pendant 8 semaines peuvent être prescrits (hors AMM). En cas de symptômes et lésions œsophagiennes récidivant quasi systématiquement à l’arrêt, ces derniers doivent être poursuivis au long cours, à dose minimale efficace.
En cas de sténose peptique, les inhibiteurs de la pompe à protons doivent être poursuivis à pleine dose au long cours. Si la sténose est symptomatique, on associe au traitement médical des dilatations endoscopiques. La chirurgie est exceptionnellement indiquée.
Absence de réponse au traitement
Il faut également savoir remettre en cause le diagnostic si le reflux n’a jamais été prouvé par une fibroscopie œso-gastro- œsophagienne ou par une pH-métrie.
La compréhension de la physiopathologie du reflux gastro- œsophagien s’est enrichie ces dernières années, mais cela ne s’est pas traduit pour l’instant par le développement de nouveaux traitements ciblant la motricité ou la sensibilité œsophagienne.
Prise en charge de l’endobrachyœsophage
L’endobrachyœsophage asymptomatique ne doit pas être traité par inhibiteurs de la pompe à protons.
Chirurgie du reflux gastro-œsophagien
La chirurgie du reflux gastro-œsophagien vise à renforcer la barrière anti-reflux par une fundoplicature, technique consistant à replier une portion d’estomac proximal autour du bas œsophage de façon à former une valve, circonférentielle (intervention de Nissen) ou partielle (intervention de Toupet), préférentiellement par voie cœlioscopique.
Les indications de chirurgie doivent être réfléchies, car les complications sont fréquentes. Les meilleurs candidats sont les patients dont les symptômes sont soulagés par les inhibiteurs de la pompe à protons mais qui ne les tolèrent pas ou ne souhaitent pas un traitement au long cours. Un bilan préopératoire rigoureux est indispensable pour éliminer une contre-indication et affirmer le reflux gastro-œsophagien : fibroscopie œso-gastro- duodénale, voire pH-métrie, manométrie œsophagienne.
Les complications fréquentes sont la dysphagie (5-10 %), des manifestations fonctionnelles telles que l’impossibilité d’éructer, des flatulences, voire des symptômes dyspeptiques plus invalidants. La dysphagie peut être passagère ou persister plusieurs mois après la chirurgie. Si elle apparaît à distance, il faut suspecter une dysfonction du montage chirurgical. Dans les 3 ans suivant la chirurgie, 7 % des patients nécessiteront une reprise chirurgicale.
Populations particulières
Chez le nourrisson
Chez les nourrissons, la remontée du contenu gastrique jusque dans la bouche est très fréquente, on parle de « régurgitations ». Elles surviennent chez la moitié des enfants, sans conséquence clinique ou endoscopique, et disparaissent spontanément avant 1 an dans 90 % des cas grâce à la maturation de la jonction œsogastrique, la verticalisation de l’enfant et la diversification alimentaire. On ne parle de reflux gastro-œsophagien que quand ces épisodes de reflux ont un retentissement clinique ou endoscopique. Dans la majorité des cas, les régurgitations sont non compliquées, ne nécessitent aucun traitement, et il faut rassurer les patients quant à leur absence de gravité.Un reflux gastro-œsophagien doit être évoqué en cas de régurgitations associées à une mauvaise croissance staturo-pondérale ou à une irritabilité post-prandiale, voire un refus de se nourrir. En cas de vomissements chroniques, un examen clinique soigneux doit écarter une maladie neurologique, une maladie métabolique ou une obstruction digestive, notamment une sténose du pylore. Les autres diagnostics différentiels sont la maladie cœliaque et l’allergie aux protéines de lait de vache.
En l’absence de signes d’alarme, la prise en charge est fondée sur la mise en place de règles hygiéno-diététiques : poursuivre l’allaitement maternel ou, en cas d’allaitement artificiel, fractionner les prises alimentaires, essayer un lait épaissi voire un lait sans protéines de lait de vache ni de soja ; placer le nourrisson en position semi-assise pendant les 20 minutes suivant les repas. Les traitements médicamenteux doivent être évités dans la mesure où il n’y a pas de preuve de leur efficacité sur les symptômes, notamment de type irritabilité ou troubles du sommeil. En cas d’absence d’efficacité de ces règles, on peut essayer un traitement par alginates pour 15 jours. S’il est efficace, il peut être poursuivi, en ménageant des pauses thérapeutiques pour vérifier la persistance du reflux.
Les examens complémentaires sont rarement nécessaires : une fibroscopie œso-gastro-duodénale est indiquée si les symptômes résistent aux règles hygiéno-diététiques et à un traitement empirique bien conduit ou en cas de signes d’alarme (hémorragie digestive, carence martiale).
En cas d’œsophagite modérée ou de symptômes persistant malgré les règles hygiéno-diététiques et les alginates, un traitement ciblant la sécrétion gastrique peut être proposé pendant 15 jours. S’il est efficace, il peut être continué pendant 3 à 6 mois puis réévalué. En cas d’œsophagite sévère, un traitement doit être pris pendant 3 à 6 mois. Les inhibiteurs de la pompe à protons sont à privilégier par rapport aux anti-H2 car leur effet sur la cicatrisation œsophagienne est supérieur.
Chez l’enfant et l’adolescent
Le reflux gastro-œsophagien est moins fréquent chez l’enfant que chez l’adulte, mais l’incidence est également en augmentation dans cette population. Il n’est pas clairement établi que le reflux chez le nourrisson ou l’enfant soit prédictif d’un reflux gastro- œsophagien chez l’adulte.Chez l’enfant et l’adolescent, les symptômes sont les mêmes que chez l’adulte.
Les diagnostics différentiels principaux sont les maladies neurologiques, les malformations digestives et les maladies métaboliques. On peut y ajouter le syndrome de rumination et les diagnostics différentiels de l’adulte. La stratégie d’explorations et le traitement se rapprochent de ceux recommandés chez l’adulte.
Grossesse et allaitement
Pendant la grossesse, il faut favoriser les règles hygiéno-diététiques et les traitements topiques. En cas d’absence d’amélioration, on privilégie les anti-H2 aux inhibiteurs de la pompe à protons.Hernie hiatale
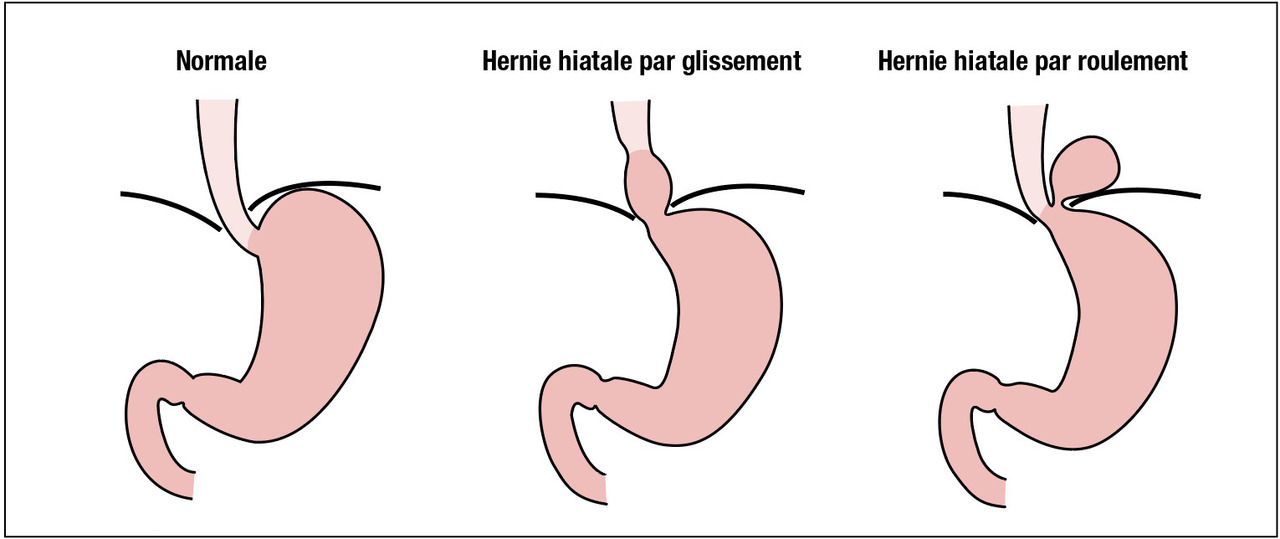
Il existe deux types de hernie hiatale : la hernie hiatale par glissement, la plus fréquente, est une migration axiale de la jonction œsogastrique dans le thorax, suivie par le fundus. C’est un phénomène fréquent, retrouvé chez environ 50 % des patients ayant un reflux gastro-œsophagien. Cependant, tous les sujets ayant une hernie hiatale ne souffrent pas de reflux gastro-œsophagien. Son rôle physiopathologique dans le reflux gastro-œsophagien est important, même s’il a longtemps été surestimé. Le diagnostic le plus fiable est fait à la manométrie œsophagienne, mais la hernie hiatale peut être également visualisée à la fibroscopie œso-gastro-duodénale ou au transit œso-gastro-duodénal. Hormis le reflux gastro-œsophagien, la principale complication de la hernie hiatale est l’ulcération liée aux frottements au niveau du collet herniaire. Le traitement est chirurgical, mais n’est indiqué qu’en cas de reflux gastro-œsophagien avec critères chirurgicaux. Il n’y a aucune indication chirurgicale en cas de hernie hiatale asymptomatique.
Dans le cas d’une hernie hiatale par roulement, la jonction œsogastrique reste en place au niveau du diaphragme, mais le fundus remonte le long de l’œsophage dans le médiastin. Ce type de hernie hiatale ne prédispose pas au reflux gastro-œsophagien puisque la barrière anti-reflux garde son intégrité.
Le diagnostic différentiel principal est la hernie diaphragmatique, qui correspond au passage de la totalité de l’estomac ou d’autres organes digestifs à travers le hiatus diaphragmatique.•
Le reflux gastro-œsophagien est une pathologie fréquente, touchant 10 à 20 % des adultes en France. Le surpoids et l’obésité sont les facteurs de risque principaux du reflux gastro-œsophagien.
Le reflux gastro-œsophagien est un facteur de risque d’endobrachyœsophage et d’adénocarcinome œsophagien.
La fibroscopie œso-gastro-duodénale est indiquée en cas de signes d’alarme, de facteurs de risque de complications ou de symptômes atypiques isolés.
Chez le nourrisson et l’enfant, la prise en charge est fondée sur les règles hygiéno-diététiques.
La hernie hiatale par glissement favorise le reflux gastro-œsophagien mais ne doit pas être traitée chirurgicalement en l’absence d’indication chirurgicale fondée sur les critères habituels de prise en charge du reflux gastro-œsophagien.
Recommandations de bonne pratique. Les anti-sécrétoires chez l’adulte. AFSSAPS 2007.
Bon usage du médicament. Les IPP. HAS 2009.
Conseil de pratique : Prise en charge du reflux gastro-œsophagien. SNFGE/GFNG, 2012.
POINTS FORTS À RETENIR
Le reflux gastro-œsophagien est une pathologie fréquente, touchant 10 à 20 % des adultes en France. Le surpoids et l’obésité sont les facteurs de risque principaux du reflux gastro-œsophagien.
Le reflux gastro-œsophagien est un facteur de risque d’endobrachyœsophage et d’adénocarcinome œsophagien.
La fibroscopie œso-gastro-duodénale est indiquée en cas de signes d’alarme, de facteurs de risque de complications ou de symptômes atypiques isolés.
Chez le nourrisson et l’enfant, la prise en charge est fondée sur les règles hygiéno-diététiques.
La hernie hiatale par glissement favorise le reflux gastro-œsophagien mais ne doit pas être traitée chirurgicalement en l’absence d’indication chirurgicale fondée sur les critères habituels de prise en charge du reflux gastro-œsophagien.

 Encadrés
Encadrés