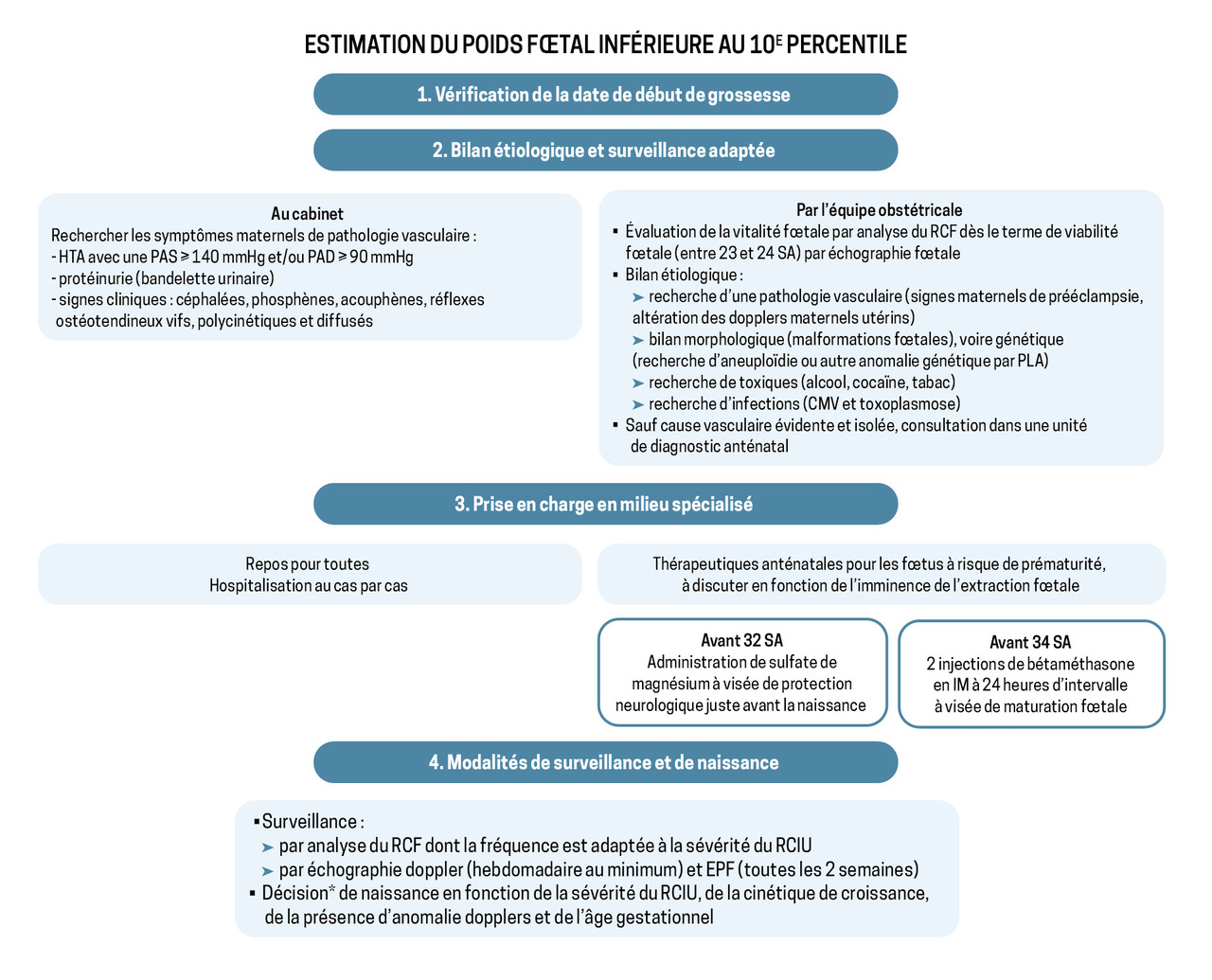
Par définition, le retard de croissance intra-utérin (RCIU) et le petit poids pour l’âge gestationnel (PAG) sont des situations obstétricales fréquentes puisque, au sein de la population générale, 10 % des fœtus ont une estimation de poids fœtal inférieur au 10e percentile. Le défi consiste à identifier, à la suite de ce dépistage, les fœtus affectés par un retard de croissance pathologique, donc à risque augmenté de morbi-mortalité, afin de proposer une prise en charge adéquate (fig. 1).
PAG et RCIU : de quoi parle-t-on ?
Le PAG est défini par une estimation du poids fœtal inférieure au 10e percentile. Il est dit sévère si l’estimation de poids fœtal est inférieure au 3e percentile.
Le RCIU (équivalent français de Fetal Growth Restriction [FGR] ou Intra-Uterine Growth Retardation [IUGR]) correspond à la situation d’un fœtus qui ne parvient pas à atteindre son potentiel de croissance, traduisant l’existence d’une pathologie sous-jacente. Il est défini par une estimation de poids fœtal inférieure au 10e percentile, associée à des arguments en faveur d’un défaut pathologique de croissance : arrêt ou infléchissement de la croissance de manière longitudinale, anomalies au doppler, diminution des mouvements actifs fœtaux, diminution de la quantité de liquide amniotique (oligo-amnios ou anamnios).1,2
Estimation du poids fœtal : consensus sur la méthode de calcul
L’estimation de poids fœtal est obtenue par mesure échographique de plusieurs biométries fœtales (fig. 2) : le périmètre céphalique (PC), le périmètre abdominal (PA) et la longueur fémorale (LF). Bien que standardisées, ces mesures font l’objet d’une importante variabilité inter- et intra-observateurs.3
De nombreuses formules mathématiques de calcul de poids fœtal existent, aboutissant à des valeurs pouvant être différentes. En revanche, le choix des courbes est sujet à controverse (encadré). Les sociétés savantes françaises concernées par l’échographie obstétricale et fœtale, à savoir le Collège national des gynécologues et obstétriciens français (CNGOF), le Collège français d’échographie fœtale (CFEF) et la Société francophone d’imagerie pédiatrique et prénatale (SFIPP), se sont accordées pour utiliser une formule correspondant au mieux à notre population, c’est-à-dire en adéquation avec le poids néonatal. Il s’agit de la formule de Hadlock : estimation du poids fœtal (EPF) = 1,326 + (0,0107 × PC) + (0,0438 × PA) + (0,158 × LF) - [(0,00326 × (PA × LF)].4
Par ailleurs, la vérification de la date de début de grossesse est essentielle – une erreur de terme pouvant faire conclure à tort à un retard de croissance. La date de début de grossesse est obtenue par mesure de la longueur cranio-caudale en échographie entre 11 et 14 semaines d’aménorrhée (SA) si la grossesse est obtenue spontanément, ou par datation précise de la fécondation dans le cadre d’une procréation médicalement assistée.
RCIU : deuxième cause de mortalité périnatale !
Le RCIU est associé à des complications anténatales ainsi qu’à des complications post-natales à court et long termes. Il s’agit de la deuxième cause de mortalité périnatale, avec un risque quatre fois plus élevé de décès périnatal ; il est responsable d’environ 30 % des morts fœtales in utero. C’est également la cause la plus fréquente d’accouchements prématurés et d’asphyxie intrapartum.5
En post-natal, le RCIU est associé à un risque de troubles neurodéveloppementaux que sont les altérations du volume cérébral, de la myélinisation et de la structure corticale. Les nouveau-nés ayant un RCIU sont également plus à risque de développer des complications liées à la prématurité, à type de syndrome de détresse respiratoire et d’entérocolite nécrosante, pour un âge gestationnel donné.
En ce qui concerne les conséquences à long terme, les enfants d’âge scolaire nés avec un retard de croissance ont des taux plus élevés de troubles de la cognition, de la mémoire, de l’attention et de la motricité globale. À l’âge adulte, le RCIU est associé à une prévalence accrue d’hypertension artérielle, de maladie coronarienne, de diabète, de syndrome métabolique et de dyslipidémie.6
Trois causes principales de RCIU
Origine vasculaire
Les causes vasculaires, également appelées insuffisance placentaire ou anomalies de la fonction placentaire, concernent la moitié des RCIU. Il s’agit du spectre des maladies hypertensives maternelles, dont fait partie la prééclampsie.
Deux entités de RCIU vasculaires sont décrites, avec une physiopathologie et une évolution différentes.
RCIU vasculaires précoces
Ils surviennent avant 32 SA et représentent environ 20 à 30 % des cas ; leur physiopathologie correspond à une anomalie de remodelage vasculaire myométriale et villositaire. Le RCIU est sévère et le risque de mortalité fœtale intra-utérine (MFIU) survient tardivement par rapport au diagnostic de RCIU. Il s’agit d’un fœtus de faible poids avec peu de besoins nutritionnels, dont l’acidose fœtale se traduit par des anomalies dopplers sévères (doppler ombilical nul ou en reverse flow ; anomalie du doppler au niveau du ductus venosus).
RCIU vasculaires tardifs
Les RCIU tardifs, survenant après 32 SA, représentent 70 à 80 % des cas ; leur physiopathologie correspond à une sénescence placentaire. Le RCIU est modéré et le risque de MFIU survient plus précocement après le diagnostic de RCIU. Il s’agit d’un ralentissement de croissance chez un fœtus de poids plus élevé, avec des besoins nutritionnels importants. Une diminution des résistances au doppler cérébral associée à une augmentation des résistances au doppler ombilical définissant la redistribution cérébroplacentaire est le reflet de l’hypoxie fœtale.
Origines chromosomique et génétique
Parmi les origines chromosomique et génétique, on retrouve en premier lieu la triploïdie et la trisomie 18, constituant environ 10 % des RCIU. L’amniocentèse, ou ponction de liquide amniotique, permet l’analyse du caryotype et la recherche d’un déséquilibre chromosomique.
Origine infectieuse
Les infections à cytomégalovirus (CMV) et la toxoplasmose sont les plus fréquentes. Une sérologie CMV peut être demandée en pratique courante en cas de dépistage de RCIU. En cas de sérologie toxoplasmique négative, une surveillance mensuelle est recommandée et permet de détecter précocement les séroconversions. La recherche du CMV par PCR ainsi que celle du parasite Toxoplasma gondii peuvent être réalisées dans le liquide amniotique par amniocentèse.
Autres causes
Les causes toxiques évitables sont liées principalement à la consommation de tabac, de cocaïne et d’alcool. La malnutrition et un faible indice de masse corporelle constituent également des causes de RCIU.7
Un grand nombre d’éléments pronostiques
Les éléments pronostiques de survie d’un fœtus en RCIU sont nombreux :
- âge gestationnel à la naissance ;
- poids de naissance ;
- lieu de naissance : il existe différentes structures de soins néonatals en fonction des besoins des enfants nés prématurément. Ainsi, un enfant né avant 32 SA requiert des soins de réanimation néonatale en maternité de type 3. S’il est pris en charge directement à la naissance dans une maternité ayant un service de réanimation néonatale, sa naissance est dite « inborn » et il a de meilleures chances de survie. A contrario, un enfant dont la prise en charge a débuté dans une maternité dont la structure n’était pas adaptée et ayant été transféré secondairement en réanimation néonatale est dit « outborn » et est plus à risque de complications néonatales ;
- sexe : le sexe féminin est un facteur protecteur ;
- traitements anténataux : en cas de prématurité, des thérapeutiques sont indiquées afin de diminuer la morbi-mortalité néonatale. La réalisation d’une cure de corticothérapie par bétaméthasone à visée de maturation fœtale est indiquée avant 34 SA (2 injections en intramusculaire à 24 heures d’intervalle). L’administration de sulfate de magnésium (en intraveineux juste avant la naissance) à visée de protection neurologique fœtale est indiquée avant 32 SA ;
- degré d’asphyxie in utero : complexe à apprécier, le risque d’asphyxie in utero est surveillé par l’analyse du rythme cardiaque fœtal et par échographie.
Deux modalités de surveillance d’un fœtus suspecté de RCIU
Les deux modalités principales de surveillance sont l’analyse du rythme cardiaque fœtal et l’échographie fœtale.
La mesure du rythme cardiaque est réalisée à l’aide d’un cardiotocographe qui enregistre des séquences minimales de vingt minutes. Son analyse est à la fois subjective et informatisée. La fréquence de cette surveillance peut varier d’une fois par semaine à deux fois par jour, en fonction de la sévérité du RCIU.
L’échographie permet d’apprécier la quantité de liquide amniotique, les mouvements actifs fœtaux, les dopplers fœtaux ainsi que la dynamique de croissance fœtale. L’estimation du poids fœtal est réalisée au minimum à deux semaines d’intervalle, ce qui permet de diminuer les faux positifs de cassure ou de ralentissement de croissance. Les dopplers fœtaux comportent celui de l’artère ombilicale estimant la résistance placentaire, le doppler cérébral au niveau de l’artère cérébrale moyenne évaluant le degré de vasodilatation des artères cérébrales, et le doppler du ductus venosus, dont l’altération signe une gravité extrême.8
Que dire à vos patientes ?
- Le retard de croissance intra-utérin (RCIU) est une pathologie fréquente de la grossesse nécessitant une prise en charge spécifique.
- Une prise en charge adaptée comporte la recherche de la cause du RCIU, puis une surveillance rapprochée dans un milieu spécialisé.
- Le repos est recommandé. Il ne s’agit pas d’un repos strict au lit, mais d’une réduction de l’activité avec la possibilité de recourir à un arrêt de travail.
- La décision de naissance dépend de l’avancée de la grossesse, de la sévérité du RCIU et de l’état de santé maternel. Cette décision est prise dès lors que la grossesse est davantage à risque pour le fœtus que de le faire naître.
Sujet de controverse : quelles courbes utiliser dans le cadre du dépistage de l’estimation du poids fœtal ?
Il existe de nombreuses courbes de poids fœtal permettant d’obtenir le percentile. Une même valeur absolue de poids fœtal peut ne pas correspondre au même percentile si l’on se place sur deux courbes différentes.
Deux approches différentes d’élaboration des courbes de poids fœtal sont possibles :
- une approche personnalisée dans laquelle les courbes intègrent le potentiel de croissance du fœtus, en prenant en compte le sexe du fœtus ainsi que le poids et la taille maternels. Cette approche n’a pas été retenue, n’ayant pas fait la preuve de son intérêt en pratique clinique dans le dépistage ;
- une approche prescriptive, s’appuyant sur un échantillon sélectionné de population à bas risque. Si les deux sociétés savantes françaises d’échographies obstétricale et fœtale se sont accordées sur l’utilisation de courbe prescriptive (Intergrowth- 21st et OMS) plutôt que personnalisée dans le cadre du dépistage, elles ont émis deux recommandations différentes sur le choix de ces courbes prescriptives : Intergrowth- 21st est recommandée par le Collège français d’échographie fœtale ; la courbe OMS par le CNGOF.
2. Melamed N, Baschat A, Yinon Y, et al. FIGO (International Federation of Gynecology and Obstetrics) initiative on fetal growth: Best practice advice for screening, diagnosis, and management of fetal growth restriction. Int J Gynecol Obstet 2021;152(S1):3-57.
3. Sarris I, Ioannou C, Chamberlain P, et al. Intra- and interobserver variability in fetal ultrasound measurements. Ultrasound Obstet Gynecol Off J Int Soc Ultrasound Obstet Gynecol 2012;39(3):266-73.
4. Melamed N, Yogev Y, Meizner I, et al. Sonographic Fetal Weight Estimation: Which Model Should Be Used? J Ultrasound Med 2009;28(5):617-29.
5. Nardozza LMM, Caetano ACR, Zamarian ACP, et al. Fetal growth restriction: current knowledge. Arch Gynecol Obstet 2017;295(5):1061-77.
6. Miller SL, Huppi PS, Mallard C. The consequences of fetal growth restriction on brain structure and neurodevelopmental outcome. J Physiol 2016;594(4):807-23.
7. Audette MC, Kingdom JC. Screening for fetal growth restriction and placental insufficiency. Semin Fetal Neonatal Med 2018;23(2):119-25.
8. Lees CC, Romero R, Stampalija T, et al. The diagnosis and management of suspected fetal growth restriction: an evidence-based approach. Am J Obstet Gynecol 2022;226(3):366-78.

 Encadrés
Encadrés