La surdité brusque est définie le plus souvent, en l’absence de consensus, par la survenue rapide, en moins de 24 heures, d’une hypoacousie neurosensorielle (surdité de perception, sans anomalie du tympan ni des osselets), isolée (pas de vertiges ni de signes neurologiques associés), d’allure idiopathique. Des acouphènes sont possibles dès le début, voire avant l’apparition du trouble. Le patient n’a pas d’antécédent otologique notable (otospongiose, otite chronique…). Si sa cause est inconnue par définition, il existe plusieurs hypothèses : virale, vasculaire, auto-immune, génétique.
Sont donc exclues les surdités de perception d’apparition brutale dont l’origine est évidente (traumatisme crânien, labyrinthite compliquant une otite moyenne aiguë [OMA]…) ainsi que les atteintes fluctuantes (installation lente, évolution marquée par des périodes d’aggravation et d’amélioration).
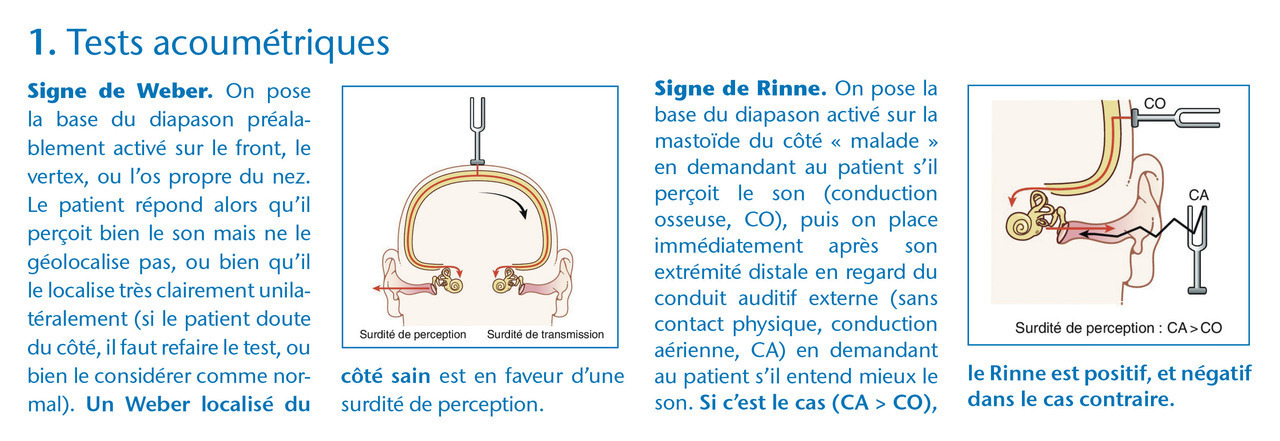
Le diagnostic n’est pas réservé à l’ORL, puisqu’il est fondé sur l’anamnèse ; des tests simples au diapason : Weber latéralisé du côté sain, Rinne positif (figure et tableau) ; une otoscopie : tympan inchangé, sans bouchon de cérumen, corps étranger ni OMA. Il est confirmé par l’ORL qui pratique une audiométrie.
Diagnostics différentiels
La surdité brusque idiopathique étant un diagnostic d’élimination, toutes les autres causes de surdité de perception à début rapide, isolée (pas de symptômes vestibulaires ni neurologiques associés) sont à écarter en premier lieu, en urgence :
- Infections : labyrinthite survenant après une OMA, otosyphilis (pouvant mimer à l’identique une maladie de Menière) chez un sujet immunocompétent ou compliquant un sida, maladie de Lyme…
- Médicaments ototoxiques : gouttes auriculaires ototoxiques (néomycine, tobramycine, gentamycine : irréversible), antibiothérapie par aminosides (idem), diurétiques de l’anse (réversible), quinine (généralement réversible), AINS (idem), chimiothérapie avec cisplatine (irréversible, atteignant 25 à 86 % des malades traités, à des degrés très variables).
- Néphropathies : insuffisance rénale chronique dialysée ou transplantée (environ 15 % des patients dialysés ou transplantés), probablement secondaire à une altération vasculaire importante.
- Sonotraumatisme : l’exposition aiguë (concert) ou chronique (ouvrier dans le bâtiment maniant un marteau-piqueur) expose à une hypoacousie de perception uni- ou bilatérale.
- Neurologiques : migraine basilaire (80 % de surdité associée), AVC vertébro-basilaire (impliquant l’artère cérébelleuse antéro-inférieure, surdité rarement isolée : instabilité, parésie faciale, hypoesthésie).
- Pathologies hématologiques : celles augmentant le risque thromboembolique peuvent être à l’origine d’épisodes ischémiques labyrinthiques mimant une surdité brusque, tels que les maladies de Vaquez, Waldenström, cryoglobulinémie, leucémies…
- Auto-immunes : la plupart des principales maladies systémiques avec auto-anticorps (lupus, Wegener, syndrome de Cogan…).
- Tumorales : neurinome de la VIIIe paire crânienne (schwannome) essentiellement. Néanmoins, ces causes sont très rares.
La surdité psychogène, principalement observée chez l’enfant, représenterait 1 à 3 % des hypoacousies brusques dans cette population. Elle touche surtout des filles, entre 8 et 13 ans, anxieuses.
Un bilan biologique et une IRM (encadré 1) sont prescrits après avoir évoqué ces causes potentielles et fait une anamnèse orientée.
Traitement
Le traitement doit être débuté dès le diagnostic, sans attendre les résultats du bilan, sauf suspicion forte de pathologie sous-jacente contre-indiquant une corticothérapie (syphilis, possibilité d’anguillulose chez les patients vivant dans les départements-régions d’outre-mer…). Néanmoins, un retard est possible sans altérer le pronostic fonctionnel : les chances de restauration (partielle ou complète) concerneraient 2 patients sur 3 s’ils sont pris en charge dans les 2 mois pour un seuil ne dépassant pas 40 dB, dans le mois pour un seuil compris entre 40 et 70 dB, et dans les 7 jours pour un seuil au-delà de 70 dB. Généralement, une récupération complète est observée chez plus de la moitié des patients avec un délai moyen de 15 jours (pouvant néanmoins atteindre plusieurs mois).
Un généraliste peut tout à fait instaurer le traitement, même si celui-ci est le plus souvent prescrit par l’ORL après l’audiogramme – le mieux étant de disposer de cet examen servant de référence préthérapeutique.
Corticothérapie systémique : quelle posologie ?
En l’absence de traitement ayant l’AMM pour cette affection, une corticothérapie systémique par prednisone ou prednisolone – la seule ayant prouvé à ce jour son efficacité – est le plus souvent prescrite en pratique courante.
La posologie n’est en revanche pas consensuelle, car les études ont rarement des méthodologies comparables. En France, le protocole le plus courant (hors AMM mais guidé par les recommandations de la Société française d’ORL) est une dose de 1 mg/kg/j pendant 7 jours, avec arrêt sans décroissance progressive. L’ajout d’un IPP tel que l’oméprazole n’est fait qu’au cas par cas (patient de plus de 70 ans, antécédents d’ulcère gastro-duodénal, gastrite). Les patients avec surdité brusque bilatérale sont le plus souvent hospitalisés en ORL pour administration intraveineuse.
D’après une nouvelle étude randomisée en triple aveugle ayant comparé l’efficacité et la sécurité de différentes doses (encadré 2), la posologie actuellement recommandée par la SFORL (1 mg/kg/j) est plus pertinente qu’une stratégie à haute dose.
Autres traitements
Les principales pistes de recherche visent à augmenter la biodisponibilité intracochléaire des corticoïdes, notamment par le biais de gels hydrosolubles à diffusion lente, apposés sur la cochlée, par injection transtympanique.
Mais une revue Cochrane publiée en 2022, qui a inclus 30 études randomisées contrôlées, a trouvé peu de différence entre l’administration intratympanique et systémique des corticostéroïdes dans la récupération de l’audition lorsqu’il s’agissait du premier traitement employé. En seconde intention, administré après l’échec d’un premier traitement, les corticostéroïdes intratympaniques semblaient toutefois entraîner une proportion beaucoup plus élevée de participants dont l’audition était améliorée, par rapport à l’absence de traitement ou au placebo (mais avec un effet faible sur le changement du seuil auditif), et le traitement combiné (systémique et local) semblait avoir un léger avantage par rapport au traitement systémique seul. Néanmoins, la plupart des données de cette revue étaient jugées de faible ou très faible niveau de certitude.
Enfin, l’appareillage auditif conventionnel est prescrit si nécessaire par l’ORL de façon secondaire : c’est un traitement palliatif de deuxième intention, l’audition pouvant encore se modifier dans les mois suivants (on peut la considérer comme stabilisée au bout d’un semestre).
Quel pronostic ?
Trois variables influencent le devenir : la sévérité de la baisse d’audition, l’aspect de l’audiogramme et l’âge :
- plus la surdité est profonde, moins les chances de récupération sont bonnes ; un audiogramme tonal et vocal à visée pronostique et de suivi est donc impératif, en semi-urgence (au mieux le jour même, sinon dans les 2 - 3 jours) ;
- les patients de plus de 40 ans et les enfants récupèrent généralement moins bien que les adultes de moins de 40 ans.
1. Quelles explorations demander ?
Bilan sanguin (dès suspicion du diagnostic) : NFS, CRP ; sérologies : VIH, TPHA-VDRL, Lyme ; ionogramme, urée, créatinine ; glycémie à jeun, exploration lipidique.
À discuter : recherche de FAN (facteurs antinucléaires) et d’ANCA (anticorps anticytoplasme des polynucléaires neutrophiles), électrophorèse des protides plasmatiques, recherche de cryoglobulinémie.
Consultation ORL avec audiogramme (dans les 3 jours).
IRM du conduit auditif interne + fosse postérieure + labyrinthe, sans urgence (dans les 3 mois), sauf signe neurologique associé.
Pas d’imagerie en urgence. Scanner si suspicion de pathologie aiguë de la fosse postérieure et si IRM indisponible (40 % de faux négatif).
2. Corticoïdes à haute dose : non supérieurs à la dose faible pour traiter la surdité brusque
Dans cette étude conduite en Allemagne et récemment parue dans le NEJM Evidence , 325 participants âgés de 18 à 80 ans ayant une surdité brusque idiopathique unilatérale (perte d’audition d’au moins 50 dB dans les 7 jours précédents) ont été recrutés.
Ils ont été aléatoirement répartis en trois bras pour recevoir, pendant 5 jours, soit de la prednisolone haute dose (250 mg/j par voie IV), soit de la dexaméthasone haute dose (40 mg/j par voie IV, soit 267 mg/j en équivalant prednisolone), soit un traitement contrôle de prednisolone per os à 60 mg/j (puis 5 jours supplémentaires en décroissance progressive, pendant lesquels les deux autres groupes recevaient un placebo oral).
Le critère de jugement principal était l’évolution de l’audition à J30, mesurée grâce au changement du seuil auditif (moyenne des sons purs : PTA pour pure tone average) dans les trois fréquences contiguës les plus affectées. À l’inclusion, la PTA médiane des trois fréquences contiguës les plus affectées dans le côté atteint des patients était de 80 Db (une valeur de PTA plus élevée indiquant une perte auditive plus importante). Les critères de jugement secondaires comprenaient la survenue d’une hypertension et d’une hyperglycémie – des effets secondaires connus de la prise de glucocorticoïdes.
Résultats : le changement moyen dans la PTA à 30 jours était de 34,2 dB dans le groupe prednisolone HD (IC95 % : 28,4 - 40,0), 41,4 dB dans le groupe dexaméthasone HD (IC95 % : 35,6 - 47,2) et de 41,0 dB dans le groupe contrôle (IC95 % : 35,2 - 46,8) [p = 0,09].
Les hautes doses n’étaient donc pas supérieures à la dose de référence en matière d’efficacité dans la récupération auditive. Elles ont engendré, en revanche, davantage d’effets indésirables : 73 EI dans le groupe prednisolone HD et 76 EI dans le groupe dexaméthasone HD ont été attribués au traitement, tandis que ce chiffre était de 46 dans le groupe contrôle. Parmi les effets secondaires d’intérêt particulier, il y a eu 18 cas d’hyperglycémie > 100 mg/L dans le groupe prednisolone HD, 21 cas dans le groupe dexaméthasone HD et 15 cas dans le groupe contrôle, ainsi que 2 cas d’augmentation de la perte auditive (> 10 dB par rapport à l’inclusion) dans le groupe prednisolone HD et 3 cas dans le groupe contrôle. Par ailleurs, une hypertension, mesurée par MAPA sur 24 heures, a été décelée à J5 chez 112 participants, avec des niveaux semblables dans les trois groupes (respectivement 44 cas, 32 cas et 36 cas).
Plontke SK, Girndt M, Meisner C, et al. High-Dose Glucocorticoids for the Treatment of Sudden Hearing Loss. N Engl J Evidence 2024;3(1):10.1056.
Plontke SK, Meisner C, Agrawal S, et al. Intratympanic corticosteroids for sudden sensorineural hearing loss. Cochrane Library 22 juillet 2022.

 Encadrés
Encadrés