Bien souvent, il est gardé sous silence, les patientes n’osant pas en parler à leur médecin alors qu’elles en souffrent au quotidien.
De quoi parle-ton ?
– vulvo-vaginaux : sécheresse, douleurs, brûlures, irritation, prurit ;
– sexuels : dyspareunie d’intromission, essentiellement. Les douleurs lors des rapports sexuels sont secondaires à l’atrophie vulvo-vaginale, en particulier au manque de lubrification et/ou à une sténose orificielle ;
– urinaires : pollakiurie (envies fréquentes d’uriner de jour comme de nuit), urgences mictionnelles (urgenturies), infections urinaires à répétition sans identification de micro-organisme (cystites à urines claires, brûlures mictionnelles).
Sa prévalence serait de 27 %2 mais semble largement sous-estimée (50 % pour certains)3.
Les signes cliniques diminuent avec la fréquence des rapports sexuels et s’aggravent avec l’âge et la durée de la ménopause.
Leurs conséquences sur la qualité de vie et la diminution de l’estime de soi impliquent de s’en enquérir lors de l’interrogatoire des femmes ménopausées. Par ailleurs, elles doivent savoir que le traitement n’a pas pour unique but d’améliorer la satisfaction sexuelle. Il évite aussi les symptômes urinaires, les voies urinaires basses ayant des récepteurs estrogéniques.
Atrophie et sécheresse
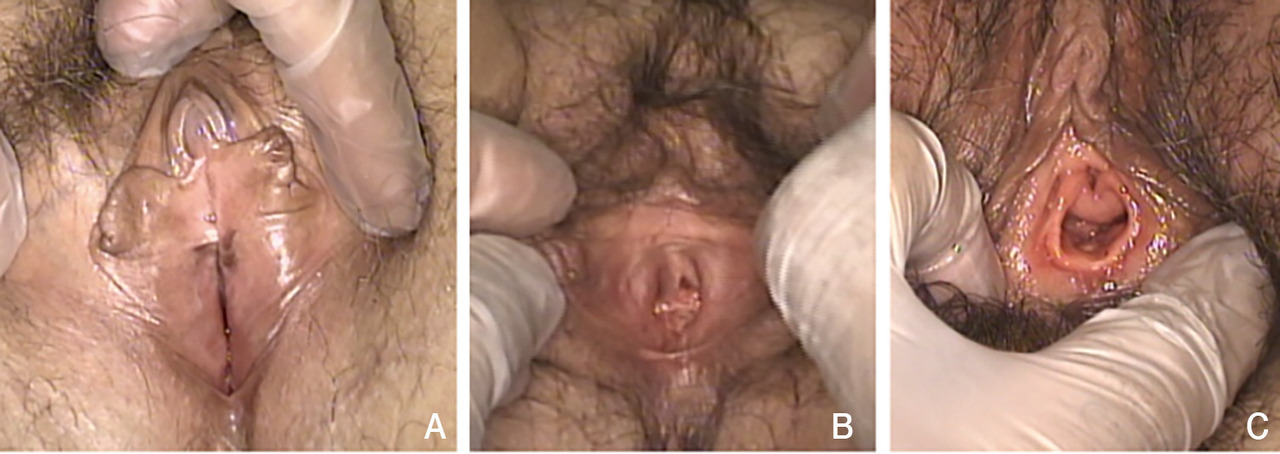
Des zones blanches, luisantes, et des signes de dermo-abrasion (liée au prurit) sont parfois observés.
Une fissure vulvaire postérieure et des pétéchies peuvent être constatées.
Le spéculum est difficile à introduire, même avec lubrifiant. Il faut l’ouvrir doucement surtout si la femme signale l’absence de rapports sexuels récents. On note une perte de souplesse du vagin.
Le toucher vaginal doit être doux, il peut ne se faire qu’à un seul doigt. L’élasticité des tissus est réduite, allant même jusqu’à la sténose orificielle avec sensation de pseudo-hymen serré alors que la femme a accouché par voie basse. On peut noter également une disparition des plis vaginaux (qui confèrent d’ordinaire l’élasticité lors du coït).
Le diagnostic positif est évoqué sur l’un des 3 signes d’appel : atrophie vulvo-vaginale, signes urinaires et sexuels.
Il est complété par une approche MPSC (médico-psycho-sociale du symptôme et du couple), comme pour toute plainte d’ordre sexuel. Outre l’aspect purement médical, l’abord psychologique fait considérer des problématiques antérieures (abus sexuels, traumatismes vulvaires) et actuelles : tendance dépressive, contexte social (difficultés professionnelles, financières, relationnelles). Le comportement du partenaire (compréhensif, attentionné, souffrant lui-même de dysfonction érectile…) est à prendre en compte.
La mesure du pH vaginal peut confirmer le déséquilibre du microbiote s’il est alcalin (> 5,5).
Plusieurs diagnostics différentiels
– Mycose : y penser devant un prurit avec pH acide < 4,5.
– Vaginose : sécrétions vaginales malodorantes avec pH > 5,5.
– Vulvodynies (douleur vulvaire intense à type de brûlure, chronique, sans anomalie clinique) et syndrome de fissure vulvaire peuvent affecter les femmes de tous âges.
– Cicatrice douloureuse (antécédent de cure de prolapsus par exemple).
– Lichen scléro-atrophique vulvaire.
Une biopsie vulvaire sous anesthésie locale est proposée en cas de doute (mycoses à répétition, hypoplasie constitutionnelle des petites lèvres, eczéma, cancer vulvaire débutant).
SGUM : 4 leviers thérapeutiques
Règles hygiénodiététiques
– hygiène simple (toilette vulvaire au savon moussant [savon de Marseille, gel douche]) ;
– éviter les douches vaginales qui altèrent le microbiote ;
– arrêt du tabac ;
– entretenir la musculature périnéale en promouvant les exercices de Kegel, si la femme contracte correctement les muscles élévateurs de l’anus. Pour le savoir, on lui demande de serrer l’anus lors de l’examen clinique, les doigts du praticien positionnés à la commissure vulvaire postérieure et en latéro-anal. La contraction musculaire est cotée de 0 à 5. Si elle n’y arrive pas ou si l’on constate une inversion de commande (la femme pousse au lieu de retenir) une rééducation par un kinésithérapeute peut être utile et aidée par la prescription d’une sonde vaginale d’électrostimulation.
L’activité sexuelle régulière augmente la vascularisation du vagin et donc l’apport de prostaglandines et d’acides gras. Par ailleurs, sa distension lors des rapports entretient la souplesse des tissus. Il faut en informer la patiente.
En cas de sténose vulvaire, l’usage de dilatateurs vaginaux de taille progressivement croissante, avec lubrifiants, est possible (Velvi, disponible sur internet).
Traitements non hormonaux
Le pH de ces produits doit être < 4,5 et l’osmolarité < 380 mOsm/kg.4 La plupart sont disponibles en pharmacie ; la préférence est actuellement accordée aux produits naturels contenant de l’acide hyaluronique (Mucogyne).
Les probiotiques restaurent la flore vaginale et diminuent le pH. Ils peuvent être adjoints à l’estriol dans le même ovule (Florgynal, Trophigil).
Hormonothérapies
L’estriol seul (Physiogine) ou la tibolone (Livial) sont également disponibles. Cette dernière a toutefois un profil de sécurité incertain, avec un risque de récurrence de cancer du sein et d’accident vasculaire cérébral. Elle semble moins efficace que le THM combiné pour soulager le SGUM.5
Différents traitements locaux sont envisageables :
– l’estradiol, diffusé à partir d’un anneau vaginal laissé 3 mois en place (Estring) ;
– l’estriol (Blissel, Physiogine, Gydrelle, Trophicrème), appliqué 2 fois par semaine ;
– la DHEA (prastérone), commercialisée en France sous le nom d’Intrarosa, prescrite quotidiennement pendant 3 mois.
La sécurité d’utilisation à long terme de ces hormonothérapies locales n’est pas connue, le recul n’étant que de 1 à 2 ans. Au-delà, il faut vérifier l’absence de retentissement sur l’endomètre. En cas de saignement, des explorations par échographie et hystéroscopie sont nécessaires.
Plusieurs méta-analyses de la Cochrane Data Base ont montré leur supériorité (vs placebo pour certains essais) dans le soulagement de la dyspareunie et des signes urinaires.6
Agents physiques
Les technologies à disposition sont nombreuses :
– lasers CO2 et Erbium-Yag font référence (DEKA, FotonaSmooth, FemiLift) ;
– LED et radiofréquences.
En août 2018, la FDA a mis en garde les praticiens sur les lasers. Leur utilisation est parfois source de complications (douleurs, brûlures, cicatrices scléreuses) et impose une meilleure évaluation prospective randomisée.
Quelles indications ?
La prise en charge doit être précoce, avant que les conséquences de l’atrophie ne deviennent irréversibles. Elle est poursuivie sur une longue durée car la pathologie est chronique.
En première intention, une approche symptomatique est proposée : règles hygiénodiététiques, lubrifiants et hydratants, dilatateurs vaginaux. Les traitements non hormonaux sont essentiellement à base de lubrifiants (à la demande lors des rapports sexuels) et d’hydratants (en entretien). Il n’existe pas d’études comparatives concernant ces produits qui utilisent des composants variés (eau, huile, silicone, acide hyaluronique, polymère polycarbophile bio-adhésif retenant l’eau). Des probiotiques contenant des lactobacilles peuvent également être associés.
Les thérapeutiques hormonales sont les plus efficaces. Les estrogènes par voie générale (THM) mais surtout locale améliorent le pH vaginal, restaurent la flore et accroissent la vascularisation locale en agissant sur les récepteurs hormonaux des voies génitales et urinaires. Les formes galéniques sont multiples (ovule, anneau, crème). En France, leur concentration en estrogènes est réduite. Le passage systémique est donc extrêmement faible. Ainsi, les taux d’estradiol plasmatique sont très bas (< 20 pg/m).
Les produits les plus usités sont à base de promestriène (crème), estrogène de synthèse, ou d’estriol, d’origine naturelle et 100 fois moins puissant que l’estradiol. Il est distribué via un anneau vaginal conservé 3 mois.
1. Symptômes génito-urinaires : 3 étapes
En première intention, les lubrifiants et hydratants sont prescrits sans réserve car leur innocuité est prouvée : tous les jours pendant 3 semaines, puis 2-3 fois par semaine pendant une période de 3 mois à 1 an.
Les traitements estrogéniques locaux sont les plus efficaces en cas d’effet insuffisant, tant pour les troubles vulvo-vaginaux que pour les signes urinaires.
Le laser est en cours d’évaluation pour l’atrophie. Il peut être proposé en première intention chez les femmes ayant une contre-indication aux estrogènes ou n’en voulant pas (exemple des cancers hormonodépendants, du sein essentiellement, surtout sous anti-aromatase).
2. SGUM : recommandations de la Société internationale de ménopause (IMS)
Les symptômes urogénitaux répondent aux estrogènes.
Un traitement à long terme est souvent nécessaire. Des risques systémiques ont été identifiés avec les estrogènes à faible dose et à puissance faible.
Lorsque l’atrophie vulvo-vaginale est le seul symptôme, les estrogènes locaux sont privilégiés.
Il est préférable de commencer tôt le traitement et de le poursuivre pour maintenir les bénéfices.
L’estrogénothérapie locale minimise l’absorption systémique et les taux sériques d’estradiol ne dépassent pas la zone normale (< 20 μg/mL) chez les femmes ménopausées.
Un progestatif supplémentaire n’est pas nécessaire.
2. Pastore LM, Carter RA, Hulka BS, Wells E. Self-reported urogenital symptoms in postmenopausal women: Women’s Health Initiative. Maturitas 2004; 49:292‑303.
3. Nappi RE, Palacios S, Panay N, Particco M, Krychman ML. Vulvar and vaginal atrophy in four European countries: evidence from the European REVIVE Survey. Climacteric 2016;19:188‑97.
4. Edwards N, Panay N. Treating vulvovaginal atrophy/genitourinary syndrome of menopause: how important is vaginal lubricant and moisturizer composition? Climateric 2016;19:151-61.
5. Formoso G, Perrone E, Maltoni S, Balduzzi S, D’Amico R, Bassi C, Basevi V, Marata AM, Magrini N, Maestri E. Short and long term effects of tibolone in postmenopausal women. Cochrane Database Syst Rev 2012;(2):CD008536.
6. Lethaby A, Ayeleke RO, Roberts H. Local oestrogen for vaginal atrophy in postmenopausal women. Cochrane Database Syst Rev 2016;(8):CD001500.
7. Ruanphoo P, Bunyavejchevin S Treatment for vaginal atrophy using microablative fractional CO2 laser: a randomized double-blinded sham-controlled trial. Menopause 2020;27:858-63.
8. Baber RJ, Panay N, Fenton A; IMS Writing Group. 2016 IMS Recommendations on women’s midlife health and menopause hormone therapy. Climacteric. 2016;19:109-50.

 Encadrés
Encadrés